文档内容
1.中国药学家屠呦呦因发现青蒿素荣获了诺贝尔奖。青蒿素的分子式为 C H O 。下列说
15 22 5
法正确的是( )
A.青蒿素的摩尔质量为282 g·mol-1
B.青蒿素中C、H、O的质量之比为15∶22∶5
C.1 mol青蒿素的体积为22.4 L
D.1 mol青蒿素中含11 mol H
2
2.下列物质中,与0.3 mol HO含有相同氢原子数的物质是( )
2
A.18.9 g HNO
3
B.0.1 mol NH HSO
4 4
C.3.612×1023个HCl分子
D.4.48 L CH(标准状况)
4
3.某硫原子的质量是a g,12C原子的质量是b g,若N 表示阿伏加德罗常数的值,则下列说
A
法正确的是( )
①该硫原子的相对原子质量为 ②m g该硫原子的物质的量为 mol ③该硫原子的摩尔质
量是aN g ④a g该硫原子所含的电子数为16N
A A
A.①③ B.②④ C.①② D.②③
4.设N 为阿伏加德罗常数的值,如果a g某气态双原子分子的分子数为p,则b g该气体
A
在标准状况下的体积V(L)是( )
A. B.
C. D.
5.据央视新闻报道,在政府工作报告中指出,建设一批光网城市,推进 5万个行政村通光
纤,让更多城乡居民享受数字化生活。光缆的主要成分为SiO。下列叙述正确的是( )
2
A.6 g光缆由0.1 mol SiO 分子构成
2
B.标准状况下,15 g SiO 的体积为5.6 L
2
C.SiO 中Si与O的质量之比为7∶8
2
D.相同质量的SiO 和CO 中含有的氧原子数相同
2 2
6.在150 ℃时碳酸铵受热可完全分解,则其完全分解后所产生的气态混合物的密度是相同
条件下氢气密度的( )
A.96倍 B.48倍 C.12倍 D.32倍
7. 如图表示1 g O 与1 g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气
2
体可能是( )A.C H B.CH C.CO D.NO
2 4 4 2
8.一定温度和压强下,用m g的CH、CO、O、SO 四种气体分别吹出四个体积大小不同
4 2 2 2
的气球。下列说法正确的是( )
A.气球②中装的是O
2
B.气球①和气球③中气体分子数相等
C.气球①和气球④中气体物质的量之比为4∶1
D.气球③和气球④中气体密度之比为2∶1
9.(2023·青岛质检)下列判断正确的是( )
A.同温、同压下,相同体积的氮气和氦气所含的原子数相等
B.标准状况下,5.6 L以任意比例混合的氯气和氧气所含的原子数为0.5N
A
C.1 mol氯气和足量NaOH溶液反应转移的电子数为2N
A
D.常温、常压下,22.4 L的NO 和CO 混合气体含有2N 个O原子
2 2 A
10.(2022·台州模拟)下列有关C H 和C H 的叙述错误的是( )
2 2 6 6
A.二者碳元素的质量分数相同
B.在标准状况下,等体积的两种物质含有的分子数相等
C.等物质的量时,二者质量之比为=
D.等质量时,二者完全燃烧消耗相同状况下的氧气的体积相等
11.在甲、乙两个体积不同的密闭容器中,分别充入质量相等的 CO、CO 气体时,两容器
2
的温度和压强均相同,则下列说法正确的是( )
A.充入的CO分子数比CO 分子数少
2
B.甲容器的体积比乙容器的体积小
C.CO的摩尔体积比CO 的摩尔体积小
2
D.甲中CO的密度比乙中CO 的密度小
2
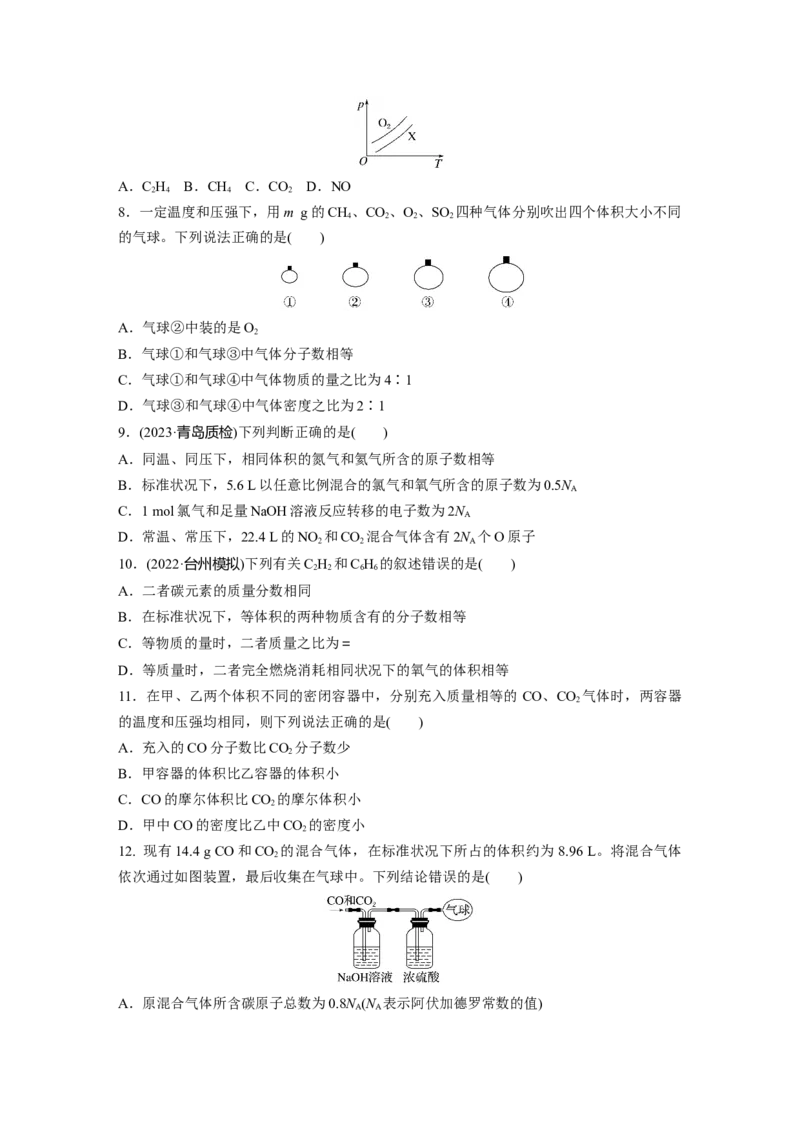
12. 现有14.4 g CO和CO 的混合气体,在标准状况下所占的体积约为 8.96 L。将混合气体
2
依次通过如图装置,最后收集在气球中。下列结论错误的是( )
A.原混合气体所含碳原子总数为0.8N (N 表示阿伏加德罗常数的值)
A AB.标准状况下,气球中收集到的气体体积为4.48 L
C.NaOH溶液增重8.8 g
D.原混合气体中CO和CO 的体积比为1∶1
2
13.Ⅰ.现有m g某气体(双原子分子),其摩尔质量为M g·mol-1,若阿伏加德罗常数的值用
N 表示,则:
A
(1)该气体的物质的量为________mol。
(2)该气体所含原子总数为________。
(3)该气体在标准状况下的体积为________L。
Ⅱ.臭氧层是地球生命的保护层,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压
放电管来制取臭氧:3O===2O ,将8 L氧气通过放电管后,恢复到原状况,得到气体6.5
2 3
L,其中臭氧为________ L。
14.如图所示,一密闭容器被无摩擦、可滑动的两隔板a和b分成甲、乙两室。标准状况下,
在乙室中充入0.6 mol HCl,甲室中充入NH 、H 的混合气体,静止时隔板位置如图。已知
3 2
甲、乙两室中气体的质量之差为10.9 g。
(1)甲室中气体的物质的量为________mol。
(2)甲室中气体的质量为________g。
(3)甲室中NH 、H 的平均相对分子质量为______________________。
3 2
(4)经过查资料知道HCl+NH ===NH Cl(NHCl常温下是固体),如果将隔板a去掉,当HCl
3 4 4
与NH 完全反应后,隔板b将静置于刻度“______”处(填数字)。
3
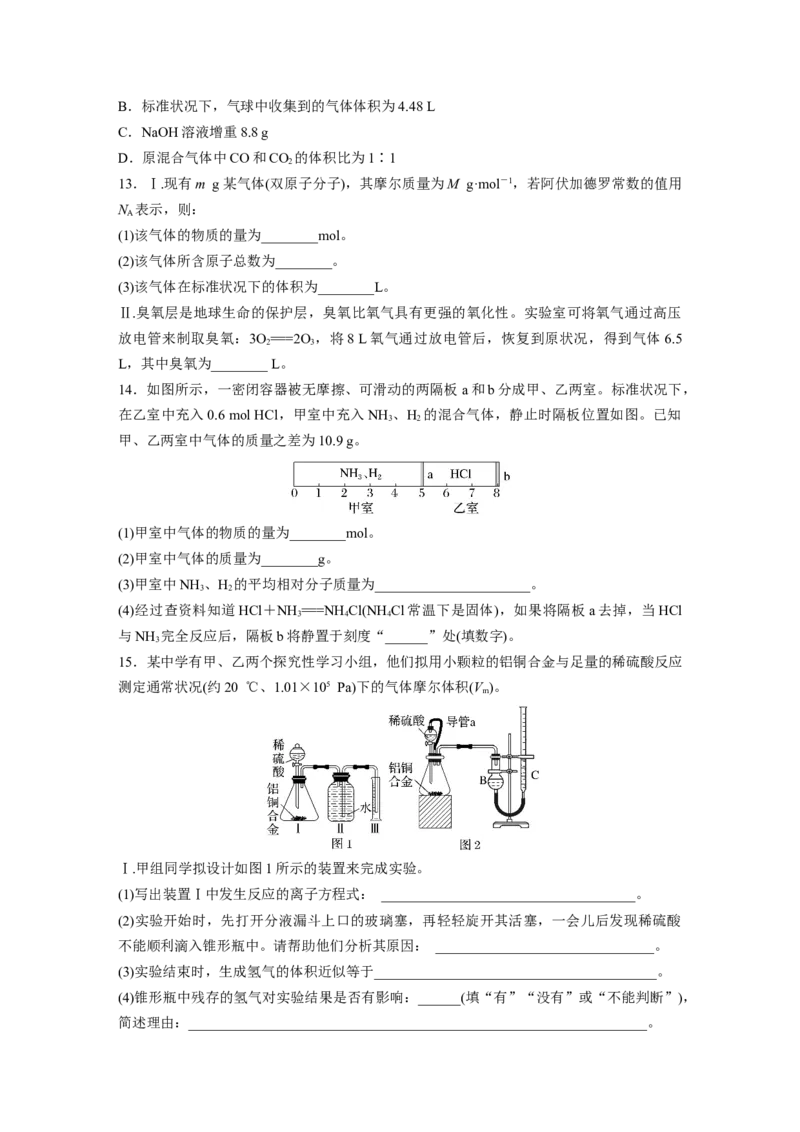
15.某中学有甲、乙两个探究性学习小组,他们拟用小颗粒的铝铜合金与足量的稀硫酸反应
测定通常状况(约20 ℃、1.01×105 Pa)下的气体摩尔体积(V )。
m
Ⅰ.甲组同学拟设计如图1所示的装置来完成实验。
(1)写出装置Ⅰ中发生反应的离子方程式: ____________________________________。
(2)实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻旋开其活塞,一会儿后发现稀硫酸
不能顺利滴入锥形瓶中。请帮助他们分析其原因: _______________________________。
(3)实验结束时,生成氢气的体积近似等于________________________________________。
(4)锥形瓶中残存的氢气对实验结果是否有影响:______(填“有”“没有”或“不能判断”),
简述理由:_________________________________________________________________。Ⅱ.乙组同学仔细分析了甲组同学的实验装置后,认为稀硫酸滴入锥形瓶中,即使不生成氢
气,也会将瓶中的空气排出,使所测氢气的体积偏大;实验结束后,连接广口瓶和量筒的导
管中有少量水存在,使所测氢气的体积偏小,于是他们设计了如图2所示的实验装置。
实验中准确测定出4个数据,如表:
实验前 实验后
铝铜合金质量/g m m
1 2
量液管(C)中液体体积/mL V V
1 2
(注:量液管大刻度在上方,小刻度在下方)
利用上述数据计算通常状况下的气体摩尔体积V =________________________。
m