文档内容
重难点 05 氧化还原反应的概念、规律、配平及计算
►命题趋势►解题策略►真题回眸►限时检测
考向一 是否为氧化还原反应的判断
考向二 氧化还原反应的相关概念
氧化还原反应的概念、规律、配平及计算 考向三 氧化还原反应的性质规律
考向四 氧化还原反应的配平
考向五 氧化还原反应的计算
氧化还原反应是高考的必考内容,从考查内容上看:
(1)借助STSE型试题判断指定反应是否是氧化还原反应、氧化还原反应中电子的转移数目在N 题
A
目中是命题的热点;
(2)物质氧化性、还原性的强弱常与离子方程式正误判断融合考查;
(3)在工艺流程题中常常涉及陌生氧化还原方程式的书写。
预测2024年高考仍可能在选择题中结合生产、生活,考查氧化还原反应的判断、氧化还原反应的概
念及相互关系、简单计算等,应予以关注。
【策略1】理顺氧化还原反应的基本概念及相互关系
概括为“升失氧、降得还,剂性一致、其他相反”。
【策略2】掌握氧化还原反应电子转移的表示方法
(1)双线桥法:①标变价、②画箭头(反应物指向生成物)、③算数目、④说变化。
。
(2)单线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标“得”“失”字
样。
资料整理【淘宝店铺:向阳百分百】。
【策略3】掌握氧化还原反应的基本规律
元素处于最高价,只有氧化性(如KMnO 中的Mn);
4
价态律 元素处于最低价,只有还原性(如S2-、I-);
元素处于中间价态,既有氧化性,又有还原性(如Fe2+、S、Cl 等)
2
氧化性:氧化剂>氧化产物;
还原性:还原剂>还原产物。
强弱律
在适宜的条件下,用氧化性(还原性)较强的物质可制备氧化性(还原性)较弱的物质,用
于比较物质的氧化性或还原性的强弱;
①同时含有几种还原剂时将按照还原性由强到弱的顺序依次反应。如:在 FeBr 溶液
2
中通入少量Cl 时,因为还原性:Fe2+>Br-,所以Fe2+先与Cl 反应。
2 2
②同时含有几种氧化剂时将按照氧化性由强到弱的顺序依次反应。如:在含有 Fe3+、
Cu2+、H+的溶液中加入铁粉,因为氧化性:Fe3+>Cu2+>H+,所以铁粉先与Fe3+反
优先律
应,然后再依次与Cu2+、H+反应。
③常见的强弱顺序
氧化性:MnO(H+)>Cl >Br >Fe3+>I >稀HSO >S,
2 2 2 2 4
还原性:Mn2+Ⅱ,C
错误;
D. 中As为+3价,S为-2价,在经过反应Ⅰ后,As的化合价没有变,S变为+2价,则1mol 失
电子3×4mol=12mol;在经过反应Ⅱ后,As变为+5价,S变为+6价,则1mol 失电子
2×2mol+3×8mol=28mol,则反应Ⅰ和Ⅱ中,氧化 转移的电子数之比为3∶7,D正确;
故选D。
资料整理【淘宝店铺:向阳百分百】9.(2022·河北·高考真题·节选)以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝
颜料。工艺流程如下:
回答下列问题:
(3)还原工序中,不生成S单质的反应的化学方程式为 。
(5)沉铁工序产生的白色沉淀 中 的化合价为 ,氧化工序发生反应的离子方程式
为 。
【答案】
(3)7Fe (SO )+FeS +8H O=15FeSO +8H SO
2 4 3 2 2 4 2 4
(5)+2; 6Fe(NH )Fe(CN) + +6H+=6Fe(NH)Fe(CN) +3H O+Cl-+
4 2 6 4 6 2
【详解】已知黄铁矿高温煅烧生成Fe O,反应原理为:4FeS+11O 2Fe O+8SO,故产生的红渣主要
2 3 2 2 2 3 2
成分为Fe O 和SiO,将红渣粉碎后加入足量的50%的HSO 溶液加热充酸浸,反应原理为:
2 3 2 2 4
Fe O+3H SO =Fe (SO )+3H O,过滤出滤渣①,主要成分为SiO,向滤液中加入黄铁矿进行还原,将
2 3 2 4 2 4 3 2 2
Fe3+还原为Fe2+,由(3)小问可知不生成S沉淀,则硫元素被氧化为 ,反应原理为:14Fe3+
+FeS +8H O=15Fe2++2 +16H+,然后进行工序①为蒸发浓缩、冷却结晶,得到FeSO 晶体和母液主要含
2 2 4
有FeSO 溶液和HSO ,加水溶解FeSO 晶体,向所得溶液中加入(NH )SO 、K[Fe(CN) ]并用HSO 调节
4 2 4 4 4 2 4 4 6 2 4
溶液的pH为3,进行沉铁过程,反应原理为:Fe2++2 +[Fe(CN)]3-=Fe(NH)Fe(CN) ↓,然后过滤出沉淀,
6 4 2 6
洗涤后加入HSO 和NaClO 进行氧化步骤,反应原理为:6Fe(NH )Fe(CN) +
2 4 3 4 2 6
+6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 ,过滤、洗涤干燥即制得Fe(NH )Fe(CN) ,据此分析解题。
4 6 2 4 6
(3)由分析可知,还原工序中,不产生S单质沉淀,则硫元素被氧化为 ,反应原理为:14Fe3+
+FeS +8H O=15Fe2++2 +16H+,故化学方程式为:7Fe (SO )+FeS +8H O=15FeSO +8H SO ,故答案为:
2 2 2 4 3 2 2 4 2 4
7Fe (SO )+FeS +8H O=15FeSO +8H SO ;
2 4 3 2 2 4 2 4
(5)沉铁工序中产生的白色沉淀Fe(NH )Fe(CN) 中Fe的化合价为+2价和[Fe(CN) ]4-中的+3价,由分析可
4 2 6 6
知,氧化工序所发生的离子方程式为:6Fe(NH )Fe(CN) + +6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 ,
4 2 6 4 6 2
故答案为:+2;6Fe(NH )Fe(CN) + +6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 ;
4 2 6 4 6 2
资料整理【淘宝店铺:向阳百分百】考向五 氧化还原反应的计算
10.(2022·北京·高考真题)某 多孔材料孔径大小和形状恰好将 “固定”,能高选择性吸附
。废气中的 被吸附后,经处理能全部转化为 。原理示意图如下。
已知:
下列说法不正确的是
A.温度升高时不利于 吸附
B.多孔材料“固定” ,促进 平衡正向移动
C.转化为 的反应是
D.每获得 时,转移电子的数目为
【答案】D
【分析】废气经过MOFs材料之后,NO 转化成NO 被吸附,进而与氧气和水反应生成硝酸,从该过程中
2 2 4
我们知道,NO 转化为NO 的程度,决定了整个废气处理的效率。
2 2 4
【详解】A.从 可以看出,这个是一个放热反应,升高温度之后,平衡逆向移动,
导致生成的NO 减少,不利于NO 的吸附,A正确;
2 4 2
B.多孔材料“固定” ,从而促进 平衡正向移动,B正确;
C.NO 和氧气、水反应生成硝酸,其方程式为 ,C正确;
2 4
D.在方程式 中,转移的电子数为4e-,则每获得 ,转移的电子数为
0.4mol,即个数为 ,D错误;
故选D。
11.(2022·浙江·统考高考真题)关于反应4CO+SiH 4CO+2HO+SiO,下列说法正确的是
2 4 2 2
A.CO是氧化产物
B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4
D.生成1molSiO 时,转移8mol电子
2
【答案】D
【详解】A.根据反应方程式,碳元素的化合价由+4价降为+2价,故CO为还原产物,A错误;
资料整理【淘宝店铺:向阳百分百】B.硅元素化合价由-4价升为+4价,故SiH 发生氧化反应,B错误;
4
C.反应中氧化剂为二氧化碳,还原剂为SiH,,则氧化剂与还原剂的物质的量之比为4:1,C错误;
4
D.根据反应方程式可知,Si元素的化合价由-4价升高至+4价,因此生成1molSiO 时,转移8mol电子,
2
D正确;
答案选D。
12.(2023·辽宁·统考高考真题)我国古代四大发明之一黑火药的爆炸反应为:
。设 为阿伏加德罗常数的值,下列说法正确的是
A. 含 键数目为
B.每生成 转移电子数目为
C. 晶体中含离子数目为
D. 溶液中含 数目为
【答案】C
【详解】A. 分子含有2个 键,题中没有说是标况条件下,气体摩尔体积未知,无法计算 键个数,
A项错误;
B.2.8g 的物质的量 ,1mol 生成转移的电子数为12 ,则0.1mol 转移的
电子数为1.2 ,B项错误;
C.0.1mol 晶体含有离子为 、 ,含有离子数目为0.2 ,C项正确;
D.因为 水解使溶液中 的数目小于0.1 ,D项错误;
答案选C。
(建议用时:35分钟)
1.(2023·陕西渭南·统考模拟预测)下列实验中的颜色变化与氧化还原反应无关的是
选项 A B C D
溶液滴入 溶 通入 溶 溶液滴入 浊
实验 石蕊溶液滴入氯水中
液中 液中 液中
产生白色沉淀,最终变为 沉淀由白色逐渐变为 溶液变红,随后迅速
现象 产生淡黄色沉淀
红褐色 黄色 褪色
A.A B.B C.C D.D
【答案】C
【详解】A.NaOH溶液滴入FeSO 溶液中,首先发生复分解反应产生Fe(OH) 白色沉淀,
4 2
2NaOH+FeSO =Fe(OH) ↓+Na SO ,Fe(OH) 具有强的还原性,又被溶解在溶液中的O 氧化为Fe(OH) ,发
4 2 2 4 2 2 3
资料整理【淘宝店铺:向阳百分百】生反应:4Fe(OH) +O +2H O=4Fe(OH) ,因此看到白色沉淀迅速变为灰绿色,最后变为红褐色,颜色变化
2 2 2 3
与氧化还原反应有关,A不符合题意;
B. 通入 溶液中,发生反应3 +2 =3S +2Na SO ,该反应中元素化合价发生变化,属于
2 3
氧化还原反应,B不符合题意;
C.KI溶液滴入AgCl浊液中,发生沉淀转化,由白色AgCl沉淀逐渐变为溶解度更小的黄色AgI沉淀,因
此看到沉淀由白色逐渐变为黄色,在反应过程中元素化合价不变,故物质的颜色变化与氧化还原反应无关,
C符合题意;
D.氯水中含有HCl、HClO电离产生的H+,溶液显酸性,使紫色石蕊试液变为红色,同时溶液中含有的
HClO、ClO-具有强氧化性,又将红色物质氧化变为无色,因此石蕊溶液滴入氯水中,看到溶液先变红,随
后迅速褪色,物质的颜色变化与氧化还原反应有关,D不符合题意;
故选C。
2.(2023·河北衡水·校考三模)酸性溶液中,在 、 的催化下, 将 氧化为
的反应过程中发生以下几个反应:① 与 生成 和 ;② 与 发生取代反应生
成 ;③ 将 氧化为 ,本身被还原为HBrO;④HBrO和 把
彻底氧化,并实现催化剂的再生。下列说法错误的是
A.①中每转移0.5mol电子时,可生成0.3mol
B.②③均属于氧化还原反应,且均使溶液中 增大
C.④的离子方程式为
D.恰好完全反应时, 与 的物质的量之比为4∶3
【答案】B
【分析】根据信息和氧化还原反应方程式的书写方法,可以写出①②③④的有关方程式:
①
②
③
④
将②③④方程式的化学计量数扩大3倍,然后将①②③④的有关方程式相加,得出总反应为
,
【详解】A.由①的离子方程式可知,每转移5mol电子时,生成3mol ,则每转移0.5mol电子时,可生
成0.3mol ,A正确;
B.②③反应中均有元素化合价改变,均属于氧化还原反应;②反应生成强酸HBr使 增大,③反应
消耗 ,使 减小,B错误;
资料整理【淘宝店铺:向阳百分百】C.根据信息,④反应中HBrO既将 氧化为 ,还要实现 和 的再生,故离子方程
式为 ,C正确;
D.由分析的总反应可知,恰好完全反应时, 与 的物质的量之比为4∶3,D正确;
故选B。
3.(2023·山东菏泽·校考二模)火是人类文明的起源,以下古文献描述中,借助“火”的过程中有氧化还
原反应发生的是
A.《天工开物》中描述“凡石灰,经火焚炼为用”
B.《传言方》中记载“白矾以炭火烧令汁尽,则其色如雪,谓之巴石以治气痢”
C.《新修本草》中关于“青矾”的记录为“本来绿色,…,烧之赤色”
D.《本草经注》中记载“以火烧之,紫青烟起为硝石”来鉴别硝石(KNO)和朴硝(Na SO )
3 2 4
【答案】C
【详解】A.碳酸钙受热分解生成氧化钙和二氧化碳,无化合价变化,不是氧化还原反应,故A错误;
B.白矾即为明矾,此过程为KAl(SO )·12H O失水得KAl(SO ),不是氧化还原反应,故B错误;
4 2 2 4 2
C.FeSO ·7H O在空气中灼烧生成Fe O,铁元素的化合价变化,是氧化还原反应,故C正确;
4 2 2 3
D.利用焰色试验鉴别KNO 和NaSO ,焰色试验没有发生化学变化,故D错误;
3 2 4
故选C。
4.(2022·浙江金华·校联考模拟预测)三草酸合铁酸钾是制备负载型活性铁催化剂的主要原料,该配合物
在光照下易分解: ,下列说法不正确的是
A.反应物中 元素只体现氧化性, 元素既体现氧化性又体现还原性
B.氧化产物和还原产物的物质的量之比为
C.若有 被还原,则被还原的 为6mol
D.每生成 ,转移电子数为
【答案】C
【详解】A.反应中Fe由+3价变为+2价,化合价降低表现氧化性被还原;碳元素化合价由+3部分变为
+2、部分变为+4, 元素既体现氧化性又体现还原性,A正确;
B.反应中氧化产物为12分子二氧化碳,还原产物为11分子一氧化碳和1分子氧化铁,故氧化产物和还原
产物的物质的量之比为 ,B正确;
C.由化学方程式可知,2个铁离子被还原的同时,11个碳被还原生成11分子CO,故两者关系为
,则若有 被还原,则被还原的 为5.5mol,C错误;
D.由化学方程式可知,反应中13个碳的化合价由+3变为+4转移13个电子生成13分子二氧化碳,电子
转移关系为 ,则每生成 ,转移电子数为 ,D正确;
故选C。
资料整理【淘宝店铺:向阳百分百】5.(2023·山东聊城·统考三模) 是分析化学中的重要试剂,不溶于冷水。实验测定 粗产品
纯度的步骤如下:①将一定质量的 粗产品加入含有足量 的强酸性溶液中,充分反应后,溶液
变为紫红色,同时生成 ;②用一定浓度的草酸( )标准溶液滴定①中反应后的溶液,通过消耗草
酸标准溶液的体积计算产品纯度。下列有关说法正确的
A.步骤①中用硝酸溶液提供强酸性环境
B.步骤①中反应的离子方程式为
C.步骤②达到滴定终点时紫红色褪去
D.步骤②中反应的还原剂和氧化产物的物质的量之比为
【答案】C
【详解】A.硝酸具有强氧化性,若用硝酸溶液提供酸性环境,则多余的硝酸会与草酸反应,导致消耗草
酸的量偏大,影响实验,A错误;
B.步骤①中NaBiO 与Mn2+反应生成Bi3+和 ,NaBiO 是沉淀,不能拆成离子的形式,正确的离子方
3 3
程式为5NaBiO+2Mn2++14H+=5Bi3++2 +7H O+5Na+,B错误;
3 2
C.步骤②中草酸与生成的高锰酸根离子反应,达到滴定终点时高锰酸根离子刚好被消耗完,溶液紫红色
褪去,C正确;
D.高锰酸根离子与草酸反应的离子方程式为5HC O+2 +6H+=10CO ↑+2Mn2++8H O,HC O 为还原
2 2 4 2 2 2 2 4
剂,氧化产物为CO,还原剂和氧化产物的物质的量之比为1:2,D错误;
2
故答案选C。
6.(2023·山东·沂水县模拟预测)NaClO 是一种重要的杀菌消毒剂, 的一种生产工艺流程如下所
2
示。已知:“有效氯含量”是指每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。下列说法错误
的是
A.在该生产过程中,有三处涉及到氧化还原反应
B.在电解过程中, 是还原产物
C.“尾气吸收”反应中,氧化剂与还原剂的物质的量之比为1:2
D. 的“有效氯含量”约为1.57g
【答案】C
【详解】A.由制备流程可知,“反应”“电解”“尾气吸收”过程均发生 元素的化合价变化,发生了
资料整理【淘宝店铺:向阳百分百】氧化还原反应,A正确;
B.电解过程中, 在阴极得电子生成 ,所以阴极反应的主要产物是 ,B正确;
C.“尾气吸收”过程发生反应的化学方程式为 ,该反应
中 中 元素化合价由-1价变为0价、Cl元素化合价由+4价变为+3价, 是氧化剂、 是还原
剂,氧化剂与还原剂的物质的量之比等于其计量数之比,即 ,C错误;
D. 的物质的量 ,依据电子转移数目相等, ,
,可知氯气的物质的量为 ,则氯气的质量为
,D正确。
故选C。
7.(2023·陕西渭南·统考一模)用 表示阿伏加德罗常数,下列说法正确的是
A.常温下, 铁与足量浓硫酸充分反应转移的电子数为
B.标准状态下, 分子中所含的 原子数为
C. 与 反应时,转移电子的数目为
D.浓度均为 的 溶液和 溶液中, 数目均为
【答案】C
【详解】A.铁遇到浓硫酸会钝化,A错误;
B.标准状况下,三氧化硫为固体,无法计算其物质的量,B错误;
C. 与 反应生成0.1molFeCl 和0.1molI ,转移电子的数目为 ,C正确;
2 2
D.没有给出溶液的体积,无法计算其物质的量,D错误;
故选C。
8.(2022·云南保山·统考一模)已知: ,下列关于
该反应的说法正确的是
A.产生22.4L(标准状况) 时,反应中转移5mol电子
B.反应中 既是氧化剂又是还原剂
C.氧化性:
D.还原产物是 ,氧化产物为
【答案】B
【详解】A.上述反应中硫酸亚铁是还原剂,过氧化钠既做氧化剂又做还原剂,2mol亚铁失去8mol电子
转化为高铁酸钠,1mol过氧化钠失去2mol电子生成氧气,故每发生1mol上述反应生成1mol氧气转移
10mol电子,故A错误;
资料整理【淘宝店铺:向阳百分百】B.反应中 既是氧化剂又是还原剂,B正确;
C.该反应中过氧化钠是氧化剂,故氧化性: ,C错误;
D.氧化产物是 和 ,还原产物为 和 ,D错误;
故选B。
9.(2023·浙江杭州·校联考模拟预测)超氧化钾( )在加热条件下可以将 氧化,该反应的化学方程
式如下: ,则下列说法不正确的是
A.该反应中化合价升高的元素是O和Cu
B. 既是氧化产物,又是还原产物
C.当反应中转移的电子数为 时,有 被氧化
D.标准状况下,生成 时,被还原的超氧化钾( )为
【答案】C
【分析】 中,Cu化合价由+2价升高到+3价, 中O的化合价由- 价一部
分升高为0价,一部分降低到-2价,2molCuO参加反应,一共转移3mol电子;
【详解】A.根据分析可知,该反应中化合价升高的元素是O和Cu,选项A正确;
B.Cu化合价由+2价升高到+3价,O元素部分由- 价降为-2价, 既是氧化产物,又是还原产物,
选项B正确;
C.反应 中,共转移3mol电子,故当反应中转移的电子数为 时,有
被氧化,选项C错误;
D. 中O的化合价由- 价一部分长高为0价,一部分降低到-2价,比例为1:1,标准状况下,生成
时,即0.1mol,被还原的超氧化钾( )为 ,选项D正确;
答案选C。
10.(2023·河北·校联考三模)二氟化氧( )可用作极强的氧化剂和氟化剂。已知:①
(NaOH溶液的浓度为2%),② 。下列说法错误的是
A. 分子的空间结构呈V形
B.反应①中,每生成 ,转移电子4mol
C.反应②中, 和 既是氧化产物又是还原产物
D.氧化性的强弱比较:
资料整理【淘宝店铺:向阳百分百】【答案】C
【详解】A. 分子中有2个 键电子对,氧原子上有2个孤电子对,故 分子的空间结构为V形,A
项正确;
B.反应①中,依据得失电子守恒,每生成 ,转移电子4mol,B项正确;
C.反应②中, 既是氧化产物又是还原产物, 仅是氧化产物,C项错误;
D.依据氧化性:氧化剂>氧化产物,氧化剂>还原剂,可得出氧化性: ,D项正确;
答案选C。
11.(2023·河北衡水·衡水市三模)某污水处理厂用“ 沉淀法”处理含铬废水(主要含 以及少量
、 )的工艺流程如图所示:
已知:①金属离子 、 、 沉淀完全时( )pH分别为6.7、5.6、2.8。
② 。
下列说法错误的是
A.“氧化”时生成 的离子方程式为
B.“沉降”过程中加入NaOH溶液,调节溶液pH>6.7
C.加入 生成 ,说明
D.“沉铬”过程中,增大溶液的pH,沉铬率提高
【答案】A
【详解】A.碱性环境中不能生成 ,A错误;
B.“沉降”过程中加入NaOH溶液,调节pH使 和 生成沉淀,故需要调节溶液的 ,B正
确;
C.在滤液中加入 通过沉淀转化生成 ,说明溶度积 ,C正确;
D.在沉铬过程中增大溶液的pH,平衡 正向移动, 浓度增大,沉铬率
提高,D正确。
故选A。
12.(2023·江西·校联考模拟预测)高铁酸钠(Na FeO)是一种绿色净水剂。
2 4
①实验室制备原理是 ;
②在酸性介质中高铁酸钠不稳定,发生反应: ,在碱性介质中能稳定
存在;
资料整理【淘宝店铺:向阳百分百】③已知氧化剂的电势是衡量其氧化性强度的主要参数,电势越高,对应条件下氧化剂的氧化性越强,酸性
条件下,电势:FeO >Cl。
2
下列叙述错误的是
A.配制NaFeO 溶液时添加少量NaOH溶液
2 4
B.由反应①知,氧化性:NaClO>Na FeO
2 4
C.由反应②知,产生11.2LO 时转移2mol电子
2
D.向NaFeO 溶液中滴加浓盐酸产生的气体不只一种
2 4
【答案】C
【详解】A.依题意,在碱性条件下高铁酸钠能稳定存在,不引入杂质,配制高铁酸钠溶液时应添加少量
氢氧化钠溶液,A项正确;
B.反应①中NaClO是氧化剂,NaFeO 是氧化产物,氧化剂的氧化性强于氧化产物的,B项正确;
2 4
C.没有指明生成O 时的温度、压强,不能根据体积计算氧气的物质的量,C项错误;
2
D.高铁酸钠具有强氧化性,能氧化氯离子,另外酸性条件下高铁酸钠不稳定,容易分解,故向高铁酸钠
中滴加浓盐酸能产生氧气、氯气等,D项正确;
故选C。
13.(2022·浙江·校联考二模)关于反应 ,下列说法
不正确的是
A. 既是氧化剂又是还原剂
B. 发生还原反应
C.若有 加反应,被 还原的 为
D.反应若生成 ,转移 电子
【答案】C
【详解】A. 中硫元素为-1价,其化合价既降低为-2价也升高为+6价,既是氧化剂又是还原剂,故A
正确;
B. 中铜元素从+2价降低至+1价,做氧化剂,发生还原反应,故B正确;
C.被 还原的 生成Cu S,即 参加反应,被还原的 为7mol,故C错误;
2
D.铜元素从+2价降低至+1价,硫元素由-1价降低为-2价, 中铜得到14mol电子, 中硫得到
7mol电子,生成12mol硫酸转移21mol电子,若生成 ,转移 电子,故D正确;
故选:C。
14.(2023·河南·校联考一模)化石燃料燃烧会产生大气污染物 、 等,科学家实验探究用硫酸铈
循环法吸收 ,其转化原理如图所示,下列说法正确的是
资料整理【淘宝店铺:向阳百分百】A.检验 可以选用盐酸酸化的 溶液
B.反应①的离子方程式为
C.反应②中氧化剂与氧化产物的物质的量之比为1:2
D.理论上每吸收标准状况下 ,一定消耗
【答案】B
【详解】A.硫酸根的检验需要先加入盐酸排查银离子的干扰,再加氯化钡产生白色沉淀证明有硫酸根,
A错误;
B.从图中看,反应①中氧化剂是 ,还原剂是 ,两者发生氧化还原反应生成 、 ,方程式
为 , B正确;
C.反应②中氧气中氧元素化合价由0变为-2,为氧化剂, 化合价升高发生氧化反应得到氧化产物
,根据电子守恒可知 ,故氧化剂与氧化产物的物质的量之比为1:4,C错误;
D.根据电子守恒可知 ,理论上每吸收标准状况下 (为0.01mol),消耗
0.005mol氧气,为0.16g,D错误;
故选B。
15.(2022·云南保山·统考一模)4.35g铜镁合金完全溶于一定浓度的硝酸,产生4480mL的 和
1120mL的NO气体(标准状况下),反应后的溶液中加入足量氢氧化钠溶液,生成的沉淀最大质量为
A.20.60g B.10.30g C.15.50g D.31.00g
【答案】B
【详解】铜镁合金与硝酸完全反应,生成4480mL的 ,即0.2mol,1120mL的NO气体,即0.05mol,由
硝酸转化为 和NO的得到的电子总数是0.2mol(5-4)+0.05mol(5-2)=0.35mol, 铜镁合金反应后由0
价转为为+2价,失去电子总数是0.35mol,则铜镁合金的量为 mol,与氢氧化钠溶液反应后生成
Cu(OH) 、Mg(OH) ,由于每个镁离子和铜离子都结合两个氢氧根离子,所以反应的氢氧根离子的量是
2 2
0.35mol,则生成的沉淀最大质量为4.35g+0.35mol×17g/mol=10.30g,故答案选B。
故答案选B。
16.(2023上·北京·高三校考模拟)完成下列问题。
(1)将 通入0.5mol/L 溶液中,一段时间后,试管中液面与空气接触部分出现红棕色气体。写出
资料整理【淘宝店铺:向阳百分百】与 反应的离子方程式 。
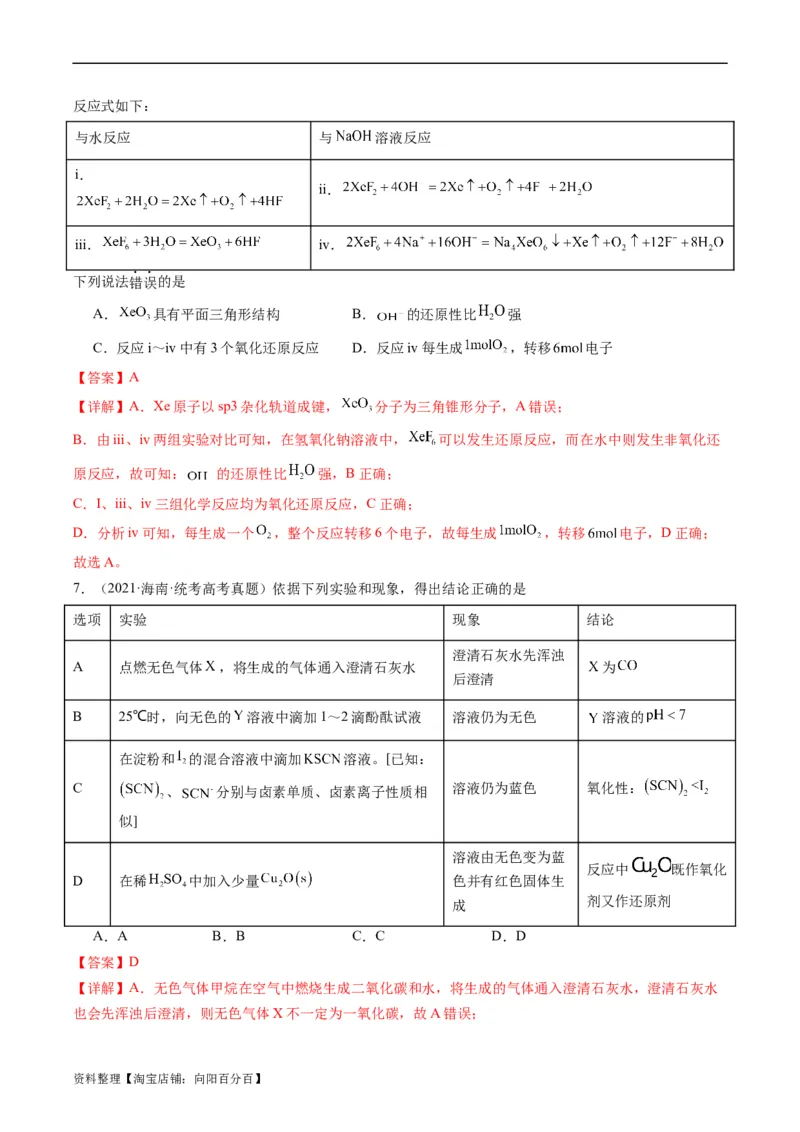
(2)NSR( 的储存和还原在不同时段交替进行)技术可有效降低稀燃柴油和汽油发动机尾气中 的排放,
其工作原理如下图。
储存阶段中Ba存储 后转化为 的化学方程式是 。
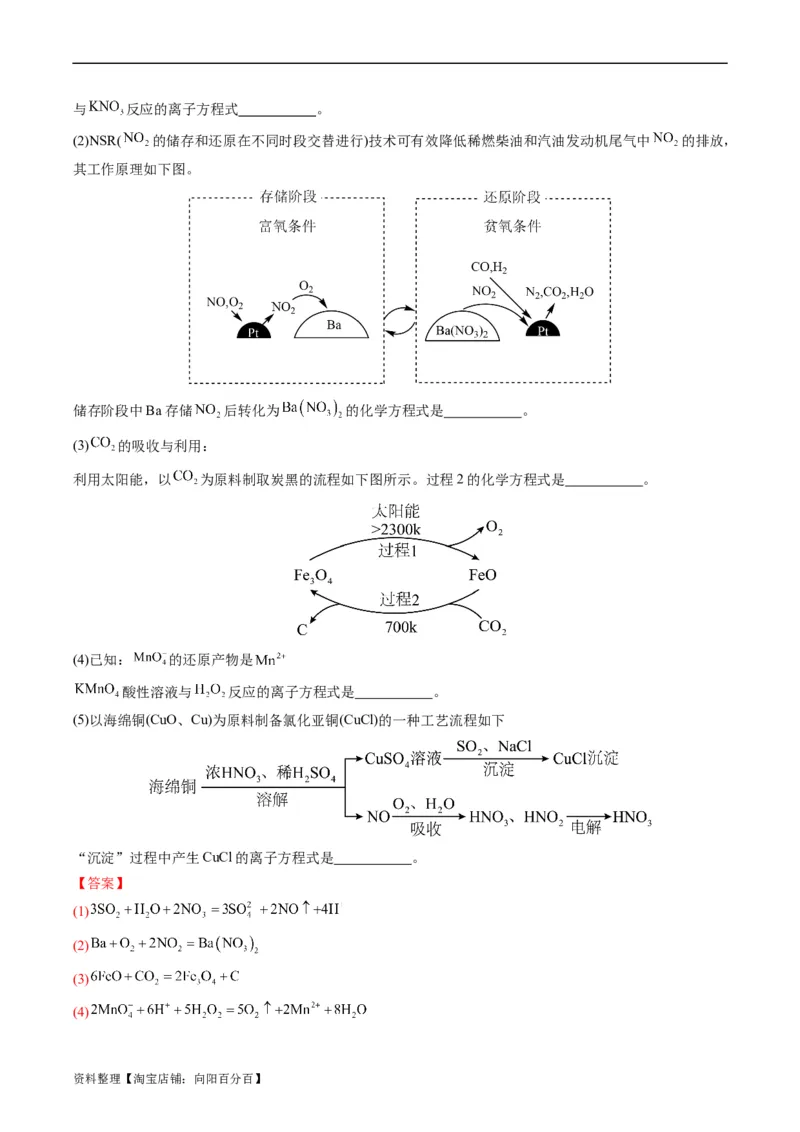
(3) 的吸收与利用:
利用太阳能,以 为原料制取炭黑的流程如下图所示。过程2的化学方程式是 。
(4)已知: 的还原产物是
酸性溶液与 反应的离子方程式是 。
(5)以海绵铜(CuO、Cu)为原料制备氯化亚铜(CuCl)的一种工艺流程如下
“沉淀”过程中产生CuCl的离子方程式是 。
【答案】
(1)
(2)
(3)
(4)
资料整理【淘宝店铺:向阳百分百】(5)
【详解】(1)试管中液面与空气接触部分出现红棕色气体,说明反应过程中生成NO,离子方程式:
;
(2)根据图像可知,储存阶段中Ba存储 后转化为 ,化学方程式:
;
(3)过程2为氧化亚铁与二氧化碳反应生成四氧化三铁和碳单质,根据得失电子守恒,化学方程式:
;
(4) 酸性溶液将 氧化生成氧气,自身被还原生成 ,离子方程式:
;
(5)硫酸铜与二氧化硫发生氧化还原反应生成氯化亚铜,离子方程式:
;
17.(2023上·河南郑州·高三校考模拟)磷化氢(PH )是粮食储备常用的高效熏蒸杀虫剂。
3
(1)A1P遇水发生复分解反应生成PH 气体和 (填化学式)。
3
(2)PH 具有强还原性,能与CuSO 溶液反应,配平该反应的化学方程式:
3 4
CuSO + PH + HO = Cu P↓+ HPO + HSO
4 3 2 3 3 4 2 4
(3)工业制备PH 的原理如图所示:
3
①白磷和烧碱溶液反应的化学方程式为 。
②从分类来看,NaH PO 属于 。
2 2
A.正盐 B.酸式盐 C.强电解质 D.弱电解质
③NaH PO 可将溶液中的Ag+还原为银,从而用于化学镀银。已知利用此原理进行化学镀银时氧化剂与还
2 2
原剂的物质的量之比为4∶1,则氧化产物为 (填化学式)。
【答案】
(1)Al(OH)
3
(2)24CuSO +11PH +12H O = 8Cu P↓+3HPO +24H SO
4 3 2 3 3 4 2 4
(3)P +3NaOH+3HO=PH ↑+3NaHPO AC H PO
4 2 3 2 2 3 4
【详解】(1)AlP遇水蒸气会发生反应放出PH 气体,根据元素守恒,该反应的另一种产物是Al(OH) ;
3 3
(2)PH 与CuSO 溶液反应过程中,Cu的价态由+2→+1,P的价态由-3→+5,根据化合价升降总数相等,
3 4
Cu P与HPO 计量数分别为8、3,则CuSO 的系数是24,HSO 系数是24,根据原子守恒,配平得该反应
3 3 4 4 2 4
的化学方程式:24CuSO +11PH +12H O = 8Cu P↓+3HPO +24H SO ;
4 3 2 3 3 4 2 4
(3)①白磷和烧碱溶液反应生成PH 气体、NaH PO ,P发生歧化反应,一部分由0价降至-3价得到PH
3 2 2 3
气体,另一部分由0价升高至+1价得到NaH PO ,根据化合价升降守恒和原子守恒,反应的化学方程式为:
2 2
资料整理【淘宝店铺:向阳百分百】P+3NaOH+3HO=PH ↑+3NaHPO ;
4 2 3 2 2
②NaH PO 能在碱溶液中存在,说明它是正盐,同时它能在水中完全电离,属于强电解质,所以从分类来
2 2
看,NaH PO 属于正盐、强电解质,选AC;
2 2
③NaH PO 可将溶液中的Ag+还原为银,则氧化剂为Ag+,还原剂为NaH PO ,氧化剂与还原剂的物质的
2 2 2 2
量之比为4∶1,银元素化合价降低一个价态,则P元素化合价升高4个价态,由+1升至+5价,故氧化产
物为HPO 。
3 4
18.(2023上·山西吕梁·高三校考模拟)氧化还原反应在工业生产、环保及科研中有广泛的应用。请根据
以下信息,结合所掌握的化学知识,回答下列问题:
Ⅰ.可以用智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取琪,相关反应如下:
___ ___ ___ ___ ____ (未配平)
(1)配平上述化学方程式,用单线桥标出电子转移的方向和数目。
Ⅱ.钒性能优良,用途广泛,有金属“维生素”之称。
(2) 能与盐酸反应生成 和一种黄绿色气体,该黄绿色气体能与 溶液反应而被吸收,则
、 、 的还原性由强到弱的顺序是 。
(3) 在碳高温还原时,在氮气气氛下氮化还原制备VN,还生成一种具有还原性的气体,则该反应的化
学方程式为 。
【答案】
(1)
(2)
(3)
【详解】(1)根据氧化还原反应中元素化合价升降总数相等进行配平,该反应中碘元素由+5价得电子变
为0价,一个 得5个电子,硫元素由+4价失电子变为+6价,一个 失去2个电子,得失电子
数的最小公倍数是10,所以碘酸钠的化学计量数是2,亚硫酸氢钠的化学计量数是5,其他未变价元素根
据原子守恒进行配平,可得该化学方程式为 ;
(2)根据题意可知 可以将盐酸氧化为 ,该过程中 作还原剂, 为还原产物,所以还原性:
;氯气可以氧化 ,该过程中 作还原剂, 为还原产物,所以还原性: ,
综上所述还原性由强到弱的顺序是 ;
(3)根据题意可知高温条件下 可与 反应生成VN,根据元素守恒,另外一种具有还原性的气
体应是CO,化学方程式为 。
资料整理【淘宝店铺:向阳百分百】资料整理【淘宝店铺:向阳百分百】