文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(新高考七省专用)
黄金卷06
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Cl 35.5 Fe 56
第Ⅰ卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.二十大报告提出科技创新是赢得未来发展主动权的必然选择。下列说法错误的是
A.“天和号”推进器上的氮化硼陶瓷属于有机高分子材料
B.量子通信材料螺旋碳纳米管与石墨烯互为同素异形体
C.“天宫”空间站中太空机械臂的主要成分为铝合金,其强度大于纯铝
D.中国研制的先进微纳米光刻机,其材料之一四甲基氢氧化铵 ,可溶于水
【答案】A
【解析】A.氮化硼陶瓷耐高温,是新型无机非金属材料,故A说法错误;B.同素异形体指由同种元素
组成的具有不同性质的单质,螺旋纳米管与石墨互为同素异形体,故B说法正确;C.合金硬度大于其成
分金属,故C正确;D.四甲基氢氧化铵 属于一元碱,易溶于水,故D说法正确;答案选
A。
2.下列有关化学用语的叙述错误的是
A. 的结构式为
B. 的电子式为
C.简单硫离子的结构示意图为
D.基态N原子的价层电子排布图为
【答案】C
【解析】A.N以三个共价键的形式结合,H有1个共价键,其结构式为 ,A正确;B.C与S之
间以双键结合,共用2对电子,其电子式为 ,B正确;C.硫的核电荷数为16,硫离子为核外电
子得到2个电子,其结构示意图为 ,C错误;D.N价层电子排布式2s2sp3,其价层电子排布图
1
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司为 ,D正确;故答案为:C。
3.物质的性质决定用途,下列两者对应关系正确的是
A.SO 具有杀菌作用,用作葡萄酒中的抗氧化剂
2
B.SiO 具有导电性,用于制造光导纤维
2
C.碳酸氢钠能与碱反应,用作食品的膨松剂
D.Na能与水反应,用作乙醚的除水剂
【答案】D
【解析】A.SO 具有还原性,用作葡萄酒中的抗氧化剂,A错误;B.SiO 没有导电性,B错误;C.碳
2 2
酸氢钠能与酸反应生成CO₂,用作食品的膨松剂,C错误;D.Na能与水反应,用作乙醚的除水剂,D正
确;故选D。
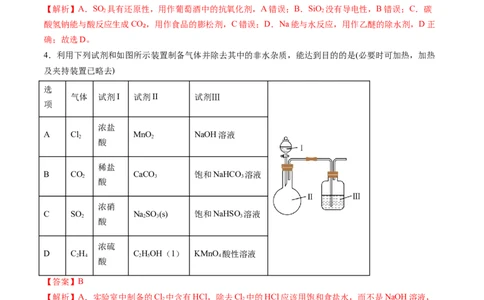
4.利用下列试剂和如图所示装置制备气体并除去其中的非水杂质,能达到目的的是(必要时可加热,加热
及夹持装置已略去)
选
气体 试剂I 试剂II 试剂Ⅲ
项
浓盐
A Cl MnO NaOH溶液
2 2
酸
稀盐
B CO CaCO 饱和NaHCO 溶液
2 3 3
酸
浓硝
C SO NaSO (s) 饱和NaHSO 溶液
2 2 3 3
酸
浓硫
D C H C HOH(1) KMnO 酸性溶液
2 4 2 5 4
酸
【答案】B
【解析】A.实验室中制备的Cl 中含有HCl,除去Cl 中的HCl应该用饱和食盐水,而不是NaOH溶液,
2 2
A不合题意;B.实验室用稀盐酸和CaCO 制备CO,此时CO 中含有少量的杂质HCl,可用饱和NaHCO
3 2 2 3
溶液来除去CO 中的HCl,B符合题意;C.浓硝酸具有强氧化性,能将NaSO 氧化为NaSO ,故不能用
2 2 3 2 4
浓硝酸和NaSO 来制备SO ,而应该用70%H SO 和NaSO 来制备SO ,B不合题意;D.实验室可以将
2 3 2 2 4 2 3 2
浓硫酸和无水乙醇的混合液迅速加热到170℃来制备乙烯,这样制得的乙烯中含有SO 、CO 和乙醇蒸气等
2 2
杂质,由于乙烯也能被酸性高锰酸钾溶液氧化,故不能用酸性高锰酸钾溶液来除杂,应该用NaOH溶液来
除杂,D不合题意;答案选B。
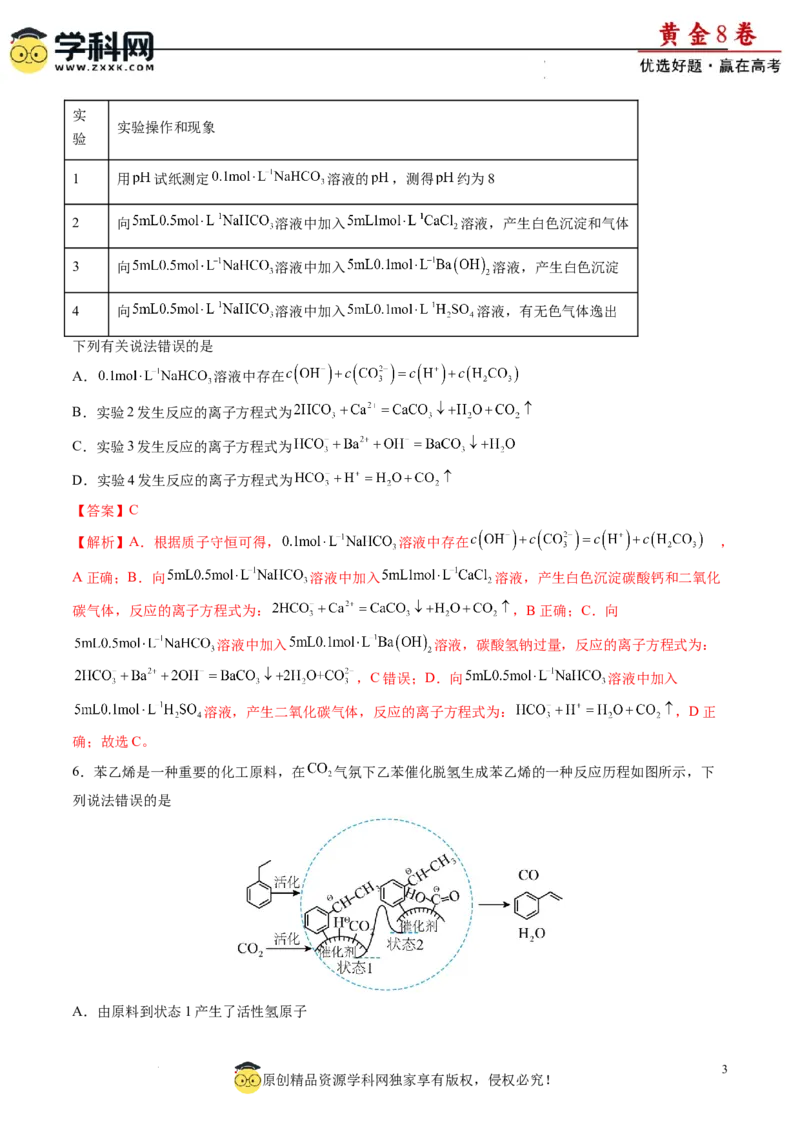
5.常温下,通过下列实验探究 的性质。
2
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司实
实验操作和现象
验
1 用 试纸测定 溶液的 ,测得 约为8
2 向 溶液中加入 溶液,产生白色沉淀和气体
3 向 溶液中加入 溶液,产生白色沉淀
4 向 溶液中加入 溶液,有无色气体逸出
下列有关说法错误的是
A. 溶液中存在
B.实验2发生反应的离子方程式为
C.实验3发生反应的离子方程式为
D.实验4发生反应的离子方程式为
【答案】C
【解析】A.根据质子守恒可得, 溶液中存在 ,
A正确;B.向 溶液中加入 溶液,产生白色沉淀碳酸钙和二氧化
碳气体,反应的离子方程式为: ,B正确;C.向
溶液中加入 溶液,碳酸氢钠过量,反应的离子方程式为:
,C错误;D.向 溶液中加入
溶液,产生二氧化碳气体,反应的离子方程式为: ,D正
确;故选C。
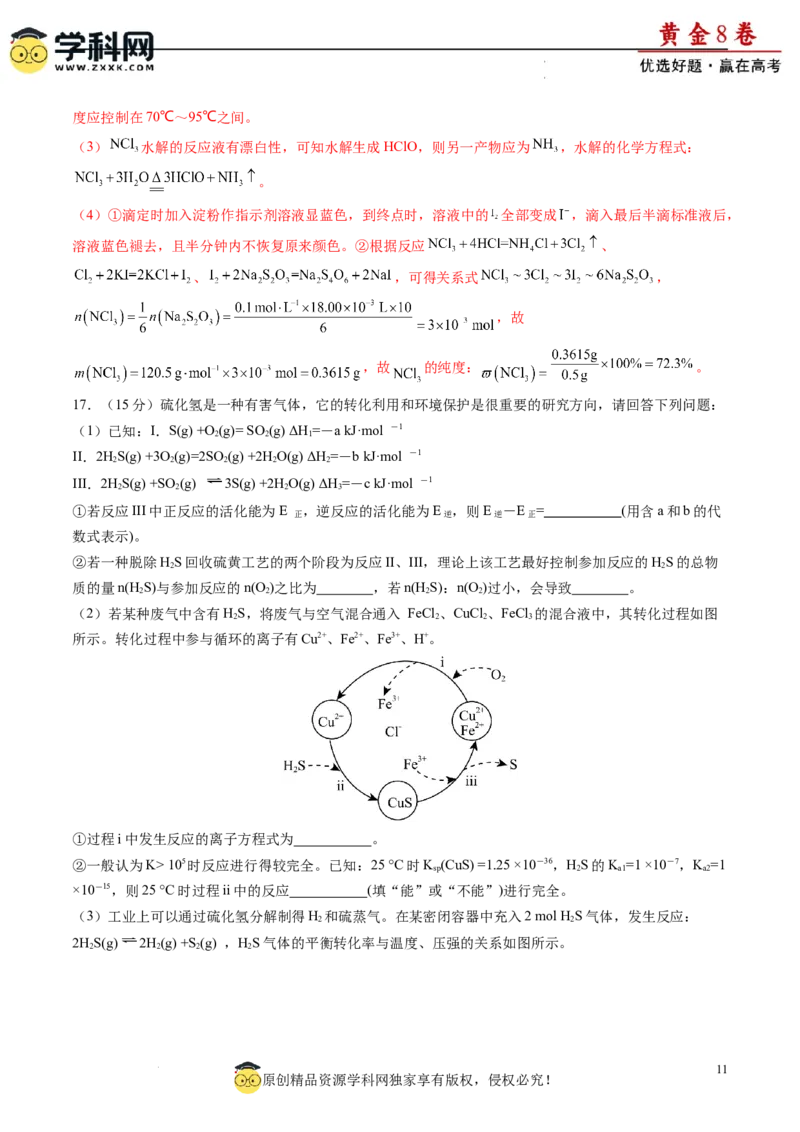
6.苯乙烯是一种重要的化工原料,在 气氛下乙苯催化脱氢生成苯乙烯的一种反应历程如图所示,下
列说法错误的是
A.由原料到状态1产生了活性氢原子
3
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司B.由状态1到状态2有极性键的断裂和形成
C.催化剂可提高苯乙烯选择性,增大苯乙烯的产率
D.由状态2到生成物只有2种元素的化合价发生了变化
【答案】D
【解析】A.观察图可知,由原料到状态1产生了活性氢原子 ,A正确;B.观察可知,状态1到状态2
二氧化碳分子的碳氧双键发生断裂,同时形成了氧氢单键,有极性键的断裂和形成,B正确;C.催化剂
可提高苯乙烯选择性,增大苯乙烯的产率,C正确;D.由状态2到生成物只有C元素的化合价发生了变
化,D错误。故选D。
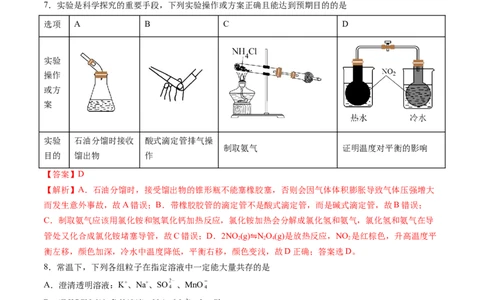
7.实验是科学探究的重要手段,下列实验操作或方案正确且能达到预期目的的是
选项 A B C D
实验
操作
或方
案
实验 石油分馏时接收 酸式滴定管排气操
制取氨气 证明温度对平衡的影响
目的 馏出物 作
【答案】D
【解析】A.石油分馏时,接受馏出物的锥形瓶不能塞橡胶塞,否则会因气体体积膨胀导致气体压强增大
而发生意外事故,故A错误;B.带橡胶胶管的滴定管不是酸式滴定管,而是碱式滴定管,故B错误;
C.制取氨气应该用氯化铵和氢氧化钙加热反应,氯化铵加热会分解成氯化氢和氨气,氯化氢和氨气在导
管处又化合成氯化铵堵塞导管,故C错误;D.2NO (g) NO(g)是放热反应,NO 是红棕色,升高温度平
2 2 4 2
衡左移,颜色加深,冷水中温度降低,平衡右移,颜色变浅,故D正确;答案选D。
⇋
8.常温下,下列各组粒子在指定溶液中一定能大量共存的是
A.澄清透明溶液:K+、Na+、SO 、MnO
B.遇KSCN变红色的溶液:Na+、Mg2+、I-、Cl-
C.pH=0的溶液: 、Fe2+、SO 、ClO-
2
D.通入足量NH 的溶液:K+、Cu2+、SO 、Cl-
3
【答案】A
【解析】A.该溶液因含MnO 而显紫色但澄清透明,且K+、Na+、SO 、MnO 两两之间不发生反应,
能大量共存,A符合题意;B.遇KSCN变红色的溶液中含有 , 能与I-发生氧化还原反应,故不能
大量存在,B不符合题意;C.pH=0的溶液显酸性,含有大量 , 能与ClO-结合生成HClO, 能与
4
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司SO 反应生成S、SO 和水,另外ClO-具有强氧化性,能与Fe2+发生氧化还原反应,故这些离子不能大量
2 2
共存,C不符合题意;D.通入足量NH 的溶液显碱性,Cu2+能结合氨分子生成 ,故不能大
3
量存在,D不符合题意;故选A。
9.科学家合成了一种高温超导材料,其晶胞结构如图所示。下列说法错误的是
A.晶体最简化学式为KCaB C
6 6
B.该晶体属于分子晶体
C.晶体中与Ca最近且等距离的B有12个
D.晶体中C原子的杂化类型为sp3
【答案】B
【解析】A.根据“均摊法”,该晶胞中含K(位于顶点):8× =1、Ca(位于体心):1、B(位于面
上):12× =6、C(位于面上):12× =6,则晶体最简化学式为KCaB C ,A项正确;B.该晶体是一
6 6
种高温超导材料,该晶体不可能属于分子晶体,B项错误;C.由晶胞结构可知,Ca位于体心,B位于面
上,晶体中与Ca最近等距离的B有12个,C项正确;D.C位于面上,结合晶胞结构知,C的价层电子对
数为4,C原子采取sp3杂化,D项正确;答案选B。
10.β﹣生育酚是天然维生素E的一种水解产物,具有较高的生物活性,其结构简式如图。下列有关β﹣生
育酚的说法正确的是
A.1个分子中含有47个氢原子 B.该分子中含有6个甲基
C.环上的一氯代物只有1种 D.能发生取代反应和加成反应
【答案】D
【解析】A.根据β﹣生育酚的结构简式可知,分子中含有48个氢原子,A错误;B.根据β﹣生育酚的结
构简式可知,含有7个甲基,B错误;C.根据β﹣生育酚的结构简式可知,环上含有3种氢原子,则环上
的一氯代物只有3种,C错误;D.结构中具有苯环、酚羟基,苯环能发生加成反应和取代反应,D正确;
故选D。
5
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司11.高效率和高选择性将CO 转化为CH 是CO 资源化利用的途径之一,我国科研工作者开发了一种空腔
2 4 2
串联反应器,为电催化还原CO 提供了一种可行的转化方案,其原理如图所示。设N 为阿伏加德罗常数的
2 A
值,下列说法正确的是
A.22g CO 通入水中得到的溶液中含有HCO 分子数为0.5N
2 2 3 A
B.lmol CH 中所含质子数和中子数均为10N
4 A
C.途径2生成标准状况下22.4L CH ,反应转移电子数为8 N
4 A
D.途径1所得产物物质的量之比为l:1,形成共价键数目为6N
A
【答案】C
【解析】A.由于 是可逆反应,因此22g CO 通入水中得到的溶液中含有HCO 分
2 2 3
子数小于0.5N ,A错误;B.一个CH 分子中含有10个质子,6 个中子,则 lmolCH 中含有 10N 质子和
A 4 4 A
6N 中子,B错误;C.标准状况下 22.4L CH 的物质的量为1 mol,途径2生成CH 的过程中C元素化合
A 4 4
价由+4 价下降到-4价,反应转移电子数为8 ,C正确;D.未说明所得产物物质的量,无法计算形成
共价键数目,D错误;故选C。
12.X、Y、Z、W 是原子序数依次增大的四种短周期元素。基态X、Z原子的电子均填充了3个能级,且
均有2个未成对电子,W的核外电子数是X原子最外层电子数的3倍。下列说法正确的是
A.第一电离能:X<Y<Z
B.元素X的氢化物的沸点一定比元素Y的氢化物低
C.Z与W组成的化合物可作耐高温材料
D.简单离子半径:r(W)>r(Z)>r(Y)
【答案】C
【分析】X、Y、Z、W 是原子序数依次增大的四种短周期元素。基态X、Z原子的电子均填充了3个能级,
且均有2个未成对电子,则X为碳、Z为氧,那么Y为氮;W的核外电子数是X原子最外层电子数的3倍,
W为12号元素镁;
【解析】A.同一周期随着原子序数变大,第一电离能变大,N的2p轨道为半充满稳定状态,第一电离能
大于同周期相邻元素,第一电离能:X<Z<Y,A错误;B.碳可以形成相对分子质量很大的烃,其沸点
可能很高,故元素X的氢化物的沸点不一定比元素Y的氢化物低,B错误;C.Z与W组成的化合物氧化
镁熔点很高,可作耐高温材,C正确;D.电子层数越多半径越大,电子层数相同时,核电荷数越大,半
径越小;简单离子半径:r(Y)>r(Z)>r(W),D错误;故选C。
13.部分含铜物质的分类与相应化合价关系如图所示,下列推断错误的是
6
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司A.f可被还原生成b
B.可存在 的转化关系
C.a可与非金属单质发生化合反应生成
D.往 溶液加入几滴 氨水,得到深蓝色溶液
【答案】D
【分析】由图可知a为铜、b氧化亚铜、c为氧化铜、d为亚铜盐、e为铜盐、f为氢氧化铜。
【解析】A.含有醛基的有机物能与新制的氢氧化铜共热反应生成氧化亚铜,故A正确;B.铜与氧化性
酸反应能生成铜盐,铜盐与碱溶液反应能生成氢氧化铜沉淀,氢氧化铜受热分解为氧化铜,氧化铜和氢气
发生置换反应生成铜,则铜元素及其化合物间存在 的转化关系,故B正确;C.铜能与
硫共热反应生成硫化亚铜,故C正确;D.可溶性铜盐溶液与少量氨水反应只能生成氢氧化铜蓝色沉淀,
不能生成深蓝色的铜氨络离子,故D错误;故选D。
14.铝硫二次电池是一种具有高能量密度、廉价原材料、有前途的替代储能装置,一种铝硫电池如图所示,
M极为表面吸附了硫的活性电极,电解质为 , ( 、 )。下列说法错误的是
A.放电时铝电极的电极反应式为
B.电池放电时的反应原理为
C.离子交换膜为阳离子交换膜
D.充电时,M极为阳极, 被氧化
【答案】D
【分析】图示为铝硫电池,该电池放电时Al失去电子发生氧化反应,为负极,电极反应式为
,M为正极,硫得到电子发生还原反应,电极反应式为 ;
7
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司【解析】A.由分析可知,放电时铝电极的电极反应式为 ,A正确;B.由分析可知,
放电总反应为 , B正确;C.充放电过程中钾离子通过离子交换膜移动,故
离子交换膜为阳离子交换膜,C正确;D.该电池放电时Al为负极、M为正极,则充电时,M极为阳极,
铝极为阴极,阴极的 被还原,D错误;故选D。
第Ⅱ卷
二、非选择题:共4小题,共58分。
15.(14分)钕铁硼废料是一种具有较高经济价值的废弃物,主要成分为稀土元素钕(Nd)、Fe、B.一种
采用分步沉淀从钕铁硼油泥中回收Nd (C O)·10H O和FeC O·2H O的工艺流程如图:
2 2 4 3 2 2 4 2
已知:①200℃下氧化焙烧,钕铁硼废料中钕和铁主要以Nd O 和Fe O 的形式存在,硼常温下稳定,加热
2 3 2 3
至300℃被氧化,不与稀酸反应。
②HCO 易与Fe3+形成多种配合物离子,易与Fe2+形成FeC O·2H O沉淀。
2 4 2 4 2
回答下列问题:
(1)“预处理”是洗去钕铁硼表面的油污,可选择 (填化学式)溶液。
(2)“滤渣1”的主要成分是 (填名称)。“浸出”时,盐酸浓度和固液比对钕、铁的浸出率影
响如图所示,则浸出过程的最佳条件是 。
(3)写出“沉钕”时生成沉淀的离子方程式: 。
(4)“沉铁”时,加入铁粉的作用是 。
(5)FeC O·2H O晶体结构片段如图所示。
2 4 2
其中,Fe2+的配位数为 ;碳原子采用 杂化。现测定草酸亚铁晶体纯度。准确称取
8
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司Wg样品于锥形瓶,加入适量的稀硫酸,用cmol·L-1KMnO 溶液滴定至终点,消耗KMnO 溶液bmL。滴定
4 4
反应: (未配平)。该样品纯度为 %。
【答案】(除标注外,每空2分)(1)NaOH(或热的NaCO)
2 3
(2)硼(1分) 6mol/L的盐酸、固液比为5:1
(3)
(4)将Fe3+还原为Fe2+,与溶液中的草酸根生成FeC O·2H O的沉淀
2 4 2
(5)6 sp2(1分)
【分析】钕铁硼废料预处理后在通入空气在200℃条件下焙烧后,加入稀盐酸浸出,滤渣1主要成分为硼;
滤液1加入草酸溶液沉钕得到Nd (C O)·10H O,滤液2加入铁粉沉铁,得到草酸亚铁晶体;
2 2 4 3 2
【解析】(1)碳酸钠水解呈碱性,油脂在碱性条件下水解,故“预处理”是洗去钕铁硼表面的油污,可
选择NaOH(或热的NaCO)溶液;
2 3
(2)根据已知信息“200℃下氧化焙烧,钕铁硼废料中钕和铁主要以Nd O 和Fe O 形式存在,硼常温下稳
2 3 2 3
定,加热至300℃被氧化,不与稀酸反应”,所以“滤渣1”的主要成分为硼。结合题意,在“浸出”时,
应尽可能地将钕和铁存在于“滤液1”中,即浸出率尽可能大,同时考虑到成本,因此选择6mol·L-1的盐酸、
固液比为5:1的条件进行浸出;
(3)根据流程图可知,“沉钕”过程用草酸将Nd3+转化为难溶的Nd (C O)·10H O;
2 2 4 3 2
(4)根据已知信息“HC O 易与Fe3+形成多种配合物离子,易与Fe2+形成FeC O·2H O沉淀”,结合题意,
2 2 4 2 4 2
需将铁元素转化成Fe2+,与溶液中的草酸根生成FeC O·2H O的沉淀;
2 4 2
(5)根据FeC O·2H O晶体结构片段,可知Fe2+与6个O原子形成配位键,配位数为6;FeC O·2H O晶
2 4 2 2 4 2
体中有碳氧双键,碳原子杂化类型为sp2.根据质量守恒和电荷守恒配平离子方程式,
,故
,故样品纯度为
。
16.(14分)三氯化氮是一种黄色油状液体,可用于漂白和杀菌。已知: 熔点为-40℃,沸点为
70℃,95℃以上易爆炸。在弱酸性溶液中稳定,在热水中易水解,遇碱则迅速反应。在实验室可用 和
溶液反应制取 ,所用仪器如图所示(忽略部分夹持装置):
9
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司回答下列问题:
(1)盛装浓盐酸的仪器名称为 ;药品X可为 ;根据气流方向,各仪器的连接顺
序为 (用各接口字母表示,各接口所需橡胶塞已省略)。
(2)待反应至油状液体不再增加,用止水夹夹住ab间的橡胶管,控制水浴加热的温度范围为 ,
将产品 蒸出。
(3) 水解的反应液有漂白性,写出 水解的化学方程式: 。
(4) 纯度测定: 的制取是可逆反应,根据反应 ,利用间接碘量法
测定氯气的量即可测定 的纯度。
实验步骤:
ⅰ.准确称量C中的产物0.5g置于三颈烧瓶中,加入10mL足量浓盐酸,使用磁力搅拌器搅拌,并鼓入氮气;
ⅱ.将混合气通入200mL 0.1 KI溶液中,待试管中无色液体变成黄色且颜色不再变化,关闭氮气(溶
液体积变化忽略不计);ⅲ.量取20.00mL吸收液,加入淀粉指示剂,用0.1 标准液进行滴
定,滴定至终点时消耗 溶液18.00mL。(已知:反应原理为 )
①确定滴定终点的现象为 。
② 的纯度为 。
【答案】(每空2分)(1)恒压滴液漏斗 [ 、 ,答其中一个均可得分]
a→b→c→f→g→d→e
(2)
(3)
(4)滴入最后半滴标准液后,溶液中蓝色褪去且半分钟内不恢复原色 72.3%
【分析】在实验室利用多种方式制取 和 溶液反应制取 ,并蒸馏、冷凝得到NCl ,并避免空
3
气中的水蒸气接触产品,需要干燥装置连接在最右边。
【解析】(1)装置A中使用恒压滴液漏斗,利用装置A制取氯气,在不加热条件下,利用浓盐酸和强氧
化剂可制取氯气,故 、 、 均可;利用装置B制取 ,利用装置D冷凝 ,
用装置C收集 ,故正确连接顺序为a→b→c→f→g→d→e。
(2)由题给信息可知,实验时,为保证三氯化氮顺利蒸出,同时防止三氯化氮发生爆炸,水浴加热的温
10
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司度应控制在70℃~95℃之间。
(3) 水解的反应液有漂白性,可知水解生成HClO,则另一产物应为 ,水解的化学方程式:
。
(4)①滴定时加入淀粉作指示剂溶液显蓝色,到终点时,溶液中的 全部变成 ,滴入最后半滴标准液后,
溶液蓝色褪去,且半分钟内不恢复原来颜色。②根据反应 、
、 ,可得关系式 ,
,故
,故 的纯度: 。
17.(15分)硫化氢是一种有害气体,它的转化利用和环境保护是很重要的研究方向,请回答下列问题:
(1)已知:I.S(g) +O (g)= SO (g) ΔH =-a kJ·mol -1
2 2 1
II.2HS(g) +3O (g)=2SO(g) +2H O(g) ΔH=-b kJ·mol -1
2 2 2 2 2
III.2HS(g) +SO (g) 3S(g) +2H O(g) ΔH=-c kJ·mol -1
2 2 2 3
①若反应III中正反应的活化能为E ,逆反应的活化能为E ,则E -E = (用含a和b的代
正 逆 逆 正
数式表示)。
②若一种脱除HS回收硫黄工艺的两个阶段为反应II、III,理论上该工艺最好控制参加反应的HS的总物
2 2
质的量n(H S)与参加反应的n(O )之比为 ,若n(H S):n(O )过小,会导致 。
2 2 2 2
(2)若某种废气中含有HS,将废气与空气混合通入 FeCl 、CuCl 、FeCl 的混合液中,其转化过程如图
2 2 2 3
所示。转化过程中参与循环的离子有Cu2+、Fe2+、Fe3+、H+。
①过程i中发生反应的离子方程式为 。
②一般认为K> 105时反应进行得较完全。已知:25 °C时K (CuS) =1.25 ×10-36,HS的K =1 ×10-7,K =1
sp 2 a1 a2
×10-15,则25 °C时过程ii中的反应 (填“能”或“不能”)进行完全。
(3)工业上可以通过硫化氢分解制得H 和硫蒸气。在某密闭容器中充入2 mol H S气体,发生反应:
2 2
2HS(g) 2H(g) +S (g) ,HS气体的平衡转化率与温度、压强的关系如图所示。
2 2 2 2
11
原创精品资源学科网独家享有版权,侵权必究!
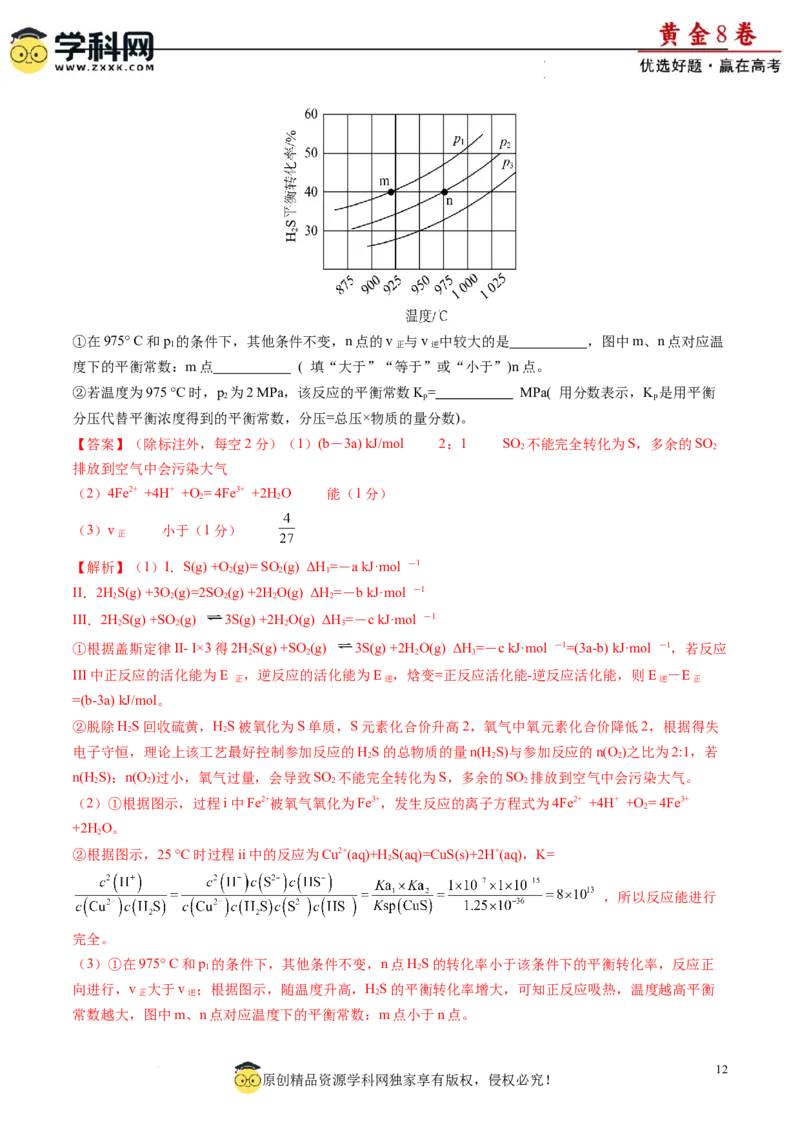
学学科科网网((北北京京))股股份份有有限限公公司司①在975° C和p 的条件下,其他条件不变,n点的v 与v 中较大的是 ,图中m、n点对应温
1 正 逆
度下的平衡常数:m点 ( 填“大于”“等于”或“小于”)n点。
②若温度为975 °C时,p 为2 MPa,该反应的平衡常数K= MPa( 用分数表示,K 是用平衡
2 p p
分压代替平衡浓度得到的平衡常数,分压=总压×物质的量分数)。
【答案】(除标注外,每空2分)(1)(b-3a) kJ/mol 2:1 SO 不能完全转化为S,多余的SO
2 2
排放到空气中会污染大气
(2)4Fe2+ +4H+ +O = 4Fe3+ +2H O 能(1分)
2 2
(3)v 小于(1分)
正
【解析】(1)I.S(g) +O (g)= SO (g) ΔH=-a kJ·mol -1
2 2 1
II.2HS(g) +3O (g)=2SO(g) +2H O(g) ΔH=-b kJ·mol -1
2 2 2 2 2
III.2HS(g) +SO (g) 3S(g) +2H O(g) ΔH=-c kJ·mol -1
2 2 2 3
①根据盖斯定律II- I×3得2HS(g) +SO (g) 3S(g) +2H O(g) ΔH=-c kJ·mol -1=(3a-b) kJ·mol -1,若反应
2 2 2 3
III中正反应的活化能为E ,逆反应的活化能为E ,焓变=正反应活化能-逆反应活化能,则E -E
正 逆 逆 正
=(b-3a) kJ/mol。
②脱除HS回收硫黄,HS被氧化为S单质,S元素化合价升高2,氧气中氧元素化合价降低2,根据得失
2 2
电子守恒,理论上该工艺最好控制参加反应的HS的总物质的量n(H S)与参加反应的n(O )之比为2:1,若
2 2 2
n(H S):n(O )过小,氧气过量,会导致SO 不能完全转化为S,多余的SO 排放到空气中会污染大气。
2 2 2 2
(2)①根据图示,过程i中Fe2+被氧气氧化为Fe3+,发生反应的离子方程式为4Fe2+ +4H+ +O = 4Fe3+
2
+2H O。
2
②根据图示,25 °C时过程ii中的反应为Cu2+(aq)+H S(aq)=CuS(s)+2H+(aq),K=
2
,所以反应能进行
完全。
(3)①在975° C和p 的条件下,其他条件不变,n点HS的转化率小于该条件下的平衡转化率,反应正
1 2
向进行,v 大于v ;根据图示,随温度升高,HS的平衡转化率增大,可知正反应吸热,温度越高平衡
正 逆 2
常数越大,图中m、n点对应温度下的平衡常数:m点小于n点。
12
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司②若温度为975 °C时,p 为2 MPa,HS的平衡转化率为40%,则平衡体系中HS的物质的量为1.2mol、
2 2 2
氢气的物质的量为0.8mol、S 的物质的量为0.4mol,该反应的平衡常数K=
2 p
MPa。
18.(15分)茉莉花香气的成分有多种,乙酸苯甲酯( )是其中的一种,它可以从茉
莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如图:
(1)写出反应①的化学方程式: 。
(2)写出③的反应类型为 ;B中官能团名称为 。
(3)C的结构简式为 。
(4)在①②③三个反应中,原子的理论利用率为100%,符合绿色化学的要求的反应
是 (填序号)。
(5)写出③的化学方程式: 。
(6)与乙酸苯甲酯具有相同官能团且能发生银镜反应的同分异构体(属于芳香族化合物)共有
种,其中核磁共振氢谱中吸收峰面积比为1∶1∶2∶6的结构简式为 。
【答案】(除标注外,每空2分)(1)2CHCHOH+O 2CHCHO+2H O
3 2 2 3 2
(2)酯化反应(或取代反应) 羧基(1分)
(3)
(4)②
(5)CHCOOH+ +H O
3 2
(6)14
【分析】分析路线图可知,乙醇发生催化氧化反应生成乙醛,A为乙醛,乙醛发生氧化反应生成乙酸,B
为乙酸;卤代烃水解反应生成醇,C为苯甲醇,苯甲醇和乙酸发生酯化反应生成乙酸苯甲酯,据此分析解
答。
13
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司【解析】(1)根据分析可知,反应①的化学方程式为2CHCHOH+O 2CHCHO+2H O;
3 2 2 3 2
(2)根据分析可知,反应③为苯甲醇和乙酸发生酯化反应,B为乙酸,官能团为羧基;
(3)C为苯甲醇,结构简式为: ;
(4)在①②③三个反应中,反应①产物为乙醇和水,反应②产物为乙酸,反应③产物为乙酸苯甲酯和水,
故原子的理论利用率为100%,符合绿色化学的要求的反应是②;
(5)反应③为苯甲醇和乙酸发生酯化反应生成乙酸苯甲酯,反应方程式为:CHCOOH+
3
+H O;
2
(6)根据题中限定条件,必须含有酯基,苯环上若含一个支链则为CHCHCOO-,有1种情况;若含
3 2
HCOO-和-CHCH 两个支链,在苯环上有邻、间、对位3种情况;若苯环上含有HCOO-、-CH 和-CH 三
2 3 3 3
个支链,有10种情况,综上符合限定条件的同分异构体共有14种;其中核磁共振氢谱中吸收峰面积之比
为1:1:2:6的结构简式中含2个-CH,且处于间位,即该同分异构体为 。
3
14
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司15
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限限公公司司