文档内容
第二章 分子结构与性质
第三节 分子结构与物质性质
2.3.2分子间的作用力 分子的手性
1.认识分子间存在相互作用,知道范德华力和氢键是两种常见的分子间作用力。
2.了解分子内氢键和分子内氢键在自然界中的广泛存在及重要作用。
3.掌握物质的溶解性与分子结构的关系,了解“相似相溶”规律。
4.结合实例初步认识分子的手性对其性质的影响。
教学重点:范德华力、氢键对物质性质的影响,物质的溶解性与分子结构的关系
教学难点:范德华力、氢键对物质性质的影响
一、范德华力及其对物质性质的影响
1.范德华力的概念
降温加压时气体会液化,降温时液体会凝固,这些事实表明,分子之间存在着相互作用力。范德华
(van der Waals)是最早研究 的科学家,因而把这类分子间作用力称为范
德华力。
【学生活动1】
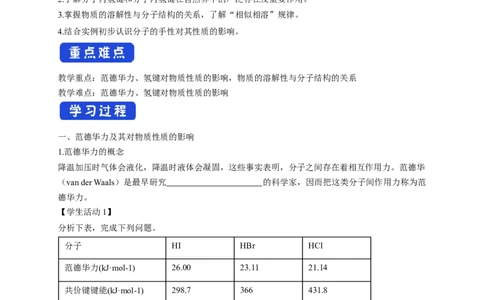
分析下表,完成下列问题。
分子 HI HBr HCl
范德华力(kJ·mol-1) 26.00 23.11 21.14
共价键键能(kJ·mol-1) 298.7 366 431.8
2.范德华力的特征
(1) 范德华力广泛存在于 ,但只有分子间 时才有分子间的相互作
用力。
(2) 范德华力不是化学键,范德华力很 ,比化学键的键能小1~2个数量级。
(3) 范德华力没有 性和 性。
【学生活动2】
(1).HCl、HBr、HI三种分子构成的物质的相对分子质量与范德华力大小的关系
分子 HI HBr HCl相对分子质量 128 81 36.5
范德华力(kJ·mol-1) 26.00 23.11 21.14
(2).CO、N 的相对分子质量、分子的极性、范德华力的关系
2
分子 相对分子质量 分子的极性 范德华力(kJ·mol-1)
CO 28 极性 8.75
N 28 非极性 8.50
2
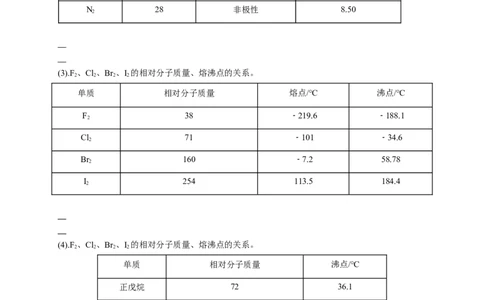
(3).F、Cl、Br 、I 的相对分子质量、熔沸点的关系。
2 2 2 2
单质 相对分子质量 熔点/℃ 沸点/℃
F 38 ﹣219.6 ﹣188.1
2
Cl 71 ﹣101 ﹣34.6
2
Br 160 ﹣7.2 58.78
2
I 254 113.5 184.4
2
(4).F、Cl、Br 、I 的相对分子质量、熔沸点的关系。
2 2 2 2
单质 相对分子质量 沸点/℃
正戊烷 72 36.1
异戊烷 72 28
新戊烷 72 10
【知识建构】
影响范德华力的因素有哪些呢?二、氢键及其对物质性质的影响
1.氢键的概念
已经与电负性很大的原子形成共价键的氢原子与另一个电负性很大的原子之间的作用力。当氢原子
与 的X原子以 结合时,它们之间的共用电子对强烈地偏向 ,使H
几乎成为“裸露”的质子,这样相对显正电性的H与另一分子中相对显负电性的X(或Y)中的
接近并产生相互作用,这种相互作用称氢键。
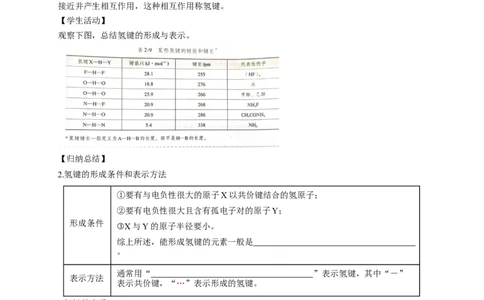
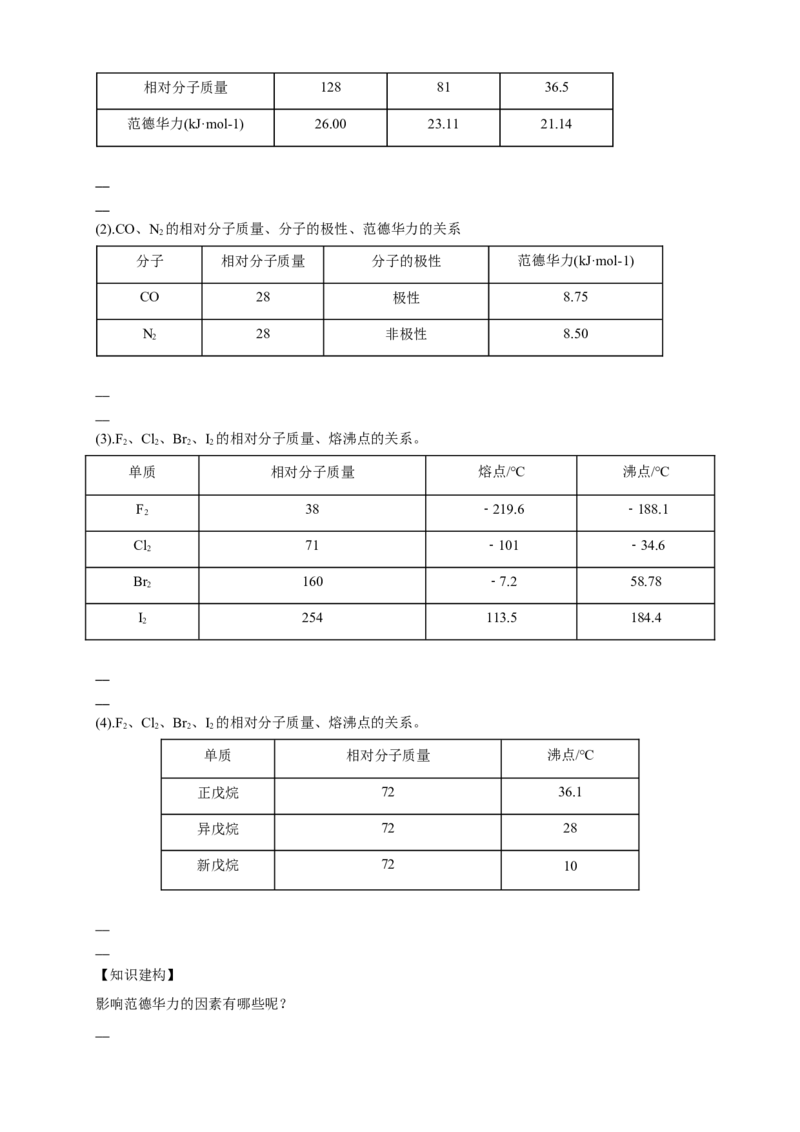
【学生活动】
观察下图,总结氢键的形成与表示。
【归纳总结】
2.氢键的形成条件和表示方法
①要有与电负性很大的原子X以共价键结合的氢原子;
②要有电负性很大且含有孤电子对的原子Y;
形成条件
③X与Y的原子半径要小。
综上所述,能形成氢键的元素一般是
。
通常用“ ”表示氢键,其中“-”
表示方法
表示共价键,“…”表示形成的氢键。
3.氢键的本质
是 作用力,它比化学键的键能小1~2个数量级。是一种比范德华力 的分子间作用
力。
4.氢键的特征
氢键既有 (X-H…Y尽可能在同一条直线上),又有 (一个X-H只能和一个Y原子
结合)5.氢键的类型: 和
【学生活动】
1.对比对羟基苯甲醛、邻羟基苯甲醛的结构,分析对羟基苯甲醛的熔、沸点高于邻羟基苯甲酸的
熔、沸点的原因。
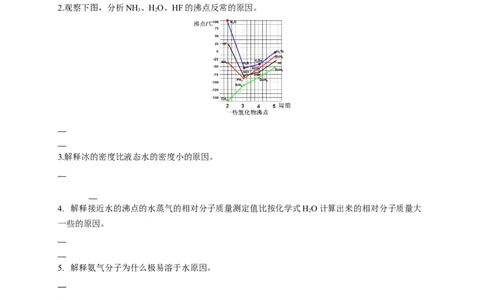
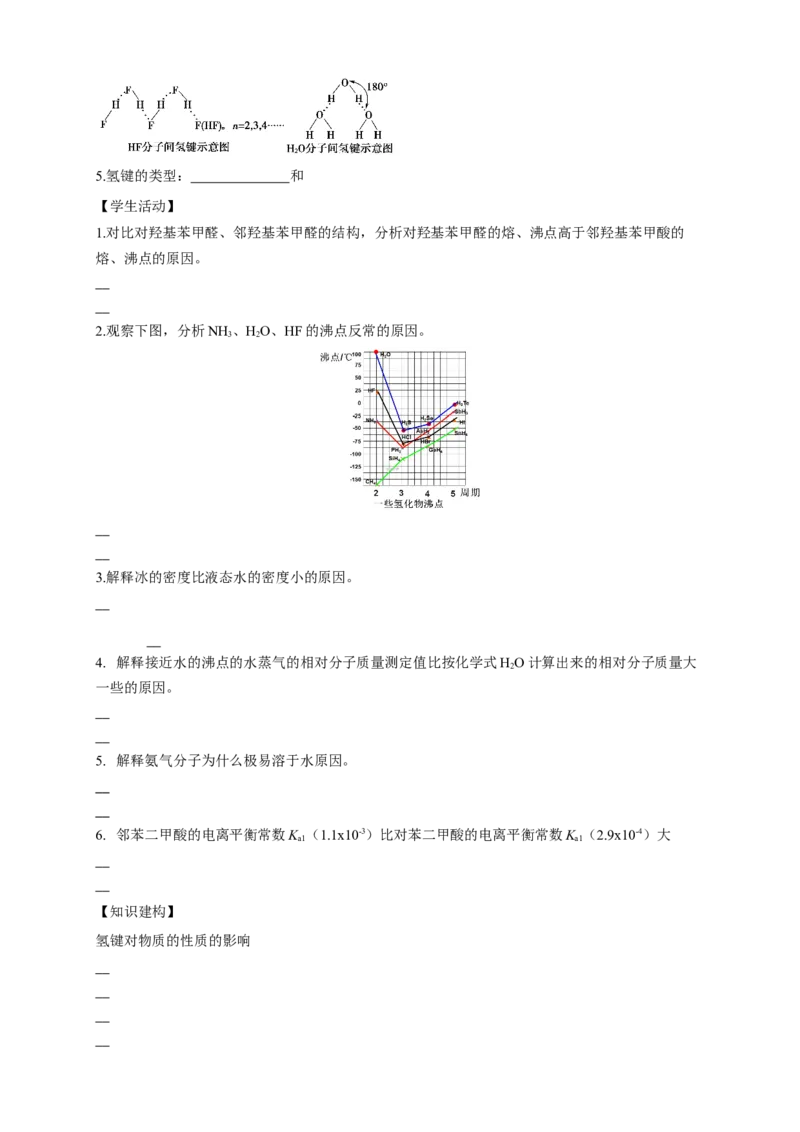
2.观察下图,分析NH 、HO、HF的沸点反常的原因。
3 2
3.解释冰的密度比液态水的密度小的原因。
4. 解释接近水的沸点的水蒸气的相对分子质量测定值比按化学式HO计算出来的相对分子质量大
2
一些的原因。
5. 解释氨气分子为什么极易溶于水原因。
6. 邻苯二甲酸的电离平衡常数K (1.1x10-3)比对苯二甲酸的电离平衡常数K (2.9x10-4)大
a1 a1
【知识建构】
氢键对物质的性质的影响三、溶解性
1.“相似相溶”规律
非极性溶质一般能溶于 ,极性溶质一般能溶于 。
【学生活动】
(1) 蔗糖和氨易溶于水,难溶于四氯化碳;而萘和碘却易溶于四氯化碳,难溶于水。分析原因。
(2) 比较NH 和CH 在水中的溶解度。怎样用“相似相溶”规律理解它们的溶解度不同?
3 4
(3) 为什么在日常生活中用有机溶剂(如乙酸乙酯等)溶解油漆而不用水?
(4) 在一个小试管里放入一小粒碘晶体,加入约5 mL蒸馏水,观察
碘在水中的溶解性(若有不溶的碘,可将碘水溶液倾倒在另一个试管
里继续下面的实验)。在碘水溶液中加入约1 mL四氯化碳(CCl),振
4
荡试管,观察碘被四氯化碳萃取,形成紫红色的碘的四氯化碳溶液。
再向试管里加入1 mL浓碘化钾(KI)水溶液,振荡试管,溶液紫色变
浅,这是由于在水溶液里可发生如下反应:I +I-=I -。实验表明碘在纯
2 3
水还是在四氯化碳中溶解性较好?为什么?
(5)利用相似相溶原理解释下表数据。
(6)乙醇、戊醇都是极性分子,为什么乙醇可以与水任意比例互溶,而戊醇的溶解度小?
【知识建构】2.影响溶解度的因素
四、分子的手性
1.手性异构体:具有完全相同的 和 的一对分子,如同左手和右手一样互为
却在三维空间里不能 ,互称手性异构体。
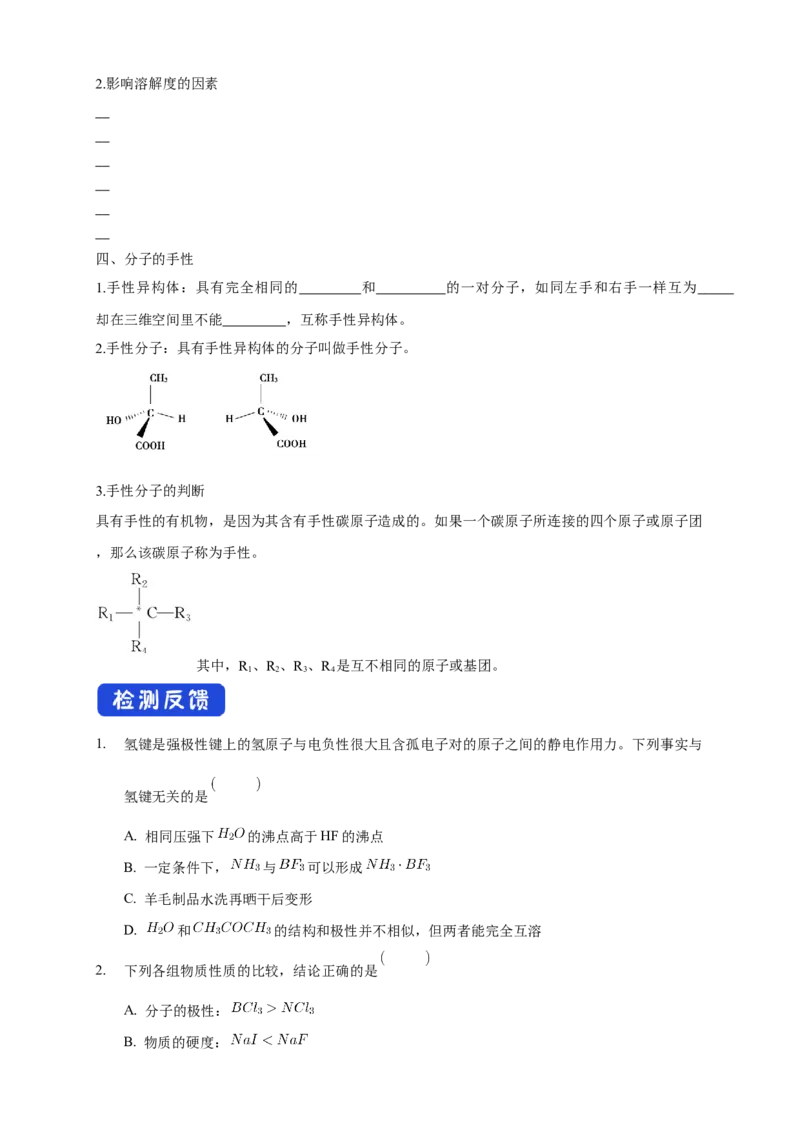
2.手性分子:具有手性异构体的分子叫做手性分子。
3.手性分子的判断
具有手性的有机物,是因为其含有手性碳原子造成的。如果一个碳原子所连接的四个原子或原子团
,那么该碳原子称为手性。
其中,R 、R 、R 、R 是互不相同的原子或基团。
1 2 3 4
1. 氢键是强极性键上的氢原子与电负性很大且含孤电子对的原子之间的静电作用力。下列事实与
氢键无关的是
A. 相同压强下 的沸点高于HF的沸点
B. 一定条件下, 与 可以形成
C. 羊毛制品水洗再晒干后变形
D. 和 的结构和极性并不相似,但两者能完全互溶
2. 下列各组物质性质的比较,结论正确的是
A. 分子的极性:
B. 物质的硬度:C. 酸性:
D. 在 中的溶解度:
3. 四组都是同一族元素所形成的不同物质,它们在101kPa时的沸点 如下表所示:
第一组 甲 乙 丙 丁
第二组
第三组 HF HCl HBr HI
第四组
下列各项判断正确的是
A. 第四组物质中 的沸点最高,是因为 中化学键键能最大
B. 第三组与第四组相比较,化合物的热稳定性:
C. 第三组物质溶于水后,同浓度溶液的酸性:
D. 第一组物质是分子晶体,一定含有共价键
4. 下列有关叙述及相关解释均正确的是
选项 叙述 解释
A 键的极性的强弱: 电负性:
B 石墨的熔点高于金刚石 碳碳键的键长:石墨 金刚石
熔点: Ⅰ形成分子内氢键,Ⅱ形成分子间氢
C
键
Ⅰ Ⅱ
HI、HBr、HCl中的范德华力逐渐减
D 酸性:
小
A. A B. B C. C D. D
5. 下列物质的性质与氢键无关的是
A. 分子比 分子稳定 B. 通常情况 极易溶于水
C. 氨易液化 D. 的沸点比 的沸点高