文档内容
第三章 晶体结构与性质
第二节 金属晶体与离子晶体
第二课时 离子晶体 过渡晶体与混合型晶体
1. 借助离子晶体等模型认识晶体的结构特点。
2. 认识离子晶体的物理性质与晶体结构的关系。
3. 知道介于典型晶体之间的过渡晶体及混合型晶体是普通存在的。
教学重点:离子晶体、过渡晶体、混合型晶体的结构特点和性质
教学难点:离子晶体、过渡晶体、混合型晶体的结构特点和性质
一、离子晶体
1.离子晶体
(1)定义:由 和 相互作用而形成的晶体。
(2)成键粒子:
(3)相互作用:阴、阳离子间以 结合
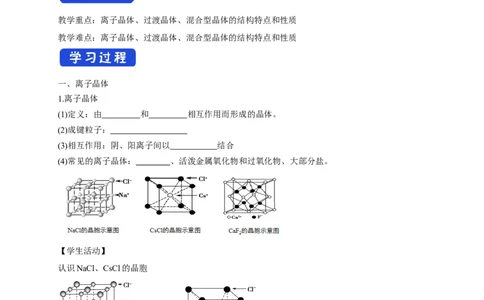
(4)常见的离子晶体: 、活泼金属氧化物和过氧化物、大部分盐。
【学生活动】
认识NaCl、CsCl的晶胞
晶体类型 NaCl CsCl
晶胞
阳离子的配位数阴离子的配位数
晶胞中所含离子数
【学生活动】
1. 为什么NaCl和CsCl的硬度大、熔沸点高?
2. NaCl的熔点比CsCl的高?
2.离子晶体的物理性质
具有较 的熔、沸点, 挥发,硬度 ,不导电,易溶于极性溶剂,难溶于非极
性溶剂。
(1)具有较高的熔、沸点,难挥发
离子晶体中,阴、阳离子间有强烈的相互作用(离子键),要克服离子间的相互作用使物质熔化和
沸腾,就需要较多的能量。因此,离子晶体具有 和 的性质。
,离子半径越 ,离子键越 , 离子晶
一般说来,阴、阳离子的电荷数越
体的熔、沸点越 。
(2)硬度
离子晶体的硬度较大,难于压缩。阴阳离子间有较强的离子键,使离子晶体的硬度较大,当晶体受
到冲击力作用时,部分离子键发生断裂,导致晶体破碎。
(3)导电性
离子晶体中,离子键较强,离子不能自由移动,即晶体中无自由移动的离子,因此,离子晶体
。当升高温度时,阴、阳离子获得足够能量克服离子间的相互作用,成为自由移动的离子,在外界
电场作用下,离子定向移动而形成电流。离子化合物 时,阴、阳离子受到水分子作用变成
了自由移动的离子(实质上是水合离子),在外界电场作用下,阴、阳离子定向移动而导电。
(4)溶解性
大多数离子晶体易溶于极性溶剂(如水),难溶于非极性溶剂(如汽油、苯等),遵循“
”规律。当把离子晶体放入水中时,极性水分子对离子晶体中的离子产生吸引作用,使晶体中的离子克服了离子间的作用而电离,变成在水中自由移动的离子。
【学生活动】
分析第三周期前几种元素的氧化物中,化学键中离子键成分的百分数的变化趋势并解释其原因。进
一步描述第三周期主族元素的氧化物的晶体类型的变化趋势。
氧化物 NaO MgO Al O SiO
2 2 3 2
离子键的百分数/% 62 50 41 33
二、过渡晶体与混合型晶体
1.过渡晶体
(1)四类典型晶体
(2)过渡晶体的概念
离子键、共价键、金属键等都是化学键的典型模型,但是,原子间形成的化学键往往是介于典型模
型之间的 ,由于微粒间的作用存在键型过渡,即使组成简单的的晶体,也可能介于离子
晶体、共价晶体、分子晶体和金属晶体之间的过渡状态,形成过渡晶体。
2.混合型晶体
(1)混合型晶体的概念
既有 又有 ,同时还存在类似金属键的作用力,兼具共价晶体、分子晶体、
金属晶体特征的晶体,称为混合型晶体。
(2)石墨的结构模型石墨结构中未参与杂化的p轨道
①结构特点——层状结构
a. 石墨晶体是层状结构的,同层内碳原子采取 杂化,以 结合,形成
结构,层内的碳原子的核间距为142 pm,层间距离为335 pm, 层与层之间靠
维系。
③石墨的二维结构内,每个碳原子的配位数为 ,有一个未参与杂化的2p电子,它的原子轨
道垂直于碳原子平面。
④由于所有的p轨道相互平行而且 ,使p轨道中的电子可在整个碳原子平面中运动。因
此,石墨有类似金属晶体的 ,而且,由于相邻碳原子平面之间相隔较远,电子不能从一个
平面跳跃到另-一个平面,所以石墨的导电性只能沿石墨平面的方向。
②晶体类型:石墨晶体中,既有 ,又有 和 ,属于 。
③性质:熔点很 、质软、易 等
【学生活动】
(1)金属阳离子的晶体一定是离子晶体吗?有阳离子的晶体中一定存在阴离子吗?
(2)离子晶体中一定含有金属元素吗?由金属元素和非金属元素组成的晶体一定是离子晶体吗?
(3)离子晶体的熔点一定低于共价晶体吗?
(4)离子晶体中除含有离子键外,是否含有共价键?
(5)比较四种晶体的结构和性质。
类型
分子晶体 原子晶体 金属晶体 离子晶体
比较
构成粒子
粒子间的
相互作用力硬度
熔、沸点
溶解性
导电、
传热性
1. 下列关于晶体的说法正确的组合是
分子晶体中都存在共价键
在晶体中只要有阳离子就一定有阴离子
金刚石、SiC、NaF、NaCl、 、 晶体的熔点依次降低
离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
晶格能由大到小顺序:
晶体中每个硅原子与两个氧原子以共价键相结合
分子晶体中分子间作用力越大,分子越稳定
A. B. C. D.
2. 下列关于化学键的说法正确的是
是一种非常稳定的化合物,这是因为分子间存在氢键
熔化破坏了离子键
、 熔点后者高是因为前者克服分子间作用力后者熔化破坏共价键
活泼金属与非金属化合时,一定能形成离子键
离子化合物中可能同时含有离子键和共价键
由非金属元素形成的化合物一定不是离子化合物
单质分子中一定含非极性键
A. B. C. D.
3. 下表所列有关晶体的说法中,有错误的是选项 A B C D
晶体名称 碘化钾 铜 石墨 碘
金属阳离子
组成晶体微粒名称 阴、阳离子 原子 分子
自由电子
范德华力
晶体内存在的作用力 离子键 金属键 共价键
共价键
A. A B. B C. C D. D
4. 已知某离子晶体的晶胞结构如图所示,其摩尔质量为
,阿伏加德罗常数的值为 ,晶体的密度为 。则下列
说法正确的是
A. 晶胞中阴、阳离子的个数都为1
B. 该晶体中两个距离最近的同种离子的核间距为
C. 阴、阳离子的配位数都是4
D. 该晶胞可能是NaCl晶体的晶胞
5. 下列有关性质的比较,正确的是
硬度:
水溶性:
沸点:
晶格能:
分子或离子中键角: ,
熔点:
沸点:
熔点:金刚石 生铁 纯铁 钠
熔点:二氧化硅 冰
A. B. C. D.