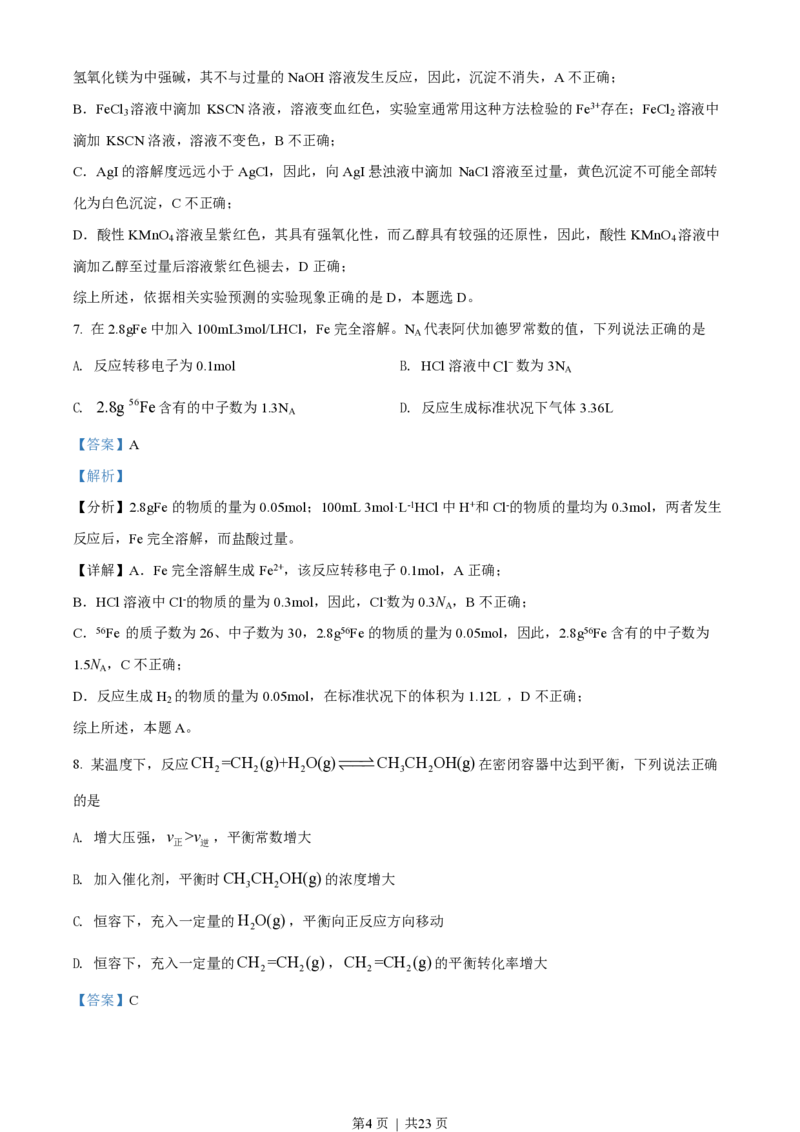文档内容
海南省 2022 年普通高中学业水平选择性考试
化学试题
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号,回答非选择题时,将答案写在答题卡上,写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 P 31 Fe 56
一、选择题:本题共 8小题,每小题 2分,共 16 分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 化学与日常生活息息相关。下列说法错误的是
A. 使用含氟牙膏能预防龋齿 B. 小苏打的主要成分是Na CO
2 3
C. 可用食醋除去水垢中的碳酸钙 D. 使用食品添加剂不应降低食品本身营养价值
【答案】B
【解析】
【详解】A.人体缺氟会导致龋齿,因此使用含氟牙膏可预防龋齿,A正确;
B.小苏打的主要成分是NaHCO ,B错误;
3
C.食醋的主要成分为CH COOH,可与碳酸钙反应生成可溶的醋酸钙、二氧化碳和水,因此食醋可除去
3
水垢中的碳酸钙,C正确;
D.食品添加剂加入到食品中的目的是为改善食品品质和色、香、味以及为防腐、保鲜和加工工艺的需
要,所以合理使用有助于改善食品品质、丰富食品营养成分,不应降低食品本身营养价值,D正确;
答案选B。
2. 《医学入门》中记载我国传统中医提纯铜绿的方法:“水洗净,细研水飞,去石澄清,慢火熬干,”其中
未涉及的操作是
A. 洗涤 B. 粉碎 C. 萃取 D. 蒸发
【答案】C
【解析】
【详解】水洗净是指洗去固体表面的可溶性污渍、泥沙等,涉及的操作方法是洗涤;细研水飞是指将固体
研成粉末后加水溶解,涉及的操作方法是溶解;去石澄清是指倾倒出澄清液,去除未溶解的固体,涉及的
第1页 | 共23页操作方法是倾倒;慢火熬干是指用小火将溶液蒸发至有少量水剩余,涉及的操作方法是蒸发;因此未涉及
的操作方法是萃取,答案选C。
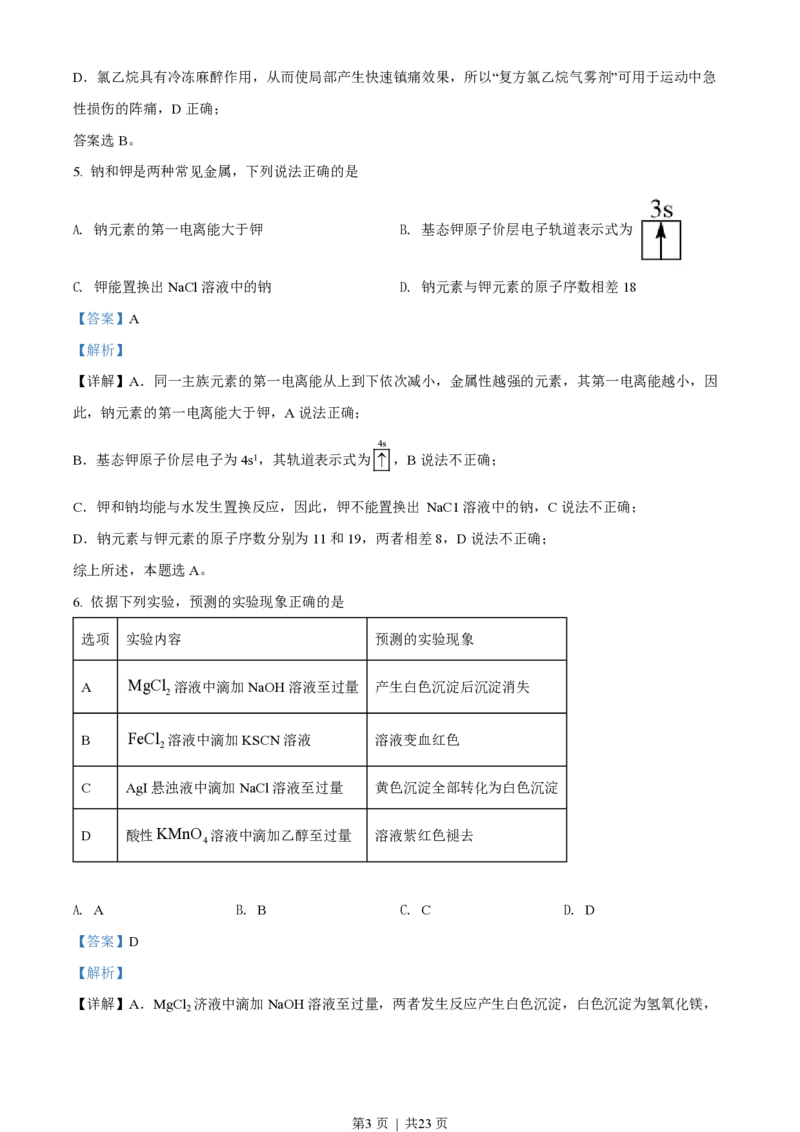
3. 下列实验操作规范的是
A.过滤 B.排空气法收集CO C.混合浓硫酸和乙醇 D.溶液的转移
2
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.过滤时,漏斗下端应紧靠烧杯内壁,A操作不规范;
B.CO 的密度大于空气,可用向上排空气法收集CO ,B操作规范;
2 2
C.混合浓硫酸和乙醇时,应将浓硫酸缓慢倒入乙醇中,并用玻璃棒不断搅拌,C操作不规范;
D.转移溶液时,应使用玻璃棒引流,D操作不规范;
答案选B。
4. 化学物质在体育领域有广泛用途。下列说法错误的是
A. 涤纶可作为制作运动服的材料
B. 纤维素可以为运动员提供能量
C. 木糖醇可用作运动饮料的甜味剂
D. “复方氯乙烷气雾剂”可用于运动中急性损伤的镇痛
【答案】B
【解析】
【详解】A.涤纶属于合成纤维,其抗皱性和保形性很好,具有较高的强度与弹性恢复能力,可作为制作
运动服的材料,A正确;
B.人体没有分解纤维素的酶,故纤维素不能为运动员提供能量,B错误;
C.木糖醇具有甜味,可用作运动饮料的甜味剂,C正确;
第2页 | 共23页D.氯乙烷具有冷冻麻醉作用,从而使局部产生快速镇痛效果,所以“复方氯乙烷气雾剂”可用于运动中急
性损伤的阵痛,D正确;
答案选B。
5. 钠和钾是两种常见金属,下列说法正确的是
A. 钠元素的第一电离能大于钾 B. 基态钾原子价层电子轨道表示式为
C. 钾能置换出NaCl溶液中的钠 D. 钠元素与钾元素的原子序数相差18
【答案】A
【解析】
【详解】A.同一主族元素的第一电离能从上到下依次减小,金属性越强的元素,其第一电离能越小,因
此,钠元素的第一电离能大于钾,A说法正确;
4s
B.基态钾原子价层电子为4s1,其轨道表示式为 ,B说法不正确;
C.钾和钠均能与水发生置换反应,因此,钾不能置换出 NaC1溶液中的钠,C说法不正确;
D.钠元素与钾元素的原子序数分别为11和19,两者相差8,D说法不正确;
综上所述,本题选A。
6. 依据下列实验,预测的实验现象正确的是
选项 实验内容 预测的实验现象
A MgCl 溶液中滴加NaOH溶液至过量 产生白色沉淀后沉淀消失
2
B FeCl 溶液中滴加KSCN溶液 溶液变血红色
2
C AgI悬浊液中滴加NaCl溶液至过量 黄色沉淀全部转化为白色沉淀
D 酸性KMnO 溶液中滴加乙醇至过量 溶液紫红色褪去
4
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.MgCl 济液中滴加NaOH溶液至过量,两者发生反应产生白色沉淀,白色沉淀为氢氧化镁,
2
第3页 | 共23页氢氧化镁为中强碱,其不与过量的NaOH溶液发生反应,因此,沉淀不消失,A不正确;
B.FeCl 溶液中滴加 KSCN洛液,溶液变血红色,实验室通常用这种方法检验的Fe3+存在;FeCl 溶液中
3 2
滴加 KSCN洛液,溶液不变色,B不正确;
C.AgI的溶解度远远小于AgCl,因此,向AgI悬浊液中滴加 NaCl溶液至过量,黄色沉淀不可能全部转
化为白色沉淀,C不正确;
D.酸性KMnO 溶液呈紫红色,其具有强氧化性,而乙醇具有较强的还原性,因此,酸性KMnO 溶液中
4 4
滴加乙醇至过量后溶液紫红色褪去,D正确;
综上所述,依据相关实验预测的实验现象正确的是D,本题选D。
7. 在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德罗常数的值,下列说法正确的是
A
A. 反应转移电子为0.1mol B. HCl溶液中Cl-数为3N
A
C. 2.8g 56Fe含有的中子数为1.3N D. 反应生成标准状况下气体3.36L
A
【答案】A
【解析】
【分析】2.8gFe的物质的量为0.05mol;100mL 3mol·L-1HCl中H+和Cl-的物质的量均为0.3mol,两者发生
反应后,Fe完全溶解,而盐酸过量。
【详解】A.Fe完全溶解生成Fe2+,该反应转移电子0.1mol,A正确;
B.HCl溶液中Cl-的物质的量为0.3mol,因此,Cl-数为0.3N ,B不正确;
A
C.56Fe 的质子数为26、中子数为30,2.8g56Fe的物质的量为0.05mol,因此,2.8g56Fe含有的中子数为
1.5N ,C不正确;
A
D.反应生成H 的物质的量为0.05mol,在标准状况下的体积为1.12L ,D不正确;
2
综上所述,本题A。
8. 某温度下,反应CH =CH (g)+H O(g)ˆˆ†CH CH OH(g)在密闭容器中达到平衡,下列说法正确
2 2 2 ‡ˆˆ 3 2
的是
A. 增大压强,v >v ,平衡常数增大
正 逆
B. 加入催化剂,平衡时CH CH OH(g)的浓度增大
3 2
C. 恒容下,充入一定量的H O(g),平衡向正反应方向移动
2
D. 恒容下,充入一定量的CH =CH (g),CH =CH (g)的平衡转化率增大
2 2 2 2
【答案】C
第4页 | 共23页【解析】
【详解】A.该反应是一个气体分子数减少的反应,增大压强可以加快化学反应速率,正反应速率增大的
幅度大于逆反应的,故v > v ,平衡向正反应方向移动,但是因为温度不变,故平衡常数不变,A不正
正 逆
确;
B.催化剂不影响化学平衡状态,因此,加入催化剂不影响平衡时CH CH OH(g)的浓度,B不正确;
3 2
C.恒容下,充入一定量的H O(g),H O(g)的浓度增大,平衡向正反应方向移动,C正确;
2 2
D.恒容下,充入一定量的CH =CH (g),平衡向正反应方向移动,但是CH =CH (g)的平衡转化率减小,
2 2 2 2
D不正确;
综上所述,本题选C。
二、选择题:本题共 6小题,每小题 4分,共 24 分。每小题有一个或两个选项符合题意。
若正确答案只包括一个选项,多选得 0分;若正确答案包括两个选项,只选一个且正确得 2
分,选两个且都正确得 4分,但只要选错一个就得 0分。
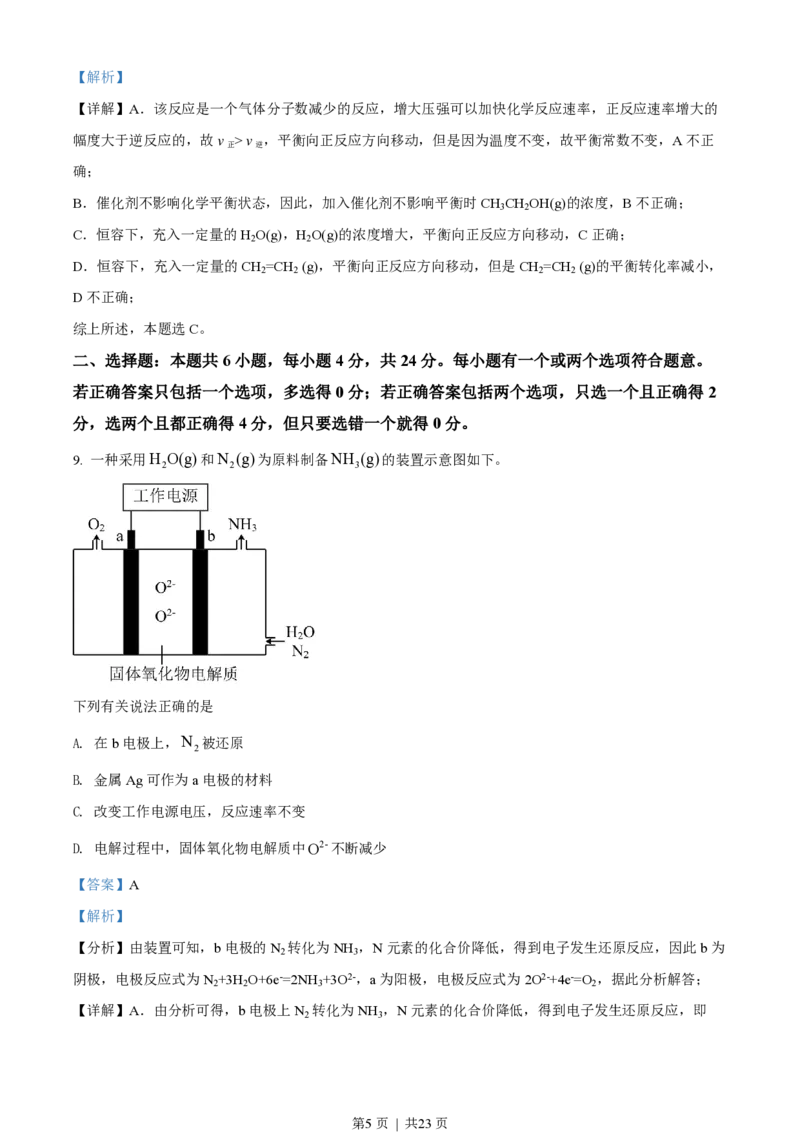
9. 一种采用H O(g)和N (g)为原料制备NH (g)的装置示意图如下。
2 2 3
下列有关说法正确的是
A. 在b电极上,N 被还原
2
B. 金属Ag可作为a电极的材料
C. 改变工作电源电压,反应速率不变
D. 电解过程中,固体氧化物电解质中O2-不断减少
【答案】A
【解析】
【分析】由装置可知,b电极的N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,因此b为
2 3
阴极,电极反应式为N +3H O+6e-=2NH +3O2-,a为阳极,电极反应式为2O2-+4e-=O ,据此分析解答;
2 2 3 2
【详解】A.由分析可得,b电极上N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,即
2 3
第5页 | 共23页N 被还原,A正确;
2
B.a为阳极,若金属Ag作a的电极材料,则金属Ag优先失去电子,B错误;
C.改变工作电源的电压,反应速率会加快,C错误;
D.电解过程中,阴极电极反应式为N +3H O+6e-=2NH +3O2-,阳极电极反应式为2O2-+4e-=O ,因此固体
2 2 3 2
氧化物电解质中O2-不会改变,D错误;
答案选A。
10. 已知CH COOH+Cl ¾I¾2®ClCH COOH+HCl,ClCH COOH的酸性比CH COOH强。下列有
3 2 2 2 3
关说法正确的是
A. HCl的电子式为 B. Cl-Cl键的键长比I-I键短
C. CH COOH分子中只有σ键 D. ClCH COOH的酸性比ICH COOH强
3 2 2
【答案】BD
【解析】
【详解】A.HCl为共价化合物,H原子和Cl原子间形成共用电子对,其电子式为 ,A错误;
B.原子半径Cl<I,故键长:Cl—Cl<I—I,B正确;
C.CH COOH分子中,羧基的碳氧双键中含有π键,C错误;
3
D.电负性Cl>I,-Cl能使-COOH上的H原子具有更大的活动性,因此ClCH COOH的酸性比
2
ICH COOH强,D正确;
2
答案选BD。
11. 短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期并相邻,Y是组成水的元素之一,
Z在同周期主族元素中金属性最强,W原子在同周期主族元素中原子半径最小,下列判断正确的是
A. XW 是非极性分子
3
B. 简单氢化物沸点:X>Y
C. Y与Z形成的化合物是离子化合物
D. X、Y、Z三种元素组成的化合物水溶液呈酸性
【答案】C
【解析】
【分析】X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y同周期并相邻,且Y是组成水的元
素之一,则Y为O元素,X为N元素,Z在同周期主族元素中金属性最强,则Z为Na元素,W原子在
第6页 | 共23页同周期主族元素中原子半径最小,则W为Cl元素,据此分析解答。
【详解】A.由分析,X为N元素,W为Cl元素,NCl 分子的空间构型为三角锥形,其正负电荷的中心
3
不重合,属于极性分子,A错误;
B.H O和NH 均含有氢键,但H O分子形成的氢键更多,故沸点H O>NH ,B错误;
2 3 2 2 3
C.Y为O元素,Z为Na元素,两者形成的化合物为Na O、Na O 均为离子化合物,C正确;
2 2 2
D.N、O、Na三种元素组成的化合物NaNO 呈中性、NaNO 呈碱性,D错误;
3 2
答案选C。
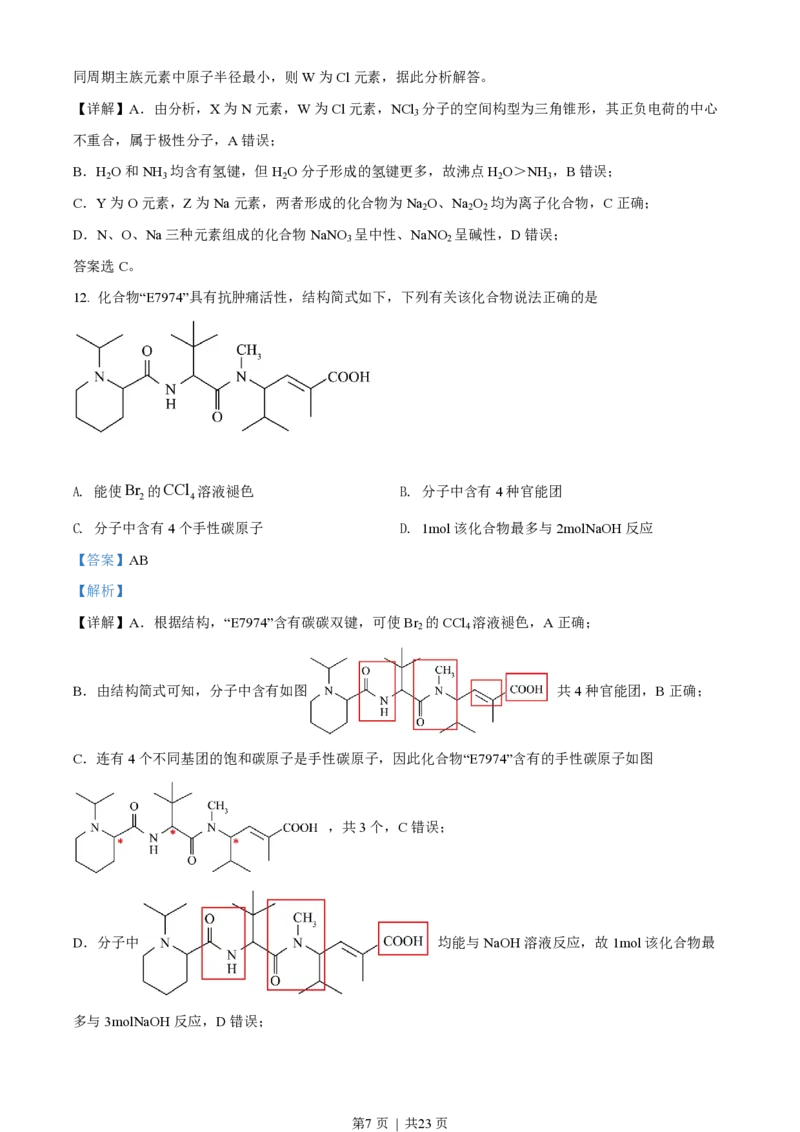
12. 化合物“E7974”具有抗肿痛活性,结构简式如下,下列有关该化合物说法正确的是
A. 能使Br 的CCl 溶液褪色 B. 分子中含有4种官能团
2 4
C. 分子中含有4个手性碳原子 D. 1mol该化合物最多与2molNaOH反应
【答案】AB
【解析】
【详解】A.根据结构,“E7974”含有碳碳双键,可使Br 的CCl 溶液褪色,A正确;
2 4
B.由结构简式可知,分子中含有如图 共4种官能团,B正确;
C.连有4个不同基团的饱和碳原子是手性碳原子,因此化合物“E7974”含有的手性碳原子如图
,共3个,C错误;
D.分子中 均能与NaOH溶液反应,故1mol该化合物最
多与3molNaOH反应,D错误;
第7页 | 共23页答案选AB。
13. NaClO溶液具有添白能力,已知25℃时,K (HClO)=4.0´10-8。下列关于NaClO溶液说法正确的是
a
A. 0.01mol/L溶液中,c ClO- <0.01mol×L-1
B. 长期露置在空气中,释放Cl ,漂白能力减弱
2
C. 通入过量SO ,反应的离子方程式为SO +ClO-+H O=HSO-+HClO
2 2 2 3
D. 25℃,pH=7.0的NaClO和HClO的混合溶液中,c(HClO)>c
ClO-
=c
Na+
【答案】AD
【解析】
【详解】A.NaClO溶液中ClO-会水解,故0.01mol/LNaClO溶液中c(ClO-)<0.01mol/L,A正确;
B.漂白粉主要成分为Ca(ClO) 和CaCl ,长期露置在空气中容易和CO 发生反应而失效,其反应的化学
2 2 2
方程式为:Ca(ClO) +CO +H O=CaCO ↓+2HClO,HClO再分解:2HClO=2HCl+O ↑,不会释放Cl ,B错
2 2 2 3 2 2
误;
C.将过量的SO 通入NaClO溶液中,SO 被氧化:SO +ClO−+H O=Cl-+SO2-+2H+,C错误;
2 2 2 2 4
D.25℃,pH=7.0的NaClO和HClO的混合溶液中,存在电荷守恒:c(ClO-)+c(OH-)=c(H+)+c(Na+),则
c(ClO-)=c(Na+),又c(HClO)>c(ClO-),所以c(HClO)>c(ClO-)=c(Na+),D正确;
答案选AD。
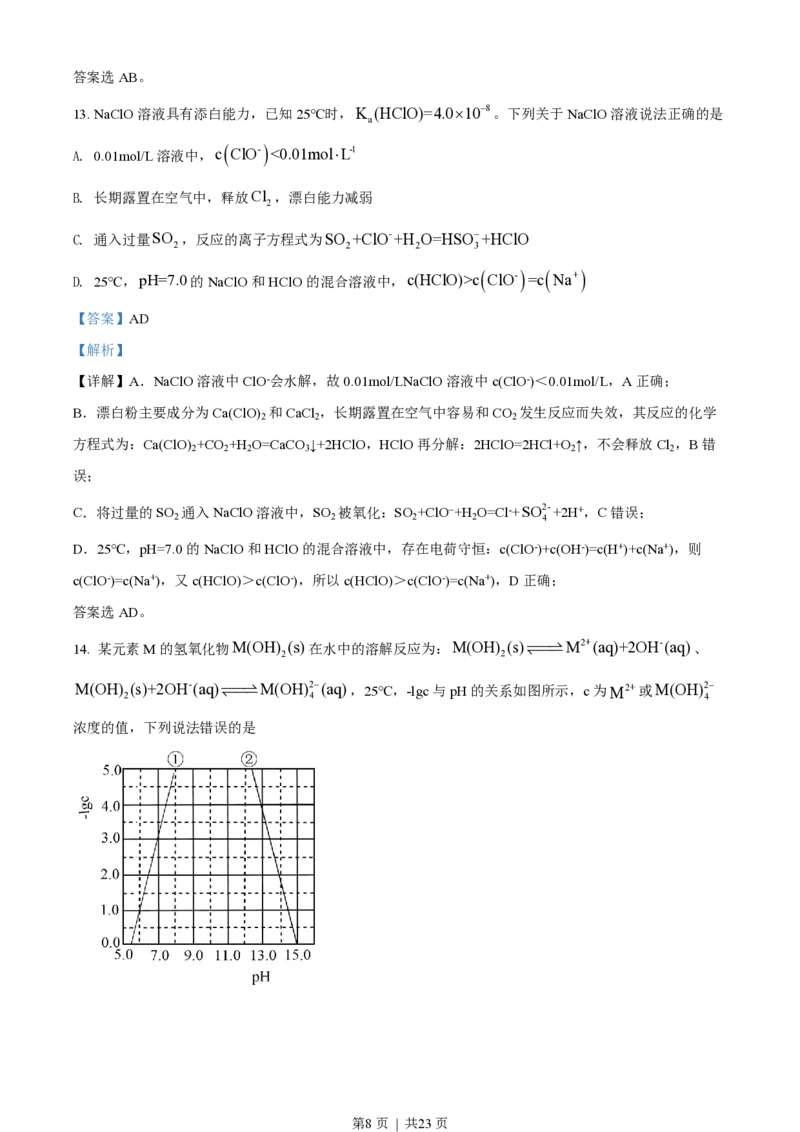
14. 某元素M的氢氧化物M(OH) (s)在水中的溶解反应为:M(OH) (s)ˆˆ†M2+(aq)+2OH-(aq)、
2 2 ‡ˆˆ
M(OH) (s)+2OH-(aq)ˆˆ†M(OH)2-(aq),25℃,-lgc与pH的关系如图所示,c为M2+或M(OH)2-
2 ‡ˆˆ 4 4
浓度的值,下列说法错误的是
第8页 | 共23页A. 曲线①代表-lgc
M2+
与pH的关系
B. M(OH) 的K 约为1´10-10
2 sp
C. 向c M2+ =0.1mol×L-1的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以M(OH) (s)存在
2
D. 向cé
ë
M(OH)2
4
-ù
û
=0.1mol×L-1的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以M2+存
在
【答案】BD
【解析】
【分析】由题干信息,M(OH) (s)ˆˆ†M2+(aq)+2OH-(aq),M(OH) (s)+2OH-(aq)ˆˆ†M(OH)2-(aq),随着
2 ‡ˆˆ 2 ‡ˆˆ 4
pH增大,c(OH-)增大,则c(M2+)减小,c[M(OH)2-]增大,即-lg c(M2+)增大,-lg c[M(OH)2-]减小,因此曲
4 4
线①代表-lg c(M2+)与pH的关系,曲线②代表-lg c[M(OH)2-]与pH的关系,据此分析解答。
4
【详解】A.由分析可知,曲线①代表-lg c(M2+)与pH的关系,A正确;
B.由图象,pH=7.0时,-lg c(M2+)=3.0,则M(OH) 的K =c(M2+)·c2(OH-)=1×10-17,B错误;
2 sp
C.向c(M2+)=0.1mol/L的溶液中加入NaOH溶液至pH=9.0,根据图像,pH=9.0时,c(M2+)、c[M(OH)2-]
4
均极小,则体系中元素M主要以M(OH) (s)存在,C正确;
2
D.c[M(OH)2-]=0.1mol/L的溶液中,由于溶解平衡是少量的,因此加入等体积的0.4mol/L的HCl后,体
4
系中元素M仍主要以M(OH)2-存在,D错误;
4
答案选BD。
三、非选择题:共 5题,共 60分。
15. 胆矾(CuSO ×5H O)是一种重要化工原料,某研究小组以生锈的铜屑为原料[主要成分是Cu,含有少
4 2
量的油污、CuO、CuCO 、Cu(OH) ]制备胆矾。流程如下。
3 2
回答问题:
(1)步骤①的目的是_______。
(2)步骤②中,若仅用浓H SO 溶解固体B,将生成_______(填化学式)污染环境。
2 4
第9页 | 共23页(3)步骤②中,在H O 存在下Cu溶于稀H SO ,反应的化学方程式为_______。
2 2 2 4
(4)经步骤④得到的胆矾,不能用水洗涤的主要原因是_______。
(5)实验证明,滤液D能将I-氧化为I 。
2
ⅰ.甲同学认为不可能是步骤②中过量H O 将I-氧化为I ,理由是_______。
2 2 2
ⅱ.乙同学通过实验证实,只能是Cu2+将I-氧化为I ,写出乙同学的实验方案及结果_______(不要求写具体
2
操作过程)。
【答案】(1)除油污 (2)SO
2
(3)Cu+H O +H SO =CuSO +2H O
2 2 2 4 4 2
(4)胆矾晶体易溶于水
(5) ①. 溶液 C 经步骤③加热浓缩后双氧水已完全分解 ②. 取滤液,向其中加入适量硫化钠,使
铜离子恰好完全沉淀,再加入I-,不能被氧化
【解析】
【分析】由流程中的信息可知,原料经碳酸钠溶液浸洗后过滤,可以除去原料表面的油污;滤渣固体B与
过量的稀硫酸、双氧水反应,其中的CuO、CuCO 、Cu(OH) 均转化为CuSO ,溶液C为硫酸铜溶液和稀
3 2 4
硫酸的混合液,加热浓缩、冷却结晶、过滤后得到胆矾。
【小问1详解】
原料表面含有少量的油污,Na CO 溶液呈碱性,可以除去原料表面的油污,因此,步骤①的目的是:除去
2 3
原料表面的油污。
【小问2详解】
在加热的条件下,铜可以与浓硫酸发生反应生成CuSO 、SO 和H O,二氧化硫是一种大气污染物,步骤
4 2 2
②中,若仅用浓H SO 溶解固体B,将生成SO 污染环境。
2 4 2
【小问3详解】
步骤②中,在H O 存在下Cu溶于稀H SO ,生成CuSO 和H O,该反应的化学方程式为Cu+ H O +
2 2 2 4 4 2 2 2
H SO =CuSO +2H O。
2 4 4 2
【小问4详解】
胆矾是一种易溶于水的晶体,因此,经步骤④得到的胆矾,不能用水洗涤的主要原因是:胆矾晶体易溶于
水,用水洗涤会导致胆矾的产率降低。
【小问5详解】
ⅰ. H O 常温下即能发生分解反应,在加热的条件下,其分解更快,因此,甲同学认为不可能是步骤②中过
2 2
第10页 | 共23页量H O 将I-氧化为I ,理由是:溶液C经步骤③加热浓缩后H O 已完全分解。
2 2 2 2 2
ⅱ. I-氧化为I 时溶液的颜色会发生变化;滤液D中含有CuSO 和H SO ,乙同学通过实验证实,只能是
2 4 2 4
Cu2+将I-氧化为I ,较简单的方案是除去溶液中的Cu2+,然后再向其中加入含有I-的溶液,观察溶液是否
2
变色;除去溶液中的Cu2+的方法有多种,可以加入适当的沉淀剂将其转化为难溶物,如加入Na S将其转
2
化为CuS沉淀,因此,乙同学的实验方案为取少量滤液D,向其中加入适量Na S溶液,直至不再有沉淀
2
生成,静置后向上层清液中加入少量KⅠ溶液;实验结果为:上层清液不变色,证明I-不能被除去Cu2+的溶
液氧化,故只能是Cu2+将I-氧化为I 。
2
16. 某空间站的生命保障系统功能之一是实现氧循环,其中涉及反应:
催化剂
CO (g)+4H (g)ˆˆˆˆ†2H O(g)+CH (g)
2 2 ‡ˆˆˆˆ 2 4
回答问题:
(1)已知:电解液态水制备1mol O (g),电解反应的ΔH=+572kJ×mol-1。由此计算H (g)的燃烧热
2 2
(焓)ΔH=_______kJ×mol-1。
催化剂
(2)已知:CO (g)+4H (g)ˆˆˆˆ†2H O(g)+CH (g)的平衡常数(K)与反应温度(t)之间的关系如图1
2 2 ‡ˆˆˆˆ 2 4
所示。
①若反应为基元反应,且反应的ΔH与活化能(Ea)的关系为 ΔH >E 。补充完成该反应过程的能量变化示
a
意图(图2)_______。
第11页 | 共23页②某研究小组模拟该反应,温度t下,向容积为10L的抽空的密闭容器中通入0.1mol CO 和
2
0.4mol H ,反应平衡后测得容器中nCH =0.05mol。则CO 的转化率为_______,反应温度t约为
2 4 2
_______℃。
(3)在相同条件下,CO (g)与H (g)还会发生不利于氧循环的副反应:
2 2
CO (g)+3H (g)ˆˆ 催 ˆ 化剂 ˆ†H O(g)+CH OH(g),在反应器中按nCO :nH =1:4通入反应物,在不
2 2 ‡ˆˆˆˆ 2 3 2 2
同温度、不同催化剂条件下,反应进行到2min时,测得反应器中CH OH、CH 浓度(μmol×L-1)如下表
3 4
所示。
t=350℃ t=400℃
催化剂
c(CH OH) cCH cCH OH c(CH )
3 4 3 4
催化剂Ⅰ 10.8 12722 345.2 42780
催化剂Ⅱ 9.2 10775 34 38932
在选择使用催化剂Ⅰ和350℃条件下反应,0~2min生成CH OH的平均反应速率为_______
3
μmol×L-1×min-1;若某空间站的生命保障系统实际选择使用催化剂Ⅱ和400℃的反应条件,原因是
_______。
【答案】(1)-286
第12页 | 共23页(2) ①. ②. 50%或 0.5 ③. 660.2(或 660.1 或
660.3,其他答案酌情给分)
(3) ①. 5.4 ②. 相同催化剂,400℃的反应速率更快,相同温度,催化剂Ⅱ副产物浓度低,甲烷与
甲醇比例高
【解析】
【小问1详解】
电解液态水制备1mol O (g),电解反应的ΔH=+572kJ×mol-1,由此可以判断,2molH (g)完全燃烧消
2 2
耗1mol O (g),生成液态水的同时放出的热量为572kJ ,故1molH (g)完全燃烧生成液态水放出的热量
2 2
为286kJ,因此,H (g)的燃烧热(焓)ΔH=-286kJ×mol-1。
2
【小问2详解】
催化剂
①由CO (g)+4H (g)ˆˆˆˆ†2H O(g)+CH (g)的平衡常数(K)与反应温度(t)之间的关系图可知,K随
2 2 ‡ˆˆˆˆ 2 4
着温度升高而减小,故该反应为放热反应。若反应为基元反应,则反应为一步完成,由于反应的ΔH与活
化能(Ea)的关系为 ΔH >E ,由图2信息可知E =akJ×mol-1,则 ΔH >akJ×mol-1,该反应为放热反
a a
应,生成物的总能量小于反应物的,因此该反应过程的能量变化示意图为:
第13页 | 共23页。
②温度t下,向容积为10L的抽空的密闭容器中通入0.1mol CO 和0.4mol H ,反应平衡后测得容器中
2 2
0.05mol
nCH =0.05mol,则CO 的转化率为 =0.5,根据C元素守恒可知,CO 的平衡量为
4 2 0.1mol 2
0.05mol,CO 和H 是按化学计量数之比投料的,则H 的平衡量为0.2mol,H O(g)的平衡量是
2 2 2 2
CH (g)的2倍,则nH O=0.1mol,CO (g)、H (g)、H O(g)、CH (g)的平衡浓度分别为
4 2 2 2 2 4
0.005mol L-1、0.02mol L-1、0.01mol L-1、0.005mol L-1,则该反应的平衡常数K=
g g g g
0.012´0.005
=625,根据图1中的信息可知,反应温度t约为660.2℃。
0.005´0.024
【小问3详解】
在选择使用催化剂Ⅰ和350℃条件下反应,由表中信息可知,0~2min CH OH的浓度由0增加到10.8
3
10.8mol×L-1
μmol×L-1,因此,0~2min生成CH OH的平均反应速率为 =5.4 μmol×L-1×min-1;由表中
3
2min
信息可知,在选择使用催化剂Ⅰ和350℃条件下反应, 0~2min CH OH的浓度由0增加到
3
10.8μmol×L-1,,c(CH ):cCH OH =12722:10.8»1178;在选择使用催化剂Ⅱ和350℃的反应条件下,
4 3
0~2min CH OH的浓度由0增加到9.2μmol×L-1,c(CH ):cCH OH =10775:9.2»1171;在选择使用
3 4 3
催化剂Ⅰ和400℃条件下反应, 0~2min CH OH的浓度由0增加到345.2μmol×L-1,c(CH ):
3 4
cCH OH =42780:345.2»124;在选择使用催化剂Ⅱ和400℃的反应条件下,0~2min CH OH的浓度由
3 3
0增加到34μmol×L-1,c(CH ):cCH OH =38932:34»1145。因此,若某空间站的生命保障系统实际
4 3
第14页 | 共23页选择使用催化剂Ⅱ和400℃的反应条件的原因是:相同催化剂,400℃的反应速率更快,相同温度,催化剂
Ⅱ副产物浓度低,甲烷与甲醇比例高。
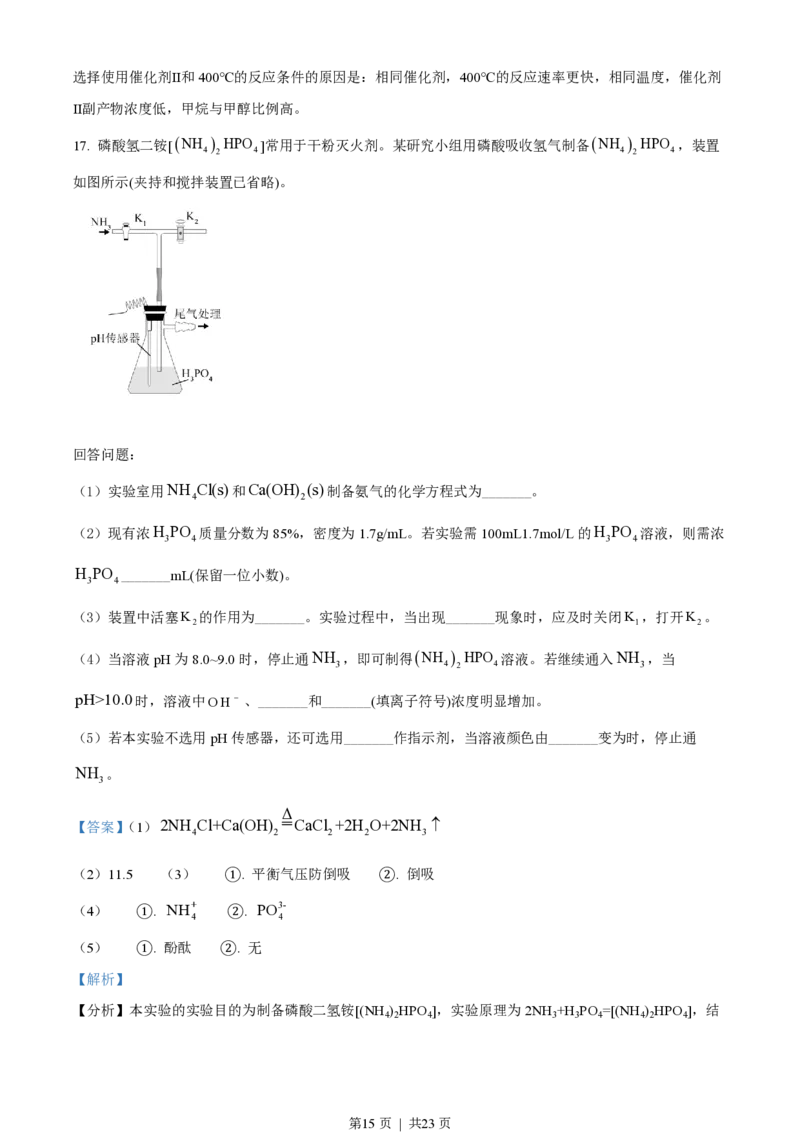
17. 磷酸氢二铵[ NH HPO ]常用于干粉灭火剂。某研究小组用磷酸吸收氢气制备NH HPO ,装置
4 2 4 4 2 4
如图所示(夹持和搅拌装置已省略)。
回答问题:
(1)实验室用NH Cl(s)和Ca(OH) (s)制备氨气的化学方程式为_______。
4 2
(2)现有浓H PO 质量分数为85%,密度为1.7g/mL。若实验需100mL1.7mol/L的H PO 溶液,则需浓
3 4 3 4
H PO _______mL(保留一位小数)。
3 4
(3)装置中活塞K 的作用为_______。实验过程中,当出现_______现象时,应及时关闭K ,打开K 。
2 1 2
(4)当溶液pH为8.0~9.0时,停止通NH ,即可制得NH HPO 溶液。若继续通入NH ,当
3 4 2 4 3
pH>10.0时,溶液中OH- 、_______和_______(填离子符号)浓度明显增加。
(5)若本实验不选用pH传感器,还可选用_______作指示剂,当溶液颜色由_______变为时,停止通
NH 。
3
Δ
【答案】(1)2NH Cl+Ca(OH) CaCl +2H O+2NH
4 2 2 2 3
(2)11.5 (3) ①. 平衡气压防倒吸 ②. 倒吸
(4) ①. NH+ ②. PO3-
4 4
(5) ①. 酚酞 ②. 无
【解析】
【分析】本实验的实验目的为制备磷酸二氢铵[(NH ) HPO ],实验原理为2NH +H PO =[(NH ) HPO ],结
4 2 4 3 3 4 4 2 4
第15页 | 共23页合相关实验基础知识分析解答问题。
【小问1详解】
Δ
实验室用NH Cl(s)和Ca(OH) (s)在加热的条件下制备氨气,反应的化学方程式为2NH Cl+Ca(OH)
4 2 4 2
CaCl +2H O+2NH ↑;
2 2 3
【小问2详解】
1000ρω 1000ρω 1000´1.7g×mL-1´85%
根据公式c= 可得,浓H PO 的浓度c= = »14.7mol/L,溶液稀
3 4
M M 98
释前后溶质的物质的量不变,因此配制100mL 1.7mol/L的H PO 溶液,需要浓H PO 的体积V=
3 4 3 4
0.1L ´ 1.7mol /L
» 0.0115L=11.5mL;
14.7mol /L
【小问3详解】
由于NH 极易溶于水,因此可选择打开活塞K 以平衡气压,防止发生倒吸,所以实验过程中,当出现倒
3 2
吸现象时,应及时关闭K ,打开K ;
1 2
【小问4详解】
继续通入NH ,(NH ) HPO 继续反应生成(NH ) PO ,当pH>10.0时,溶液中OH-、NH+、PO3-的浓度
3 4 2 4 4 3 4 4 4
明显增加;
【小问5详解】
由(4)小问可知,当pH为8.0~9.0时,可制得(NH ) HPO ,说明(NH ) HPO 溶液显碱性,因此若不选用pH
4 2 4 4 2 4
传感器,还可以选用酚酞作指示剂,当溶液颜色由无色变为浅红时,停止通入NH ,即可制得(NH ) HPO
3 4 2 4
溶液。
18. 黄酮哌酯是一种解痉药,可通过如下路线合成:
回答问题:
(1)A→B的反应类型为_______。
(2)已知B为一元强酸,室温下B与NaOH溶液反应的化学方程式为_______。
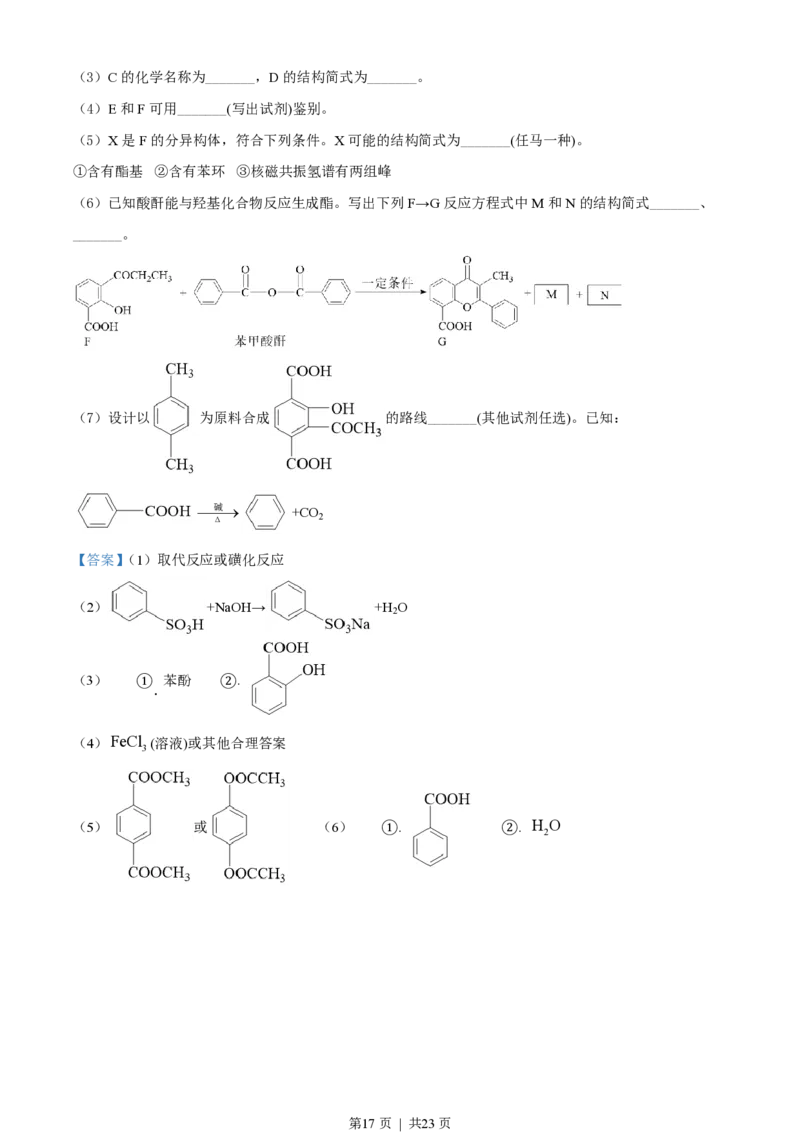
第16页 | 共23页(3)C的化学名称为_______,D的结构简式为_______。
(4)E和F可用_______(写出试剂)鉴别。
(5)X是F的分异构体,符合下列条件。X可能的结构简式为_______(任马一种)。
①含有酯基 ②含有苯环 ③核磁共振氢谱有两组峰
(6)已知酸酐能与羟基化合物反应生成酯。写出下列F→G反应方程式中M和N的结构简式_______、
_______。
(7)设计以 为原料合成 的路线_______(其他试剂任选)。已知:
¾碱¾® +CO
Δ 2
【答案】(1)取代反应或磺化反应
(2) +NaOH→ +H O
2
(3) ① 苯酚 ②.
.
(4)FeCl (溶液)或其他合理答案
3
(5) 或 (6) ①. ②. H O
2
第17页 | 共23页(7)
【解析】
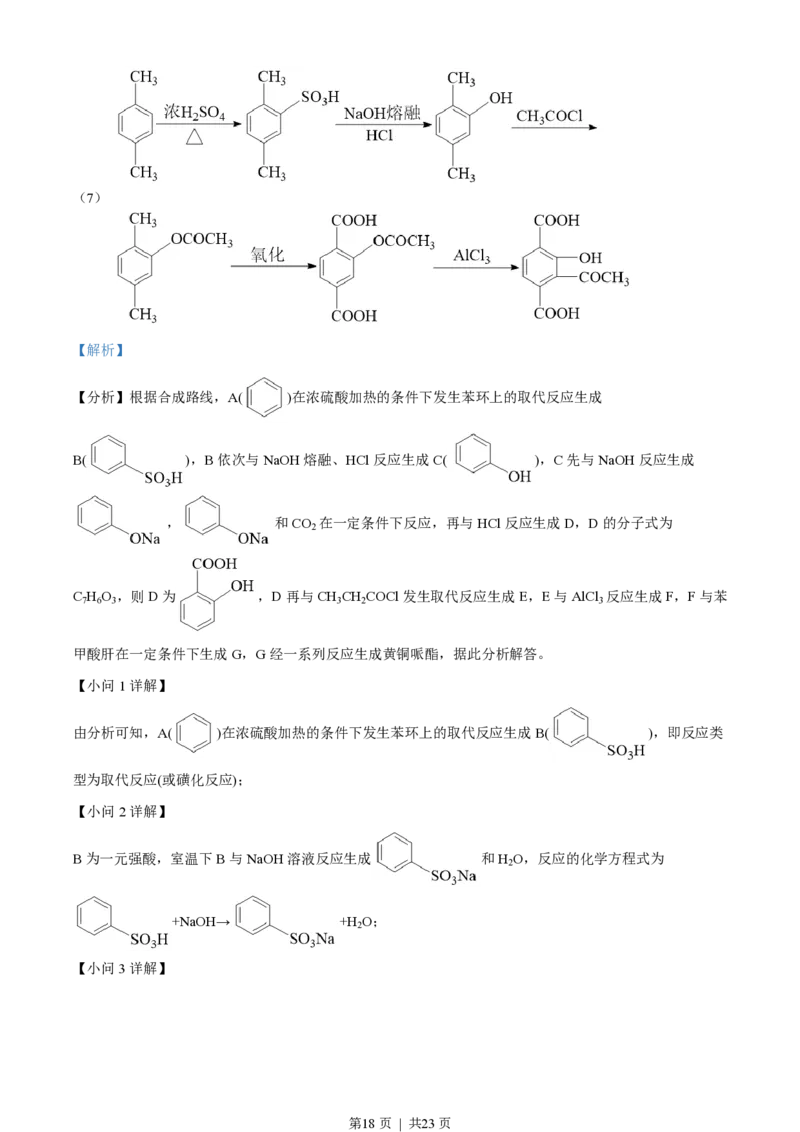
【分析】根据合成路线,A( )在浓硫酸加热的条件下发生苯环上的取代反应生成
B( ),B依次与NaOH熔融、HCl反应生成C( ),C先与NaOH反应生成
, 和CO 在一定条件下反应,再与HCl反应生成D,D的分子式为
2
C H O ,则D为 ,D再与CH CH COCl发生取代反应生成E,E与AlCl 反应生成F,F与苯
7 6 3 3 2 3
甲酸肝在一定条件下生成G,G经一系列反应生成黄铜哌酯,据此分析解答。
【小问1详解】
由分析可知,A( )在浓硫酸加热的条件下发生苯环上的取代反应生成B( ),即反应类
型为取代反应(或磺化反应);
【小问2详解】
B为一元强酸,室温下B与NaOH溶液反应生成 和H O,反应的化学方程式为
2
+NaOH→ +H O;
2
【小问3详解】
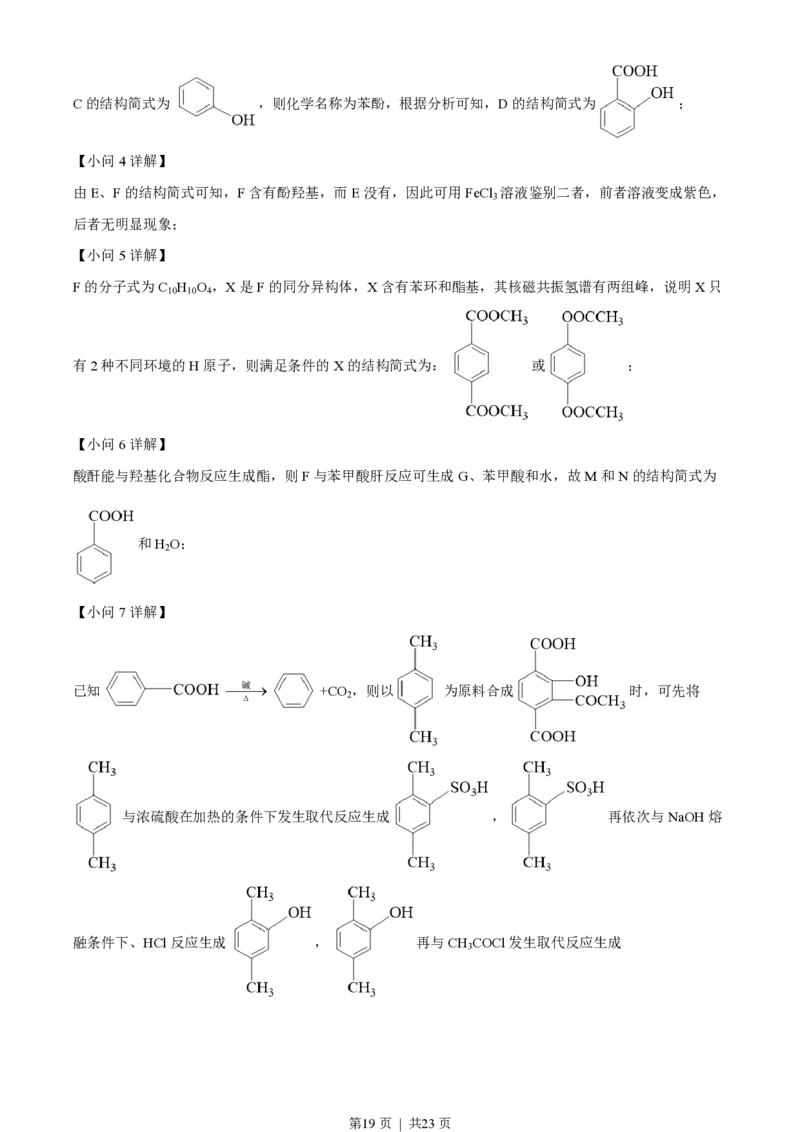
第18页 | 共23页C的结构简式为 ,则化学名称为苯酚,根据分析可知,D的结构简式为 ;
【小问4详解】
由E、F的结构简式可知,F含有酚羟基,而E没有,因此可用FeCl 溶液鉴别二者,前者溶液变成紫色,
3
后者无明显现象;
【小问5详解】
F的分子式为C H O ,X是F的同分异构体,X含有苯环和酯基,其核磁共振氢谱有两组峰,说明X只
10 10 4
有2种不同环境的H原子,则满足条件的X的结构简式为: 或 ;
【小问6详解】
酸酐能与羟基化合物反应生成酯,则F与苯甲酸肝反应可生成G、苯甲酸和水,故M和N的结构简式为
和H O;
2
【小问7详解】
已知 ¾碱¾® +CO ,则以 为原料合成 时,可先将
Δ 2
与浓硫酸在加热的条件下发生取代反应生成 , 再依次与NaOH熔
融条件下、HCl反应生成 , 再与CH COCl发生取代反应生成
3
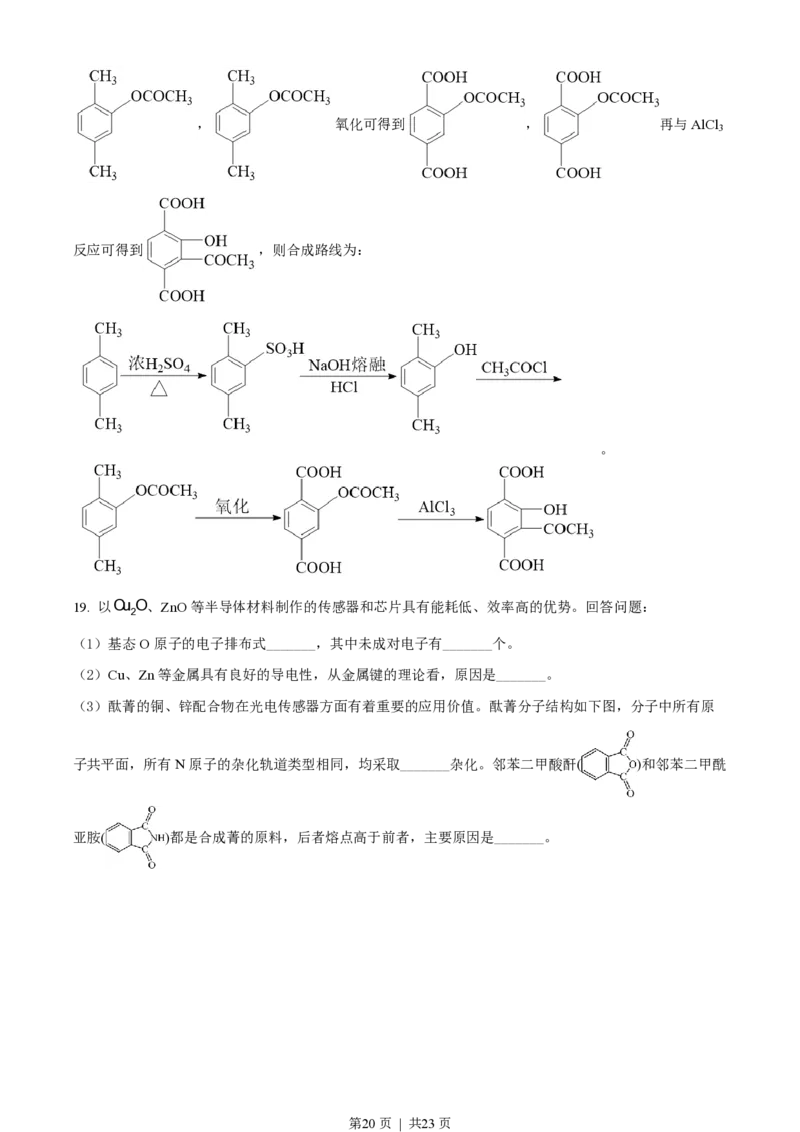
第19页 | 共23页, 氧化可得到 , 再与AlCl
3
反应可得到 ,则合成路线为:
。
19. 以Cu O、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
2
(1)基态O原子的电子排布式_______,其中未成对电子有_______个。
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是_______。
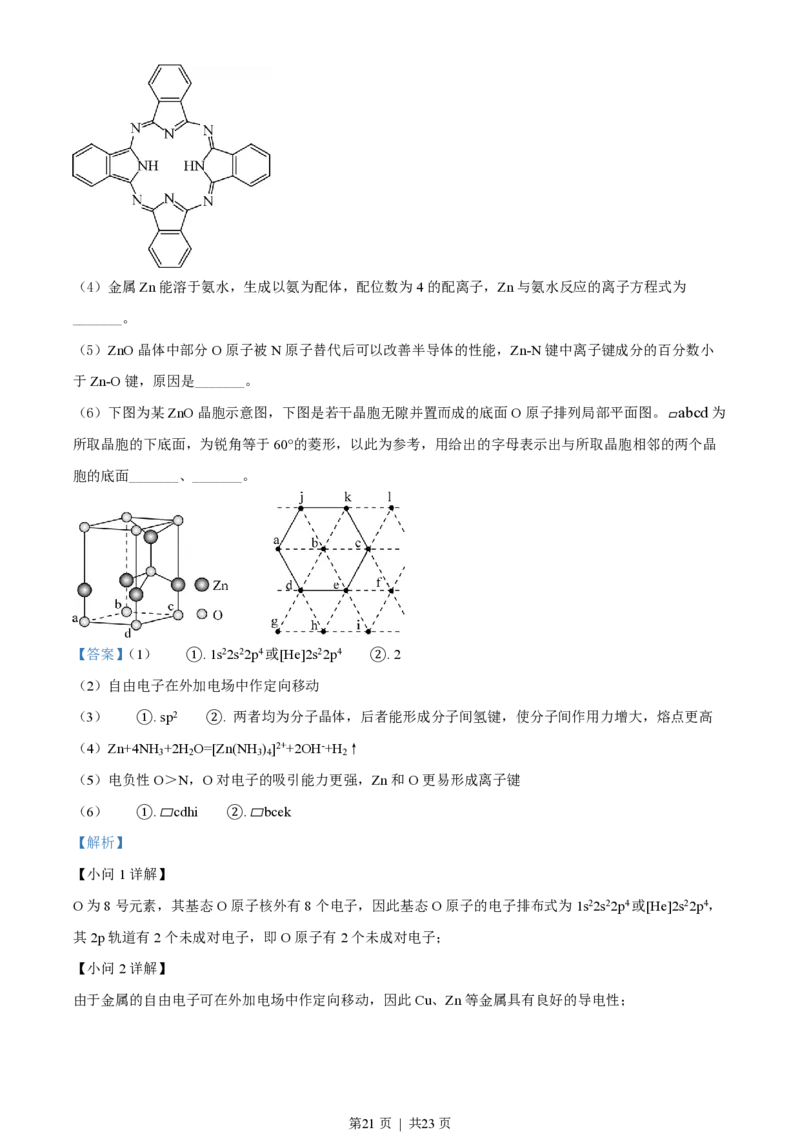
(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原
子共平面,所有N原子的杂化轨道类型相同,均采取_______杂化。邻苯二甲酸酐( )和邻苯二甲酰
亚胺( )都是合成菁的原料,后者熔点高于前者,主要原因是_______。
第20页 | 共23页(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为
_______。
(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小
于Zn-O键,原因是_______。
(6)下图为某ZnO晶胞示意图,下图是若干晶胞无隙并置而成的底面O原子排列局部平面图。 abcd为
Y
所取晶胞的下底面,为锐角等于60°的菱形,以此为参考,用给出的字母表示出与所取晶胞相邻的两个晶
胞的底面_______、_______。
【答案】(1) ①. 1s22s22p4或[He]2s22p4 ②. 2
(2)自由电子在外加电场中作定向移动
(3) ①. sp2 ②. 两者均为分子晶体,后者能形成分子间氢键,使分子间作用力增大,熔点更高
(4)Zn+4NH +2H O=[Zn(NH ) ]2++2OH-+H ↑
3 2 3 4 2
(5)电负性O>N,O对电子的吸引能力更强,Zn和O更易形成离子键
(6) ①. ▱cdhi ②. ▱bcek
【解析】
【小问1详解】
O为8号元素,其基态O原子核外有8个电子,因此基态O原子的电子排布式为1s22s22p4或[He]2s22p4,
其2p轨道有2个未成对电子,即O原子有2个未成对电子;
【小问2详解】
由于金属的自由电子可在外加电场中作定向移动,因此Cu、Zn等金属具有良好的导电性;
第21页 | 共23页【小问3详解】
根据结构式可知,N原子均形成双键,故N原子的杂化方式均为sp2,由于邻苯二甲酸酐和邻苯二甲酰亚
胺均为分子晶体,而后者能形成分子间氢键,使分子间作用力增大,因此熔点更高;
【小问4详解】
金属Zn与氨水反应可生成[Zn(NH ) ](OH) 和H ,反应的离子方程式为
3 4 2 2
Zn+4NH +2H O=[Zn(NH ) ]2++2OH-+H ↑;
3 2 3 4 2
【小问5详解】
由于电负性O>N,O对电子的吸引能力更强,Zn和O更易形成离子键,因此Zn—N键中离子键成分的
百分数小于Zn—O键;
【小问6详解】
根据晶胞示意图,一个晶胞中8个O原子位于晶胞的顶点,1个O原子位于晶胞体内,4个Zn原子位于
晶胞的棱上,1个Zn原子位于晶胞体内,棱上的3个Zn原子和体内的Zn原子、O原子形成四面体结
构,则于其相邻的晶胞与该晶胞共用bc和cd,则相邻的两个晶胞的底面为▱cdhi和▱bcek。
第22页 | 共23页第23页 | 共23页