文档内容
2025-2026 学年高二化学上学期第一次月考卷
(考试时间:90 分钟 试卷满分:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第 1~2 章(鲁科版 2019 选择性必修 1)。
5.难度系数:0.66
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Cl 35.5 Cu 64
第Ⅰ卷(选择题 共 40 分)
一、选择题:本题共 10 小题,每小题 2 分,共 20 分。每小题只有一个选项符合题目要求。
1.下列有关中和热和燃烧热的说法中,正确的是
A.反应热就是热量
B.在稀溶液中, 和 完全中和时放出的热量小于
C. 溶液与稀 溶液恰好完全反应时,放出 的热量
D.已知 所以,C 的燃烧热是 220.7
【答案】B
【解析】A.在一定温度下,化学反应吸收或放出的热量叫做反应热,A 错误;B.醋酸为弱电解质,电
离吸热,在稀溶液中, 和 完全中和时放出的热量小于 ,B 正确;C.中
和热是指强酸和强碱的稀溶液反应生成 水所释放的热量,所以 的 与稀 溶液
恰好完全反应时放出 的热量,C 错误;D.C 的燃烧热是 C 完全燃烧生成 所放出的热量,D
错误;故选 B。
2.研究化学反应进行的方向对于反应设计等具有重要意义,下列说法正确的是
A.ΔH<0、ΔS>0 的反应在温度低时不能自发进行
B.一定温度下,反应 MgCl (l) Mg(l)+Cl (g)的ΔH>0、ΔS>0
2 2
C.反应 CaCO (s)=CaO(s)+CO (g)在室温下不能自发进行,说明该反应的ΔH<0
3 2
D.在其他外界条件不变的情况下,汽车排气管中使用催化剂,可以改变产生尾气的反应方向
【答案】B
/【解析】A.ΔH<0、ΔS>0 的反应,一定存在ΔH-TΔS<0,在温度低时能自发进行,故 A 错误;B.一定
温度下,反应 MgCl
2
(l)⇌Mg(l)+Cl
2
(g)的气体体积增大,反应条件是电解,
ΔH>0、ΔS>0,故 B 正确;C.
反应 CaCO (s)=CaO(s)+CO (g)在室温下不能自发进行,该反应的ΔS>0,则满足ΔH-TΔS>0 时,说明该反
3 2
应的ΔH>0,故 C 错误;D.在其他外界条件不变的情况下,汽车排气管中使用催化剂,不能改变产生尾
气的反应方向,故 D 错误;故选:B。
3.某课外兴趣小组用浓度均为 0.1 mol/L 的 NaSO 溶液和稀硫酸探究影响化学反应速率的因素,设计实
2 2 3
验方案如下表。下列说法不正确的是
液体体积/mL
实验编号 反应温度/°C
NaSO 稀硫酸 HO
2 2 3 2
① 25 10 20 0
② 25 V 20 5
③ 50 10 20 0
A.该实验的化学方程式为 NaSO+H SO =Na SO +S↓+SO↑+H O
2 2 3 2 4 2 4 2 2
B.实验①和②是探究 NaSO 溶液浓度对反应速率的影响,V=10
2 2 3
C.实验①和③是探究温度对反应速率的影响,③的反应速率更快
D.该实验可通过产生浑浊的时间或单位时间内产生气体的体积判断反应的快慢
【答案】B
【分析】NaSO 溶液和稀硫酸发生反应生成 NaSO 、S、SO 、HO,该反应的化学方程式为:NaSO
2 2 3 2 4 2 2 2 2 3
+H SO =Na SO +S↓+SO↑+H O,在探究二者反应速率的影响因素时要采用控制变量方法进行研究,
2 4 2 4 2 2
其它条件相同,只改变一个外界条件,根据化学反应速率与该变量的关系分析判断。
【解析】A.NaSO 溶液和稀硫酸发生反应生成 NaSO 、S、SO 、HO,该反应的化学方程式为:NaSO
2 2 3 2 4 2 2 2 2 3
+H SO =Na SO +S↓+SO↑+H O,A 正确;B.要采用控制变量方法进行研究,根据实验①可知混合溶
2 4 2 4 2 2
液总体积是 30 mL,实验①、②的硫酸浓度相同,体积也相同,则实验②是改变 NaSO 溶液的浓度,
2 2 3
NaSO 溶液体积应该是 5 mL,B 错误;C.实验①和③只有反应温度不同,其它条件相同,故实验①
2 2 3
和③是探究温度对反应速率的影响,其中实验③的反应温度比实验①高,升高温度,化学反应速率更快,
C 正确;D.该反应产生了难溶于水的 S 单质使溶液变浑浊,因此可通过产生浑浊的时间长短判断反应
的快慢;由于反应产生了 SO 气体,因此也可以通过测定单位时间内产生气体的体积判断反应的快慢,
2
D 正确;故合理选项是 B。
4.化学电源在日常生活和高科技领域中都有广泛应用,如图所示为两种常见的化学电源示意图,下列有关
说法不正确的是
/A.锌锰干电池属于一次电池,铅酸蓄电池属于二次电池
B.锌锰干电池中的带铜帽的石墨棒为负极,锌筒为正极
C.铅酸蓄电池供电时 Pb 电极上的反应为
D.铅酸蓄电池供电时电子由 Pb 电极经外电路流向 电极
【答案】B
【分析】锌锰电池属于一次电池,锌筒为负极。铅酸电池属于二次电池,电池的总反应 PbO
2
+Pb+2H SO =2PbSO +2H O,其中 Pb 为负极,反应式为:Pb-2e-+ =PbSO,PbO 为正极,反应式
2 4 4 2 4 2
为 PbO
2
+4H++2e-+ =PbSO
4
+2H
2
O,据此分析。
【解析】A.锌锰电池是不可充电电池属于一次电池,铅酸电池属于可充电电池是二次电池,A 正确;
B.锌是活泼金属失电子发生氧化反应,锌筒为负极,带铜帽的石墨棒为正极,B 错误;
C.铅酸蓄电池供电时 Pb 电极是负极,发生氧化反应,失去电子,电极反应式为:
,C 正确;
D.原电池中电子由负极经过外电路流向正极,Pb 是负极,PbO 为正极,电子由 Pb 电极经外电路流向
2
电极,D 正确;
答案选 B。
5.在一密闭容器中发生反应 ,3min 达到平衡状态, 增加了 0.6mol·L-1,
下列说法正确的是
A.0~3min,
B.在 2min 末,
C.第 4min 时, 和 表示的反应速率的值相等
D.若相同时间内, ,则这两段时间内反应速率相等
【答案】C
【解析】A.由反应方程式可知,A 呈固态,不能用 A 的浓度变化表示反应速率,A 不正确;B.反应
进行 3min 时,达到平衡状态, 增加了 0.6mol·L-1,则 ,此
速率表示反应进行 3min 内的平均速率,不等于 2min 末的速率,B 不正确;C.3min 达到平衡状态,此
时 = = ,第 4min 时反应仍保持平衡状态,所以 和 表示的反应速率的值相
/等,C 正确;D.由于 B、D 的化学计量数不等,所以 表示反应进行到不
同阶段时的反应速率,则这两段时间内反应速率不相等,D 不正确;故选 C。
6.一定温度下,向某恒容密闭容器中充入 和 ,在催化剂作用下发生反应:
,下列说法正确的是
A.使用催化剂可实现 的 100%转化
B.达到平衡状态时, 的浓度不再发生变化
C.达到平衡状态时, 与 物质的量之比为 1:1
D.以 或 O 浓度的变化均可表示反应速率,两者的数值相等
2
【答案】B
【解析】A.催化剂不能改变平衡状态,因此使用催化剂不能实现的 100%转化,A 错误;B.达到平衡
状态时正逆反应速率相等,因此 的浓度不再发生变化,B 正确;C.达到平衡状态时,由于转化率不
确定,所以 与 物质的量之比不一定为 1:1,C 错误;D.以 或 O 浓度的变化均可表示反应
2
速率,速率之比是化学计量数之比,所以根据方程式可判断两者的数值不相等,D 错误;故选 B。
7.已知工业合成氨的过程中发生 ,其中催化剂的成分有 Fe O、
3 4
Al O、KO、CaO 等。下列措施既能提高化学反应速率,又能提高 NH 产率的是
2 3 2 3
A.升高反应温度 B.充入一定量的 He
C.缩小体积来增大压强 D.调节催化剂中各物质的比例
【答案】C
【解析】A.升高反应温度可以提高速率,但正反应是放热反应,平衡左移,NH 产率降低,A 错误;B.
3
充入一定量的 He,不影响反应物浓度,不影响反应速率和平衡移动,B 错误;C.反应为气体分子减小
的反应,缩小体积来增大压强平衡右移,可以提高氨气产率,缩小体积浓度变大,可以增大反应速率,
C 正确;D.催化剂只能改变反应速率,不能改变转化率,D 错误;故选 C。
8.已知反应① 和反应② 在 T℃时的
平衡常数分别为 和 ,该温度下反应③ 的平衡常数为 ,则下
列说法正确的是
A.反应①的平衡常数
B.反应②中,增大氢气浓度,平衡正移, 增大
C.对于反应②,T℃时,
D.对于反应②,恒容时,温度升高,K 值减小,则该反应为放热反应
【答案】D
/【解析】A.反应①的平衡常数 ,故 A 错误;B.平衡常数只与温度有关,所以温度不变时
增大氢气浓度,平衡常数不变,故 B 错误;C.由盖斯定律,反应③=反应①-反应②,所以 ,故
C 错误;D.对于反应②,恒容时升高温度,K 值减小,说明升温平衡逆向移动,所以该反应为放热反
应,故 D 正确;故答案为:D。
9.已知 CH(g) +2NO (g) CO(g) +N (g) +2H O(l) ΔH < 0,NO 的平衡转化率随温度、压强的变化如图
4 2 2 2 2 2
所示,下列说法正确的是
A.X 和 Y 分别代表压强和温度
B.Y>Y
1 2
C.平衡常数:K < K < K
a b c
D.适当降低温度,NO 的平衡转化率增大
2
【答案】D
【解析】A.该反应为放热反应,升高温度,平衡逆向进行,NO 平衡转化率降低,该反应为气体物质
2
的量减少反应,增大压强,平衡正向进行,NO 平衡转化率增大,根据图像可知,X 代表温度,Y 代表
2
压强,故 A 错误;B.在温度相同时,增大压强,平衡正向进行,NO 平衡转化率增大,根据图像,推
2
出 Y>Y,故 B 错误;C.利用“放热反应,升高温度,平衡常数减小”,该反应为放热反应,三点中,
2 1
c 温度最高,平衡常数最小,故 C 错误;D.该反应为放热反应,降低温度,平衡正向移动,NO 平衡
2
转化率增大,故 D 正确;答案为 D。
10.电解法制备 的工作原理如图所示。下列说法正确的是
A.M 为电源的负极
B.阳极上的电极反应式为
/C.阴离子交换膜应能允许 通过而能阻止 的扩散
D.理论上每转移 0.1mol ,阴极上会产生 1.12L 气体
【答案】C
【分析】电解法制备 的工作原理如图所示,Fe 为电解池的阳极,M 为电源的正极,电极反应
式为 Fe-6e-+8OH-= +4H O,Pt 为电解池的阴极,N 为电源的负极,电极反应:2HO+2e-=H ↑+
2 2 2
2OH-,阴离子交换膜能允许 OH-通过而能阻止 的扩散,据此分析解题。
【解析】A.由分析可知,M 为电源的正极,A 错误;
B.由分析可知,阳极上的电极反应式为 Fe-6e-+8OH-= +4H O,B 错误;
2
C.由分析可知,负极生成氢氧根,正极需要氢氧根作为反应物,故阴离子交换膜能允许 OH-通过而能
阻止 的扩散,C 正确;
D.由分析可知,阴极电极反应为:2HO+2e-=H ↑+2OH-,根据电子守恒可知,理论上每转移 0.1mol e
2 2
-,阴极上会产生标准状况下 0.05molH 即 0.05mol×22.4L/mol=1.12L 气体,但是题干中没有标明气体状
2
态,D 错误;
故答案为:C。
二、选择题:本题共 5 小题,每小题 4 分,共 20 分。每小题有一个或两个选项符合题目要求,全部选对得
4 分,选对但不全的得 2 分,有选错的得 0 分。
11.根据如下能量关系示意图,下列说法正确的是
A.反应 中每生成 吸收 热量
B.由 的热化学方程式为:
C.反应 中反应物的总能量高于生成物的总能量
D.根据图像可知,相同条件下, 比 稳定
【答案】C
【解析】A.根据图像可知,反应物的总能量高于生成物的总能量,该反应是放热反应,每生成 1 mol
CO(g)放出 393.5 kJ 热量,A 错误;B.由图可知,1molC(s)和 0.5molO(g)转化为 1mol 的 CO(g),放出
2 2
热量为:393.5 kJ-282.9 kJ=110.6 kJ,所以 2C(s)+O(g)=2CO(g) ΔH=-221.2 kJ·mol-1 ,B 错误;C.
2
根据图像可知 为放热反应,所以反应物的总能量高于生成物的总能量,C 正确;D.
/由图可知,1molCO(g)和 0.5molO(g)的总能量大于 1molCO (g),无法判断 1moCO(g)和 1molCO (g)的能
2 2 2
量大小,则在相同条件下,无法判断 CO (g)和 CO(g)的稳定性,D 错误;故选 C。
2
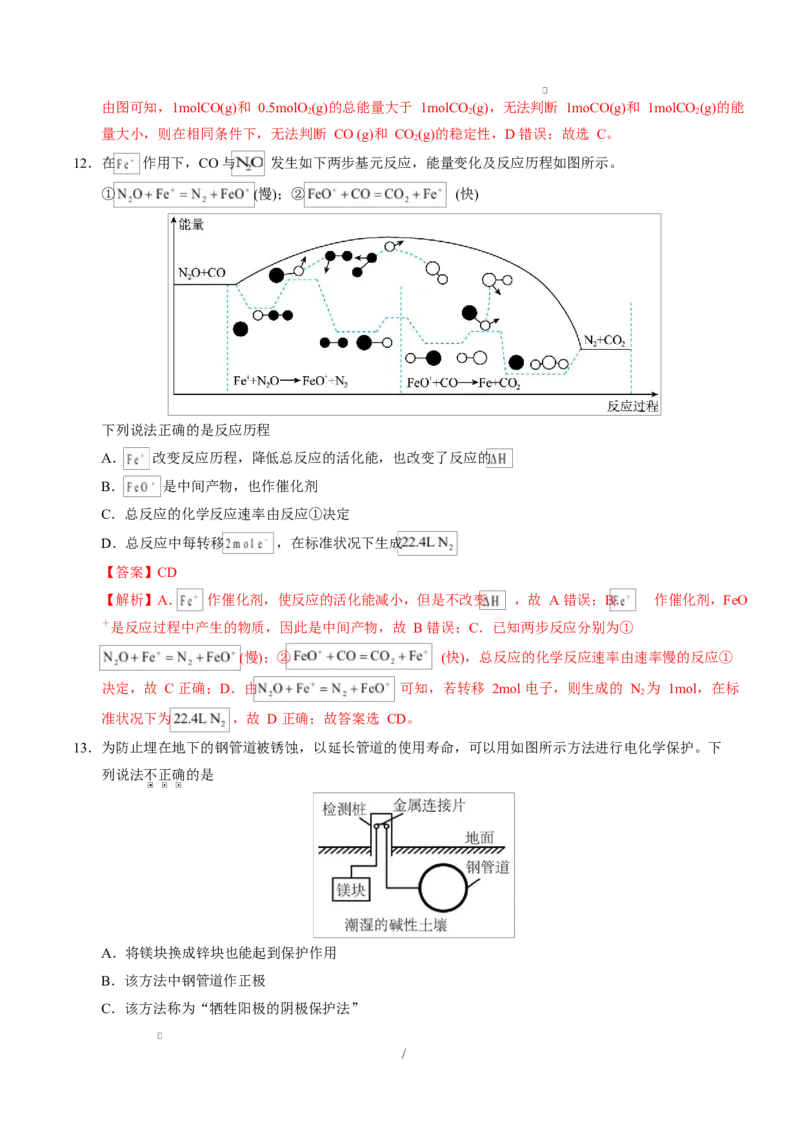
12.在 作用下,CO 与 发生如下两步基元反应,能量变化及反应历程如图所示。
① (慢);② (快)
下列说法正确的是反应历程
A. 改变反应历程,降低总反应的活化能,也改变了反应的
B. 是中间产物,也作催化剂
C.总反应的化学反应速率由反应①决定
D.总反应中每转移 ,在标准状况下生成
【答案】CD
【解析】A. 作催化剂,使反应的活化能减小,但是不改变 ,故 A 错误;B. 作催化剂,FeO
+是反应过程中产生的物质,因此是中间产物,故 B 错误;C.已知两步反应分别为①
(慢);② (快),总反应的化学反应速率由速率慢的反应①
决定,故 C 正确;D.由 可知,若转移 2mol 电子,则生成的 N 为 1mol,在标
2
准状况下为 ,故 D 正确;故答案选 CD。
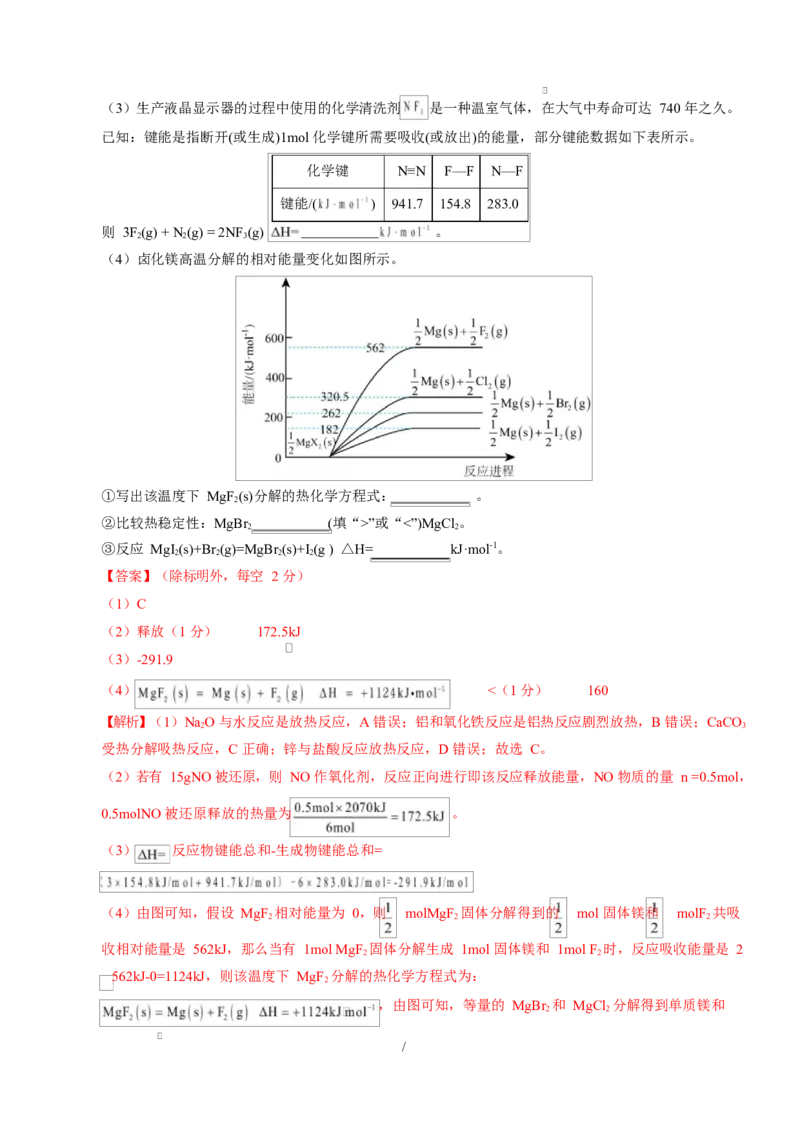
13.为防止埋在地下的钢管道被锈蚀,以延长管道的使用寿命,可以用如图所示方法进行电化学保护。下
列说法不正确的是
A.将镁块换成锌块也能起到保护作用
B.该方法中钢管道作正极
C.该方法称为“牺牲阳极的阴极保护法”
/D.镁块上发生的电极反应为
【答案】D
【解析】A.钢管道-镁块-潮湿的碱性土壤构成原电池,镁块作为负极被消耗,钢管道作为正极被保护,
换为锌块后,锌比铁活泼,因此仍是锌块作为负极被消耗,钢管道作为正极被保护,故 A 正确;
B.根据图片知钢管道-镁块-潮湿的碱性土壤构成原电池,镁比铁更活泼,可知钢管道作正极,故 B 正
确;
C.牺牲阳极的阴极保护法的是原电池原理,外加电流的阴极保护法的是电解池原理,根据图片知,该
金属防护措施采用的是牺牲阳极的阴极保护法,故 C 正确;
D.镁块作负极,电极反应: ,故 D 错误;
故答案选 D。
14.电化学“大气固碳”方法是我国科学家研究发现的,相关装置如图所示。下列说法错误的是
A.放电时电极 A 为负极,该电池可选用含水电解液
B.放电时,电极 B 上发生的反应是:
C.充电时 的移动方向是从电极 B 移向电极 A
D.放电时,电路中每通过 电子,正极区质量增加 80 g
【答案】AD
【分析】放电时,A 为负极,电极反应为 ,B 为正极,电极反应为
,充电时,A 为阴极,电极反应式为 ,B 为阳极,电极反
应为 ,据此分析。
【解析】A.放电时电极 A 为负极,电极材料为 Li,会与水反应,因此该电池只可选用无水电解液,A
错误;
B.放电时,B 为正极,电极反应为 ,B 正确;
C.充电时,阳离子移向阴极,则 Li+ 的移动方向是从电极 B 移向电极 A,C 正确;
D.当有 4mol 电子转移时,增加的质量为(3×44+4×7)g=160g,则电路中每通过 1mol 电子时,正极区质
量增加 40g,D 错误;
故选 AD。
15.如图,I 是恒压密闭容器,II 是恒容密闭容器。其它条件相同时,在 I、II 中分别加入 2molX 和 2molY,
/起始时容器体积均为 VL,发生如下反应并达到平衡:2X(?)+Y(?) aZ(g)(X、Y 状态未知)。此时 I
中 X、Y、Z 的物质的量之比为 1:3:2,则下列说法一定正确的是
A.若 X、Y 均为气态,则平衡时的压强:II>I
B.若 X 为固态,Y 为气态,则 I、II 中从起始到平衡所需时间相同
C.若 X、Y 不均为气态,则平衡时气体平均摩尔质量:I>II
D.平衡时 I 容器的体积小于 VL
【答案】B
【分析】
达到平衡时,I 中 X、Y、Z 的物质的量之比为 1∶3∶2,则 ,n=0.8, ,a=1。
【解析】A.X、Y 均为气态,正向反应气体分子数减少,II 容积不变,压强减小,则平衡时的压强:
II”“<”或“=”)。
Ⅲ.用如图所示的装置测定中和反应反应热。
/(3)从实验装置上看,还缺少 ,其能否用铁质材料替代? (填“能”或“不能”)。
(4)装置中隔热层的作用是 。
(5)实验中如果用相同体积、相同浓度的醋酸代替盐酸,测得的中和反应反应热的数值将
(填偏大、偏小或无影响)。
【答案】(每空 2 分)
(1)M
(2)>
(3)环形玻璃搅拌棒或玻璃搅拌器 不能
(4)保温,防止热量散失
(5)偏小
【解析】(1)有机物 M 经过太阳光光照可转化成 N,△H=+88.6kJ•mol-1,过程是吸热反应,M 的能量
低,说明 M 稳定。
(2) 的燃烧热 ,说明 1mol 完全燃烧生成 和
放出-akJ 能量,又因为 转化为 要吸热,则 1mol 完全燃烧生成 和
放出的热量小于-akJ, >akJ/mol。
(3)由简易量热计的构造可知该装置缺少的仪器是环形玻璃搅拌棒或玻璃搅拌器;金属材料易散热,
会使实验误差增大,所以不可以用铜质材料替代玻璃搅拌器。
(4)做中和反应反应热的测定实验要做好保温工作,隔热层的作用是减少实验过程中的热量损失。
(5)醋酸是弱电解质,在溶液中电离吸热,实验中如果用相同体积、相同浓度的醋酸代替盐酸,测得
的中和反应反应热的数值将偏小。
17.(12 分)化学反应伴随着能量变化,根据所学知识,回答下列问题:
(1)下列反应中,属于吸热反应的是___________(填字母)。
A.NaO 与水反应 B.铝和氧化铁反应
2
C.CaCO 受热分解 D.锌与盐酸反应
3
(2) 还原法可将 还原为 脱除,已知:4NH (g) + 6NO(g) = 5N (g) + 6HO(g)
3 2 2
。若有 15g NO 被还原,则该反应 (填“释放”或“吸收”)的能量
为 。
/(3)生产液晶显示器的过程中使用的化学清洗剂 是一种温室气体,在大气中寿命可达 740 年之久。
已知:键能是指断开(或生成)1mol 化学键所需要吸收(或放出)的能量,部分键能数据如下表所示。
化学键 N≡N F—F N—F
键能/( ) 941.7 154.8 283.0
则 3F(g) + N(g) = 2NF (g) 。
2 2 3
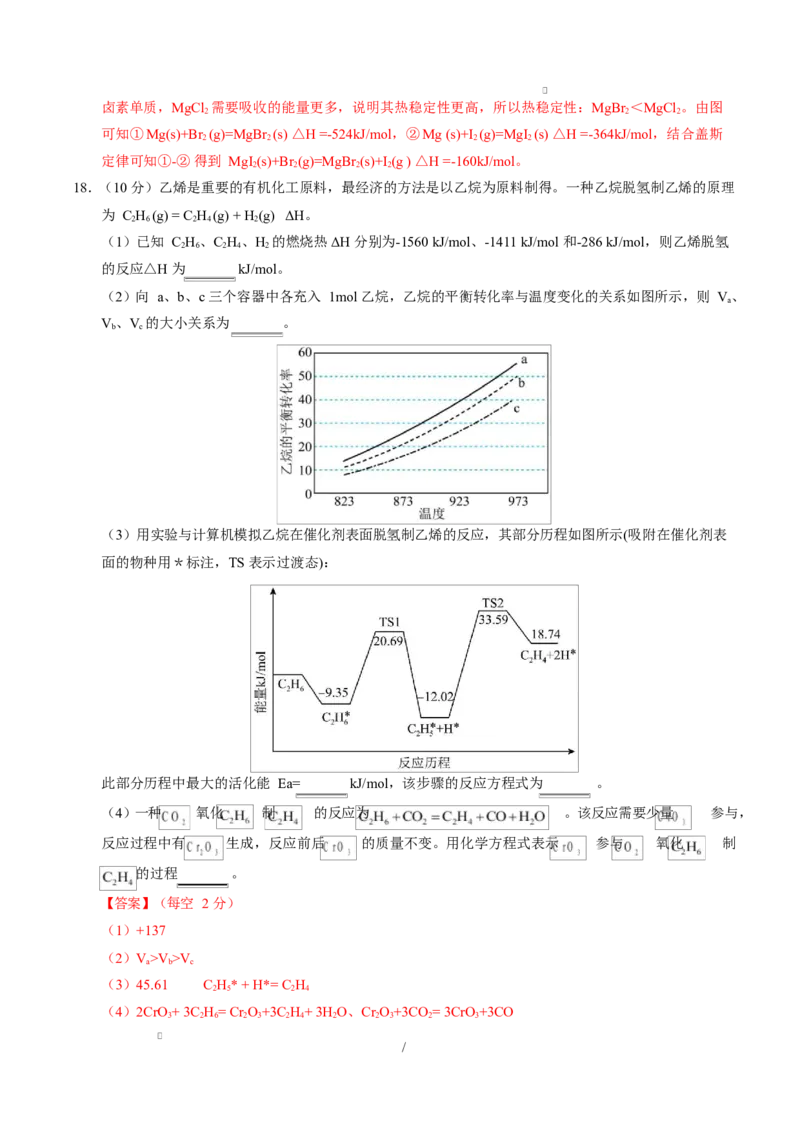
(4)卤化镁高温分解的相对能量变化如图所示。
①写出该温度下 MgF (s)分解的热化学方程式: 。
2
②比较热稳定性:MgBr (填“>”或“<”)MgCl 。
2 2
③反应 MgI (s)+Br (g)=MgBr (s)+I(g ) △H= kJ·mol-1。
2 2 2 2
【答案】(除标明外,每空 2 分)
(1)C
(2)释放(1 分) 172.5kJ
(3)-291.9
(4) <(1 分) 160
【解析】(1)NaO 与水反应是放热反应,A 错误;铝和氧化铁反应是铝热反应剧烈放热,B 错误;CaCO
2 3
受热分解吸热反应,C 正确;锌与盐酸反应放热反应,D 错误;故选 C。
(2)若有 15gNO 被还原,则 NO 作氧化剂,反应正向进行即该反应释放能量,NO 物质的量 n =0.5mol,
0.5molNO 被还原释放的热量为 。
(3) 反应物键能总和-生成物键能总和=
(4)由图可知,假设 MgF 相对能量为 0,则 molMgF 固体分解得到的 mol 固体镁和 molF 共吸
2 2 2
收相对能量是 562kJ,那么当有 1mol MgF 固体分解生成 1mol 固体镁和 1mol F 时,反应吸收能量是 2
2 2
562kJ-0=1124kJ,则该温度下 MgF 分解的热化学方程式为:
2
,由图可知,等量的 MgBr 和 MgCl 分解得到单质镁和
2 2
/卤素单质,MgCl 需要吸收的能量更多,说明其热稳定性更高,所以热稳定性:MgBr <MgCl 。由图
2 2 2
可知①Mg(s)+Br (g)=MgBr (s) △H =-524kJ/mol,②Mg (s)+I (g)=MgI (s) △H =-364kJ/mol,结合盖斯
2 2 2 2
定律可知①-②得到 MgI (s)+Br (g)=MgBr (s)+I(g ) △H =-160kJ/mol。
2 2 2 2
18.(10 分)乙烯是重要的有机化工原料,最经济的方法是以乙烷为原料制得。一种乙烷脱氢制乙烯的原理
为 C H (g) = C H (g) + H(g) ΔH。
2 6 2 4 2
(1)已知 C H、C H、H 的燃烧热ΔH 分别为-1560 kJ/mol、-1411 kJ/mol 和-286 kJ/mol,则乙烯脱氢
2 6 2 4 2
的反应△H 为 kJ/mol。
(2)向 a、b、c 三个容器中各充入 1mol 乙烷,乙烷的平衡转化率与温度变化的关系如图所示,则 V、
a
V、V 的大小关系为 。
b c
(3)用实验与计算机模拟乙烷在催化剂表面脱氢制乙烯的反应,其部分历程如图所示(吸附在催化剂表
面的物种用*标注,TS 表示过渡态):
此部分历程中最大的活化能 Ea= kJ/mol,该步骤的反应方程式为 。
(4)一种 氧化 制 的反应为 。该反应需要少量 参与,
反应过程中有 生成,反应前后 的质量不变。用化学方程式表示 参与 氧化 制
的过程 。
【答案】(每空 2 分)
(1)+137
(2)V>V >V
a b c
(3)45.61 C H* + H*= C H
2 5 2 4
(4)2CrO+ 3C H= CrO+3C H+ 3H O、Cr O+3CO = 3CrO +3CO
3 2 6 2 3 2 4 2 2 3 2 3
/【解析】(1)燃烧热是在 101 kPa 时,1 mol 物质完全燃烧生成稳定的氧化物时所放出的热量;已知 C H、
2 6
C H、H 的燃烧热ΔH 分别为-1560 kJ/mol、-1411 kJ/mol 和-286 kJ/mol,则存在:
2 4 2
①C H (g)+ O=2CO (g)+3HO(l) ΔH=-1560 kJ/mol
2 6 2 2 2
②C H (g)+3O=2CO (g)+2HO(l) ΔH=-1411kJ/mol
2 4 2 2 2
③H(g)+ O=H O(l) ΔH=-286kJ/mol
2 2 2
由盖斯定律可知,①-②-③得反应 C H (g) = C H (g) + H(g),故其ΔH=+137kJ/mol;
2 6 2 4 2
(2)反应为气体分子数增加的反应,相同条件下,增大体积利于平衡正向移动,乙烷转化率增大,结
合图可知,V>V >V;
a b c
(3)过渡态物质的总能量与反应物总能量的差值为活化能,即图中峰值越大则活化能越大,此部分历
程中最大的活化能 Ea=(33.59-(-12.02))kJ/mol=45.61kJ/mol,该步骤为 C H* 和 H*反应生成 C H,反应
2 5 2 4
方程式为 C H* + H*= C H;
2 5 2 4
(4)该反应需要少量 参与,反应过程中有 生成,反应前后 的质量不变,则 为反
应的催化剂,结合总反应可知,初始 和乙烷反应转化为 和乙烯、水, 再和二氧化碳转
化为 CO 和 ,反应历程为:2CrO+ 3C H= CrO+3C H+ 3H O、Cr O+3CO = 3CrO +3CO。
3 2 6 2 3 2 4 2 2 3 2 3
19.(14 分)某同学设计如下电化学串联装置图,反应起始从装置甲右侧打开止水夹,通入一定时间 b 气体
后,关闭止水夹,串联电化学装置亦会继续运行,可见丙装置湿润红色布条褪色,回答下列问题。
(1)甲装置中 a 通入的气体是 ,写出通入该气体一极的电极反应方程式: 。
(2)乙装置中,总反应的化学方程式是 。
(3)丙装置中使红色布条褪色的具体物质的结构式为 ,淀粉 KI 溶液中发生反应的离子方
程式: 。
(4)丁装置为电解精炼粗铜装置,当 c 极质量 (填“增加”或“减少”)12.8g 时,装置乙中产生气
体的总物质的量为 ,装置戊中电解质溶液质量减少 。
【答案】(除标明外,每空 2 分)
(1) (1 分)
(2)
/(3)
(4)增加(1 分) 0.4 mol 27g
【解析】(1)丙装置红色布条褪色,说明乙装置右管产生氯气,左管产生氢气,则甲装置 a 通入的气体是 ,该极的
电极反应反应方程式: ;
(2)乙装置为电解饱和氯化钠溶液装置,总反应的化学方程式是 ;
(3)丙装置中使红色布条褪色的具体物质的结构式为: ,淀粉 KI 溶液中发生反应的离子方程式:
;
(4)丁装置为电解精炼粗铜装置,c 极为阴极,铜离子在上面放电析出,导致 c 极质量增加,当 c 极质量增加 12.8 g 时,
即析出铜 0.2 mol,转移电子数为 ,装置乙中产生气体的总物质的量 0.4 mol,装置戊中电解质溶液质量减少 0.2
mol 氯化铜即为 27 g。
20.(12 分)随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
Ⅰ.以 和 为原料合成尿素 。
(1)有利于提高 平衡转化率的措施是 (填序号)。
A.高温低压 B.低温高压 C.高温高压
(2)研究发现,合成尿素反应分两步完成,其能量变化如下图甲所示:
第一步:
第二步:
①图中 。
②反应速率较快的是 反应(填“第一步”或“第二步”)。
Ⅱ.以 和 催化重整制备合成气: 。
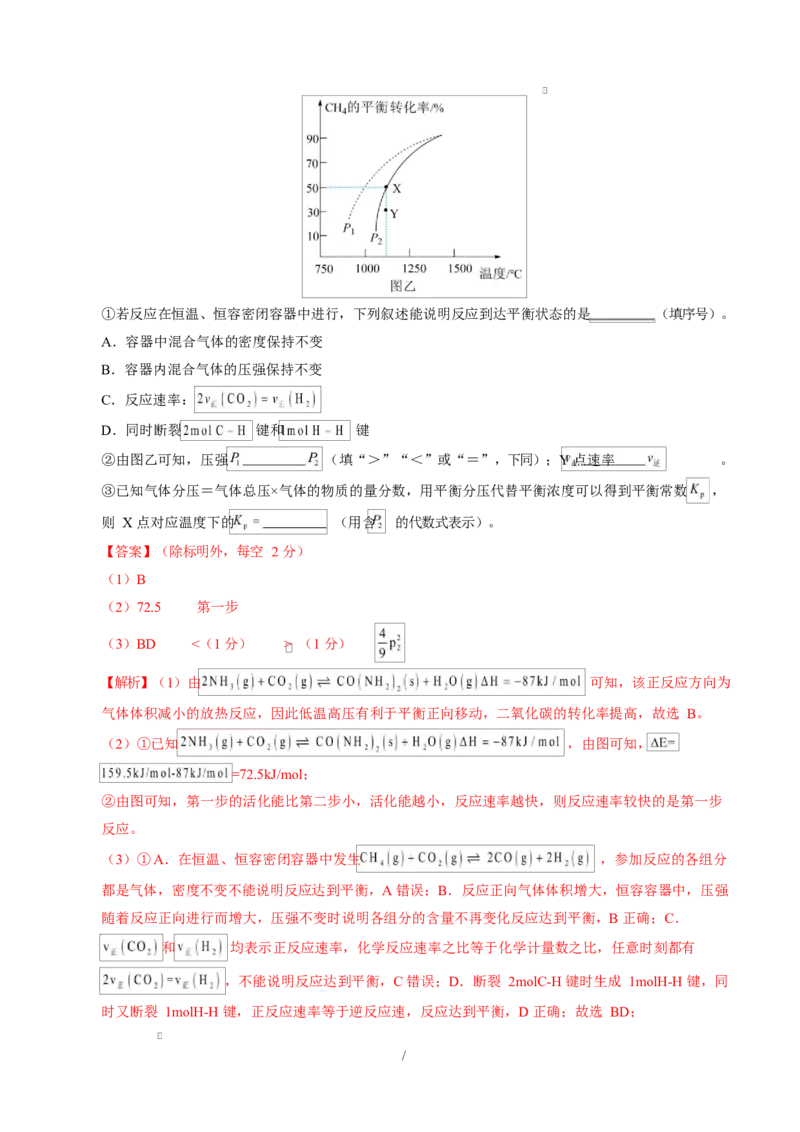
(3)在密闭容器中通入物质的量均为 的 和 ,在一定条件下发生反应
, 的平衡转化率随温度、压强的变化关系如图乙所示。
/①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是 (填序号)。
A.容器中混合气体的密度保持不变
B.容器内混合气体的压强保持不变
C.反应速率:
D.同时断裂 键和 键
②由图乙可知,压强 (填“>”“<”或“=”,下同);Y 点速率 。
③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ,
则 X 点对应温度下的 (用含 的代数式表示)。
【答案】(除标明外,每空 2 分)
(1)B
(2)72.5 第一步
(3)BD <(1 分) > (1 分)
【解析】(1)由 可知,该正反应方向为
气体体积减小的放热反应,因此低温高压有利于平衡正向移动,二氧化碳的转化率提高,故选 B。
(2)①已知 ,由图可知,
=72.5kJ/mol;
②由图可知,第一步的活化能比第二步小,活化能越小,反应速率越快,则反应速率较快的是第一步
反应。
(3)①A.在恒温、恒容密闭容器中发生 ,参加反应的各组分
都是气体,密度不变不能说明反应达到平衡,A 错误;B.反应正向气体体积增大,恒容容器中,压强
随着反应正向进行而增大,压强不变时说明各组分的含量不再变化反应达到平衡,B 正确;C.
和 均表示正反应速率,化学反应速率之比等于化学计量数之比,任意时刻都有
,不能说明反应达到平衡,C 错误;D.断裂 2molC-H 键时生成 1molH-H 键,同
时又断裂 1molH-H 键,正反应速率等于逆反应速,反应达到平衡,D 正确;故选 BD;
/② 反应正向气体体积增大,增大压强,平衡逆向移动,甲烷的转
化率减小,结合图中信息可知,pv ;
1 2 正 逆
③X 点对应温度下甲烷的平衡转化率为 50%,可列三段式:
平衡常数 K= 。
p
/