文档内容
诸暨市 2025 年 5 月高三适应性考试试题
化 学
选择题部分
相对原子质量:H 1 Li 7 C 12 N 14 O 16 F 19 Ti 48 Cl 35.5
一、选择题(本大题共16小题,每小题3分,共48分,每小题列出的四个备选项中只有一个
是符合题目要求的,不选、多选、错选均不得分)
1.下列物质属于强电解质的是
A.CH Cl B.C H NH Cl C.SO₃ D.Mg(OH)₂
3 2 5 3
2.下列表示不正确的是
A.As原子的简化电子排布式:[Ar]3d104s24p3
B.SO 2-的空间结构为: (四面体形)
3
C. 的系统命名为:2,2,5-三甲基己烷
D.苯分子中的π键:
3.化学与人类社会可持续发展息息相关。下列说法不正确的是
...
A.在质地较软的铝中加入合金元素,可以改变铝原子的排列结构,使其成为硬铝
B.煤的气化是通过化学变化将煤转化为可燃性气体的过程
C.纳米晶体是颗粒尺寸在纳米量级的晶体,其熔点随晶粒大小的减小而降低
D.等离子体是一种特殊的液体,由带电的阳离子、电子及电中性粒子的组成
4.下列实验装置使用正确的是
A.图甲装置用于趁热过滤出苯甲酸溶液中的难溶性杂质
B.图乙装置用于验证乙炔的还原性
C.图丙装置用于排出盛有KMnO 溶液的滴定管尖嘴处的气泡
4
化学试题卷 第 1 页(共8页)
D.图丁装置用于碘晶体(含NH Cl)的提纯
4
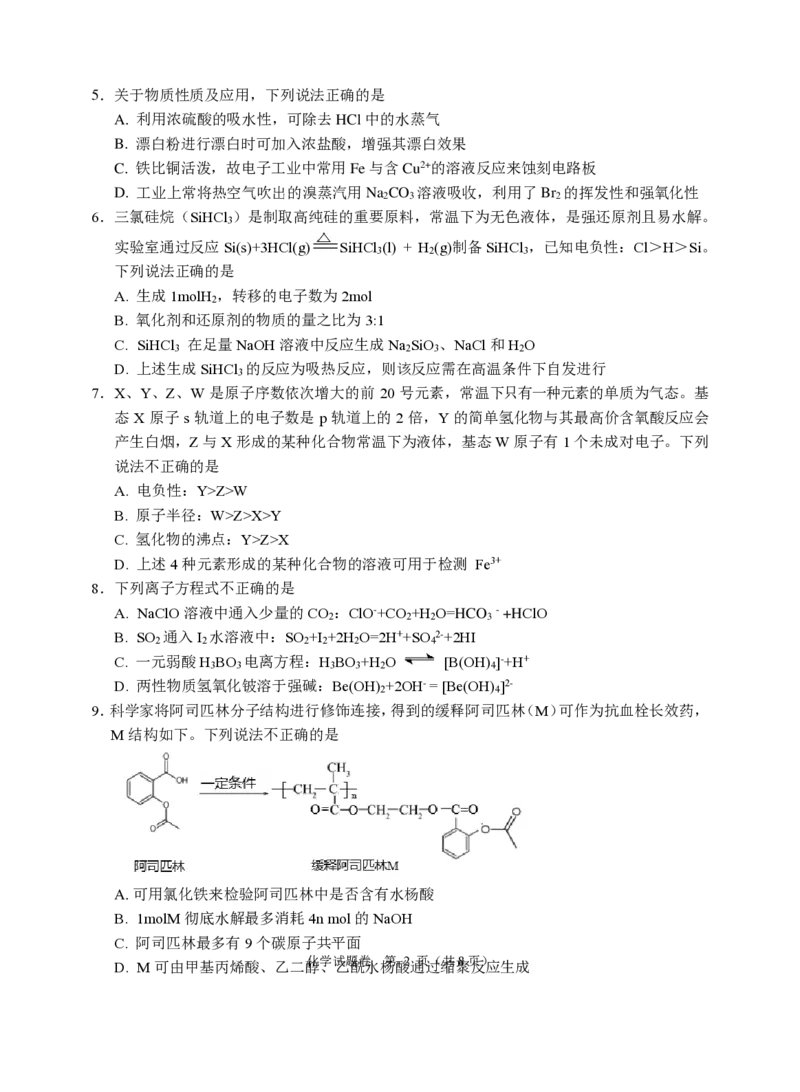
学科网(北京)股份有限公司5.关于物质性质及应用,下列说法正确的是
A. 利用浓硫酸的吸水性,可除去HCl中的水蒸气
B. 漂白粉进行漂白时可加入浓盐酸,增强其漂白效果
C. 铁比铜活泼,故电子工业中常用Fe与含Cu2+的溶液反应来蚀刻电路板
D. 工业上常将热空气吹出的溴蒸汽用Na CO 溶液吸收,利用了Br 的挥发性和强氧化性
2 3 2
6.三氯硅烷(SiHCl )是制取高纯硅的重要原料,常温下为无色液体,是强还原剂且易水解。
3
实验室通过反应Si(s)+3HCl(g) SiHCl (l) + H (g)制备SiHCl ,已知电负性:Cl>H>Si。
3 2 3
下列说法正确的是
A. 生成1molH ,转移的电子数为2mol
2
B. 氧化剂和还原剂的物质的量之比为3:1
C. SiHCl 在足量NaOH溶液中反应生成Na SiO 、NaCl和H O
3 2 3 2
D. 上述生成SiHCl 的反应为吸热反应,则该反应需在高温条件下自发进行
3
7.X、Y、Z、W 是原子序数依次增大的前 20 号元素,常温下只有一种元素的单质为气态。基
态 X 原子 s 轨道上的电子数是 p 轨道上的 2 倍,Y 的简单氢化物与其最高价含氧酸反应会
产生白烟,Z与X形成的某种化合物常温下为液体,基态W原子有1个未成对电子。下列
说法不正确的是
A. 电负性:Y>Z>W
B. 原子半径:W>Z>X>Y
C. 氢化物的沸点:Y>Z>X
D. 上述4种元素形成的某种化合物的溶液可用于检测 Fe3+
8.下列离子方程式不正确的是
A. NaClO溶液中通入少量的CO :ClO-+CO +H O=HCO - +HClO
2 2 2 3
B. SO 通入I 水溶液中:SO +I +2H O=2H++SO 2-+2HI
2 2 2 2 2 4
C. 一元弱酸H BO 电离方程:H BO +H O [B(OH) ]-+H+
3 3 3 3 2 4
D. 两性物质氢氧化铍溶于强碱:Be(OH) +2OH- = [Be(OH) ]2-
2 4
9.科学家将阿司匹林分子结构进行修饰连接,得到的缓释阿司匹林(M)可作为抗血栓长效药,
M结构如下。下列说法不正确的是
A. 可用氯化铁来检验阿司匹林中是否含有水杨酸
B. 1molM彻底水解最多消耗4n mol的NaOH
C. 阿司匹林最多有9个碳原子共平面
化学试题卷 第 2 页(共8页)
D. M可由甲基丙烯酸、乙二醇、乙酰水杨酸通过缩聚反应生成
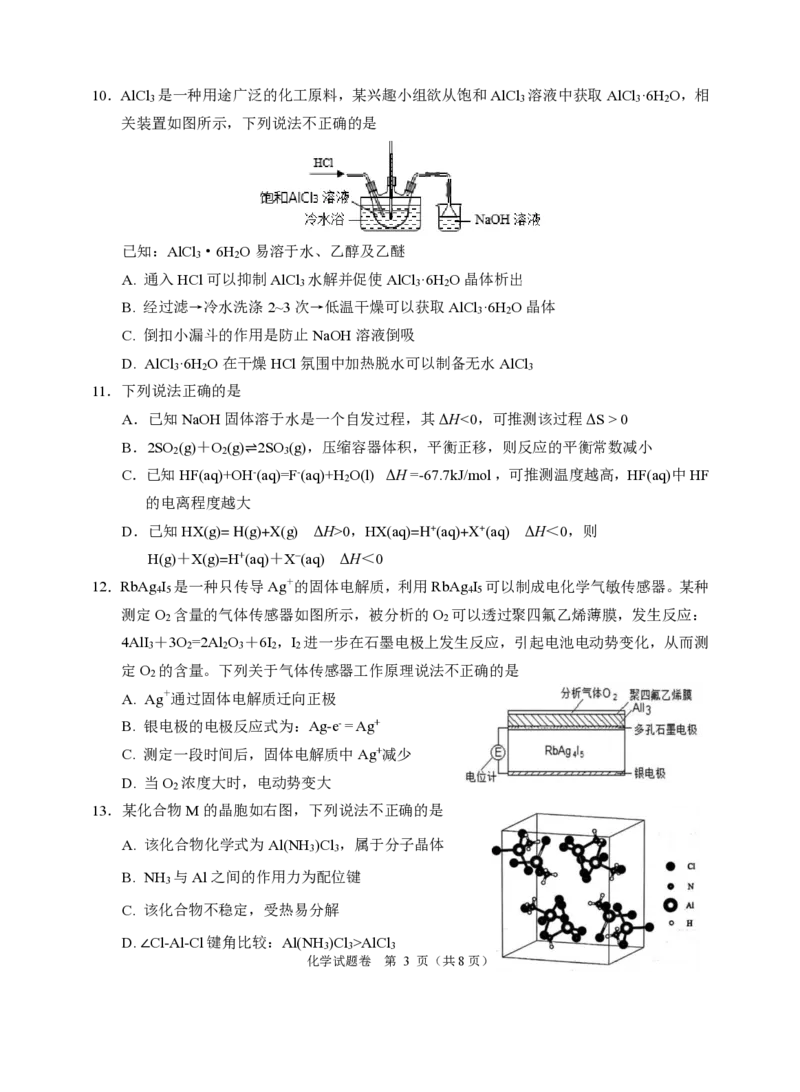
学科网(北京)股份有限公司10.AlCl 是一种用途广泛的化工原料,某兴趣小组欲从饱和AlCl 溶液中获取AlCl ·6H O,相
3 3 3 2
关装置如图所示,下列说法不正确的是
已知:AlCl ·6H O易溶于水、乙醇及乙醚
3 2
A. 通入HCl可以抑制AlCl 水解并促使AlCl ·6H O晶体析出
3 3 2
B. 经过滤→冷水洗涤2~3次→低温干燥可以获取AlCl ·6H O晶体
3 2
C. 倒扣小漏斗的作用是防止NaOH溶液倒吸
D. AlCl ·6H O在干燥HCl氛围中加热脱水可以制备无水AlCl
3 2 3
11.下列说法正确的是
A.已知NaOH固体溶于水是一个自发过程,其ΔH<0,可推测该过程ΔS > 0
B.2SO (g)+O (g)⇌2SO (g),压缩容器体积,平衡正移,则反应的平衡常数减小
2 2 3
C.已知HF(aq)+OH-(aq)=F-(aq)+H O(l) ΔH =-67.7kJ/mol ,可推测温度越高,HF(aq)中HF
2
的电离程度越大
D.已知HX(g)= H(g)+X(g) ΔH>0,HX(aq)=H+(aq)+X+(aq) ΔH<0,则
H(g)+X(g)=H+(aq)+X−(aq) ΔH<0
12.RbAg I 是一种只传导Ag+的固体电解质,利用RbAg I 可以制成电化学气敏传感器。某种
4 5 4 5
测定O 含量的气体传感器如图所示,被分析的O 可以透过聚四氟乙烯薄膜,发生反应:
2 2
4AlI +3O =2Al O +6I ,I 进一步在石墨电极上发生反应,引起电池电动势变化,从而测
3 2 2 3 2 2
定O 的含量。下列关于气体传感器工作原理说法不正确的是
2
A. Ag+通过固体电解质迁向正极
B. 银电极的电极反应式为:Ag-e- = Ag+
C. 测定一段时间后,固体电解质中Ag+减少
D. 当O 浓度大时,电动势变大
2
13.某化合物M的晶胞如右图,下列说法不正确的是
A. 该化合物化学式为Al(NH )Cl ,属于分子晶体
3 3
B. NH 与Al之间的作用力为配位键
3
C. 该化合物不稳定,受热易分解
D. ∠Cl-Al-Cl键角比较:Al(NH )Cl >AlCl
3 3 3
化学试题卷 第 3 页(共8页)
学科网(北京)股份有限公司14.COX 、POX 的水解(取代)机理不同(X 表示卤原子),具体过程如图所示。下列说法
2 3
不正确的是
A. POX 在NaOH溶液中彻底水解后可形成两种盐(不考虑阴离子的水解)
3
B. 由于键能C-Br<C-Cl,故COBr 的水解速率大于COCl
2 2
C. COX 与POX 的中心原子分别为sp2和sp3杂化
2 3
D. COX 水解过程先发生加成反应再发生消去反应
2
15.25℃,向 10mL 浓度均为 0.1mol/L 的 Na CO 和 NaHCO 混合溶液中,逐滴加入 0.1mol/L
2 3 3
的 MgCl 溶液。H CO 的电离常数 K =4.5×10-7,K =4.7×10-11; Ksp(MgCO )=4×10-6。
2 2 3 a1 a2 3
下列有关说法正确的是
A. 25℃时,MgCO 饱和溶液中,含碳微粒最主要以HCO -形式存在
3 3
B. 25℃时,0.1molMgCO 固体不可全部溶于1L0.2mol/L的盐酸中
3
C. 加入10mL的MgCl 溶液后,溶液中存在c(Na+)=c(CO 2-)+c(HCO -)+c(H CO )
2 3 3 2 3
D. 将上述MgCl 溶液加入到0.1mol/L NaHCO 溶液中无明显现象
2 3
16.三氯乙醛(CCl CHO)是无色油状液体,常用于制取农药。其纯度的测定如下(杂质不参
3
与反应)。已知:I + 2S O 2 - =2I- + S O 2-,下列说法不正确的是
2 2 3 4 6
样品 加水配成 取溶液 加适量 CHCl 3 与 用溶液调pH 加淀粉指示剂 算三氯乙
mg 100mL溶液 10mL Na 2 CO 3 HCOO-溶液 加0.1mol/L I 2 , 25mL 消耗0.02mol/L 醛纯度
NaSO, VmL
2 2 3
步骤Ⅰ 步骤Ⅱ 步骤Ⅲ 步骤Ⅳ
A. 步骤Ⅰ,需用100mL容量瓶进行配制
B. 步骤Ⅲ,发生的反应为:HCOO- + I + 2OH- 2I - + CO 2-+ H O+ H+
2 3 2
C. 步骤Ⅳ,滴定终点的现象为:加入最后半滴Na S O 溶液,锥形瓶中溶液蓝色恰好褪去,
2 2 3
且半分钟内不变色
(25×0.1-0.01×V)M×10-2
D. 三氯乙醛(摩尔质量为M g·mol-1)的纯度为
化学试题卷 第 4 页( 共 8 页 ) m
学科网(北京)股份有限公司二、非选择题(本大题共4小题,共52分)
17.(16分)卤族元素在生产生活中扮演中着重要的角色。
(1)关于VIIA族元素的描述,下列说法正确的是 。
A. 基态Br原子的核外电子排布式为[Ar]4s24p3,其价层电子数等于最外层电子数
B. 键能:HF>HCl>HBr>HI,导致酸性:HF<HCl<HBr<HI
C. 根据VSEPR模型,可推测OF 和I +空间构型均为V形
2 3
D. 已知AlCl 为分子晶体,则可推测沸点:AlI >AlBr >AlCl
3 3 3 3
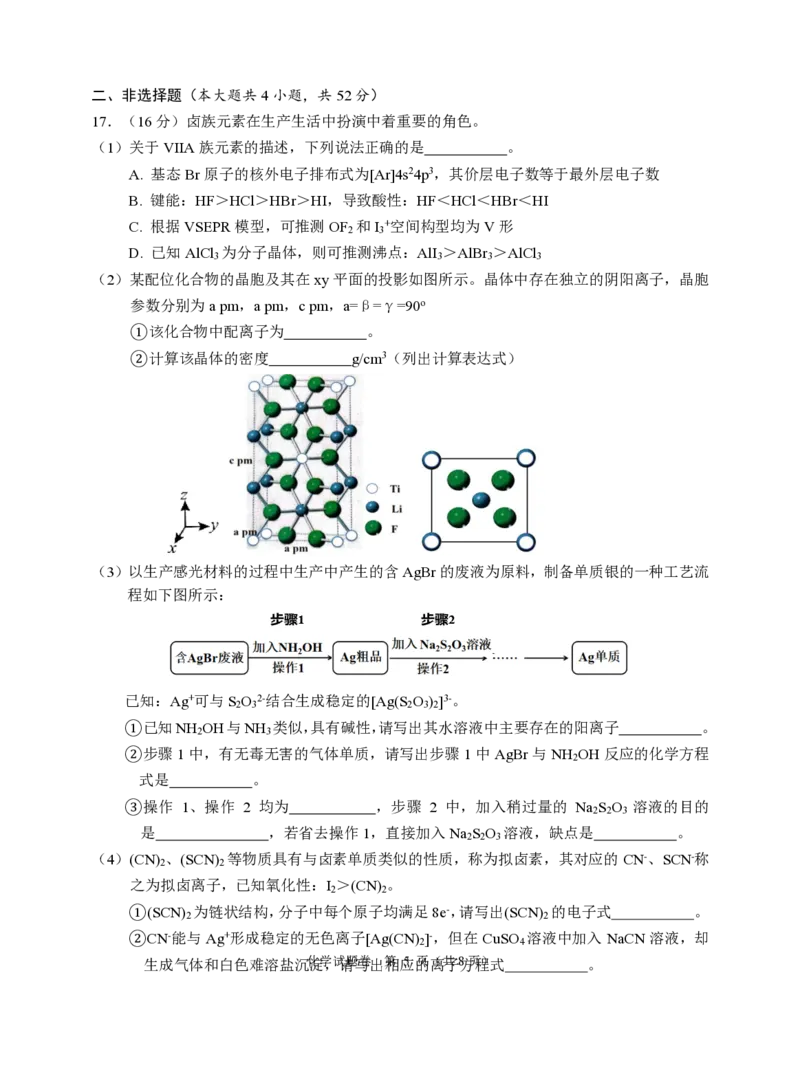
(2)某配位化合物的晶胞及其在xy平面的投影如图所示。晶体中存在独立的阴阳离子,晶胞
参数分别为a pm,a pm,c pm,a=β=γ=90o
①该化合物中配离子为 。
②计算该晶体的密度 g/cm3(列出计算表达式)
(3)以生产感光材料的过程中生产中产生的含AgBr的废液为原料,制备单质银的一种工艺流
程如下图所示:
已知:Ag+可与S O 2-结合生成稳定的[Ag(S O ) ]3-。
2 3 2 3 2
①已知NH OH与NH 类似,具有碱性,请写出其水溶液中主要存在的阳离子 。
2 3
②步骤1中,有无毒无害的气体单质,请写出步骤1中AgBr与NH OH反应的化学方程
2
式是 。
③操作 1、操作 2 均为 ,步骤 2 中,加入稍过量的 Na S O 溶液的目的
2 2 3
是 ,若省去操作1,直接加入Na S O 溶液,缺点是 。
2 2 3
(4)(CN) 、(SCN) 等物质具有与卤素单质类似的性质,称为拟卤素,其对应的 CN-、SCN-称
2 2
之为拟卤离子,已知氧化性:I >(CN) 。
2 2
①(SCN) 为链状结构,分子中每个原子均满足8e-,请写出(SCN) 的电子式 。
2 2
②CN-能与Ag+形成稳定的无色离子[Ag(CN) ]-,但在 CuSO 溶液中加入 NaCN 溶液,却
2 4
生成气体和白色难溶盐沉化淀学,试请题写卷出 第相 应5 的页(离共子8方页程)式 。
学科网(北京)股份有限公司18.(12分)甲醇(CH OH)、甲酸甲酯(HCOOCH )均是用途广泛的化工原料。请回答:
3 3
(1)二氧化碳加氢制甲醇的总反应:CO (g)+3H (g)⇌CH OH(g)+H O(g),一般认为该反应分为
2 2 3 2
两步,体系能量-反应进程如图所示:
①一定条件下,反应I能自发进行,则反应I在该条件下的
ΔS 0(填“>”、“<”或“=”)。
②下列说法不正确的是 。
A. 反应II:CO (g)+H (g)⇌CO(g)+H O(g) ΔH>0
2 2 2
B. 上述反应建立平衡后,移走CH OH,反应I、II平衡均右移
3
C. 适当升温有利于提高一定时间内反应的速率和产率
D. 催化剂能提高甲醇的平衡转化率
(2)通过电解含有甲醇的NaOH溶液可用于制备甲酸盐,生成甲酸盐的电极反应式为 。
(3)已知HCOONa的K =5.6×10-9,若电解一段时间后所得HCOONa溶液的浓度为1.8mol/L,
h
则将 HCOONa 溶液完全转化为 HCOOH 溶液需调节溶液中 H+浓度约为 ,所得甲酸
溶液进一步处理后可用于制备甲酸甲酯。
(4)甲醇催化氧化也可用于制备甲酸甲酯,其工艺过程包含以下反应:
ⅠII:2CH OH(g)+O (g)⇌HCOOCH (g)+2H O(g) ΔH=+51.2kJ•mol-1
3 2 3 2
IV:HCOOCH (g)⇌2CO(g)+2H (g) ΔH= +129.1kJ•mol-1
3 2
已知:CH OH 和 O 在催化剂表面的反应过程如下(M*表示催化剂表面的吸附物种,部
3 2
分产物已省略)
a. 氧在催化剂表面活化:O →2O*
2
b. 甲醇的化学吸附:CH OH+O*→CH O*
3 3
c. 生成弱吸附的甲醛:CH O*+O*→HCHO*
3
d. 生成甲酸甲酯并脱附:HCHO*+CH O*→HCOOCH
3 3
①步骤b是HCOOCH 合成决速步骤,在相同的温度和压强下,以一定的流速通过不同的
3
催化剂表面,反应相同时间,测得实验数据如下:
T(K) 催化剂 甲醇氧化为甲醛的转化率 甲酸甲酯的选择性
353 Au@SiO 40% 98%
2
353 Auδ+@SiO 85% 100%
2
研究表明在金离子存在的条件下,甲酸甲酯的产率明显提高,可能原因
是 。
②实际工业生产中,采用的温度约为353K,温度不能太高的理由是(不考虑催化剂活性降
低活失活) 。
19.(12 分)二氯二茂钛(M=249g/mol)为红色片状晶体,溶于水和极性溶剂,性质较稳定;
其对烯烃聚合具有很高的催化活性,以下是合成二氯二茂钛的一种方法,具体流程如下:
化学试题卷 第 6 页(共8页)
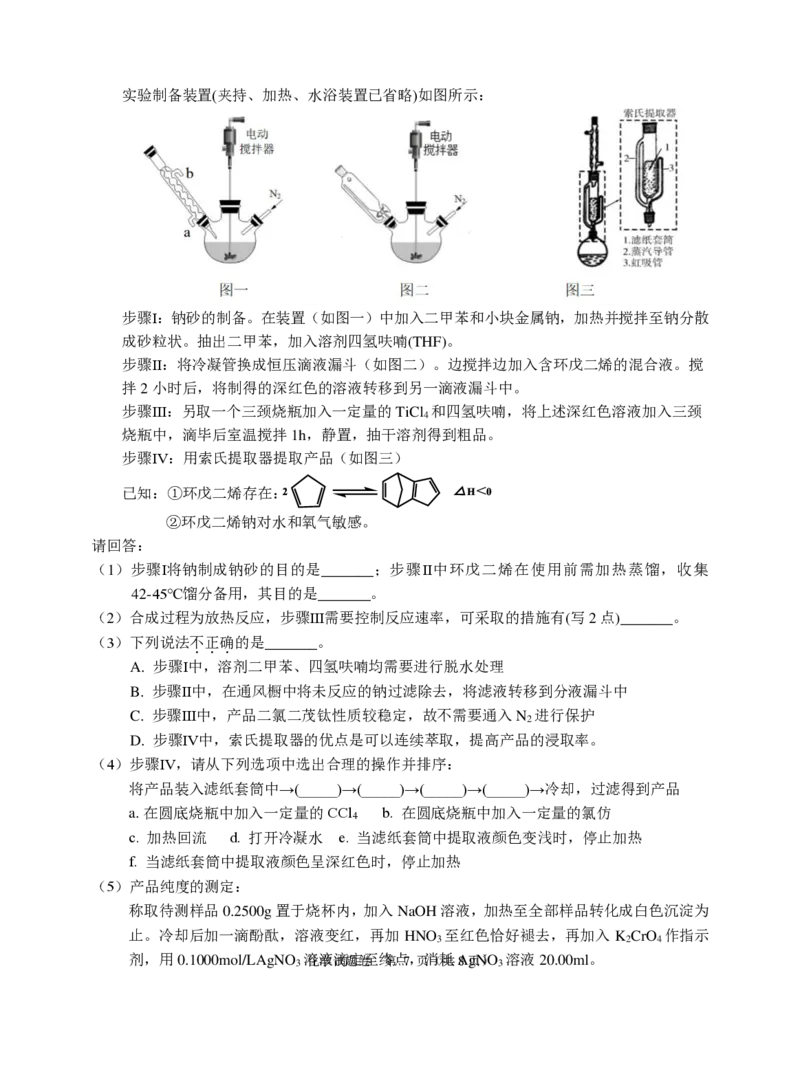
学科网(北京)股份有限公司实验制备装置(夹持、加热、水浴装置已省略)如图所示:
步骤Ⅰ:钠砂的制备。在装置(如图一)中加入二甲苯和小块金属钠,加热并搅拌至钠分散
成砂粒状。抽出二甲苯,加入溶剂四氢呋喃(THF)。
步骤Ⅱ:将冷凝管换成恒压滴液漏斗(如图二)。边搅拌边加入含环戊二烯的混合液。搅
拌2小时后,将制得的深红色的溶液转移到另一滴液漏斗中。
步骤Ⅲ:另取一个三颈烧瓶加入一定量的TiCl 和四氢呋喃,将上述深红色溶液加入三颈
4
烧瓶中,滴毕后室温搅拌1h,静置,抽干溶剂得到粗品。
步骤Ⅳ:用索氏提取器提取产品(如图三)
已知:①环戊二烯存在:
②环戊二烯钠对水和氧气敏感。
请回答:
(1)步骤Ⅰ将钠制成钠砂的目的是_______;步骤Ⅱ中环戊二烯在使用前需加热蒸馏,收集
42-45℃馏分备用,其目的是_______。
(2)合成过程为放热反应,步骤Ⅲ需要控制反应速率,可采取的措施有(写2点)_______。
(3)下列说法不正确的是_______。
...
A. 步骤Ⅰ中,溶剂二甲苯、四氢呋喃均需要进行脱水处理
B. 步骤Ⅱ中,在通风橱中将未反应的钠过滤除去,将滤液转移到分液漏斗中
C. 步骤Ⅲ中,产品二氯二茂钛性质较稳定,故不需要通入N 进行保护
2
D. 步骤Ⅳ中,索氏提取器的优点是可以连续萃取,提高产品的浸取率。
(4)步骤Ⅳ,请从下列选项中选出合理的操作并排序:
将产品装入滤纸套筒中→(_____)→(_____)→(_____)→(_____)→冷却,过滤得到产品
a. 在圆底烧瓶中加入一定量的CCl b. 在圆底烧瓶中加入一定量的氯仿
4
c. 加热回流 d. 打开冷凝水 e. 当滤纸套筒中提取液颜色变浅时,停止加热
f. 当滤纸套筒中提取液颜色呈深红色时,停止加热
(5)产品纯度的测定:
称取待测样品0.2500g置于烧杯内,加入NaOH溶液,加热至全部样品转化成白色沉淀为
止。冷却后加一滴酚酞,溶液变红,再加 HNO 至红色恰好褪去,再加入 K CrO 作指示
3 2 4
剂,用0.1000mol/LAgNO
3
溶化液学试滴题定卷至 终第点 7, 页消(耗共A8页gN)O
3
溶液20.00ml。
学科网(北京)股份有限公司已知:K =1.8×10-10,K =1.1×10-12,Ag CrO 为砖红色沉淀。
sp(AgCl) sp(Ag2CrO4) 2 4
①滴定终点现象为_______。
②计算得到二氯二茂钛的纯度为_______。
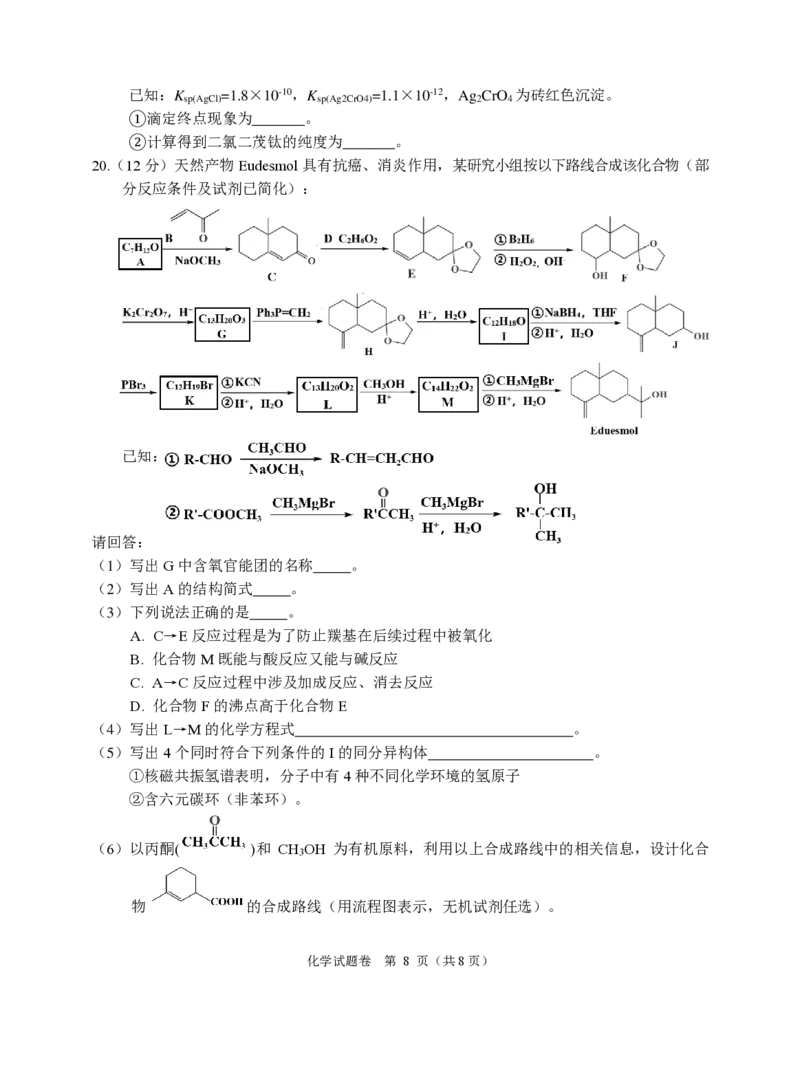
20.(12分)天然产物Eudesmol具有抗癌、消炎作用,某研究小组按以下路线合成该化合物(部
分反应条件及试剂已简化):
已知:
请回答:
(1)写出G中含氧官能团的名称 。
(2)写出A的结构简式 。
(3)下列说法正确的是 。
A. C→E反应过程是为了防止羰基在后续过程中被氧化
B. 化合物M既能与酸反应又能与碱反应
C. A→C反应过程中涉及加成反应、消去反应
D. 化合物F的沸点高于化合物E
(4)写出L→M的化学方程式 。
(5)写出4个同时符合下列条件的I的同分异构体 。
①核磁共振氢谱表明,分子中有4种不同化学环境的氢原子
②含六元碳环(非苯环)。
(6)以丙酮( )和 CH OH 为有机原料,利用以上合成路线中的相关信息,设计化合
3
物 的合成路线(用流程图表示,无机试剂任选)。
化学试题卷 第 8 页(共8页)
学科网(北京)股份有限公司