文档内容
绝密★启用前
邯郸市2025届高三年级第一次调研监测
化学
本试卷共8页,满分100分,考试用时75分钟.
注意事项:
1.答卷前,考生务必将自己的姓名、班级、考场号、座位号、考生号填写在答题卡上.
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑.如需改动,
用橡皮擦干净后,再选涂其他答案标号.回答非选择题时,将答案写在答题卡上.写在本试卷
上无效.
3.考试结束后,将本试卷和答题卡一并交回.
可能用到的相对原子质量: H 1 C12 O 16 S32 Cl35.5 Fe56 As 75 In 115
一、选择题:本题共14小题,每小题3分,共42分.在每小题给出的四个选项中,只有一项是符
合题目要求的.
1.邯郸“城南夜市”是盛夏市民消夏纳凉、品味美食的理想去处,人间烟火气,最抚凡人心,居民烟火气点亮
城市夜经济.下列关于夜市美食的说法正确的是( )
A.炸薯条用的植物油主要成分是天然有机高分子 B.煎饼主要成分(淀粉)的分子式为 C H O
6 10 5
C.甜品含有的蔗糖是还原糖 D.烤肉过程中蛋白质发生盐析
2.关于试剂保存、取用和除杂,下列表述错误的是( )
A.实验结束后剩余的金属钠不能放回原试剂瓶
B.液溴保存在棕色细口瓶中,加水液封
C.FeCl 溶液中混有FeCl 杂质,加过量铁粉除去
2 3
D.除去乙醇中混有的乙酸,加生石灰后蒸馏
3.如今高分子材料已经渗透到我们生活的方方面面,下列说法错误的是( )
A.聚乙烯分子结构中只有σ键,故聚乙烯(PE)保鲜膜形变伴随σ键旋转
B.聚对苯二甲酰对苯二胺(芳纶1414)是通过加聚反应制得的,可用作防弹装甲
C.聚乳酸在人体内可降解,可用作手术缝合线
D.聚乙炔含有共轭大π键,可用作导电材料
4.市面上一种空气净化凝胶对甲醛的去除具有明显的效果,其去除原理为
4ClO 5HCHO5CO 4HCl3H O,N 为阿伏加德罗常数的值.下列说法正确的是( )
2 2 2 A
A.13.5gClO 含有的电子数目为6.6N
2 A
B.标准状况下,吸收22.4LHCHO转移电子数目为2N
A
学科网(北京)股份有限公司C.pH1的盐酸溶液中含有H数目大于N
A
D.1mol冰中含有氢键数目为4N
A
5.有机物M是一种新型靶向药物,能够用作“分子胶水”将蛋白“黏住”,结构如图所示.下列关于M的说法错
误的是( )
A.所有原子可能共平面
B.可能发生取代反应、加成反应、缩聚反应
C.1molM 分别与Na 和NaOH反应,最多消耗二者的物质的量之比为1:2
D.环上有8种一氯代物
6.下列实验操作能够验证实验目的的是( )
选项 实验目的 实验操作
将Mg、Al用导线连接后放入NaOH溶液中,观察
A 验证Mg金属性强于Al
Al片上是否有气体生成
向浓硝酸中加入红热的木炭,观察是否有红棕色气体
B 验证碳和浓硝酸反应
生成
向NaBr溶液中滴加少量氯水,再加入淀粉KI溶
C 验证氧化性:Cl Br I
2 2 2 液,观察颜色变化
向反应后的黑色固体中加入盐酸,用K Fe(CN)
D 验证还原铁粉与水蒸气反应生成Fe O 3 6
3 4
溶液检验,观察是否有蓝色沉淀生成
A.A B.B C.C D.D
7.大苏打是一种常见的硫代硫酸盐,在酸性溶液中会迅速分解生成乳白色浑浊和有刺激性气味的气体,反应
的化学方程式为Z Q Y 2XR 2ZRQQY X Y,X、Y、Z、Q、R 分别为短周期元素,且
2 2 3 2 2
原子序数依次增大.下列说法正确的是( )
A.简单离子半径:QR ZY B.电负性:YQR X
C.简单氢化物沸点:YQ D.最高价氧化物对应水化物的酸性:QR
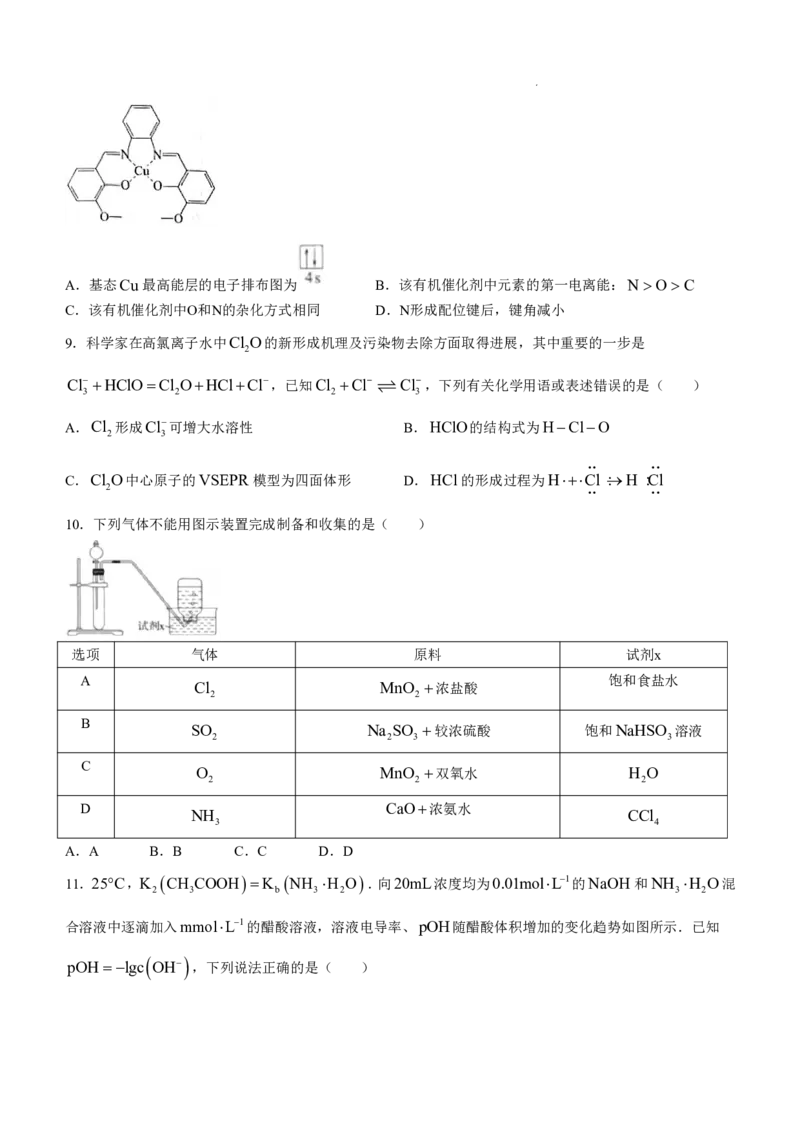
8.我国科学家成功研制出了一种铜基有机催化剂(结构如图所示),在常温常压条件下通过CO 和NO的
2 3
共还原实现选择性合成尿素和氨.下列说法正确的是( )
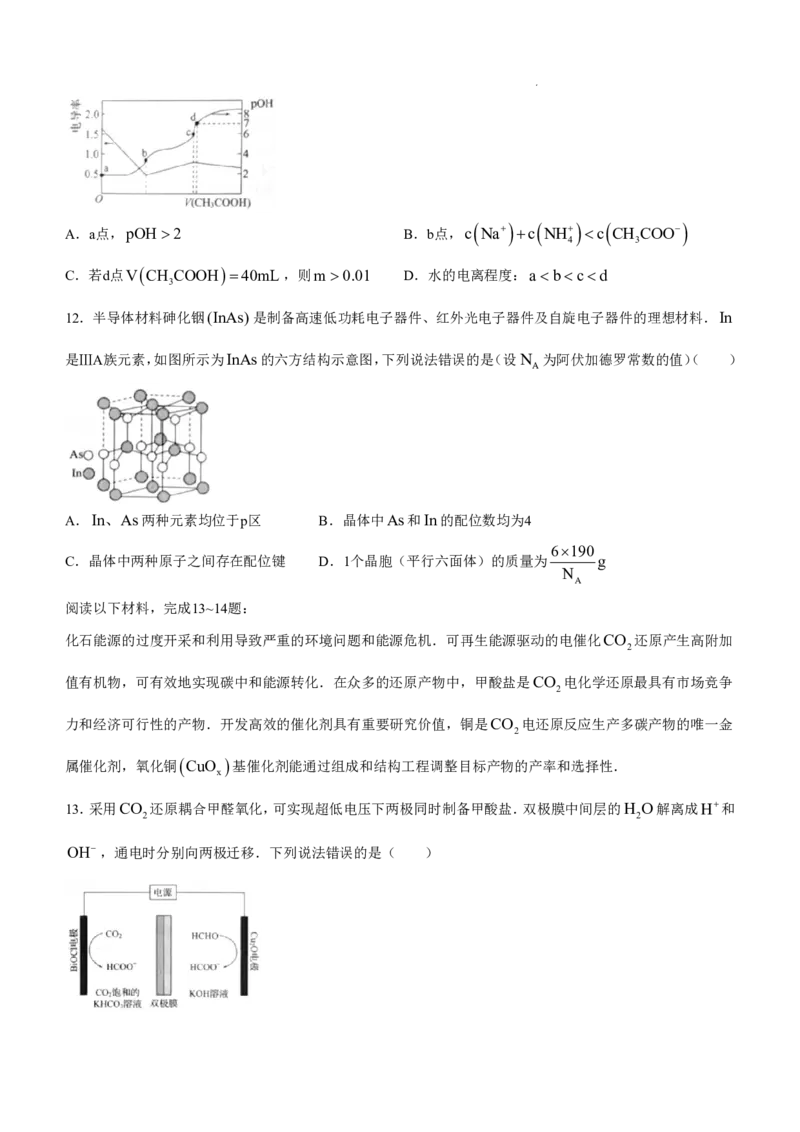
学科网(北京)股份有限公司A.基态Cu最高能层的电子排布图为 B.该有机催化剂中元素的第一电离能:N OC
C.该有机催化剂中O和N的杂化方式相同 D.N形成配位键后,键角减小
9.科学家在高氯离子水中Cl O的新形成机理及污染物去除方面取得进展,其中重要的一步是
2
Cl HClOCl OHClCl,已知Cl Cl Cl,下列有关化学用语或表述错误的是( )
3 2 2 3
A.Cl 形成Cl可增大水溶性 B.HClO的结构式为HClO
2 3
C.Cl O中心原子的VSEPR模型为四面体形 D.HCl的形成过程为HCl∶H∶Cl∶
2
10.下列气体不能用图示装置完成制备和收集的是( )
选项 气体 原料 试剂x
A 饱和食盐水
Cl MnO 浓盐酸
2 2
B
SO Na SO 较浓硫酸 饱和NaHSO 溶液
2 2 3 3
C
O MnO 双氧水 H O
2 2 2
D CaO浓氨水
NH CCl
3 4
A.A B.B C.C D.D
11.25C,K CH COOH K NH H O .向20mL浓度均为0.01molL1的NaOH和NH H O混
2 3 b 3 2 3 2
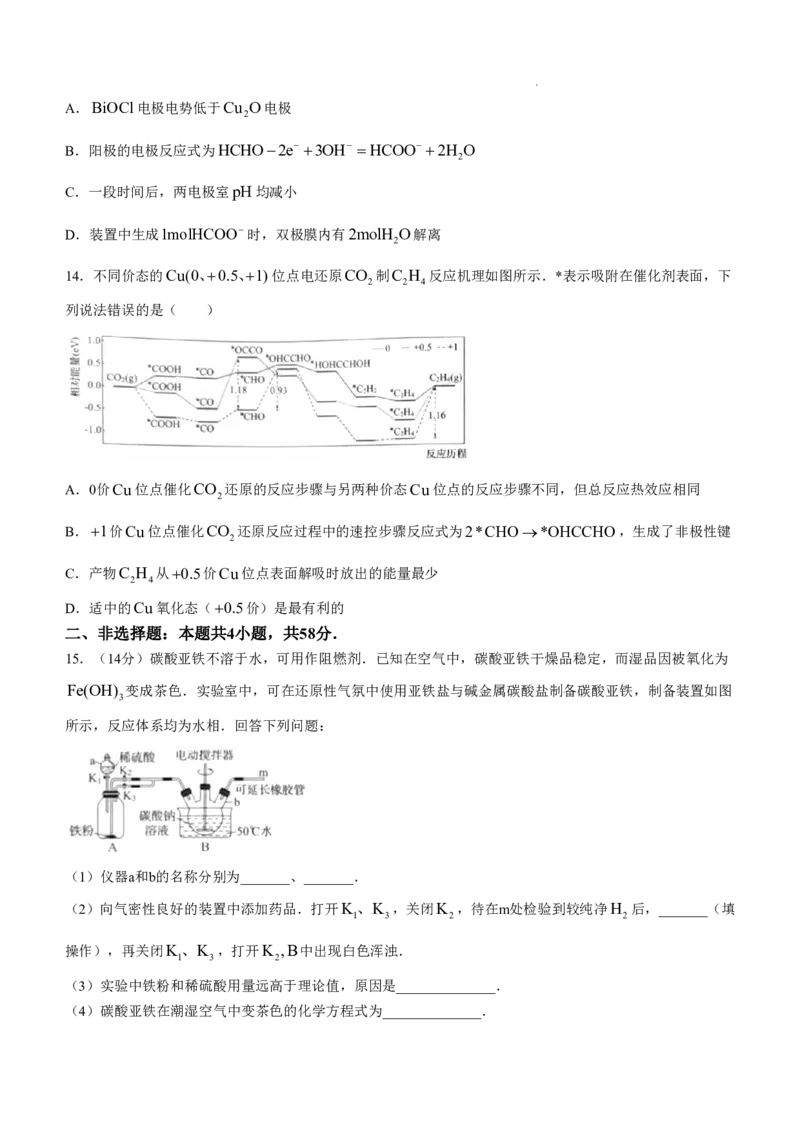
合溶液中逐滴加入mmolL1的醋酸溶液,溶液电导率、pOH随醋酸体积增加的变化趋势如图所示.已知
pOHlgc
OH
,下列说法正确的是( )
学科网(北京)股份有限公司A.a点,pOH 2 B.b点,c
Na
c
NH
c
CH
COO
4 3
C.若d点V CH COOH 40mL,则m 0.01 D.水的电离程度:a bcd
3
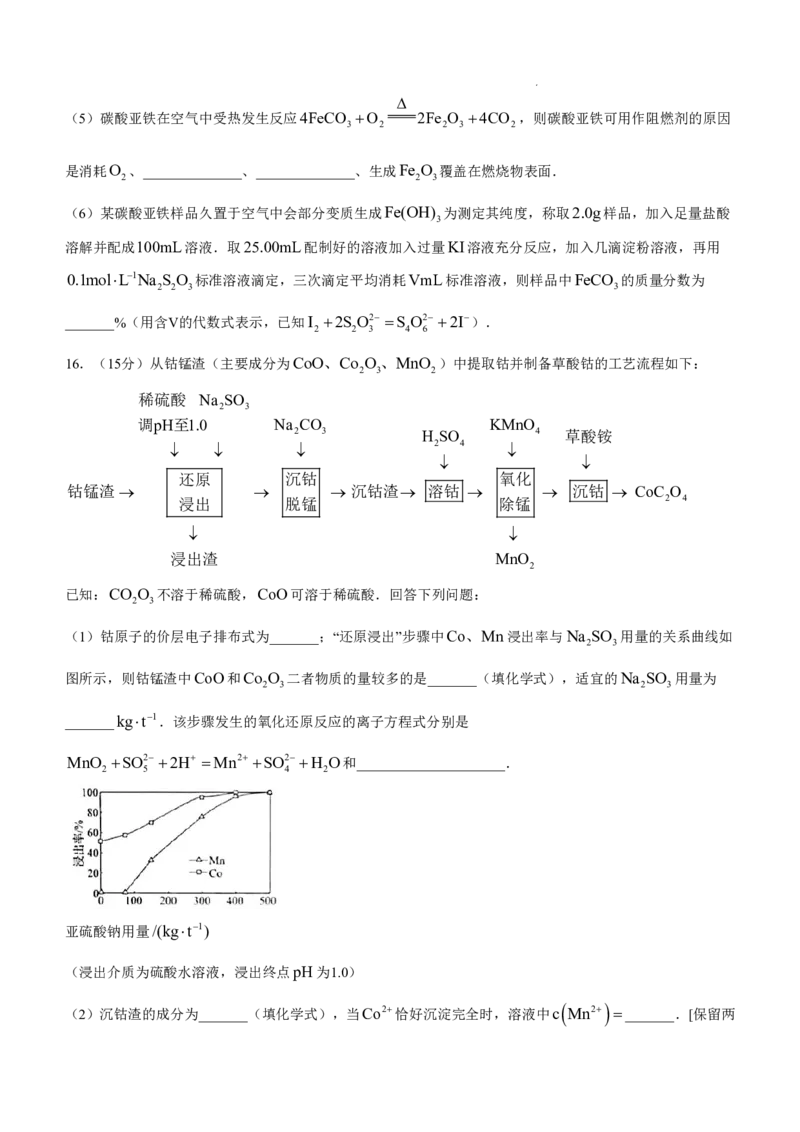
12.半导体材料砷化铟(InAs)是制备高速低功耗电子器件、红外光电子器件及自旋电子器件的理想材料.In
是ⅢA族元素,如图所示为InAs的六方结构示意图,下列说法错误的是(设N 为阿伏加德罗常数的值)( )
A
A.In、As两种元素均位于p区 B.晶体中As和In的配位数均为4
6190
C.晶体中两种原子之间存在配位键 D.1个晶胞(平行六面体)的质量为 g
N
A
阅读以下材料,完成13~14题:
化石能源的过度开采和利用导致严重的环境问题和能源危机.可再生能源驱动的电催化CO 还原产生高附加
2
值有机物,可有效地实现碳中和能源转化.在众多的还原产物中,甲酸盐是CO 电化学还原最具有市场竞争
2
力和经济可行性的产物.开发高效的催化剂具有重要研究价值,铜是CO 电还原反应生产多碳产物的唯一金
2
属催化剂,氧化铜
CuO
基催化剂能通过组成和结构工程调整目标产物的产率和选择性.
x
13.采用CO 还原耦合甲醛氧化,可实现超低电压下两极同时制备甲酸盐.双极膜中间层的H O解离成H和
2 2
OH,通电时分别向两极迁移.下列说法错误的是( )
学科网(北京)股份有限公司A.BiOCl电极电势低于Cu O电极
2
B.阳极的电极反应式为HCHO2e 3OH HCOO 2H O
2
C.一段时间后,两电极室pH均减小
D.装置中生成1molHCOO时,双极膜内有2molH O解离
2
14.不同价态的Cu(0、0.5、1) 位点电还原CO 制C H 反应机理如图所示.*表示吸附在催化剂表面,下
2 2 4
列说法错误的是( )
A.0价Cu位点催化CO 还原的反应步骤与另两种价态Cu位点的反应步骤不同,但总反应热效应相同
2
B.1价Cu位点催化CO 还原反应过程中的速控步骤反应式为2*CHO*OHCCHO,生成了非极性键
2
C.产物C H 从0.5价Cu位点表面解吸时放出的能量最少
2 4
D.适中的Cu氧化态(0.5价)是最有利的
二、非选择题:本题共4小题,共58分.
15.(14分)碳酸亚铁不溶于水,可用作阻燃剂.已知在空气中,碳酸亚铁干燥品稳定,而湿品因被氧化为
Fe(OH) 变成茶色.实验室中,可在还原性气氛中使用亚铁盐与碱金属碳酸盐制备碳酸亚铁,制备装置如图
3
所示,反应体系均为水相.回答下列问题:
(1)仪器a和b的名称分别为_______、_______.
(2)向气密性良好的装置中添加药品.打开K、K ,关闭K ,待在m处检验到较纯净H 后,_______(填
1 3 2 2
操作),再关闭K、K ,打开K ,B中出现白色浑浊.
1 3 2
(3)实验中铁粉和稀硫酸用量远高于理论值,原因是______________.
(4)碳酸亚铁在潮湿空气中变茶色的化学方程式为______________.
学科网(北京)股份有限公司
(5)碳酸亚铁在空气中受热发生反应4FeCO O 2Fe O 4CO ,则碳酸亚铁可用作阻燃剂的原因
3 2 2 3 2
是消耗O 、______________、______________、生成Fe O 覆盖在燃烧物表面.
2 2 3
(6)某碳酸亚铁样品久置于空气中会部分变质生成Fe(OH) 为测定其纯度,称取2.0g样品,加入足量盐酸
3
溶解并配成100mL溶液.取25.00mL配制好的溶液加入过量KI溶液充分反应,加入几滴淀粉溶液,再用
0.1molL1Na S O 标准溶液滴定,三次滴定平均消耗VmL标准溶液,则样品中FeCO 的质量分数为
2 2 3 3
_______%(用含V的代数式表示,已知I 2S O2 S O2 2I).
2 2 3 4 6
16.(15分)从钴锰渣(主要成分为CoO、Co O、MnO )中提取钴并制备草酸钴的工艺流程如下:
2 3 2
稀硫酸 Na SO
2 3
调pH至1.0 Na CO KMnO
2 3 H SO 4 草酸铵
2 4
还原 沉钴 氧化
钴锰渣 沉钴渣 溶钴 沉钴 CoC O
浸出 脱锰 除锰 2 4
浸出渣 MnO
2
已知:CO O 不溶于稀硫酸,CoO可溶于稀硫酸.回答下列问题:
2 3
(1)钴原子的价层电子排布式为_______;“还原浸出”步骤中Co、Mn浸出率与Na SO 用量的关系曲线如
2 3
图所示,则钴锰渣中CoO和Co O 二者物质的量较多的是_______(填化学式),适宜的Na SO 用量为
2 3 2 3
_______kgt1.该步骤发生的氧化还原反应的离子方程式分别是
MnO SO2 2H Mn2 SO2 H O和_____________________.
2 5 4 2
亚硫酸钠用量/(kgt1)
(浸出介质为硫酸水溶液,浸出终点pH为1.0)
(2)沉钴渣的成分为_______(填化学式),当Co2恰好沉淀完全时,溶液中c Mn2 _______.[保留两
学科网(北京)股份有限公司位有效数字,溶液中离子浓度105molL1时可认为沉淀完全,
K
CoCO
1.41013,K
MnCO
1.81011]
sp 3 sp 3
(3)“溶钴”时不能选用盐酸,原因是_____________________.
(4)“氧化除锰”步骤中消耗的KMnO 与生成的MnO 的物质的量之比为_______,还原性:Co2 _______
4 2
(填“>”“<”或“=”)Mn2.
17.(15分)合成气(CO和H )制醇是煤、天然气等非石油基碳资源的高值化转化的重要途径之一.已知
2
合成气制甲醇的反应为
CO(g)2H (g)CH OH(g) HakJmol1(a 0)
2 3
(1)若逆反应活化能E bkJmol1,则正反应活化能E _______kJmol1(用含a、b的代数式表
a逆 a正
示).合成气制甲醇的反应在_______(填“高温”“低温”或“任意温度”)条件下自发.
(2)向四个容积均为2L的容器中分别充入1molCO和nmolH ,n值分别为1.4、1.7、1.8、2.0时CO的平衡转
2
化率随温度变化曲线如图1所示.
①T温度下,下列表述不能说明反应达到平衡状态的是_______(填序号).
1
A.CO的消耗速率等于甲醇的生成速率
B.单位时间内,断裂HH键的数目是断裂OH键的数目的2倍
C.混合气体密度不再改变
D.混合气体平均摩尔质量不再变化
②表示n 1.8的是曲线_______,理由是_____________________.
③T温度下,投料比n(CO):n H 10:17时,反应达到平衡后混合气体中甲醇的物质的量分数
1 2
x CH OH _______%,物质的量分数平衡常数K _______.(用物质的量分数代替浓度计算平衡常数)
3 x
图1 图2
(3)科学家合成了硫化钼纳米片作催化剂,利用合成气制备多种醇.T 温度下,分别投入1molCO和2molH ,
2 2
经历tmin达到平衡,实现了80%的CO转化率和70%的甲醇选择性(如图2所示),则平均反应速率
学科网(北京)股份有限公司v
CH OH
_______gmin1(用含t的计算式表示).
3
18.(14分)吡妥布替尼(M)是一种布鲁顿氏酪氨酸激酶抑制剂,用于复发或难治性套细胞淋巴瘤患者的治
疗.M的一种合成路线如下(部分试剂和条件省略):
已知:RCOOHSOCl 2RCOCl
回答下列问题:
(1)反应①的反应类型为_______.
(2)反应②的化学方程式为______________.
(3)E的分子式为_______.
(4)C的芳香族同分异构体中,满足下列条件的有_______种.
a.苯环上有两个取代基;
O
||
b.红外光谱中没有“CO”吸收峰;
c.碱性条件下水解生成NH .
3
其中,核磁共振氢谱显示为四组峰,且峰面积之比为3:2:2:2的结构简式为_______.
(5)D中含氧官能团名称为羧基、_______,D被足量H 还原后生成的物质中有_______个手性碳原子.
2
(6)反应④中有机碱的作用是_____________________.
学科网(北京)股份有限公司