文档内容
[复习目标] 1.掌握速率、平衡图像的分析方法及类型。2.掌握实际工业生产中的陌生图像
的分析方法。
1.(2022·全国甲卷,28)金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前
生产钛的方法之一是将金红石(TiO)转化为TiCl ,再进一步还原得到钛。回答下列问题:
2 4
(1)TiO 转化为TiCl 有直接氯化法和碳氯化法。在1 000 ℃时反应的热化学方程式及其平衡
2 4
常数如下:
(ⅰ)直接氯化:TiO(s)+2Cl(g)===TiCl (g)+O(g) ΔH=+172 kJ·mol-1,K =1.0×10-2
2 2 4 2 1 p1
(ⅱ)碳氯化:TiO(s)+2Cl(g)+2C(s)===TiCl (g)+2CO(g) ΔH =-51 kJ·mol-1,K =
2 2 4 2 p2
1.2×1012 Pa
①反应2C(s)+O(g)===2CO(g)的ΔH为________ kJ·mol-1,K =__________Pa。
2 p
②碳氯化的反应趋势远大于直接氯化,其原因是______________________________。
③对于碳氯化反应:增大压强,平衡________移动(填“向左”“向右”或“不”);温度升
高,平衡转化率________(填“变大”“变小”或“不变”)。
(2)在1.0×105 Pa,将TiO 、C、Cl 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组
2 2
成比例(物质的量分数)随温度变化的理论计算结果如图所示。
①反应C(s)+CO(g)===2CO(g)的平衡常数K (1 400 ℃)=__________Pa。
2 p
②图中显示,在200 ℃平衡时TiO 几乎完全转化为TiCl ,但实际生产中反应温度却远高于
2 4
此温度,其原因是_________________________________________________________。
(3)TiO 碳氯化是一个“气-固-固”反应,有利于 TiO-C“固-固”接触的措施是
2 2
____________
_______________________________________________________________________________
。答案 (1)①-223 1.2×1014 ②碳氯化反应气体分子数增加,ΔH<0,是熵增、放热过程,
根据ΔG=ΔH-TΔS可知ΔG<0,故该反应能自发进行,而直接氯化的体系气体分子数不变
且是吸热过程,反应趋势远小于碳氯化 ③向左 变小
(2)①7.2×105 ②为了提高反应速率,在相同时间内得到更多的TiCl 产品,提高效益
4
(3)将两固体粉碎后混合,同时鼓入Cl,使固体粉末“沸腾”
2
解析 (1)①根据盖斯定律,将“反应(ⅱ)-反应(ⅰ)”得到反应2C(s)+O(g)===2CO(g),则
2
ΔH=-51 kJ·mol-1-(+172 kJ·mol-1)=-223 kJ·mol-1;则K == Pa=1.2×
p
1014 Pa;②碳氯化的反应趋势远大于直接氯化,因为碳氯化反应气体分子数增加,ΔH<0,
是熵增、放热过程,根据ΔG=ΔH-TΔS可知ΔG<0,故该反应能自发进行,而直接氯化的
体系气体分子数不变且是吸热过程,反应趋势远小于碳氯化;③对于碳氯化反应,气体分子
数增大,依据勒夏特列原理,增大压强,平衡向气体分子数减少的方向移动,即平衡向左移
动;该反应是放热反应,温度升高,平衡向吸热方向移动,即向左移动,则平衡转化率变小。
(2)①从图中可知,1 400 ℃时,体系中气体平衡组成比例CO 是0.05,TiCl 是0.35,CO是
2 4
0.6,反应C(s)+CO(g)===2CO(g)的平衡常数K (1 400 ℃)==Pa=7.2×105 Pa;②实际生
2 p
产中需要综合考虑反应的速率、产率等,以达到最佳效益,实际反应温度远高于 200 ℃,
就是为了提高反应速率,在相同时间内得到更多的TiCl 产品。
4
(3)固体颗粒越小,比表面积越大,反应接触面积越大。有利于 TiO-C“固-固”接触的措施
2
为将两者粉碎后混合,同时鼓入Cl,使固体粉末“沸腾”,增大接触面积。
2
2.[2019·北京,27(1)]氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
甲烷水蒸气催化重整是制高纯氢的方法之一。
①反应器中初始反应的生成物为H 和CO ,其物质的量之比为4∶1,甲烷和水蒸气反应的
2 2
方程式是_______________________________________________________________________。
②已知反应器中还存在如下反应:
ⅰ.CH (g)+HO(g)===CO(g)+3H(g) ΔH
4 2 2 1
ⅱ.CO(g)+HO(g)===CO(g)+H(g) ΔH
2 2 2 2
ⅲ.CH (g)===C(s)+2H(g) ΔH
4 2 3
……
ⅲ为积炭反应,利用 ΔH 和ΔH 计算 ΔH 时,还需要利用____________________反应的
1 2 3
ΔH。
③反应物投料比采用 n(H O)∶n(CH)=4∶1,大于初始反应的化学计量数之比,目的是
2 4
________(填字母)。
a.促进CH 转化
4
b.促进CO转化为CO
2
c.减少积炭生成
④用CaO可以去除CO。H 体积分数和CaO消耗率随时间变化关系如图所示。
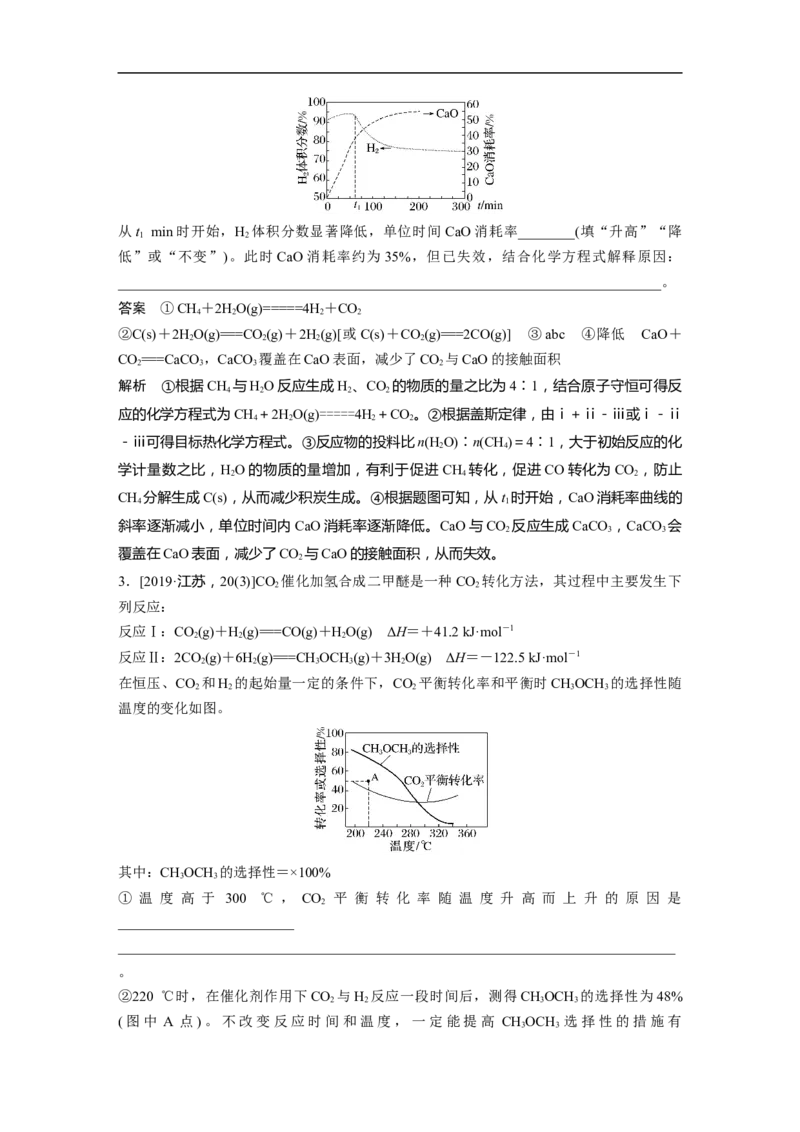
2 2从t min时开始,H 体积分数显著降低,单位时间 CaO消耗率________(填“升高”“降
1 2
低”或“不变”)。此时CaO消耗率约为35%,但已失效,结合化学方程式解释原因:
_____________________________________________________________________________。
答案 ①CH+2HO(g)=====4H+CO
4 2 2 2
②C(s)+2HO(g)===CO(g)+2H(g)[或C(s)+CO(g)===2CO(g)] ③abc ④降低 CaO+
2 2 2 2
CO===CaCO ,CaCO 覆盖在CaO表面,减少了CO 与CaO的接触面积
2 3 3 2
解析 ①根据CH 与HO反应生成H 、CO 的物质的量之比为4∶1,结合原子守恒可得反
4 2 2 2
应的化学方程式为CH+2HO(g)=====4H+CO。②根据盖斯定律,由ⅰ+ⅱ-ⅲ或ⅰ-ⅱ
4 2 2 2
-ⅲ可得目标热化学方程式。③反应物的投料比n(H O)∶n(CH)=4∶1,大于初始反应的化
2 4
学计量数之比,HO的物质的量增加,有利于促进 CH 转化,促进CO转化为CO ,防止
2 4 2
CH 分解生成C(s),从而减少积炭生成。④根据题图可知,从t 时开始,CaO消耗率曲线的
4 1
斜率逐渐减小,单位时间内CaO消耗率逐渐降低。CaO与CO 反应生成CaCO ,CaCO 会
2 3 3
覆盖在CaO表面,减少了CO 与CaO的接触面积,从而失效。
2
3.[2019·江苏,20(3)]CO 催化加氢合成二甲醚是一种CO 转化方法,其过程中主要发生下
2 2
列反应:
反应Ⅰ:CO(g)+H(g)===CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2
反应Ⅱ:2CO(g)+6H(g)===CHOCH (g)+3HO(g) ΔH=-122.5 kJ·mol-1
2 2 3 3 2
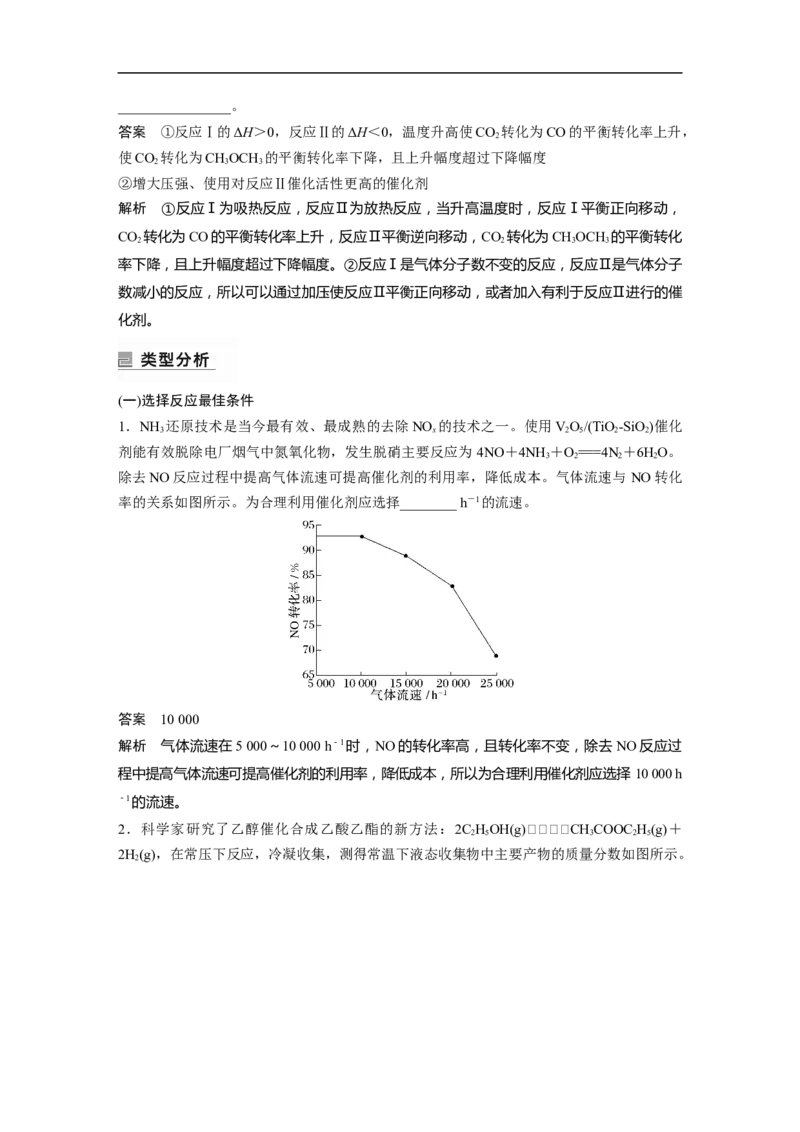
在恒压、CO 和H 的起始量一定的条件下,CO 平衡转化率和平衡时CHOCH 的选择性随
2 2 2 3 3
温度的变化如图。
其中:CHOCH 的选择性=×100%
3 3
① 温 度 高 于 300 ℃ , CO 平 衡 转 化 率 随 温 度 升 高 而 上 升 的 原 因 是
2
_________________________
_______________________________________________________________________________
。
②220 ℃时,在催化剂作用下CO 与H 反应一段时间后,测得CHOCH 的选择性为48%
2 2 3 3
(图中 A 点)。不改变反应时间和温度,一定能提高 CHOCH 选择性的措施有
3 3________________。
答案 ①反应Ⅰ的ΔH>0,反应Ⅱ的ΔH<0,温度升高使CO 转化为CO的平衡转化率上升,
2
使CO 转化为CHOCH 的平衡转化率下降,且上升幅度超过下降幅度
2 3 3
②增大压强、使用对反应Ⅱ催化活性更高的催化剂
解析 ①反应Ⅰ为吸热反应,反应Ⅱ为放热反应,当升高温度时,反应Ⅰ平衡正向移动,
CO 转化为CO的平衡转化率上升,反应Ⅱ平衡逆向移动,CO 转化为CHOCH 的平衡转化
2 2 3 3
率下降,且上升幅度超过下降幅度。②反应Ⅰ是气体分子数不变的反应,反应Ⅱ是气体分子
数减小的反应,所以可以通过加压使反应Ⅱ平衡正向移动,或者加入有利于反应Ⅱ进行的催
化剂。
(一)选择反应最佳条件
1.NH 还原技术是当今最有效、最成熟的去除NO 的技术之一。使用VO/(TiO -SiO)催化
3 x 2 5 2 2
剂能有效脱除电厂烟气中氮氧化物,发生脱硝主要反应为 4NO+4NH +O===4N +6HO。
3 2 2 2
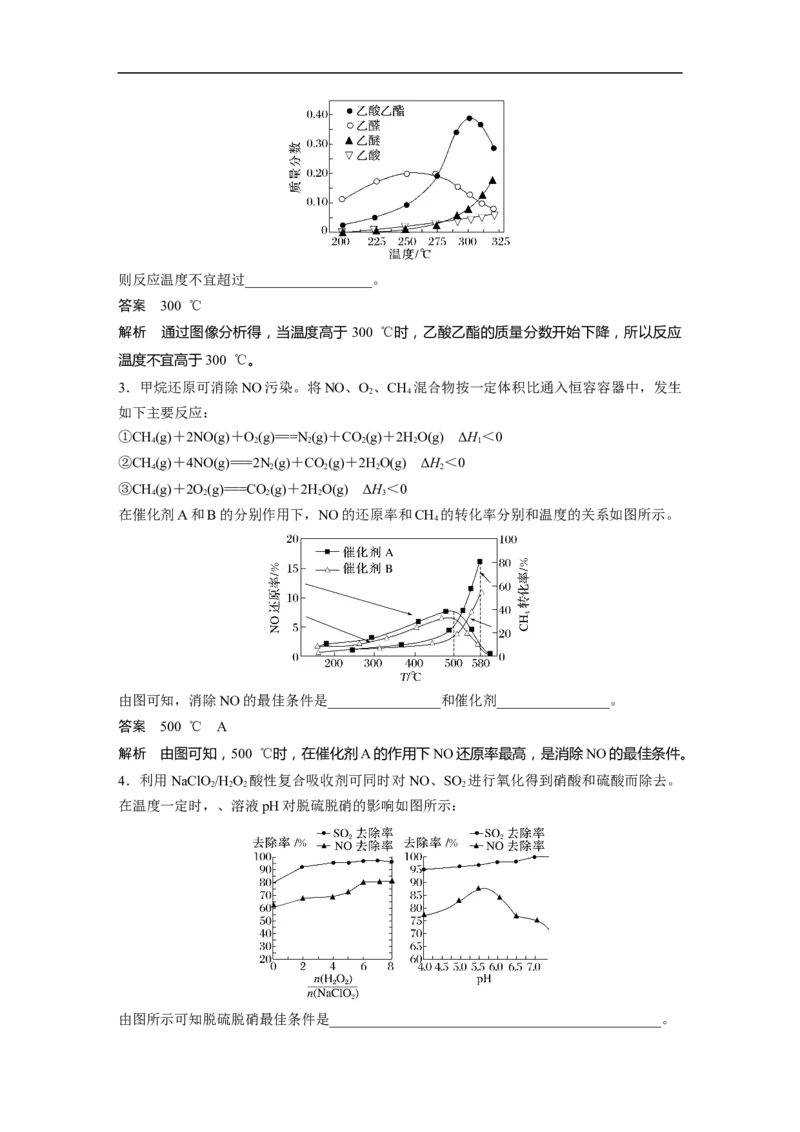
除去NO反应过程中提高气体流速可提高催化剂的利用率,降低成本。气体流速与 NO转化
率的关系如图所示。为合理利用催化剂应选择________ h-1的流速。
答案 10 000
解析 气体流速在5 000~10 000 h-1时,NO的转化率高,且转化率不变,除去NO反应过
程中提高气体流速可提高催化剂的利用率,降低成本,所以为合理利用催化剂应选择 10 000 h
-1的流速。
2.科学家研究了乙醇催化合成乙酸乙酯的新方法:2C HOH(g)CHCOOC H(g)+
2 5 3 2 5
2H(g),在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图所示。
2则反应温度不宜超过__________________。
答案 300 ℃
解析 通过图像分析得,当温度高于300 ℃时,乙酸乙酯的质量分数开始下降,所以反应
温度不宜高于300 ℃。
3.甲烷还原可消除NO污染。将NO、O 、CH 混合物按一定体积比通入恒容容器中,发生
2 4
如下主要反应:
①CH(g)+2NO(g)+O(g)===N(g)+CO(g)+2HO(g) ΔH<0
4 2 2 2 2 1
②CH(g)+4NO(g)===2N(g)+CO(g)+2HO(g) ΔH<0
4 2 2 2 2
③CH(g)+2O(g)===CO(g)+2HO(g) ΔH<0
4 2 2 2 3
在催化剂A和B的分别作用下,NO的还原率和CH 的转化率分别和温度的关系如图所示。
4
由图可知,消除NO的最佳条件是________________和催化剂________________。
答案 500 ℃ A
解析 由图可知,500 ℃时,在催化剂A的作用下NO还原率最高,是消除NO的最佳条件。
4.利用NaClO/H O 酸性复合吸收剂可同时对NO、SO 进行氧化得到硝酸和硫酸而除去。
2 2 2 2
在温度一定时,、溶液pH对脱硫脱硝的影响如图所示:
由图所示可知脱硫脱硝最佳条件是_______________________________________________。答案 pH在5.5~6.0、=6
解析 根据图示,pH在5.5~6.0、=6时NO、SO 去除率最高。
2
(二)解释曲线发生某种现象的原因
5.甲烷裂解制氢的反应为CH(g)===C(s)+2H(g) ΔH=+75 kJ·mol-1,Ni和活性炭均可作
4 2
该反应催化剂。在相同气体流量条件下,不同催化剂和进料比[]对甲烷转化率的影响如图所
示。
使用活性炭催化剂,且其他条件相同时,随着进料比的增大,甲烷的转化率逐渐增大的原因
是___________________________________________________________________________。
答案 气体流量相同,V(CH)越少,则反应越充分,转化率越大
4
6.CO 催化加氢直接合成二甲醚的反应为2CO(g)+6H(g)CHOCH (g)+3HO(g) ΔH
2 2 2 3 3 2
=-122.54 kJ·mol-1。有时还会发生副反应:CO(g)+H(g)CO(g)+HO(g) ΔH=+41.2
2 2 2
kJ·
mol-1,其他条件相同时,反应温度对CO 平衡总转化率及反应2.5小时的CO 实际总转化
2 2
率影响如图1所示;反应温度对二甲醚的平衡选择性及反应2.5小时的二甲醚实际选择性影
响如图2所示。(已知:CHOCH 的选择性=×100%)
3 3(1)图 1 中,温度高于 290 ℃,CO 平衡总转化率随温度升高而上升的原因可能是
2
____________
_______________________________________________________________________________
。
(2)图2中,在240~300 ℃范围内,相同温度下,二甲醚的实际选择性高于其平衡值,从化
学反应速率的角度解释原因:_________________________________________________。
答案 (1)温度高于290 ℃,随着温度升高,CO(g)+H(g)CO(g)+HO(g)平衡向右移动
2 2 2
的程度大于2CO(g)+6H(g)CHOCH (g)+3HO(g)平衡向左移动的程度,使CO 的平衡
2 2 3 3 2 2
总转化率上升 (2)CO 催化加氢直接合成二甲醚的反应活化能较低,而合成二甲醚时的副反
2
应CO(g)+H(g)CO(g)+HO(g)活化能较高,所以二甲醚的实际选择性高于其平衡值
2 2 2
7.甲基环己烷催化脱氢( )是石油工业制氢常见方法,以 Ni-
Cu为催化剂,固定反应温度为650 K,以氮气为载气,在不同载气流速情况下,甲基环己
烷 脱 氢 转 化 率 如 图 所 示 , b 点 转 化 率 能 与 a 点 保 持 相 当 的 原 因 是
____________________________。
答案 a点载气流速较小,甲基环己烷的浓度较大,其在催化剂表面吸附及发生脱氢反应的
百分率较小,故其转化率较小;适当加快载气流速可以减小反应物的浓度,使反应物在催化
剂表面吸附及发生脱氢反应的百分率变大,故甲基环己烷转化率随载气流速适当加快而提高;
b点载气流速过快,会使甲基环己烷在催化剂表面的反应时间减少,导致甲基环己烷转化率
降低,因此,b点转化率能与a点保持相当
8.工业上用 SiO 和焦炭高温下反应制得粗硅,再经如下 2 步反应制得精硅:Si(s)+
2
3HCl(g)===
SiHCl (g)+H(g) ΔH=-141.8 kJ·mol-1,SiHCl (g)+H(g)===Si(s)+3HCl(g),反应过程中
3 2 3 2
可能会生成SiCl 。
4
如图所示,当>3,SiHCl 平衡产率减小的原因是_______________________________。
3答案 SiHCl 参与了其他的反应,导致平衡体系内SiHCl 浓度降低,产率降低
3 3
1.工业上可以通过硫化氢分解制得H 和硫蒸气,其中HS气体的平衡转化率与温度、压强
2 2
的关系如图所示。
(1)由图可知,2H(g)+S(g)2HS(g) ΔH________(填“>”或“<”)0。
2 2 2
(2) 图 中 压 强 (p 、 p 、 p) 的 大 小 顺 序 为 ______________________ , 理 由 是
1 2 3
___________________
_______________________________________________________________________________
。
答案 (1)< (2)p>p>p 增大压强,2HS(g)2H(g)+S(g)平衡逆向移动,HS气体的平
3 2 1 2 2 2 2
衡转化率降低
2.CO 催化(固体催化剂)加氢合成甲烷
2
主反应:CO(g)+4H(g)CH(g)+2HO(g) ΔH=-165 kJ·mol-1
2 2 4 2 1
副反应:CO(g)+H(g)CO(g)+HO(g) ΔH=+41.1 kJ·mol-1
2 2 2 2
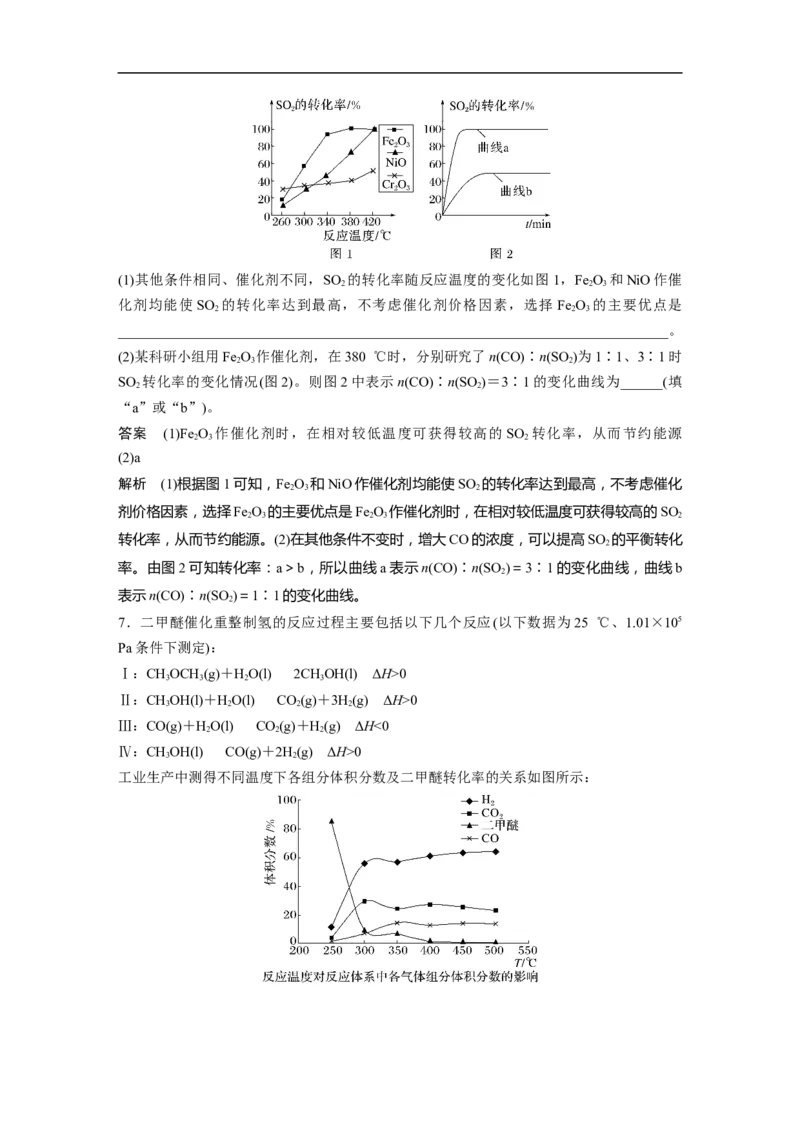
在不同催化剂条件下反应相同时间,测得 CO 转化率和生成 CH 选择性[CH 选择性=
2 4 4
×100%]随温度变化的影响如图所示。对比上述三种催化剂的催化性能,工业上选择的催化剂是Ni-20CeO/MCM-41,其使用
2
的合适温度为________(填字母) ℃左右。
A.300 B.340
C.380 D.420
当温度高于 400 ℃时,CO 转化率和生成 CH 选择性均有所下降,其原因可能是
2 4
___________________________________________________________________________(答出
一点即可)。
答案 C CO 甲烷化为放热反应,升温,该反应受到抑制;催化剂活性降低(催化剂表面积
2
碳);发生了其他副反应(甲烷水蒸气重整等)(任写一条即可)
解析 据图可知在使用Ni-20CeO/MCM-41催化剂、温度为380 ℃时CO 转化率和生成
2 2
CH 选择性均较高,故选C。
4
3.2021年9月24日,我国科学家在《Science》上发表论文《无细胞化学酶法从二氧化碳
合成淀粉》,代表着人类人工合成淀粉领域的重大颠覆性和原创性突破。该实验方法首先将
CO 催化还原为CHOH。探究CHOH合成反应的化学平衡影响因素,有利于提高 CHOH
2 3 3 3
的产率。CO 和H 在某种催化剂作用下可同时发生以下两个反应:
2 2
Ⅰ.CO (g)+3H(g)CHOH(g)+HO(g) ΔH=-48.5 kJ·mol-1
2 2 3 2
Ⅱ.2CO (g)+5H(g)C H(g)+4HO(g) ΔH=+37.1 kJ·mol-1
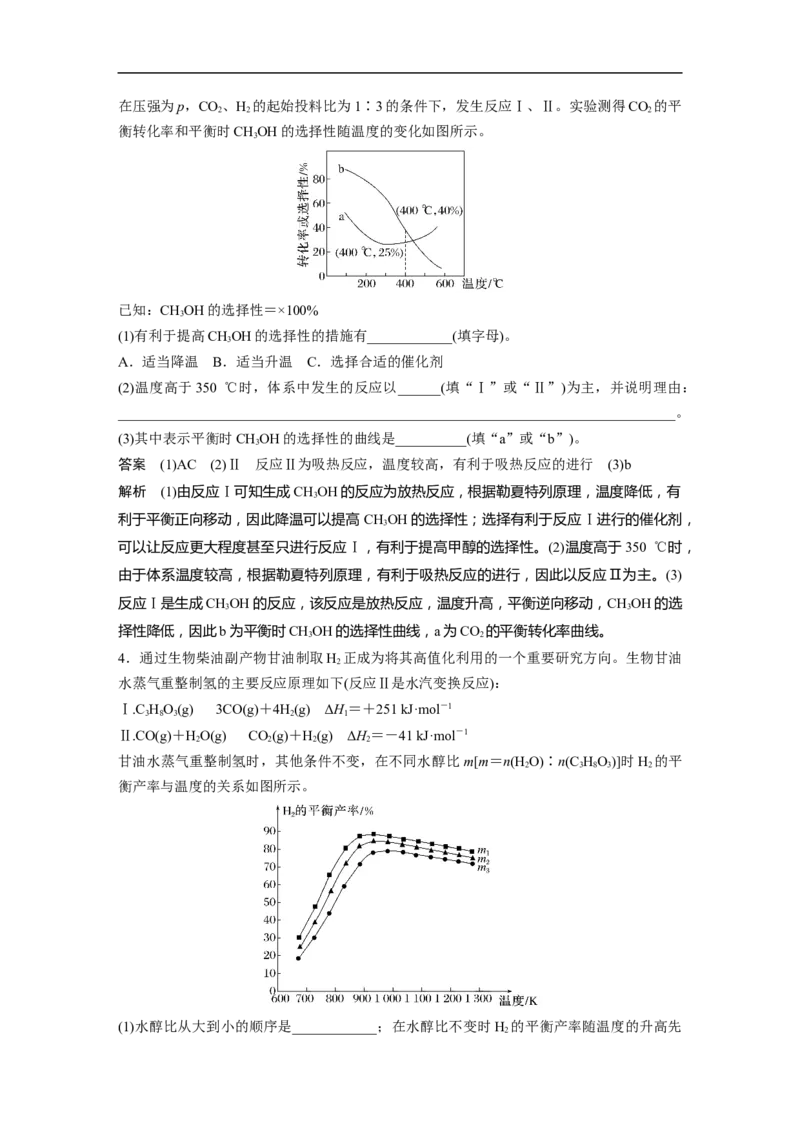
2 2 2 2 2在压强为p,CO、H 的起始投料比为1∶3的条件下,发生反应Ⅰ、Ⅱ。实验测得CO 的平
2 2 2
衡转化率和平衡时CHOH的选择性随温度的变化如图所示。
3
已知:CHOH的选择性=×100%
3
(1)有利于提高CHOH的选择性的措施有____________(填字母)。
3
A.适当降温 B.适当升温 C.选择合适的催化剂
(2)温度高于350 ℃时,体系中发生的反应以______(填“Ⅰ”或“Ⅱ”)为主,并说明理由:
_______________________________________________________________________________。
(3)其中表示平衡时CHOH的选择性的曲线是__________(填“a”或“b”)。
3
答案 (1)AC (2)Ⅱ 反应Ⅱ为吸热反应,温度较高,有利于吸热反应的进行 (3)b
解析 (1)由反应Ⅰ可知生成CHOH的反应为放热反应,根据勒夏特列原理,温度降低,有
3
利于平衡正向移动,因此降温可以提高CHOH的选择性;选择有利于反应Ⅰ进行的催化剂,
3
可以让反应更大程度甚至只进行反应Ⅰ,有利于提高甲醇的选择性。(2)温度高于350 ℃时,
由于体系温度较高,根据勒夏特列原理,有利于吸热反应的进行,因此以反应Ⅱ为主。(3)
反应Ⅰ是生成CHOH的反应,该反应是放热反应,温度升高,平衡逆向移动,CHOH的选
3 3
择性降低,因此b为平衡时CHOH的选择性曲线,a为CO 的平衡转化率曲线。
3 2
4.通过生物柴油副产物甘油制取H 正成为将其高值化利用的一个重要研究方向。生物甘油
2
水蒸气重整制氢的主要反应原理如下(反应Ⅱ是水汽变换反应):
Ⅰ.C HO(g)3CO(g)+4H(g) ΔH=+251 kJ·mol-1
3 8 3 2 1
Ⅱ.CO(g)+HO(g)CO(g)+H(g) ΔH=-41 kJ·mol-1
2 2 2 2
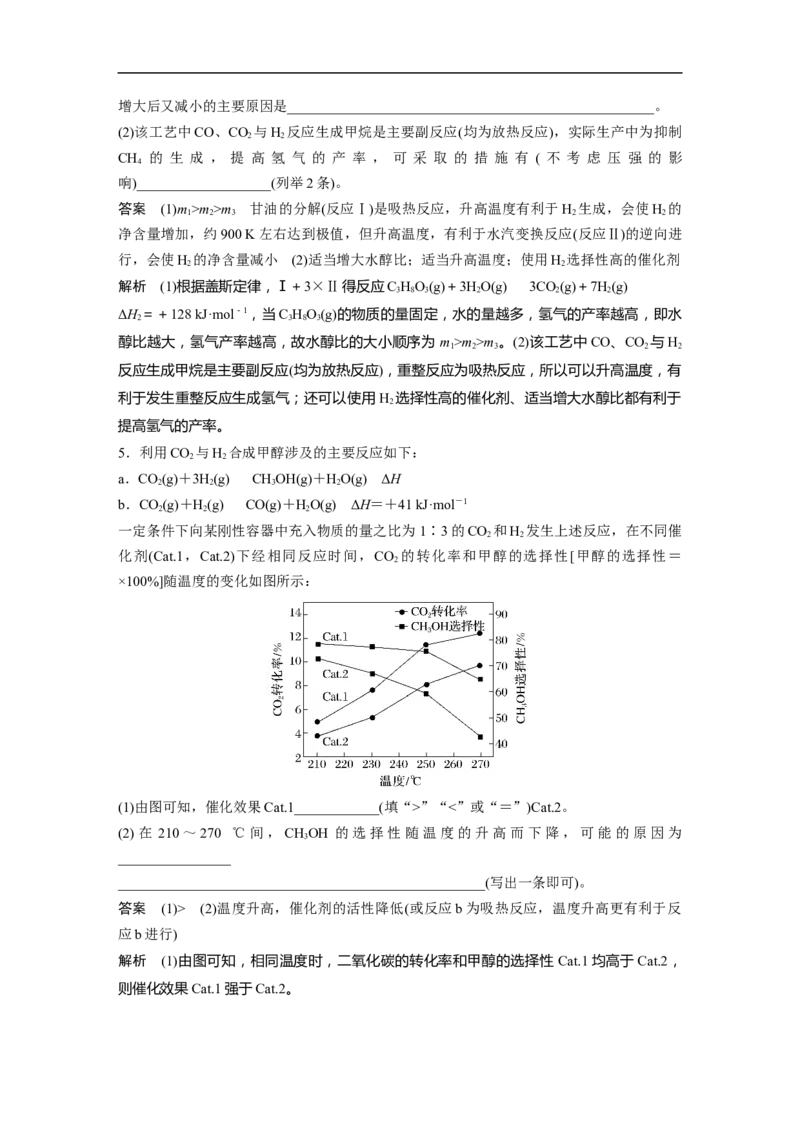
甘油水蒸气重整制氢时,其他条件不变,在不同水醇比m[m=n(H O)∶n(C HO)]时H 的平
2 3 8 3 2
衡产率与温度的关系如图所示。
(1)水醇比从大到小的顺序是____________;在水醇比不变时H 的平衡产率随温度的升高先
2增大后又减小的主要原因是____________________________________________________。
(2)该工艺中CO、CO 与H 反应生成甲烷是主要副反应(均为放热反应),实际生产中为抑制
2 2
CH 的 生 成 , 提 高 氢 气 的 产 率 , 可 采 取 的 措 施 有 ( 不 考 虑 压 强 的 影
4
响)___________________(列举2条)。
答案 (1)m>m>m 甘油的分解(反应Ⅰ)是吸热反应,升高温度有利于H 生成,会使H 的
1 2 3 2 2
净含量增加,约900 K左右达到极值,但升高温度,有利于水汽变换反应(反应Ⅱ)的逆向进
行,会使H 的净含量减小 (2)适当增大水醇比;适当升高温度;使用H 选择性高的催化剂
2 2
解析 (1)根据盖斯定律,Ⅰ+3×Ⅱ得反应C HO(g)+3HO(g)3CO(g)+7H(g)
3 8 3 2 2 2
ΔH =+128 kJ·mol-1,当C HO(g)的物质的量固定,水的量越多,氢气的产率越高,即水
2 3 8 3
醇比越大,氢气产率越高,故水醇比的大小顺序为 m>m>m 。(2)该工艺中CO、CO 与H
1 2 3 2 2
反应生成甲烷是主要副反应(均为放热反应),重整反应为吸热反应,所以可以升高温度,有
利于发生重整反应生成氢气;还可以使用 H 选择性高的催化剂、适当增大水醇比都有利于
2
提高氢气的产率。
5.利用CO 与H 合成甲醇涉及的主要反应如下:
2 2
a.CO(g)+3H(g)CHOH(g)+HO(g) ΔH
2 2 3 2
b.CO(g)+H(g)CO(g)+HO(g) ΔH=+41 kJ·mol-1
2 2 2
一定条件下向某刚性容器中充入物质的量之比为1∶3的CO 和H 发生上述反应,在不同催
2 2
化剂(Cat.1,Cat.2)下经相同反应时间,CO 的转化率和甲醇的选择性[甲醇的选择性=
2
×100%]随温度的变化如图所示:
(1)由图可知,催化效果Cat.1____________(填“>”“<”或“=”)Cat.2。
(2)在 210~270 ℃间,CHOH 的选择性随温度的升高而下降,可能的原因为
3
________________
____________________________________________________(写出一条即可)。
答案 (1)> (2)温度升高,催化剂的活性降低(或反应b为吸热反应,温度升高更有利于反
应b进行)
解析 (1)由图可知,相同温度时,二氧化碳的转化率和甲醇的选择性 Cat.1均高于Cat.2,
则催化效果Cat.1强于Cat.2。专题强化练
1.研究碳及其化合物的资源化利用具有重要的意义。已知下列热化学方程式:
反应Ⅰ:CO(g)+4H(g)CH(g)+2HO(g) ΔH=-164.9 kJ·mol-1
2 2 4 2 1
反应Ⅱ:CO(g)+H(g)CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2 2
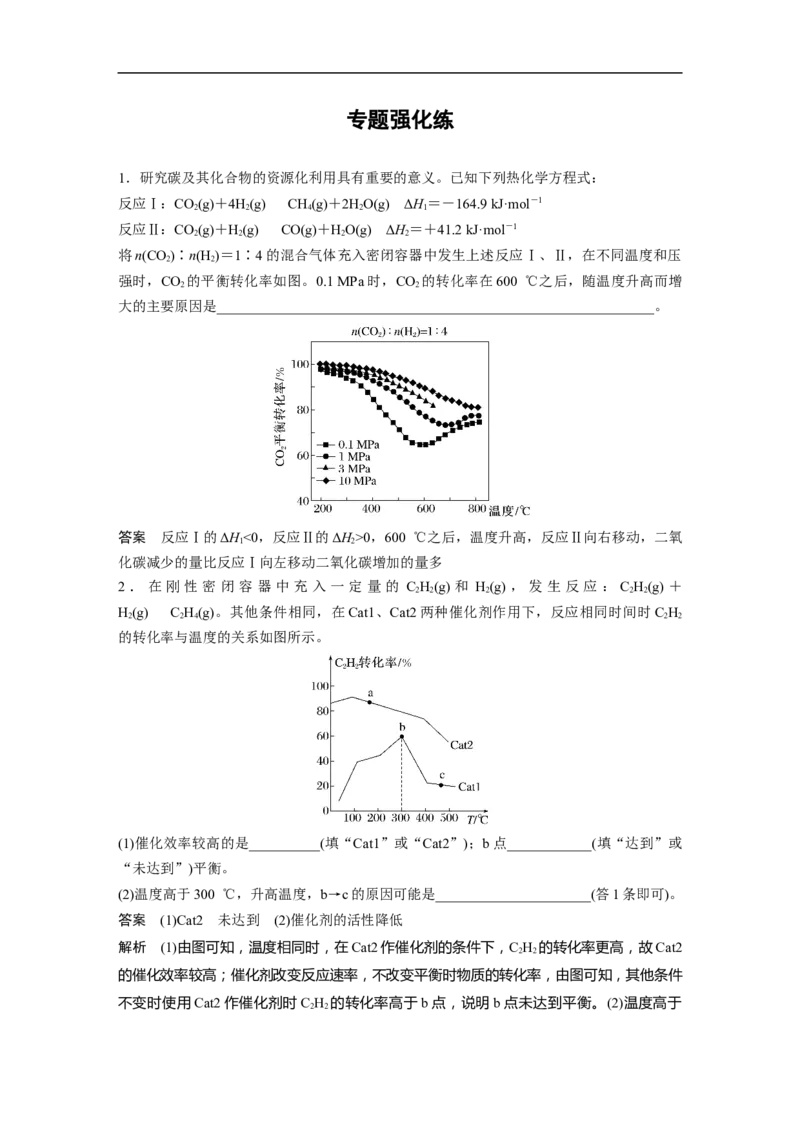
将n(CO)∶n(H )=1∶4的混合气体充入密闭容器中发生上述反应Ⅰ、Ⅱ,在不同温度和压
2 2
强时,CO 的平衡转化率如图。0.1 MPa时,CO 的转化率在600 ℃之后,随温度升高而增
2 2
大的主要原因是______________________________________________________________。
答案 反应Ⅰ的ΔH<0,反应Ⅱ的ΔH>0,600 ℃之后,温度升高,反应Ⅱ向右移动,二氧
1 2
化碳减少的量比反应Ⅰ向左移动二氧化碳增加的量多
2 . 在 刚 性 密 闭 容 器 中 充 入 一 定 量 的 C H(g) 和 H(g) , 发 生 反 应 : C H(g) +
2 2 2 2 2
H(g)C H(g)。其他条件相同,在Cat1、Cat2两种催化剂作用下,反应相同时间时C H
2 2 4 2 2
的转化率与温度的关系如图所示。
(1)催化效率较高的是__________(填“Cat1”或“Cat2”);b点____________(填“达到”或
“未达到”)平衡。
(2)温度高于300 ℃,升高温度,b→c的原因可能是______________________(答1条即可)。
答案 (1)Cat2 未达到 (2)催化剂的活性降低
解析 (1)由图可知,温度相同时,在Cat2作催化剂的条件下,C H 的转化率更高,故Cat2
2 2
的催化效率较高;催化剂改变反应速率,不改变平衡时物质的转化率,由图可知,其他条件
不变时使用Cat2作催化剂时C H 的转化率高于b点,说明b点未达到平衡。(2)温度高于
2 2300 ℃,升高温度,b→c段C H 的转化率降低,原因可能是催化剂的活性降低。
2 2
3.煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:
CO(g)+HO(g)H(g)+CO(g)中CO的平衡转化率随比例及温度变化关系如图所示:
2 2 2
(1)上述反应的正反应是____________(填“吸热”或“放热”)反应。
(2)若提高比例,则该反应的平衡常数K会________(填“变大”“变小”或“不变”)。
(3)若降低温度,反应重新达到平衡,则v正 ______(填“增大”“减小”或“不变”,下同);
CO转化率__________________。
(4)在使用铁镁催化剂的实际流程中,一般采用 400 ℃左右,采用此温度的原因是
_____________________________________________________________________________。
答案 (1)放热 (2)不变 (3)减小 增大 (4)催化剂活性最高
解析 (1)由图像知,相同时,随温度升高,CO的平衡转化率降低,所以正反应是放热反应。
(2)平衡常数只与温度有关,若提高比例,则该反应的平衡常数K不变。
(3)若降低温度,平衡正向移动,CO的浓度减小,反应重新达到平衡,则v 减小,CO的
正
转化率增大。
4.二甲醚既是重要的工业品,也是燃料电池制氢的重要原料。二甲醚水蒸气重整制氢的总
反应为CHOCH (g)+(1+2x)H O(g)(4+2x)H (g)+(2-2x)CO(g)+2xCO(g),其过程包括:
3 3 2 2 2
Ⅰ.CH OCH (g)+HO(g)2CHOH(g) ΔH=+23.6 kJ·mol-1
3 3 2 3 1
Ⅱ.CH OH(g)+HO(g)CO(g)+3H(g) ΔH=+49.5 kJ·mol-1
3 2 2 2 2
Ⅲ.CH OH(g)CO(g)+2H(g) ΔH=+90.7 kJ·mol-1
3 2 3
Ⅳ.CO(g)+HO(g)CO(g)+H(g) ΔH=-41.2 kJ·mol-1
2 2 2 4
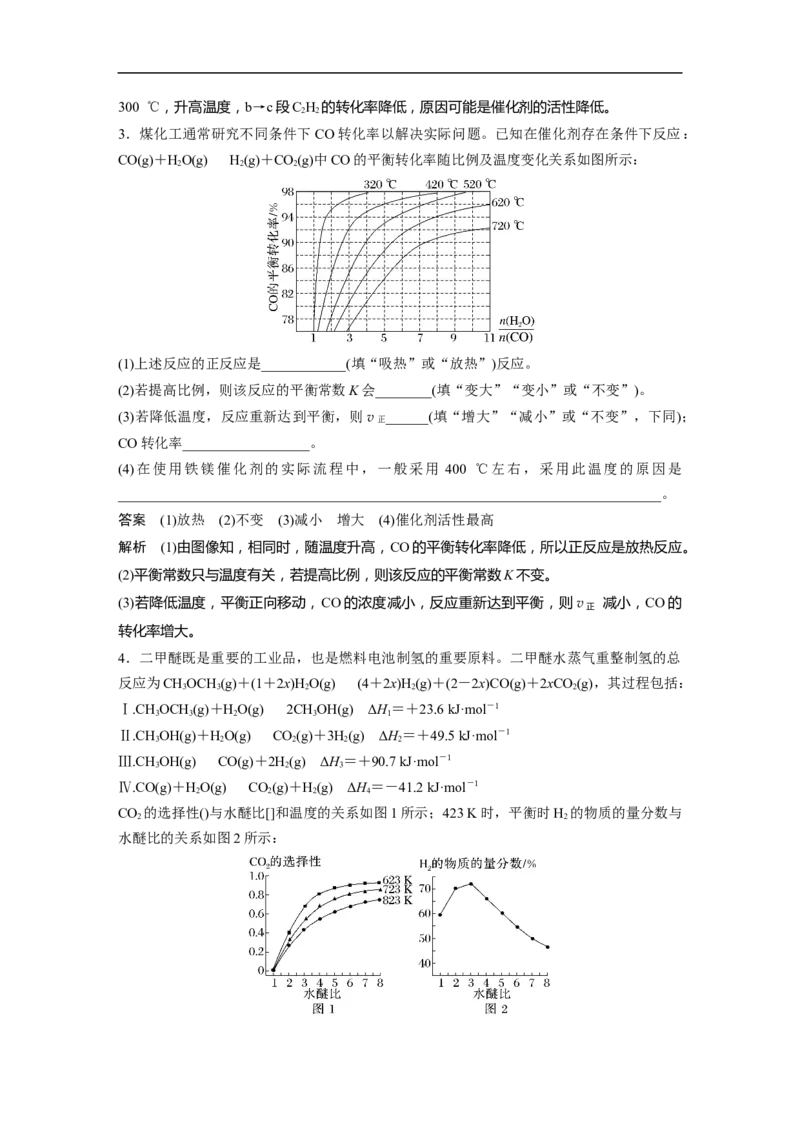
CO 的选择性()与水醚比[]和温度的关系如图1所示;423 K时,平衡时H 的物质的量分数与
2 2
水醚比的关系如图2所示:(1)图1中相同温度下,水醚比越大,CO 的选择性越高的原因是________________________;
2
相同水醚比时,温度升高,CO 的选择性降低的原因是______________________________。
2
(2)图 2 中水醚比大于 3 时,随水醚比的增大 H 的物质的量分数减小的原因是
2
______________
_______________________________________________________________________________
。
答案 (1)提高水醚比有利于反应Ⅱ、Ⅳ正向进行 温度升高时,反应Ⅱ正向进行增加的
CO 的量小于反应Ⅳ逆向进行减少的CO 的量 (2)水醚比大于3时,再增大水醚比,气体的
2 2
总物质的量及HO(g)的物质的量分数均增大(或过量的水蒸气产生稀释作用)
2
解析 (1)反应Ⅱ、Ⅳ会生成CO ,提高水醚比有利于反应Ⅱ、Ⅳ正向进行;反应Ⅱ为吸热
2
反应,反应Ⅳ为放热反应,温度升高时,反应Ⅱ正向进行增加的CO 的量小于反应Ⅳ逆向进
2
行减少的CO 的量,导致CO 的选择性降低。(2)水醚比大于3时,再增大水醚比,气体的
2 2
总物质的量及HO(g)的物质的量分数均增大,且过量的水蒸气产生稀释作用,所以随水醚
2
比的增大H 的物质的量分数减小。
2
5.CO 和H 合成甲烷也是CO 资源化利用的重要方法。对于反应CO(g)+4H(g)CH(g)
2 2 2 2 2 4
+2HO(g) ΔH=-165 kJ·mol-1,催化剂的选择是CO 甲烷化技术的核心。在两种不同催
2 2
化剂条件下反应相同时间,测得CO 转化率和生成CH 选择性随温度变化的影响如图所示:
2 4
(1)高于320 ℃后,以Ni-CeO 为催化剂,CO 转化率略有下降,而以Ni为催化剂,CO 转
2 2 2
化率仍在上升,其原因是______________________________________________________。
(2)对比上述两种催化剂的催化性能,工业上应选择的催化剂是____________________,使
用的合适温度为______________________。
答案 (1)320 ℃时,以Ni-CeO 为催化剂,CO 甲烷化反应已达平衡,升高温度平衡左移;
2 2
以Ni为催化剂,CO 甲烷化反应速率较慢,升高温度反应速率加快,反应相同时间时 CO
2 2
转化率增加 (2)Ni-CeO 320 ℃
2
解析 (2)根据图像分析可知,温度适宜(320 ℃)时,以Ni-CeO 为催化剂明显比以Ni为催化
2
剂时CO 转化率高,且催化剂选择性强,所以应选择 Ni-CeO 为催化剂,最佳温度为 320
2 2
℃。
6.一定条件下,用 Fe O 、NiO 或 Cr O 作催化剂对燃煤烟气回收。反应为 2CO(g)+
2 3 2 3
SO (g)2CO(g)+S(l) ΔH=-270 kJ·mol-1。
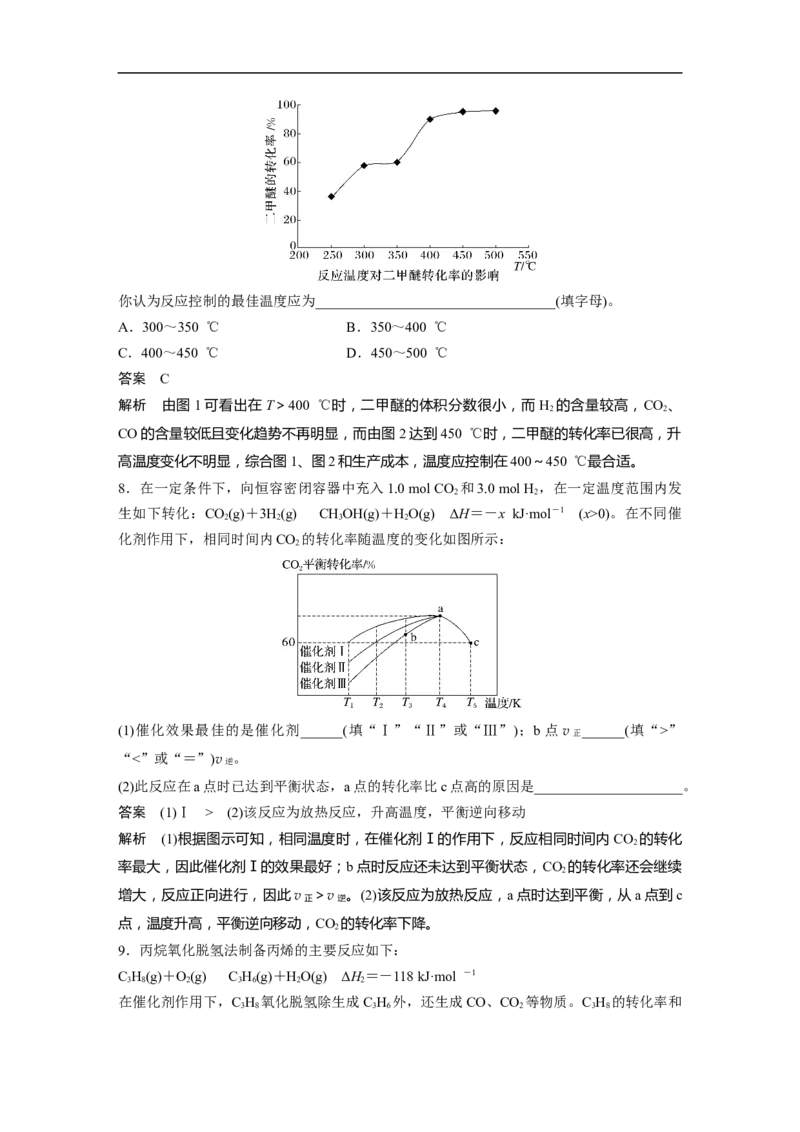
2 2(1)其他条件相同、催化剂不同,SO 的转化率随反应温度的变化如图1,Fe O 和NiO作催
2 2 3
化剂均能使SO 的转化率达到最高,不考虑催化剂价格因素,选择 Fe O 的主要优点是
2 2 3
______________________________________________________________________________。
(2)某科研小组用Fe O 作催化剂,在380 ℃时,分别研究了n(CO)∶n(SO )为1∶1、3∶1时
2 3 2
SO 转化率的变化情况(图2)。则图2中表示n(CO)∶n(SO )=3∶1的变化曲线为______(填
2 2
“a”或“b”)。
答案 (1)Fe O 作催化剂时,在相对较低温度可获得较高的 SO 转化率,从而节约能源
2 3 2
(2)a
解析 (1)根据图1可知,Fe O 和NiO作催化剂均能使SO 的转化率达到最高,不考虑催化
2 3 2
剂价格因素,选择Fe O 的主要优点是Fe O 作催化剂时,在相对较低温度可获得较高的SO
2 3 2 3 2
转化率,从而节约能源。(2)在其他条件不变时,增大CO的浓度,可以提高SO 的平衡转化
2
率。由图2可知转化率:a>b,所以曲线a表示n(CO)∶n(SO )=3∶1的变化曲线,曲线b
2
表示n(CO)∶n(SO )=1∶1的变化曲线。
2
7.二甲醚催化重整制氢的反应过程主要包括以下几个反应(以下数据为25 ℃、1.01×105
Pa条件下测定):
Ⅰ:CHOCH (g)+HO(l)2CHOH(l) ΔH>0
3 3 2 3
Ⅱ:CHOH(l)+HO(l)CO(g)+3H(g) ΔH>0
3 2 2 2
Ⅲ:CO(g)+HO(l)CO(g)+H(g) ΔH<0
2 2 2
Ⅳ:CHOH(l)CO(g)+2H(g) ΔH>0
3 2
工业生产中测得不同温度下各组分体积分数及二甲醚转化率的关系如图所示:你认为反应控制的最佳温度应为__________________________________(填字母)。
A.300~350 ℃ B.350~400 ℃
C.400~450 ℃ D.450~500 ℃
答案 C
解析 由图1可看出在T>400 ℃时,二甲醚的体积分数很小,而 H 的含量较高,CO 、
2 2
CO的含量较低且变化趋势不再明显,而由图2达到450 ℃时,二甲醚的转化率已很高,升
高温度变化不明显,综合图1、图2和生产成本,温度应控制在400~450 ℃最合适。
8.在一定条件下,向恒容密闭容器中充入1.0 mol CO 和3.0 mol H ,在一定温度范围内发
2 2
生如下转化:CO(g)+3H(g)CHOH(g)+HO(g) ΔH=-x kJ·mol-1 (x>0)。在不同催
2 2 3 2
化剂作用下,相同时间内CO 的转化率随温度的变化如图所示:
2
(1)催化效果最佳的是催化剂______(填“Ⅰ”“Ⅱ”或“Ⅲ”);b点v正 ______(填“>”
“<”或“=”)v逆 。
(2)此反应在a点时已达到平衡状态,a点的转化率比c点高的原因是_____________________。
答案 (1)Ⅰ > (2)该反应为放热反应,升高温度,平衡逆向移动
解析 (1)根据图示可知,相同温度时,在催化剂Ⅰ的作用下,反应相同时间内CO 的转化
2
率最大,因此催化剂Ⅰ的效果最好;b点时反应还未达到平衡状态,CO 的转化率还会继续
2
增大,反应正向进行,因此v >v 。(2)该反应为放热反应,a点时达到平衡,从a点到c
正 逆
点,温度升高,平衡逆向移动,CO 的转化率下降。
2
9.丙烷氧化脱氢法制备丙烯的主要反应如下:
C H(g)+O(g)C H(g)+HO(g) ΔH=-118 kJ·mol -1
3 8 2 3 6 2 2
在催化剂作用下,C H 氧化脱氢除生成C H 外,还生成CO、CO 等物质。C H 的转化率和
3 8 3 6 2 3 8C H 的产率随温度变化关系如图所示。
3 6
(1)图中C H 的转化率随温度升高而上升的原因是__________________________。
3 8
(2)575 ℃时,C H 的选择性为_______________________________。(结果保留3位有效数字,
3 6
C H 的选择性=×100%)
3 6
(3)基于本研究结果,能提高C H 选择性的措施是_______________________________。
3 6
答案 (1)温度升高,催化剂的活性增大 (2)51.5% (3)选择相对较低的温度
解析 (1)该反应为放热反应,升高温度,平衡逆向移动,C H 的转化率应该降低,但实际
3 8
上C H 的转化率随温度升高而上升,可能是升高温度,催化剂的活性增大导致的。(2)根据
3 8
图像,575 ℃时,C H 的转化率为33%,C H 的产率为17%,假设参加反应的C H 为100
3 8 3 6 3 8
mol,生成的C H 为17 mol,C H 的选择性为×100%≈51.5%。(3)根据图像,535 ℃时,
3 6 3 6
C H 的选择性为×100%≈66.7%,550 ℃时,C H 的选择性为×100%≈61.5%,575 ℃时,C H
3 6 3 6 3 6
的选择性为×100%≈51.5%,故选择相对较低的温度能够提高C H 选择性。
3 6
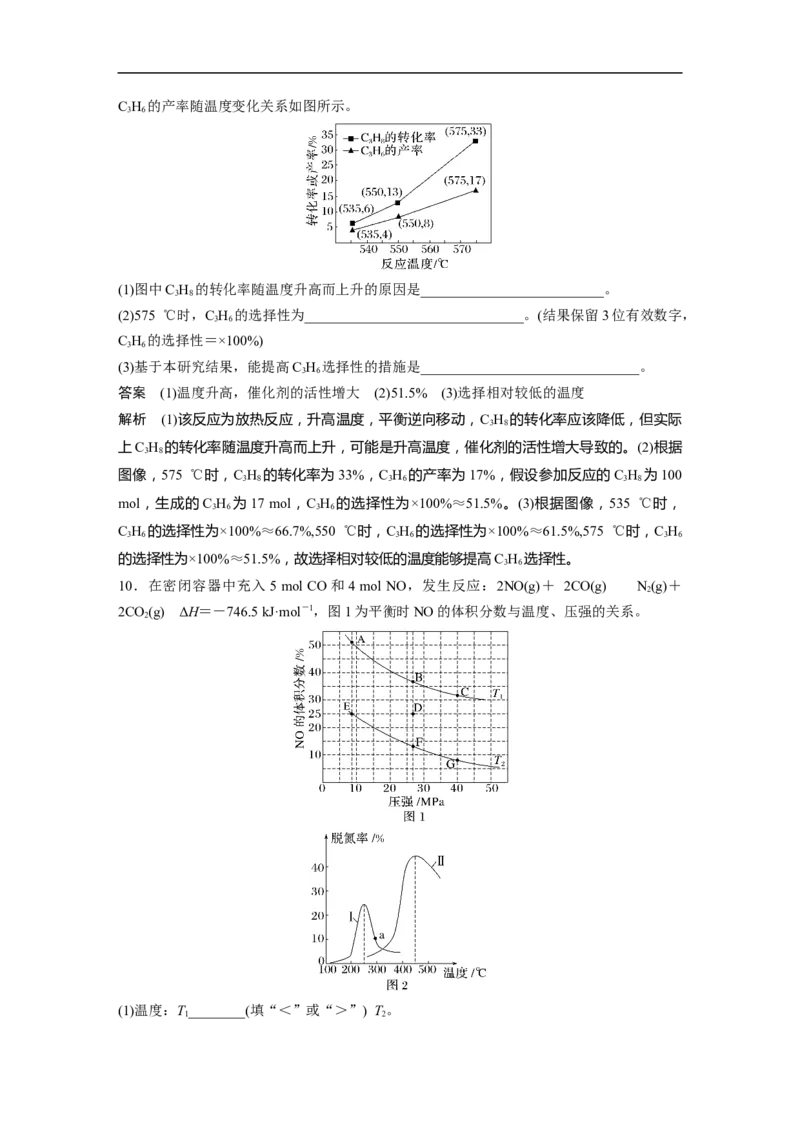
10.在密闭容器中充入5 mol CO和4 mol NO,发生反应:2NO(g)+ 2CO(g) N(g)+
2
2CO(g) ΔH=-746.5 kJ·mol-1,图1为平衡时NO的体积分数与温度、压强的关系。
2
(1)温度:T________(填“<”或“>”) T。
1 2(2)若在D点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是
图中A~G点中的________点。
(3)某研究小组探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不
同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率
即NO的转化率),结果如图2所示。温度低于200 ℃时,图2中曲线Ⅰ脱氮率随温度升高
而变化不大的主要原因为_________________________________;a点________(填“是”或
“ 不 是 ” ) 对 应 温 度 下 的 平 衡 脱 氮 率 , 说 明 其 理 由 :
_______________________________________。
答案 (1)> (2)A (3)温度较低时,催化剂的活性偏低 不是 该反应为放热反应,根据
曲线Ⅱ可知,a点对应温度下的平衡脱氮率应该更高
解析 (1)根据反应2CO(g)+2NO(g)N(g)+2CO(g) ΔH=-746.5 kJ·mol-1,升高温度,
2 2
平衡逆向移动,所以NO的体积分数会增大,即T>T。(2)若在D点对反应容器升温的同时
1 2
扩大体积使体系压强减小,则平衡会逆向移动,NO的体积分数增加,重新达到的平衡状态
可能是图中A点。
(3)根据图像可知,温度较低时,催化剂的活性偏低,因此温度低于 200 ℃,曲线Ⅰ脱氮率
随温度升高变化不大;a点不是对应温度下的平衡脱氮率,因为该反应为放热反应,根据曲
线Ⅱ可知,a点对应温度下的平衡脱氮率应该更高。
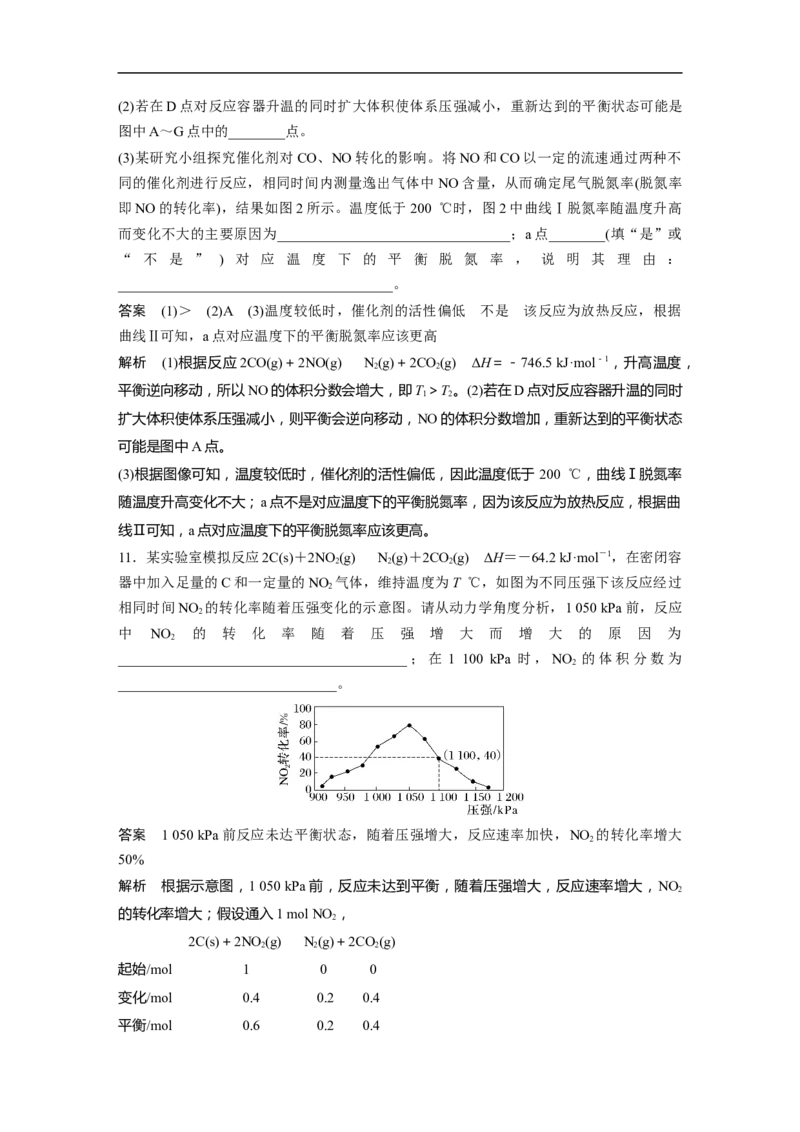
11.某实验室模拟反应2C(s)+2NO (g)N(g)+2CO(g) ΔH=-64.2 kJ·mol-1,在密闭容
2 2 2
器中加入足量的C和一定量的NO 气体,维持温度为T ℃,如图为不同压强下该反应经过
2
相同时间NO 的转化率随着压强变化的示意图。请从动力学角度分析,1 050 kPa前,反应
2
中 NO 的 转 化 率 随 着 压 强 增 大 而 增 大 的 原 因 为
2
_________________________________________;在 1 100 kPa 时,NO 的体积分数为
2
_______________________________。
答案 1 050 kPa前反应未达平衡状态,随着压强增大,反应速率加快,NO 的转化率增大
2
50%
解析 根据示意图,1 050 kPa前,反应未达到平衡,随着压强增大,反应速率增大,NO
2
的转化率增大;假设通入1 mol NO ,
2
2C(s)+2NO (g)N(g)+2CO(g)
2 2 2
起始/mol 1 0 0
变化/mol 0.4 0.2 0.4
平衡/mol 0.6 0.2 0.41 100 kPa时,NO 的体积分数为×100%=50%。
2
12.T ℃时,向一恒容密闭容器中加入 3 mol H 和 1 mol Se,发生反应:H(g)+
2 2
Se(s)HSe (g) ΔH<0,温度对HSe产率的影响如图:
2 2
550 ℃时HSe产率最大的原因:____________________________________________。
2
答案 低于550 ℃时,温度越高反应速率越快,HSe的产率越大;高于550 ℃时,反应达
2
到平衡,该反应为放热反应,温度升高平衡逆向移动,HSe的产率减小
2
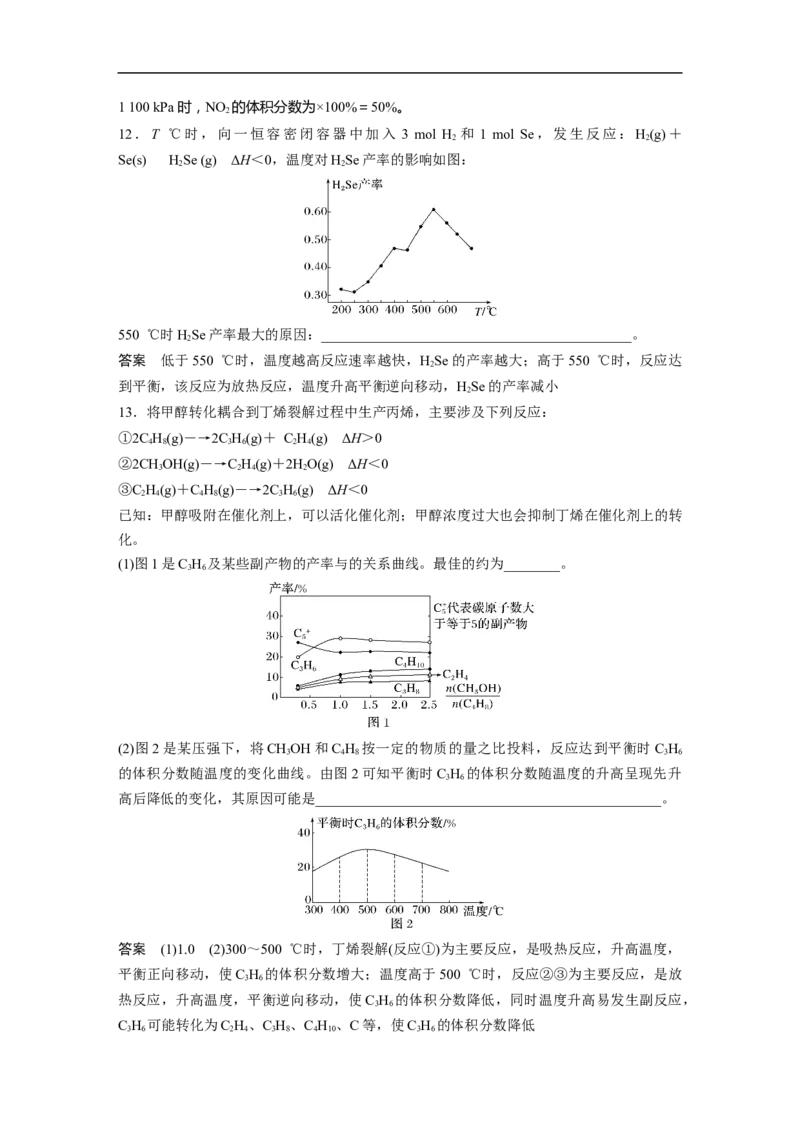
13.将甲醇转化耦合到丁烯裂解过程中生产丙烯,主要涉及下列反应:
①2C H(g)―→2C H(g)+ C H(g) ΔH>0
4 8 3 6 2 4
②2CHOH(g)―→C H(g)+2HO(g) ΔH<0
3 2 4 2
③C H(g)+C H(g)―→2C H(g) ΔH<0
2 4 4 8 3 6
已知:甲醇吸附在催化剂上,可以活化催化剂;甲醇浓度过大也会抑制丁烯在催化剂上的转
化。
(1)图1是C H 及某些副产物的产率与的关系曲线。最佳的约为________。
3 6
(2)图2是某压强下,将CHOH和C H 按一定的物质的量之比投料,反应达到平衡时C H
3 4 8 3 6
的体积分数随温度的变化曲线。由图2可知平衡时C H 的体积分数随温度的升高呈现先升
3 6
高后降低的变化,其原因可能是_________________________________________________。
答案 (1)1.0 (2)300~500 ℃时,丁烯裂解(反应①)为主要反应,是吸热反应,升高温度,
平衡正向移动,使C H 的体积分数增大;温度高于500 ℃时,反应②③为主要反应,是放
3 6
热反应,升高温度,平衡逆向移动,使C H 的体积分数降低,同时温度升高易发生副反应,
3 6
C H 可能转化为C H、C H、C H 、C等,使C H 的体积分数降低
3 6 2 4 3 8 4 10 3 6解析 (1)由图1可知当约为1.0时,C H 的产率是最高的。
3 6