文档内容
2025届高三化学一轮专题复习讲义(01)
专题一 基本概念
1-1 化学与STSE 化学用语(1课时)
【复习目标】
1.通过化学在生产和生活中的热点问题,掌握化学与STSE所涉及的原因分析。
2.掌握根据物质的组成对物质分类的方法,理解常见的不同类型物质的相互联系和转化关系。
3.知道胶体是常见的分散系,了解胶体与溶液的简单鉴别方法和胶体在生产、生活中的应用。
【重点突破】
1.知道化学在生产、生活中的热点应用及原因分析。
2.掌握物质的分类和胶体的性质。
【真题再现】
例1.(2023·江苏高考)我国提出2060年实现碳中和的目标,体现了大国担当。“碳中和”中的
“碳”是指
A.碳原子 B.二氧化碳 C.碳元素 D.含碳物质
解析:碳中和,节能减排术语。一般是指国家、企业、产品、活动或个人在一定时间内直接或间接
产生的二氧化碳或温室气体排放总量,通过植树造林、节能减排等形式,以抵消自身产生的二
氧化碳或温室气体排放量,实现正负抵消,达到相对“零排放”。故“碳中和”中的“碳”指
的是二氧化碳。
答案:B
小结:关注社会热点问题,从化学的视角解决生活中的问题。围绕与化学应用相关的社会热点设置
选项,判断其中的化学基本原理,体现科学精神与社会责任,是近年来江苏高考试题的稳定题
型。
【知能整合】
例2.(2023·江苏高考)反应NH Cl+NaNO ===NaCl+N ↑+2H O应用于石油开采。下列说法正确
4 2 2 2
的是
A.NH +的电子式为 B.NO -中N元素的化合价为+5
4 2
C.N 分子中存在N≡N键 D.HO为非极性分子
2 2
解析:A项,NH +的电子式为 ,错误;B项.NO -中N元素的化合价为+3,错误;C项,
4 2
N 分子,根据共价键的成键特点,分子中存在N≡N键,正确;D项,HO分子正负电荷中心
2 2
不重合,中心原子化合价不等于主族序数,为极性分子,错误。
答案:C
例3.(2022·江苏高考)少量NaO 与HO反应生成HO 和NaOH。下列说法正确的是
2 2 2 2 2
A.NaO 的电子式为 B.HO的空间构型为直线形
2 2 2
C.HO 中O元素的化合价为-1 D.NaOH仅含离子键
2 2
解析:A项,过氧化钠是离子化合物,电子式是 ,错误;B项.HO中氧原子的
2
成键电子对是2,孤电子对是2,价层电子对为4,根据价层电子对互斥理论,其空间构型为V
形,错误;C项,HO 中H显+1价,根据正负化合价为0,可计算出O的化合价为-1,正确;
2 2
D项,NaOH中O和H之间是共价键,错误。
答案:C
例4.(2021·江苏高考)反应 Cl+ 2NaOH=NaClO + NaCl + H O 可用于制备含氯消毒剂。下列说
2 2法正确的是
A.Cl 是极性分子 B.NaOH 的电子式为
2
C.NaClO 既含离子键又含共价键 D.Cl-与Na+具有相同的电子层结构
解析:A项,Cl 是非极性分子,错误;B项,NaOH是强碱,是离子化合物,含钠离子和氢氧根离
2
子,错误;C项,NaClO 是由钠离子和次氯酸根离子构成,是既含离子键又含共价键,正确;
D项,Cl-与Na+电子层结构不相同,错误。
答案:C
小结:近几年江苏高考的化学用语主要涉及:1.微粒电子式或元素电子排布式的表达;2.微粒中元
素化合价的判断;3.化学键的表示或化学键类型的判断;4.分子或微粒结构或杂化类型的判断;
5.分子极性的判断。在对原子构成的符号表达中,要分清元素符号的左下标、左上标与对应的
原子核中各微粒数之间的关系;对核外电子排布式或结构示意图的认识,主要是要辨别是原子
还是离子;在物质的电子式书写方面往往表现在对化学键类型的区分以及分子中孤对电子的缺
失。有机物结构简式忽略原子团在苯环上的位置,如:间二甲苯的结构简式错写成:
或价键的连接位置,如硝基苯易错写成: 。
【知能整合】
选项 注意要点
核素符号 质子数、中子数、质量数之间的关系;核素的符号表达;质子数与元素符号的对应关系
离子键 原子团与简单离子的组合:NH4Cl、NaOH、Na2O2
氢化物:CH4、NH3、H2O、HCl;含重键的物质:N2、CO2、C2H4、C2H2
电子式 共价键 等;复杂化合物:CH2O、COCl2、CO(NH2)2、CCl4 等(注意 O、N、Cl 等
原子的孤电子对)
原(离)子结构示意简 当原子变为离子时,核电荷数不发生改变。离子的核外电子排布满足稳定结构
图
注意基态原子(或离子)核外电子排布式、外围电子排布式、轨道表达式的
核外电子排布式
区别。
官能团在苯环上的位置;官能团中各原子与苯环连接的顺序(如:-NO2、-
有机物的结构简式
OH 等)
球棍模型和空间填充
模型 如甲烷的球棍模型为 、空间填充模型为
概念辨析 分子式、实验式、结构式、结构简式等
例5.化学与生活密切相关,下列说法正确的是
A.苯甲酸钠可作为食品防腐剂是由于其具有酸性
B.豆浆能产生丁达尔效应是由于胶体粒子对光线的散射
C.SO 可用于丝织品漂白是由于其能氧化丝织品中有色成分
2
D.维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
解析:A项,苯甲酸钠属于强碱弱酸盐,其水溶液呈碱性,因此,其可作为食品防腐剂不是由于其
具有酸性,不正确;B项,胶体具有丁达尔效应,是因为胶体粒子对光线发生了散射;豆浆属
于胶体,因此,其能产生丁达尔效应是由于胶体粒子对光线的散射,正确;C项,SO 可用于
2
丝织品漂白是由于其能与丝织品中有色成分化合为不稳定的无色物质,不正确;D项,维生素
C具有很强的还原性,因此,其可用作水果罐头的抗氧化剂是由于其容易被氧气氧化,从而防
止水果被氧化,不正确
答案:B
例题6.(2021·江苏模拟题重组)判断下列说法的正误,正确的打“√”,错误的打“×”。
(1)浓氨水中滴加FeCl 饱和溶液可制得Fe(OH) 胶体。( )
3 3
(2)明矾易溶于水,故可用作净水剂。( )(3)向沸水中滴入几滴FeCl 饱和溶液,煮沸,用激光笔照射,出现一条光亮通路,证明有
3
Fe(OH) 胶体生成。( )
3
(4)明矾溶于水产生Al(OH) 胶体:Al3++3HO===Al(OH) ↓+3H+。( )
3 2 3
(5)利用丁达尔效应可区别蛋白质溶液和食盐水。( )
(6)向NaCl粉末中加入适量酒精,充分振荡形成无色透明液体,用激光笔照射,出现一条光
亮通路,形成的分散系是胶体。( )
解析:(1)得到的是Fe(OH) 沉淀。(2)明矾溶于水后,Al3+水解得到Al(OH) 胶体,吸附水中
3 3
的悬浮物,从而起到净水作用。
答案:××√×√√
【知能整合】
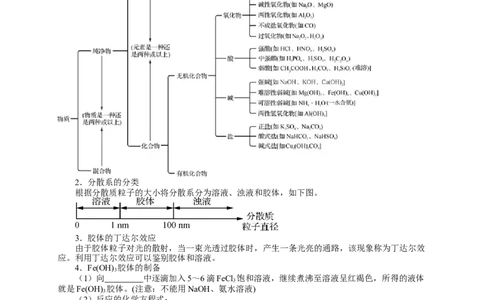
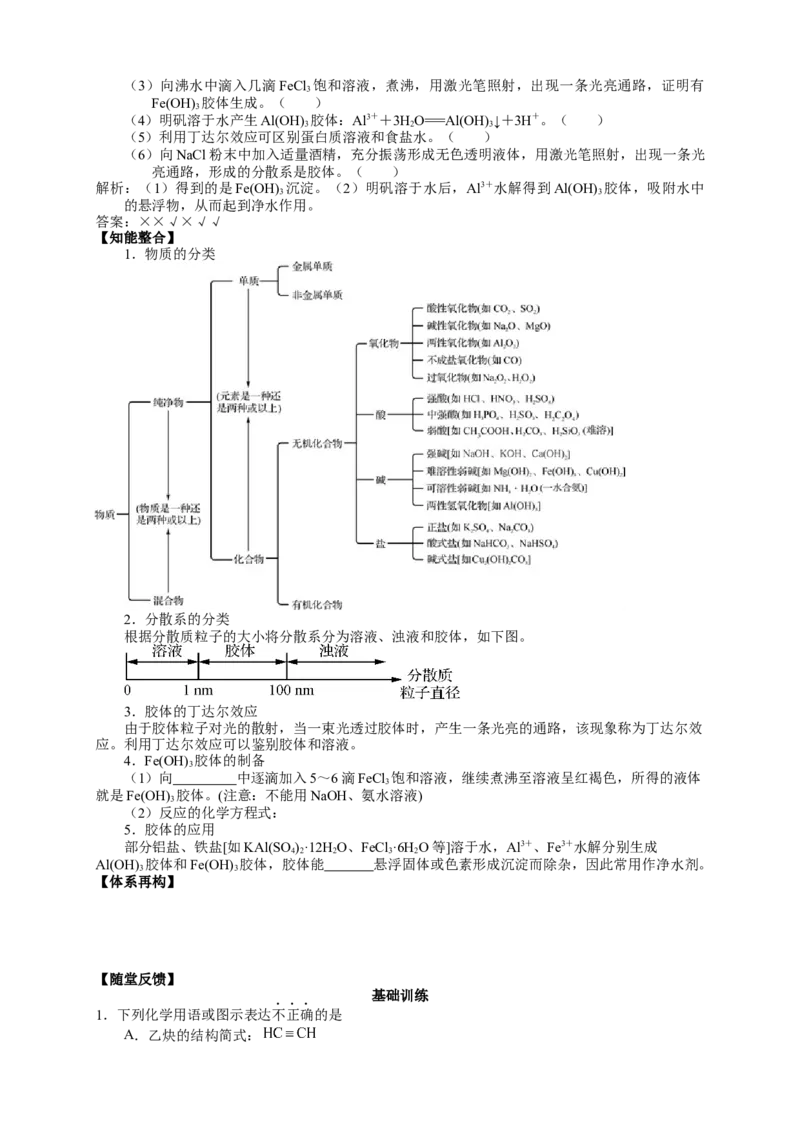
1.物质的分类
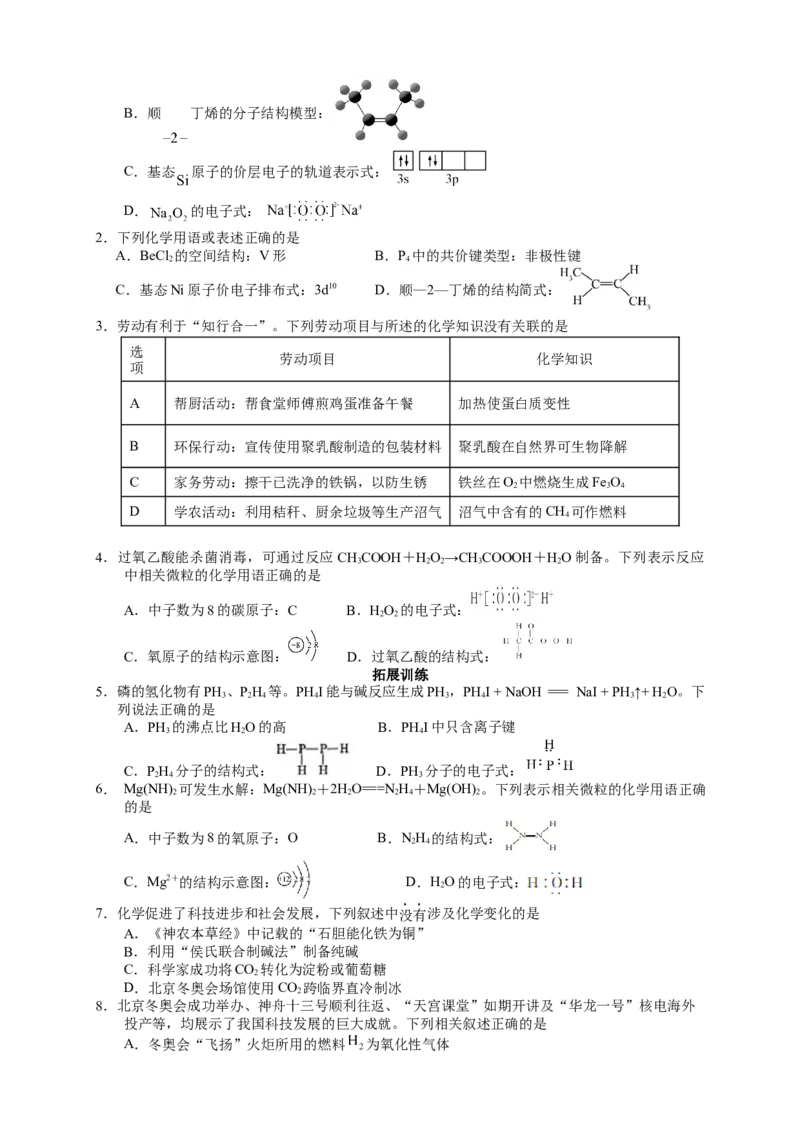
2.分散系的分类
根据分散质粒子的大小将分散系分为溶液、浊液和胶体,如下图。
3.胶体的丁达尔效应
由于胶体粒子对光的散射,当一束光透过胶体时,产生一条光亮的通路,该现象称为丁达尔效
应。利用丁达尔效应可以鉴别胶体和溶液。
4.Fe(OH) 胶体的制备
3
(1)向 中逐滴加入5~6滴FeCl 饱和溶液,继续煮沸至溶液呈红褐色,所得的液体
3
就是Fe(OH) 胶体。(注意:不能用NaOH、氨水溶液)
3
(2)反应的化学方程式:
5.胶体的应用
部分铝盐、铁盐[如KAl(SO )·12H O、FeCl ·6H O等]溶于水,Al3+、Fe3+水解分别生成
4 2 2 3 2
Al(OH) 胶体和Fe(OH) 胶体,胶体能 悬浮固体或色素形成沉淀而除杂,因此常用作净水剂。
3 3
【体系再构】
【随堂反馈】
基础训练
1.下列化学用语或图示表达不正确的是
A.乙炔的结构简式:B.顺 丁烯的分子结构模型:
C.基态 原子的价层电子的轨道表示式:
D. 的电子式:
2.下列化学用语或表述正确的是
A.BeCl 的空间结构:V形 B.P 中的共价键类型:非极性键
2 4
C.基态Ni原子价电子排布式:3d10 D.顺—2—丁烯的结构简式:
3.劳动有利于“知行合一”。下列劳动项目与所述的化学知识没有关联的是
选
劳动项目 化学知识
项
A 帮厨活动:帮食堂师傅煎鸡蛋准备午餐 加热使蛋白质变性
B 环保行动:宣传使用聚乳酸制造的包装材料 聚乳酸在自然界可生物降解
C 家务劳动:擦干已洗净的铁锅,以防生锈 铁丝在O 中燃烧生成Fe O
2 3 4
D 学农活动:利用秸秆、厨余垃圾等生产沼气 沼气中含有的CH 可作燃料
4
4.过氧乙酸能杀菌消毒,可通过反应 CHCOOH+HO→CHCOOOH+HO制备。下列表示反应
3 2 2 3 2
中相关微粒的化学用语正确的是
A.中子数为8的碳原子:C B.HO 的电子式:
2 2
C.氧原子的结构示意图: D.过氧乙酸的结构式:
拓展训练
5.磷的氢化物有PH 、PH 等。PH I能与碱反应生成PH ,PH I + NaOH === NaI + PH ↑+ H O。下
3 2 4 4 3 4 3 2
列说法正确的是
A.PH 的沸点比HO的高 B.PH I中只含离子键
3 2 4
C.PH 分子的结构式: D.PH 分子的电子式:
2 4 3
6. Mg(NH) 可发生水解:Mg(NH) +2HO===N H+Mg(OH) 。下列表示相关微粒的化学用语正确
2 2 2 2 4 2
的是
A.中子数为8的氧原子:O B.NH 的结构式:
2 4
C.Mg2+的结构示意图: D.HO的电子式:
2
7.化学促进了科技进步和社会发展,下列叙述中没有涉及化学变化的是
A.《神农本草经》中记载的“石胆能化铁为铜”
B.利用“侯氏联合制碱法”制备纯碱
C.科学家成功将CO 转化为淀粉或葡萄糖
2
D.北京冬奥会场馆使用CO 跨临界直冷制冰
2
8.北京冬奥会成功举办、神舟十三号顺利往返、“天宫课堂”如期开讲及“华龙一号”核电海外
投产等,均展示了我国科技发展的巨大成就。下列相关叙述正确的是
A.冬奥会“飞扬”火炬所用的燃料 为氧化性气体B.飞船返回舱表层材料中的玻璃纤维属于天然有机高分子
C.乙酸钠过饱和溶液析出晶体并放热的过程仅涉及化学变化
D.核电站反应堆所用铀棒中含有的 与 互为同位素
【随堂反馈】答案
1.C 2.B 3.C 4.D 5.C 6.D 7.D 8.D
【课后作业】
1.科教兴国,“可上九天揽月,可下五洋捉鳖”。下列说法正确的是
A.“天舟六号”为中国空间站送去推进剂Xe气,Xe是第ⅠA族元素
B.火星全球影像彩图显示了火星表土颜色,表土中赤铁矿主要成分为FeO
C.创造了可控核聚变运行纪录的“人造太阳”,其原料中的2H与3H互为同位素
D.“深地一号”为进军万米深度提供核心装备,制造钻头用的金刚石为金属晶体
2.下列表述正确的是
A.NaO 的电子式:
2 2
B.N 的共价键类型:σ键和π键
2
C.中子数为30的Fe原子符号:Fe
D.SO 分子的立体构型:三角锥形
3
3.下列化学用语表示正确的是
A.HS分子的球棍模型: B.AlCl 的价层电子对互斥模型:
2 3
C.KI的电子式: D. 的名称:3−甲基戊烷
4.下列说法错误的是
A.新榨油脂不及时干燥脱水易变质 B.聚氯乙烯可制作食品内包装材料
C.维生素C可作预包装食品抗氧剂 D.卤水点豆腐本质属于蛋白质聚沉
5.下列化学用语表示正确的是
A.中子数为18的氯原子:Cl
B.碳的基态原子轨道表示式:
C.BF 的空间结构: (平面三角形)
3
D.HCl的形成过程:
6.下列化学用语或图示表达正确的是
A.NaCl的电子式为
B.NH 的VSEPR模型为
3
C. 电子云图为
D.基态 Cr原子的价层电子轨道表示式为
24
7.下列化学用语表述错误的是A.HClO的电子式:
B.中子数为10的氧原子:O
C.NH 分子的VSEPR模型:
3
D.基态N原子的价层电子排布图:
【课后作业】答案
1.C 2.B 3.D 4.B 5.C 6.C 7.C