文档内容
一、选择题
1.(2019·阜阳高三检测)甲、乙是周期表中同一主族的两种元素,若甲的原子序数为x,则
乙的原子序数不可能是( )
A.x+2 B.x+4
C.x+8 D.x+18
解析:选B。元素周期表有7个周期,16个族,主族是长、短周期共同组成的族,同一主族
的两元素原子序数差值是有规律的。同主族相邻两周期原子序数差值可能为2、8、18、32等,
很显然上下两周期两元素的原子序数的差值不可能为4,即正确答案为B。
2.(2019·江西百所名校第一次联考)2017年5月9日中国科学院正式向社会发布113号、
115号、117号和118号元素的中文名称。已知117号元素有多种原子,如Ts、Ts 等。下列说法
中正确的是( )
A.Ts和Ts的化学性质不同
B.Ts和Ts质子数相同,中子数不同
C.Ts位于周期表的第六周期ⅦA族
D.元素Ts的相对原子质量为293.5
解析:选B。Ts和Ts互为同位素,化学性质几乎相同,A项错误;Ts和Ts互为同位素,它
们的质子数均为117,中子数分别为176和177,B项正确;Ts的核电荷数为117,位于周期表
的第七周期ⅦA族,C项错误;117号元素有多种原子,如Ts、Ts等,且所占的原子个数百分
比不一定相等,其相对原子质量不一定为293.5,D项错误。
3.下列有关元素的性质及其递变规律正确的是( )
A.第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强
B.第二周期元素从左到右,最高正价从+1递增到+7
C.同周期元素(0族元素除外)从左到右,原子半径逐渐减小
D.同周期金属元素的化合价越高,其原子失电子能力越强
解析:选C。同主族元素从上到下,非金属性逐渐减弱,氢化物的稳定性逐渐减弱,A错
误;第二周期元素中,O没有最高正价,F没有正价,B错误;同周期元素(0族元素除外)从左
到右,随着核电荷数的逐渐增多,原子核对外层电子的吸引力逐渐增强,因此原子半径逐渐
减小,C正确;在第三周期的元素中,Al为+3价,Na为+1价,但失电子能力Na>Al,D错误。
4.元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理
的是( )
A.由水溶液的酸性:HCl>HF,不能推断出元素的非金属性:Cl>F
B.人们可以在周期表的过渡元素中寻找催化剂和耐腐蚀、耐高温的合金材料
C.短周期元素正化合价数值和其族序数相同
D.短周期元素形成的微粒X2-和Y2+核外电子排布相同,离子半径:X2->Y2+
解析:选C。A项,非金属性的强弱应根据最高价氧化物对应水化物的酸性比较,不能根
据氢化物的酸性进行比较,HF的酸性比HCl弱,但非金属性:F>Cl,正确;B项,优良的催化
剂及耐高温和耐腐蚀的合金材料(如镍、铂等)大多属于过渡元素,正确;C项,短周期元素正
化合价数值和其族序数不一定相同,如C有+2、+4价,错误;D项,微粒X2-与Y2+核外电
子排布相同,核电荷数:Y>X,核电荷数越大,离子半径越小,故离子半径:X2->Y2+,正确。
5.(2019·茂名一模)前20号元素M、W、X、Y、Z的原子序数依次增大,M和W形成的某
种化合物可用作制冷剂,Y和Z能形成ZY 型离子化合物,ZY 的电子总数为38。下列有关叙
2 2
述中正确的是( )
A.W和X形成的化合物只有5种B.M和W形成的一种化合物的水溶液显碱性
C.W、X、Y三种元素的简单氢化物的沸点:Y>X>W
D.X和Z形成的化合物ZX 中,阳离子和阴离子的数目之比为1∶2
2
解析:选B。前20号元素M、W、X、Y、Z的原子序数依次增大,M和W形成的某种化合
物可用作制冷剂,则M为氢元素,W为氮元素;Y和Z能形成ZY 型离子化合物,ZY 的电子
2 2
总数为38,则Y为氟元素,Z为钙元素;根据M、W、X、Y、Z的原子序数依次增大可知,X为
氧元素。氮元素和氧元素形成的化合物有NO、NO、NO、NO 、NO、NO 等,A项错误;M
2 2 3 2 2 4 2 5
为氢元素,W为氮元素,二者可以形成化合物NH ,其水溶液显碱性,B项正确;W、X、Y三
3
种元素的简单氢化物分别为NH 、HO、HF,沸点:NH X>Y>Z
D.X、W、Q最高价氧化物对应水化物的酸性Q>X >W
解析:选B。这几种元素都是短周期元素,根据元素在周期表中的位置知,X、Y位于第二
周期,Z、W、Q位于第三周期,W原子的质子数是其M层电子数的3倍,设其M层电子数为
x,则W原子质子数=2+8+x,2+8+x=3x,所以x=5,则W为P元素,则X是N、Y是O、
Z是Al、Q是Cl。A.X、Y分别是N、O元素,二者能形成多种氮氧化物,如NO、NO、NO 、
2 2
NO、NO 等,所以X与Y可形成的化合物在5种以上,故A正确;B.Z是Al元素,氯化铝为
2 4 2 5
共价化合物,熔融状态下不导电,所以工业上采用电解熔融氧化铝的方法冶炼Al,故B错误;
C.电子层数越多其离子半径越大,电子层结构相同的离子,离子半径随着原子序数增大而减
小,所以离子半径:Q>X>Y>Z,故C正确;D.元素的非金属性越强,最高价氧化物对应水
化物的酸性越强,非金属性:Q>X>W,则最高价氧化物对应水化物的酸性Q>X >W,故D正
确。
7.(2019·岳阳高三质检)短周期W、X、Y、Z、Q五种元素的原子序数依次递增,W和Z位
于同一主族。已知W的氢化物可与Q单质在光照条件下反应生成多种化合物,Y的氧化物是
一种比较好的耐火材料,也是工业上冶炼Y的原料,X的最高价氧化物对应的水化物可与Z
单质反应产生常见的还原性气体单质E。下列说法不正确的是( )
A.X、Z的最高价氧化物相互化合,生成的产物可用作防火剂
B.电解X、Q元素组成的化合物的饱和溶液常被用于工业上制备X单质
C.W、X、Q三种元素都能形成多种氧化物
D.Y、Q形成的化合物是强电解质
解析:选B。由题中所给条件可推出,W为C,X为Na,Y为Al,Z为Si,Q为Cl。A项,
NaO和SiO 化合后生成硅酸钠,硅酸钠可用作防火剂,正确;B项,电解饱和氯化钠溶液可
2 2
得到氢气、氯气和NaOH,得不到金属钠,错误;C项,碳能形成CO和CO 两种氧化物,钠也
2
能形成NaO和NaO 两种氧化物,氯能形成ClO、ClO、ClO 、ClO 等多种氧化物,正确;D
2 2 2 2 2 3 2 2 5
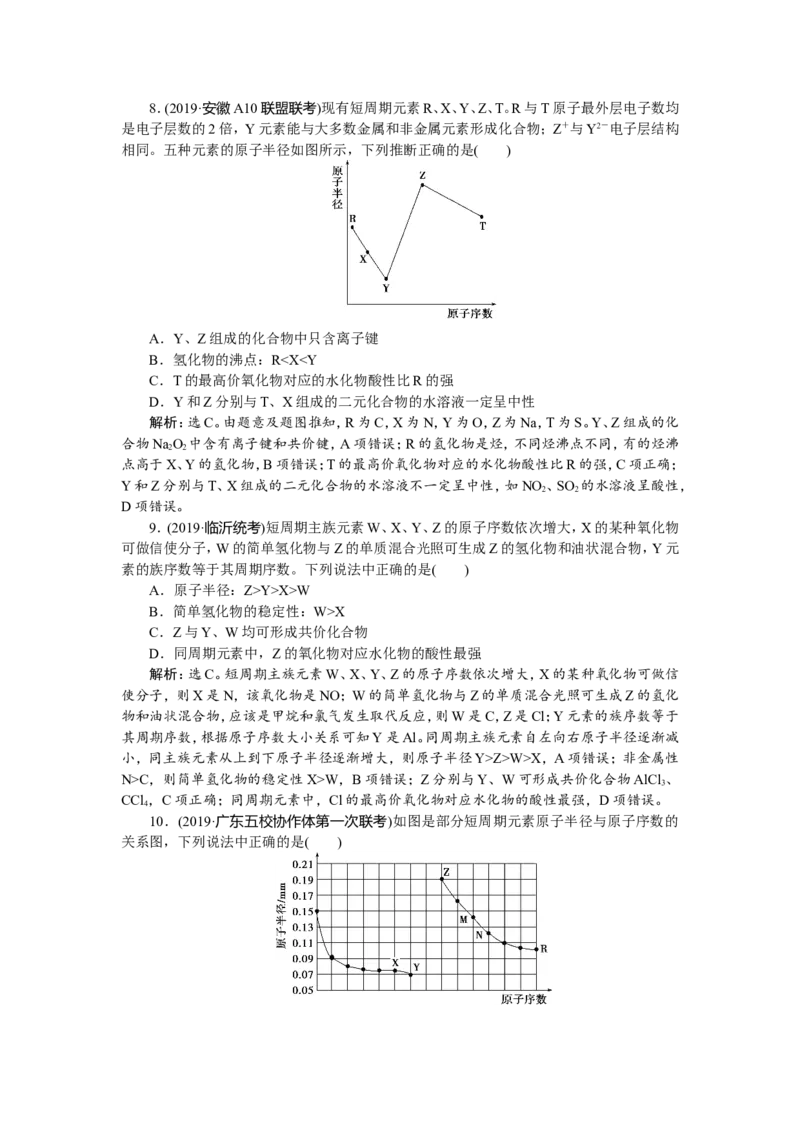
项,氯化铝在水中完全电离,为强电解质,正确。8.(2019·安徽A10联盟联考)现有短周期元素R、X、Y、Z、T。R与T原子最外层电子数均
是电子层数的2倍,Y元素能与大多数金属和非金属元素形成化合物;Z+与Y2-电子层结构
相同。五种元素的原子半径如图所示,下列推断正确的是( )
A.Y、Z组成的化合物中只含离子键
B.氢化物的沸点:RY>X>W
B.简单氢化物的稳定性:W>X
C.Z与Y、W均可形成共价化合物
D.同周期元素中,Z的氧化物对应水化物的酸性最强
解析:选C。短周期主族元素W、X、Y、Z的原子序数依次增大,X的某种氧化物可做信
使分子,则X是N,该氧化物是NO;W的简单氢化物与Z的单质混合光照可生成Z的氢化
物和油状混合物,应该是甲烷和氯气发生取代反应,则W是C,Z是Cl;Y元素的族序数等于
其周期序数,根据原子序数大小关系可知Y是Al。同周期主族元素自左向右原子半径逐渐减
小,同主族元素从上到下原子半径逐渐增大,则原子半径Y>Z>W>X,A项错误;非金属性
N>C,则简单氢化物的稳定性X>W,B项错误;Z分别与Y、W可形成共价化合物AlCl 、
3
CCl ,C项正确;同周期元素中,Cl的最高价氧化物对应水化物的酸性最强,D项错误。
4
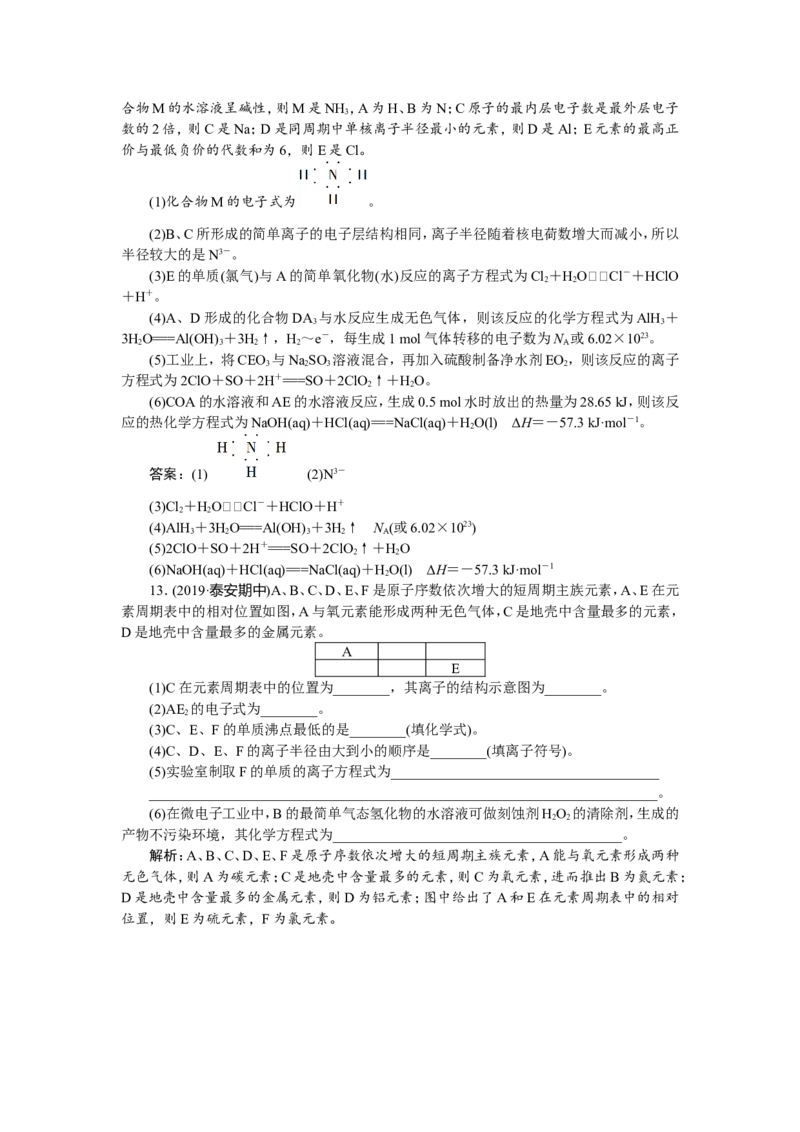
10.(2019·广东五校协作体第一次联考)如图是部分短周期元素原子半径与原子序数的
关系图,下列说法中正确的是( )A.M的最高价氧化物对应的水化物能分别与Z、R的最高价氧化物对应的水化物反应
B.Y的单质能从含R简单离子的水溶液中置换出R单质
C.X、N两种元素组成的化合物熔点很低
D.简单离子的半径:ZNa+>Al3+,D项错误。
二、非选择题
11.下表是元素周期表中的一部分。
族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
一 A
二 E F H J
三 B C D G I
根据A~J在周期表中的位置,用元素符号或化学式回答下列问题:
(1)化学性质最不活泼的元素是________,氧化性最强的单质是________,还原性最强的
单质是________。
(2)最高价氧化物对应的水化物中,碱性最强的是________,酸性最强的是________,呈
两性的是________。
(3)A分别与E、F、G、H、I形成的化合物中,最稳定的是________。
(4)在B、C、D、G、I中,原子半径最大的是________。
解析:由元素在周期表中的位置可知,A为H,B为Na,C为Mg,D为Al,E为C,F为
N,G为S,H为F,I为Cl,J为Ne。
答案:(1)Ne F Na (2)NaOH HClO Al(OH)
2 4 3
(3)HF (4)Na
12.(2019·安徽A10联盟联考)已知A、B、C、D、E为原子序数依次增大的五种短周期元
素,A与B形成的最简单共价化合物M的水溶液呈碱性,C原子的最内层电子数是最外层电
子数的2倍,D是同周期中单核离子半径最小的元素,E元素的最高正价与最低负价的代数
和为6。请回答下列问题:
(1)化合物M的电子式为________________。
(2)B、C所形成的简单离子中,半径较大的是________(用离子符号表示)。
(3)E的单质与A的简单氧化物反应的离子方程式为
________________________________________________________________________。
(4)A、D 形成的化合物 DA 与水反应生成无色气体,则该反应的化学方程式为
3
__________________________,每生成1 mol气体转移的电子数为________。
(5)工业上,将CEO 与NaSO 溶液混合,再加入硫酸制备净水剂EO,则该反应的离子
3 2 3 2
方程式为_________________________________________________________________
________________________________________________________________________。
(6)COA的水溶液和AE的水溶液反应生成0.5 mol水时放出的热量为28.65 kJ,则该反
应的热化学方程式为
________________________________________________________________________。
解析:已知A、B、C、D、E为原子序数依次增大的五种短周期元素,A与B形成的共价化合物M的水溶液呈碱性,则M是NH ,A为H、B为N;C原子的最内层电子数是最外层电子
3
数的2倍,则C是Na;D是同周期中单核离子半径最小的元素,则D是Al;E元素的最高正
价与最低负价的代数和为6,则E是Cl。
(1)化合物M的电子式为 。
(2)B、C所形成的简单离子的电子层结构相同,离子半径随着核电荷数增大而减小,所以
半径较大的是N3-。
(3)E的单质(氯气)与A的简单氧化物(水)反应的离子方程式为Cl +HOCl-+HClO
2 2
+H+。
(4)A、D形成的化合物DA 与水反应生成无色气体,则该反应的化学方程式为AlH +
3 3
3HO===Al(OH) +3H↑,H~e-,每生成1 mol气体转移的电子数为N 或6.02×1023。
2 3 2 2 A
(5)工业上,将CEO 与NaSO 溶液混合,再加入硫酸制备净水剂EO,则该反应的离子
3 2 3 2
方程式为2ClO+SO+2H+===SO+2ClO ↑+HO。
2 2
(6)COA的水溶液和AE的水溶液反应,生成0.5 mol水时放出的热量为28.65 kJ,则该反
应的热化学方程式为NaOH(aq)+HCl(aq)===NaCl(aq)+HO(l) ΔH=-57.3 kJ·mol-1。
2
答案:(1) (2)N3-
(3)Cl +HOCl-+HClO+H+
2 2
(4)AlH +3HO===Al(OH) +3H↑ N (或6.02×1023)
3 2 3 2 A
(5)2ClO+SO+2H+===SO+2ClO ↑+HO
2 2
(6)NaOH(aq)+HCl(aq)===NaCl(aq)+HO(l) ΔH=-57.3 kJ·mol-1
2
13.(2019·泰安期中)A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A、E在元
素周期表中的相对位置如图,A与氧元素能形成两种无色气体,C是地壳中含量最多的元素,
D是地壳中含量最多的金属元素。
A
E
(1)C在元素周期表中的位置为________,其离子的结构示意图为________。
(2)AE 的电子式为________。
2
(3)C、E、F的单质沸点最低的是________(填化学式)。
(4)C、D、E、F的离子半径由大到小的顺序是________(填离子符号)。
(5)实验室制取F的单质的离子方程式为______________________________________
________________________________________________________________________。
(6)在微电子工业中,B的最简单气态氢化物的水溶液可做刻蚀剂HO 的清除剂,生成的
2 2
产物不污染环境,其化学方程式为_________________________________________。
解析:A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A能与氧元素形成两种
无色气体,则A为碳元素;C是地壳中含量最多的元素,则C为氧元素,进而推出B为氮元素;
D是地壳中含量最多的金属元素,则D为铝元素;图中给出了A和E在元素周期表中的相对
位置,则E为硫元素,F为氯元素。(4)S2->Cl->O2->Al3+
(5)MnO +4H++2Cl-=====Mn2++Cl↑+2HO
2 2 2
(6)2NH ·H O+3HO===N ↑+8HO
3 2 2 2 2 2
14.X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为
1∶2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R
的氧化物均能形成酸雨。请回答下列问题:
(1)元素X的最高价氧化物的电子式为____________;元素Z的离子结构示意图为
____________________。
(2)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(3)元素W位于周期表的第________族,其非金属性比R弱,用原子结构的知识解释原
因:________________________________________________________________________
________________________________________________________________________。
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液做该氧化物
的吸收剂,写出吸收剂与足量该氧化物反应的离子方程式:_____________________
________________________________________________________________________。
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和
Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1∶3,则该反应的化
学方程式为______________________________________________。
解析:由X原子核外各层电子数之比为1∶2,推出X为C;由Y的氧化物和R的氧化物
均能形成酸雨且R的原子序数大于Y,推出Y和R分别为N和S;由W和R是同周期相邻
元素且R的原子序数大于W,推出W为P;由Y原子和Z原子的核外电子数之和为20,推出
Z为Al。(4)氨水与足量SO 反应生成NH HSO 。
2 4 3
答案:(1) ,
(2)3Cu+8HNO(稀)===3Cu(NO)+2NO↑+4HO
3 3 2 2
(3)ⅤA P原子和S原子的电子层数相同,P原子半径较大,得电子能力较弱
(4)SO +NH ·H O===HSO+NH
2 3 2
(5)AlO+3C+N=====2AlN+3CO
2 3 2