文档内容
章末综合检测(四)
(时间:45分钟 分值:100分)
一、选择题(本题包括10小题,每小题6分,共60分)
1.(2019·抚顺一模)化学与生活、社会发展息息相关,下列说法正确的是( )
A.华为自主研发的“麒麟”芯片与光导纤维是同种材料
B.近期出现在抚顺的雾霾是一种分散系,含活性炭的口罩防雾霾的原理是吸附作用
C.煤炭经蒸馏、气化和液化等过程,可获得清洁能源和重要的化工原料
D.“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料
解析:选B。硅为良好的半导体,用作芯片,光导纤维的主要成分为二氧化硅,为绝缘体,
它们不是同种材料,A错误。活性炭具有疏松多孔的结构,具有吸附性,而雾霾是一种分散系,
分散剂是空气,含活性炭的口罩防雾霾的原理是吸附作用,B正确。煤炭气化生成CO和氢气,
液化生成甲醇,可获得清洁能源和重要的化工原料,蒸馏为分离液体混合物的方法,故煤炭不
能蒸馏,C错误。特种钢缆为金属材料,不是非金属材料,D错误。
2.(2019·张家口高三模拟)“飘尘”是物质燃烧时产生的粒状漂浮物,颗粒很小(直径小于
10-7 m),不宜沉降(可漂浮数小时甚至数年),它与空气中的SO 、O 接触时,SO 会转化为
2 2 2
SO ,使空气酸度增加,飘尘所起的主要作用与下列变化中硫酸的作用相同的是( )
3
A.胆矾中加浓硫酸
B.浓硫酸与木炭共热
C.乙酸乙酯与稀硫酸共热
D.浓硫酸滴到蔗糖中制“黑面包”
解析:选C。题中“飘尘”起催化剂的作用,C中稀硫酸做催化剂。
3.N、O、Si、S是重要的非金属元素。下列说法正确的是( )
A.N、O、S、Si的原子半径逐渐增大,非金属性逐渐减弱
B.氮的氧化物和硫的氧化物既是形成光化学烟雾的主要物质,又是形成酸雨的主要物质
C.汽车尾气中排放的氮氧化物主要是由游离态氮转化来的
D.N、Si、S的单质均能和氧气反应,生成的产物分别是NO 、SiO 和SO
2 2 2
解析:选C。同周期元素自左向右原子半径逐渐减小,非金属性逐渐增强。同主族元素自
上而下原子半径逐渐增大,则O、N、S、Si的原子半径逐渐增大,非金属性逐渐减弱,A错误;
硫的氧化物不能形成光化学烟雾,B错误;汽车尾气中的NO 主要是空气中的N、O 在汽车汽
x 2 2
缸内化合生成的,C正确;N 和O 反应生成NO,得不到NO ,D错误。
2 2 2
4.(2019·安阳高三模拟)根据下列实验操作和现象所得到的结论正确的是( )
选项 实验操作和现象 结论
强酸性溶液X中加入Ba(NO ) 溶液,静
3 2
A 置后再加入KSCN溶液,先生成白色沉 溶液X中一定含有SO和Fe3+
淀,后溶液变红
检验HCl气体中是否含有Cl,将气体通
2
B 入品红溶液中,品红溶液褪色,加热后溶 证明含有Cl
2
液不恢复成红色
室温下,向FeCl 溶液中滴加少量KI溶
C 3 Fe3+的还原性比I 的强
液,再滴加几滴淀粉溶液,溶液变蓝色 2
加热盛有NH Cl固体的试管,试管底部
D 4 NH Cl固体易升华
固体消失,试管口有晶体凝结 4
解析:选B。氯气与水反应生成HClO,可使品红溶液褪色,加热不恢复,则证明HCl气体
中含有Cl,故B正确。
25.(2019·高考全国卷Ⅲ)下列实验不能达到目的的是( )
选项 目的 实验
A 制取较高浓度的次氯酸溶液 将Cl 通入碳酸钠溶液中
2
B 加快氧气的生成速率 在过氧化氢溶液中加入少量MnO
2
C 除去乙酸乙酯中的少量乙酸 加入饱和碳酸钠溶液洗涤、分液
D 制备少量二氧化硫气体 向饱和亚硫酸钠溶液中滴加浓硫酸
解析:选A。Cl 与水反应生成HCl和HClO,且该反应为可逆反应,NaCO 水解使溶液呈
2 2 3
碱性,水解产生的OH-能同时消耗HCl和HClO,A符合题意;向过氧化氢溶液中加入少量
MnO 能加快HO 的分解,从而加快氧气的生成速率,B不符合题意;饱和碳酸钠溶液可除去
2 2 2
乙酸乙酯中的少量乙酸,而且能降低乙酸乙酯的溶解度,便于分液,C不符合题意;向饱和亚
硫酸钠溶液中滴加浓硫酸,符合用强酸制备弱酸的原理,可制备少量二氧化硫气体,D不符合
题意。
6.某化学兴趣小组进行有关Cu、硝酸、硫酸化学性质的实验,实验过程如图所示。下列有
关说法正确的是( )
A.实验①中溶液呈蓝色,试管口有红棕色气体产生,稀硝酸被还原为NO
2
B.实验③中反应的化学方程式:3Cu+Cu(NO )+4HSO ===4CuSO+2NO↑+4HO
3 2 2 4 4 2
C.实验③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强
D.由上述实验可知,Cu在常温下既可与稀硝酸反应,也可与稀硫酸反应
解析:选B。A项,实验①中溶液呈蓝色,试管口有红棕色气体产生,稀硝酸被Cu还原为
NO,NO在试管口遇到空气中的氧气生成NO ,错误;B项,③中反应的化学方程式为3Cu+
2
Cu(NO )+4HSO ===4CuSO+2NO↑+4HO,正确;C项,实验③中滴加稀硫酸,提供H+,
3 2 2 4 4 2
铜片继续溶解,硝酸根离子在酸性条件下等同于硝酸,错误;D项,由题述实验可得出结论:硝
酸根离子在酸性条件下等同于硝酸,错误。
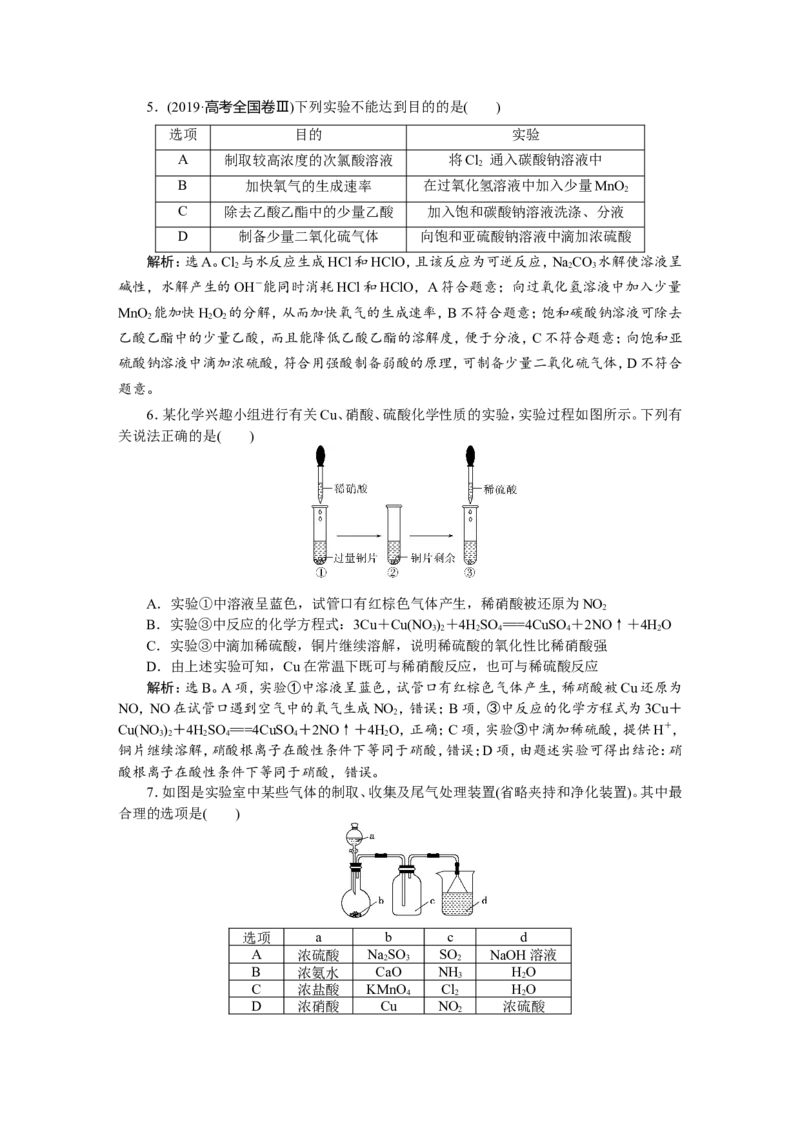
7.如图是实验室中某些气体的制取、收集及尾气处理装置(省略夹持和净化装置)。其中最
合理的选项是( )
选项 a b c d
A 浓硫酸 NaSO SO NaOH溶液
2 3 2
B 浓氨水 CaO NH HO
3 2
C 浓盐酸 KMnO Cl HO
4 2 2
D 浓硝酸 Cu NO 浓硫酸
2解析:选A。SO 可以被NaOH溶液吸收,A正确;NH 的密度小于空气,应从短管进入,B
2 3
错误;Cl 不能用水吸收,C错误;NO 应用碱液吸收,D错误。
2 2
8.A是中学化学中常见的单质,B、C为化合物。它们有如图所示的转化关系(部分产物及
反应条件省略)。下列判断正确的是( )
A.A可能是金属,也可能是非金属
B.A、B、C含有一种相同的元素
C.B、C的水溶液一定都呈碱性
D.反应①②不一定都是氧化还原反应
解析:选B。A单质在碱性条件下发生反应生成B、C两种化合物,发生了氧化还原反应,
元素A的化合价既升高又降低,存在负化合价,应为非金属元素,金属元素不存在负化合价,
A项错误;A单质发生歧化反应生成B、C两种化合物,则A、B、C含有一种相同的元素,B项
正确;若A单质为氯气,与氢氧化钠反应生成氯化钠和次氯酸钠,氯化钠的水溶液呈中性,C
项错误;单质生成化合物,元素的化合价发生变化,化合物生成单质,元素的化合价也发生变
化,所以反应①和反应②一定都属于氧化还原反应,D项错误。
9.(2019·湖北九校联考)甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它
们之间具有如下转化关系:甲――→乙丙。下列有关物质的推断不正确的是( )
A.若甲为AlCl 溶液,则丁可能是NaOH溶液
3
B.若甲为氮气,则丁可能是O
2
C.若甲为Fe,则丁可能是稀硝酸
D.若甲为NaOH溶液,则丁可能是CO
2
解析:选B。若甲为AlCl 溶液,丁是NaOH溶液,则乙是氢氧化铝,丙是偏铝酸钠,AlO和
3
Al3+发生双水解可生成乙(氢氧化铝),能够实现转化,A正确。若甲为氮气,丁是O,则乙是
2
NO,丙是NO ,但NO 和氮气不能反应生成NO,不能实现转化,B错误。若甲为Fe,丁是稀硝
2 2
酸,过量的铁和硝酸反应生成硝酸亚铁(乙),硝酸亚铁再与硝酸反应生成硝酸铁,硝酸铁和铁
能反应生成硝酸亚铁,能够实现转化,C正确。若甲为NaOH溶液,丁是CO,则乙是碳酸钠,
2
丙是碳酸氢钠,碳酸氢钠和氢氧化钠反应生成碳酸钠,能够实现转化,D正确。
10.将6.4 g铜与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO 混合气体的
2
体积为3.36 L(标准状况),其中NO的体积为(标准状况)( )
A.0.56 L B.1.344 L
C.2.016 L D.2.8 L
解析:选A。6.4 g铜的物质的量是0.1 mol,标准状况下3.36 L气体的物质的量是0.15
mol,设NO的物质的量为x,NO 的物质的量为y,则x+y=0.15 mol,3x+y=0.1 mol×2,解
2
得x=0.025 mol,y=0.125 mol,标准状况下NO的体积为0.025 mol×22.4 L·mol-1=0.56 L。
二、非选择题(本题包括3小题,共40分)
11.(13分)碳、硅及其化合物的开发由来已久,在现代生活中有广泛应用。
(1)SiO 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃应用橡胶塞的原因是
2
________________________________________________________________________
(用化学方程式表示)。
(2)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多
种路线,其中一种工艺流程示意图及主要反应如下:
HCl H
2↓ ↓
―→―→―→高纯硅
电弧炉 流化床反应器 还原炉
① 用 石 英 砂 和 焦 炭 在 电 弧 炉 中 制 粗 硅 , 该 反 应 的 化 学 方 程 式 为
________________________________________________________________________。
②在流化床反应的产物中,SiHCl 大约占85%,还有SiCl 、SiHCl、SiHCl等,有关物质
3 4 2 2 3
的沸点数据如表所示,提纯SiHCl 的主要工艺操作依次是沉降、冷凝和________。
3
物质 Si SiCl SiHCl SiHCl SiHCl HCl SiH
4 3 2 2 3 4
沸点/℃ 2 355 57.6 31.8 8.2 -30.4 -84.9 -111.9
③SiHCl 极易水解,其完全水解的化学方程式为_____________________________
3
________________________________________________________________________。
(3)某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹
持仪器已略去,气密性已检验),实验操作步骤:
Ⅰ.打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ.A中看到白色沉淀时,关闭弹簧夹1,打开弹簧夹2,关闭活塞a。
①B中反应的离子方程式是_______________________________________________。
②通过步骤Ⅰ知浓盐酸具有的性质是________(填字母)。
A.挥发性 B.还原性
C.氧化性 D.酸性
③ C 装置中的试剂 X 是________(填化学式)。D 中反应的化学方程式是
________________________________________________________________________。
④碳、硅的非金属性逐渐减弱的原因:______________________________________
________________________________________________________________________。
解析:(1)玻璃中的二氧化硅与NaOH溶液反应。
(2)①石英砂的主要成分为二氧化硅,二氧化硅和碳在高温条件下反应生成硅和一氧化碳;
②由于SiHCl 与SiCl 、SiHCl 等的沸点相差较大,可以使用蒸馏的方法提纯;
3 4 2 2
③SiHCl 中Si是+4价,氢元素、氯元素均为-1价,SiHCl 完全水解时,Si以HSiO 形
3 3 2 3
式存在,-1价的氢元素与HO反应后生成H。
2 2
(3)①B中盐酸与碳酸钙发生反应的离子方程式是CaCO +2H+===Ca2++CO↑+HO;
3 2 2
②步骤Ⅰ是为了验证浓盐酸是否具有挥发性(看A中是否产生沉淀)和酸性(与盐反应);
③因为浓盐酸具有挥发性,所以C装置的作用是将HCl气体除去,可以使用的试剂为饱
和NaHCO 溶液;D中反应的化学方程式是NaSiO+CO+HO===H SiO↓+NaCO,也可
3 2 3 2 2 2 3 2 3
以生成NaHCO ,答案合理即可;
3
④由于碳和硅位于同一主族,从上到下,原子半径逐渐增大,得电子的能力减弱,非金属
性减弱,所以碳、硅的非金属性逐渐减弱。
答案:(1)SiO+2NaOH===Na SiO+HO
2 2 3 2
(2)①SiO+2C=====Si+2CO↑
2②蒸馏
③SiHCl +4HO===H SiO↓+H↑+3HCl↑(或SiHCl +3HO===H SiO↓+H↑+
3 2 4 4 2 3 2 2 3 2
3HCl↑)
(3)①CaCO +2H+===Ca2++CO↑+HO ②AD
3 2 2
③NaHCO NaSiO +CO +HO===H SiO↓+NaCO(答案合理即可) ④碳和硅位于
3 2 3 2 2 2 3 2 3
同一主族,从上到下,原子半径逐渐增大,得电子的能力逐渐减弱,非金属性逐渐减弱
12.(13分)某化学学习小组采用下列装置,对浓硝酸与木炭的反应进行探究(已知:
4HNO=====4NO ↑+O↑+2HO)。
3 2 2 2
请回答下列问题:
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,立即伸入三颈烧
瓶 中 , 并 塞 紧 瓶 塞 , 滴 加 浓 硝 酸 , 可 观 察 到 三 颈 烧 瓶 中 气 体 的 颜 色 为
________________________________________________________________________,
产生该气体的主要化学反应方程式是________________________________________
________________________________________________________________________。
(2)装置C中盛有足量Ba(OH) 溶液,反应一段时间后可观察到C中出现白色沉淀,该白
2
色沉淀为________________________________________________________________________
(填化学式)。其中的Ba(OH) 溶液________(填“能”或“不能”)用Ca(OH) 溶液代替,
2 2
理由是________________________________________________________________________
________________________________________________________________________。
(3)装置B的作用是_______________________________________________。
(4)装置D中收集到了无色气体,部分同学认为是NO,还有部分同学认为是O。
2
①下列对该气体的检验方法合适的是______(填序号)。
A.敞口观察集气瓶内气体的颜色变化
B.将润湿的蓝色石蕊试纸伸入集气瓶内,观察试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
② 如 果 集 气 瓶 中 收 集 到 的 无 色 气 体 是 氧 气 , 则 氧 气 的 来 源 是
________________________________________________________________________。
解析:(1)装置A中发生的是浓硝酸与木炭的反应,生成NO 、CO、HO,由于NO 为红棕
2 2 2 2
色气体,故三颈烧瓶中的气体颜色为红棕色。(2)将NO 、CO 通入Ba(OH) 溶液中分别生成
2 2 2
Ba(NO ) 和BaCO ,由于Ba(OH) 溶液足量,故溶液为碱性环境,BaCO 不溶解以沉淀形式析
3 2 3 2 3
出。Ba(OH) 溶液不能用Ca(OH) 溶液代替,因为Ca(OH) 微溶于水,溶液中Ca(OH) 含量太
2 2 2 2
少,浓度太低,不足以完全吸收生成的酸性气体,导致溶液呈酸性,从而不能生成CaCO 沉淀。
3
(3)装置B可以防止装置C中酸性气体因溶解速率太快而出现倒吸。(4)①NO与O 反应生成
2
红棕色的NO ,A正确;NO和O 均不具有酸性,B错误;O 能使带火星的木条复燃,而NO不
2 2 2
能,C正确。②装置A中除发生木炭与浓硝酸的反应外,还发生浓硝酸的分解反应。
答案:(1)红棕色 C+4HNO(浓)=====4NO ↑+CO↑+2HO (2)BaCO 不能
3 2 2 2 3
Ca(OH) 溶液中Ca(OH) 浓度较低,不能形成CaCO 沉淀
2 2 3
(3)防倒吸(4)①AC ②浓硝酸的分解
13.(14分)世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效
“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈
黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热。实
验室以电解法制备ClO 的流程如下:
2
已知:①NCl 是黄色黏稠状液体或斜方形晶体,极易爆炸,有类似氯气的刺激性气味,自
3
燃爆炸点为95 ℃,在热水中易分解,在空气中易挥发,不稳定。
②气体B能使湿润的红色石蕊试纸变蓝。
回答下列问题:
(1)电解时,发生反应的化学方程式为____________________________________
________________________________________________________________________。
实验室制备气体B的化学方程式为____________________________________
________________________________________________________________________。
为保证实验的安全,在电解时需注意的问题是
①控制好生成NCl 的浓度;
3
②________________________________________________________________________。
(2)NCl 与NaClO(亚氯酸钠)按物质的量之比为1∶6混合,在溶液中恰好反应生成ClO ,
3 2 2
该反应的离子方程式为______________________________________________________。
(3)ClO 很不稳定,需随用随制,产物用水吸收得到ClO 溶液。为测定所得溶液中ClO 的
2 2 2
含量,进行了下列实验:
步骤1:准确量取ClO 溶液10 mL,稀释成100 mL试样;
2
步骤2:量取V mL试样加入锥形瓶中,调节试样的pH≤2.0,加入足量的KI晶体,摇匀,
1
在暗处静置30 min;
步骤3:以淀粉溶液做指示剂,用c mol·L-1 NaSO 溶液滴定至终点,消耗NaSO 溶液
2 2 3 2 2 3
V mL。(已知I+2SO===2I-+SO)
2 2 2 4
①上述步骤3中滴定终点的现象是_________________________________
________________________________________________________________________;
②根据上述步骤可计算出原ClO 溶液的密度为________g·L-1(用含字母的代数式表示)。
2
解析:(1)NH Cl溶液中加入盐酸进行电解得到NCl ,结合元素守恒及离子放电顺序可知
4 3
A为氢气,故电解反应的化学方程式为NH Cl+2HCl=====3H↑+NCl ;气体B能使湿润的
4 2 3
红色石蕊试纸变蓝,则B为氨,实验室制氨的化学方程式为2NH Cl+Ca(OH) =====CaCl +
4 2 2
2NH ↑+2HO;由于NCl 自燃爆炸点为95 ℃,在热水中易分解,所以在电解时除控制好生成
3 2 3
NCl 的浓度外,还要控制好反应温度。
3
(2)NCl 与ClO反应生成NH 、ClO ,离子方程式为NCl +6ClO+3HO===6ClO ↑+
3 3 2 3 2 2
NH ↑+3Cl-+3OH-。
3
(3)①上述步骤3中,滴定前溶液中含碘单质,所以淀粉溶液为蓝色,滴定过程中碘单质
逐渐消耗,蓝色逐渐变浅,所以滴定终点的现象是滴入最后一滴NaSO 溶液后,溶液从蓝色
2 2 3
变成无色,且30 s内不变色;
②由题知,2ClO ~5I~10SO,n(S O)=cV×10-3 mol,原溶液中n(ClO )=×= mol,
2 2 2 2 2 2
m(ClO )= g= g,所以原ClO 溶液的密度为= g·L-1。
2 2答案:(1)NH Cl+2HCl=====3H↑+NCl
4 2 3
2NH Cl+Ca(OH) =====CaCl +2NH ↑+2HO
4 2 2 3 2
控制好反应温度
(2)NCl +6ClO+3HO===6ClO ↑+NH ↑+3Cl-+3OH-
3 2 2 3
(3)①滴入最后一滴NaSO 溶液后,溶液从蓝色变成无色,且30 s内不变色
2 2 3
②