文档内容
专练 9 氧化还原反应基本概念
一、单项选择题
1.[2022·浙江1月,10]关于反应4CO +SiH=====4CO+2HO+SiO ,下列说法正确
2 4 2 2
的是( )
A.CO是氧化产物
B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4
D.生成1 mol SiO 时,转移8 mol电子
2
2.[2021·浙江1月]关于反应8NH +6NO ===7N +12HO,下列说法正确的是( )
3 2 2 2
A.NH 中H元素被氧化
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为3∶4
D.氧化产物与还原产物的质量之比为4∶3
3.[2020·山东,2]下列叙述不涉及氧化还原反应的是( )
A.谷物发酵酿造食醋
B.小苏打用作食品膨松剂
C.含氯消毒剂用于环境消毒
D.大气中NO 参与酸雨形成
2
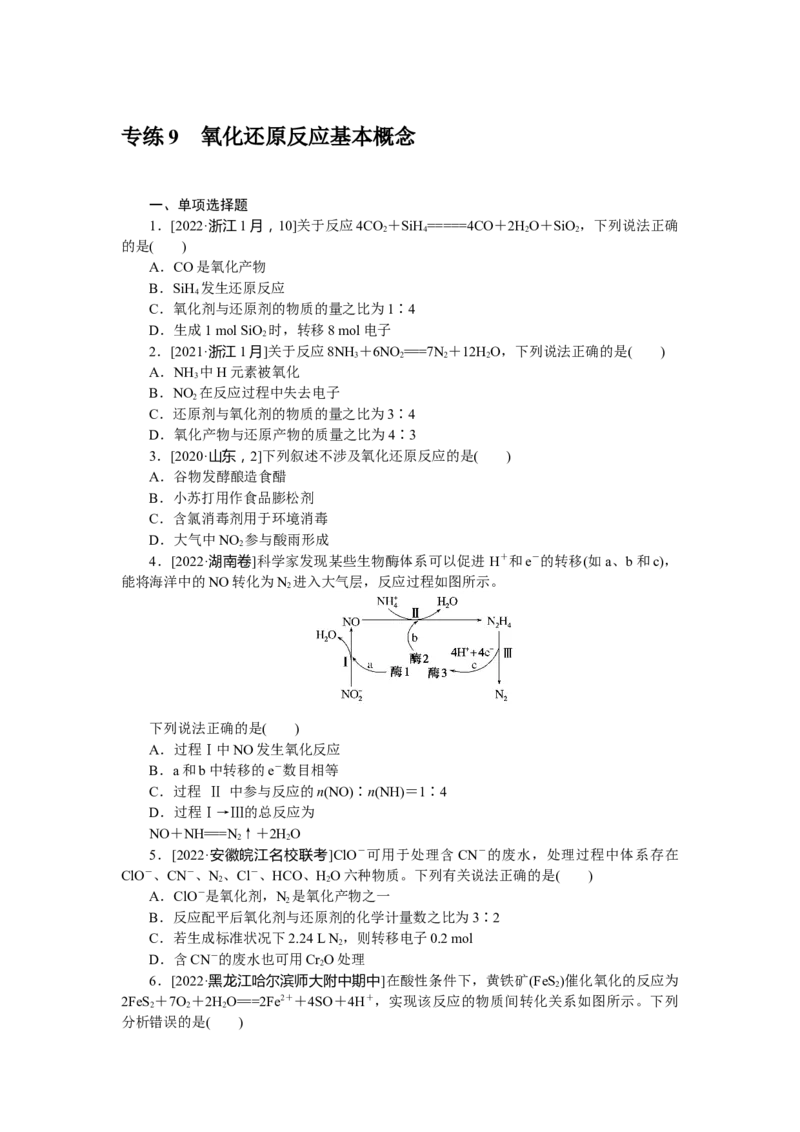
4.[2022·湖南卷]科学家发现某些生物酶体系可以促进 H+和e-的转移(如a、b和c),
能将海洋中的NO转化为N 进入大气层,反应过程如图所示。
2
下列说法正确的是( )
A.过程Ⅰ中NO发生氧化反应
B.a和b中转移的e-数目相等
C.过程 Ⅱ 中参与反应的n(NO)∶n(NH)=1∶4
D.过程Ⅰ→Ⅲ的总反应为
NO+NH===N ↑+2HO
2 2
5.[2022·安徽皖江名校联考]ClO-可用于处理含CN-的废水,处理过程中体系存在
ClO-、CN-、N、Cl-、HCO、HO六种物质。下列有关说法正确的是( )
2 2
A.ClO-是氧化剂,N 是氧化产物之一
2
B.反应配平后氧化剂与还原剂的化学计量数之比为3∶2
C.若生成标准状况下2.24 L N ,则转移电子0.2 mol
2
D.含CN-的废水也可用Cr O处理
2
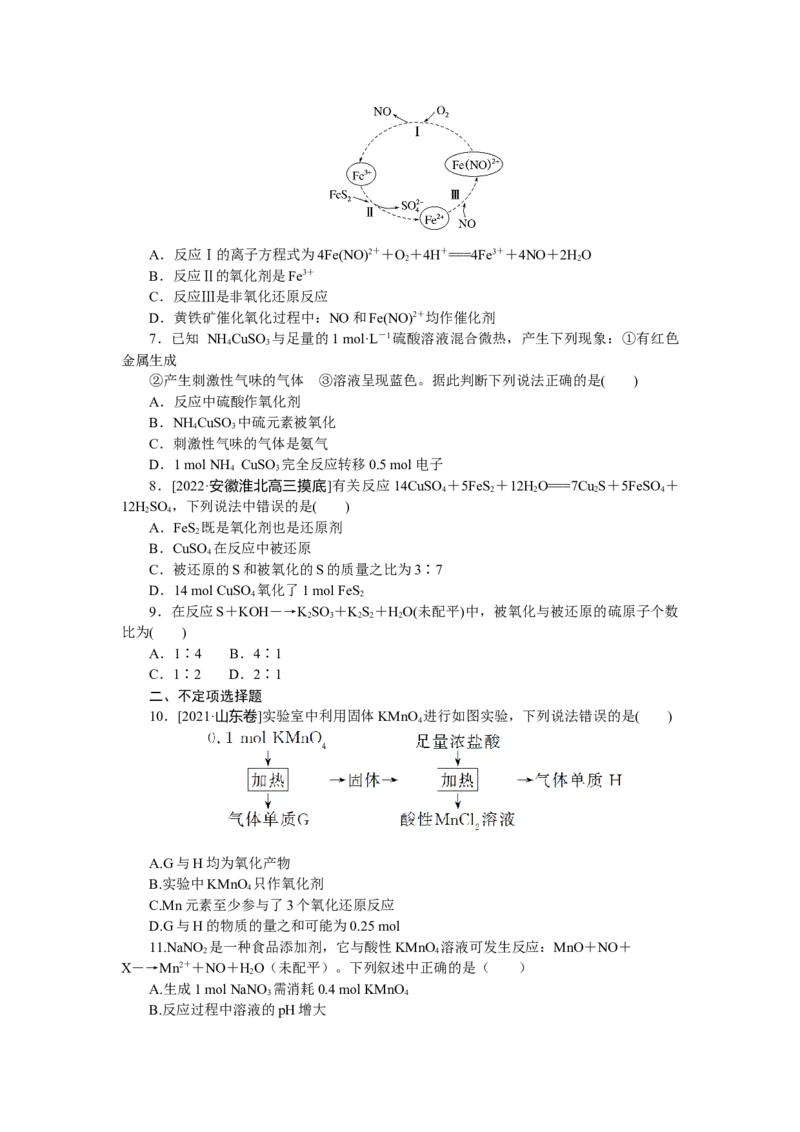
6.[2022·黑龙江哈尔滨师大附中期中]在酸性条件下,黄铁矿(FeS )催化氧化的反应为
2
2FeS +7O +2HO===2Fe2++4SO+4H+,实现该反应的物质间转化关系如图所示。下列
2 2 2
分析错误的是( )A.反应Ⅰ的离子方程式为4Fe(NO)2++O+4H+===4Fe3++4NO+2HO
2 2
B.反应Ⅱ的氧化剂是Fe3+
C.反应Ⅲ是非氧化还原反应
D.黄铁矿催化氧化过程中:NO和Fe(NO)2+均作催化剂
7.已知 NH CuSO 与足量的1 mol·L-1硫酸溶液混合微热,产生下列现象:①有红色
4 3
金属生成
②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是( )
A.反应中硫酸作氧化剂
B.NH CuSO 中硫元素被氧化
4 3
C.刺激性气味的气体是氨气
D.1 mol NH CuSO 完全反应转移0.5 mol电子
4 3
8.[2022·安徽淮北高三摸底]有关反应14CuSO +5FeS +12HO===7Cu S+5FeSO +
4 2 2 2 4
12HSO ,下列说法中错误的是( )
2 4
A.FeS 既是氧化剂也是还原剂
2
B.CuSO 在反应中被还原
4
C.被还原的S和被氧化的S的质量之比为3∶7
D.14 mol CuSO 氧化了1 mol FeS
4 2
9.在反应S+KOH―→KSO +KS +HO(未配平)中,被氧化与被还原的硫原子个数
2 3 2 2 2
比为( )
A.1∶4 B.4∶1
C.1∶2 D.2∶1
二、不定项选择题
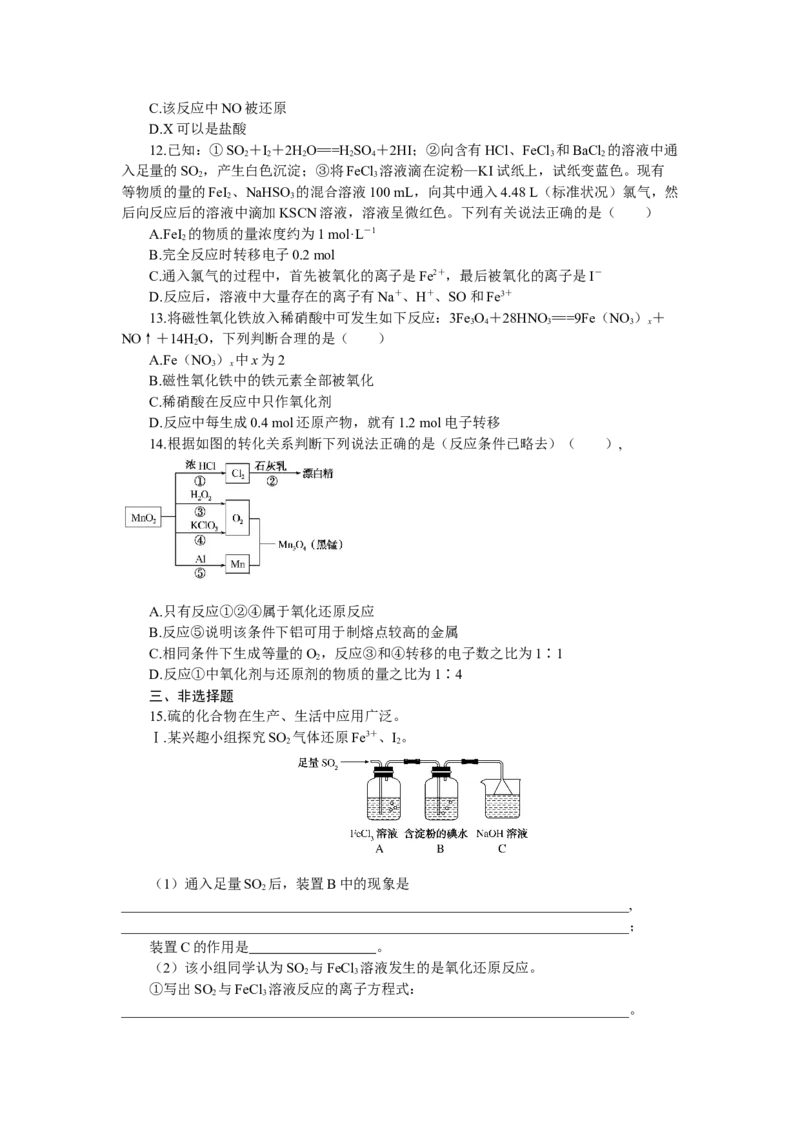
10.[2021·山东卷]实验室中利用固体KMnO 进行如图实验,下列说法错误的是( )
4
A.G与H均为氧化产物
B.实验中KMnO 只作氧化剂
4
C.Mn元素至少参与了3个氧化还原反应
D.G与H的物质的量之和可能为0.25 mol
11.NaNO 是一种食品添加剂,它与酸性KMnO 溶液可发生反应:MnO+NO+
2 4
X―→Mn2++NO+HO(未配平)。下列叙述中正确的是( )
2
A.生成1 mol NaNO 需消耗0.4 mol KMnO
3 4
B.反应过程中溶液的pH增大C.该反应中NO被还原
D.X可以是盐酸
12.已知:①SO +I+2HO===H SO +2HI;②向含有HCl、FeCl 和BaCl 的溶液中通
2 2 2 2 4 3 2
入足量的SO ,产生白色沉淀;③将FeCl 溶液滴在淀粉—KI试纸上,试纸变蓝色。现有
2 3
等物质的量的FeI、NaHSO 的混合溶液100 mL,向其中通入4.48 L(标准状况)氯气,然
2 3
后向反应后的溶液中滴加KSCN溶液,溶液呈微红色。下列有关说法正确的是( )
A.FeI 的物质的量浓度约为1 mol·L-1
2
B.完全反应时转移电子0.2 mol
C.通入氯气的过程中,首先被氧化的离子是Fe2+,最后被氧化的离子是I-
D.反应后,溶液中大量存在的离子有Na+、H+、SO和Fe3+
13.将磁性氧化铁放入稀硝酸中可发生如下反应:3Fe O+28HNO===9Fe(NO )+
3 4 3 3 x
NO↑+14HO,下列判断合理的是( )
2
A.Fe(NO ) 中x为2
3 x
B.磁性氧化铁中的铁元素全部被氧化
C.稀硝酸在反应中只作氧化剂
D.反应中每生成0.4 mol还原产物,就有1.2 mol电子转移
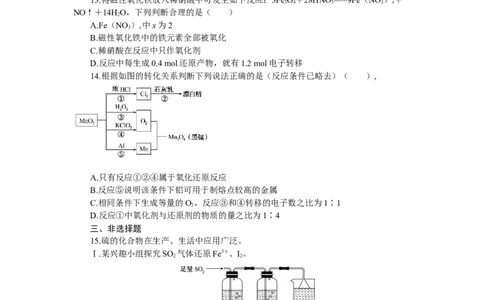
14.根据如图的转化关系判断下列说法正确的是(反应条件已略去)( ),
A.只有反应①②④属于氧化还原反应
B.反应⑤说明该条件下铝可用于制熔点较高的金属
C.相同条件下生成等量的O,反应③和④转移的电子数之比为1∶1
2
D.反应①中氧化剂与还原剂的物质的量之比为1∶4
三、非选择题
15.硫的化合物在生产、生活中应用广泛。
Ⅰ.某兴趣小组探究SO 气体还原Fe3+、I。
2 2
(1)通入足量SO 后,装置B中的现象是
2
________________________________________________________________________,
________________________________________________________________________;
装置C的作用是 。
(2)该小组同学认为SO 与FeCl 溶液发生的是氧化还原反应。
2 3
①写出SO 与FeCl 溶液反应的离子方程式:
2 3
________________________________________________________________________。②请设计实验方案验证有Fe2+生成:
________________________________________________________________________,
________________________________________________________________________,
________________________________________________________________________。
Ⅱ.一些食品添加剂、抗氧化剂中含有焦亚硫酸钠(NaSO),大量的焦亚硫酸钠会损
2 2 5
伤细胞,具有生物毒性。
(3)铬是环境中的一种主要污染物,可以用焦亚硫酸钠(NaSO)处理含铬酸性废
2 2 5
水(含有CrO),利用氧化还原反应,将六价铬还原为三价铬,SO被氧化为SO,该反应
2
中氧化剂与还原剂的物质的量之比为 。
(4)已知:NaSO 溶于水会生成NaHSO。检验NaSO 晶体在空气中已被氧化的实
2 2 5 3 2 2 5
验方法是
________________________________________________________________________
________________________________________________________________________。