文档内容
第三篇 化学反应与能量
专项 22 二次电池
利用化学反应的可逆性,可以组建成一个新电池,即当一个化学反应转化为电能之后,还可以用电能
使化学体系修复,然后再利用化学反应转化为电能,所以叫二次电池,又称为充电电池或蓄电池。充电电
池的充放电循环可达数千次到上万次,故其相对干电池而言更经济实用。市场上主要充电电池有镍氢电池、
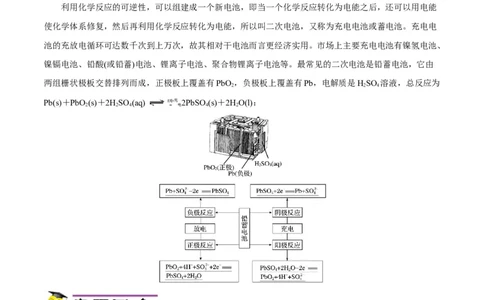
镍镉电池、铅酸(或铅蓄)电池、锂离子电池、聚合物锂离子电池等。最常见的二次电池是铅蓄电池,它由
两组栅状极板交替排列而成,正极板上覆盖有PbO ,负极板上覆盖有Pb,电解质是HSO 溶液,总反应为
2 2 4
Pb(s)+PbO (s)+2HSO (aq) 放电=充 2PbSO (s)+2HO(l):
2 2 4 == 电 4 2
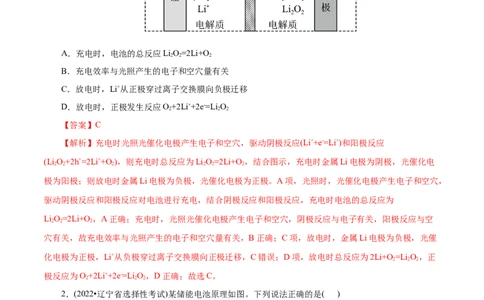
1.(2022•全国乙卷) 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研
究了一种光照充电Li-O 电池(如图所示)。光照时,光催化电极产生电子(e-)和空穴(h+),驱动阴极反应(Li+
2
+e-=Li+)和阳极反应(Li O+2h+=2Li++O )对电池进行充电。下列叙述错误的是( )
2 2 2
1
原创精品资源学科网独家享有版权,侵权必究!
1
学科网(北京)股份有限公司A.充电时,电池的总反应LiO=2Li+O
2 2 2
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应O+2Li++2e-=Li O
2 2 2
【答案】C
【解析】充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应
(Li O+2h+=2Li++O ),则充电时总反应为LiO=2Li+O ,结合图示,充电时金属Li电极为阴极,光催化电
2 2 2 2 2 2
极为阳极;则放电时金属Li电极为负极,光催化电极为正极。A项,光照时,光催化电极产生电子和空穴,
驱动阴极反应和阳极反应对电池进行充电,结合阴极反应和阳极反应,充电时电池的总反应为
LiO=2Li+O ,A正确;充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空
2 2 2
穴有关,故充电效率与光照产生的电子和空穴量有关,B正确;C项,放电时,金属Li电极为负极,光催
化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;D项,放电时总反应为2Li+O=Li O,正
2 2 2
极反应为O+2Li++2e-=Li O,D正确;故选C。
2 2 2
2.(2022•辽宁省选择性考试)某储能电池原理如图。下列说法正确的是( )
A.放电时负极反应:NaTi (PO )-2e-= NaTi (PO )+2Na+
3 2 4 3 2 4 3
2
原创精品资源学科网独家享有版权,侵权必究!
2
学科网(北京)股份有限公司B.放电时Cl-透过多孔活性炭电极向CCl 中迁移
4
C.放电时每转移1 mol电子,理论上CCl 吸收0.5 mol Cl
4 2
D.充电过程中,NaCl溶液浓度增大
【答案】A
【解析】放电时负极反应:NaTi (PO )-2e-= NaTi (PO )+2Na+,正极反应:Cl+2e-=2Cl-,消耗氯气,
3 2 4 3 2 4 3 2
放电时,阴离子移向负极,充电时阳极:2Cl--2e-=Cl,由此解析。A项,放电时负极失电子,发生氧化反
2
应,电极反应:NaTi (PO )-2e-= NaTi (PO )+2Na+,故A正确;B项,放电时,阴离子移向负极,放电时
3 2 4 3 2 4 3
Cl-透过多孔活性炭电极向NaCl中迁移,故B错误;C项,放电时每转移1 mol电子,正极:Cl+2e-=2Cl-,
2
理论上CCl 释放0.5 mol Cl ,故C错误;D项,充电过程中,阳极:2Cl--2e-=Cl,消耗氯离子,NaCl溶液
4 2 2
浓度减小,故D错误;故选A。
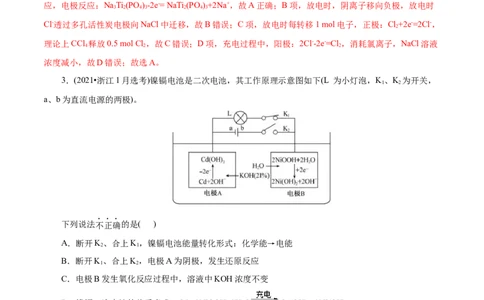
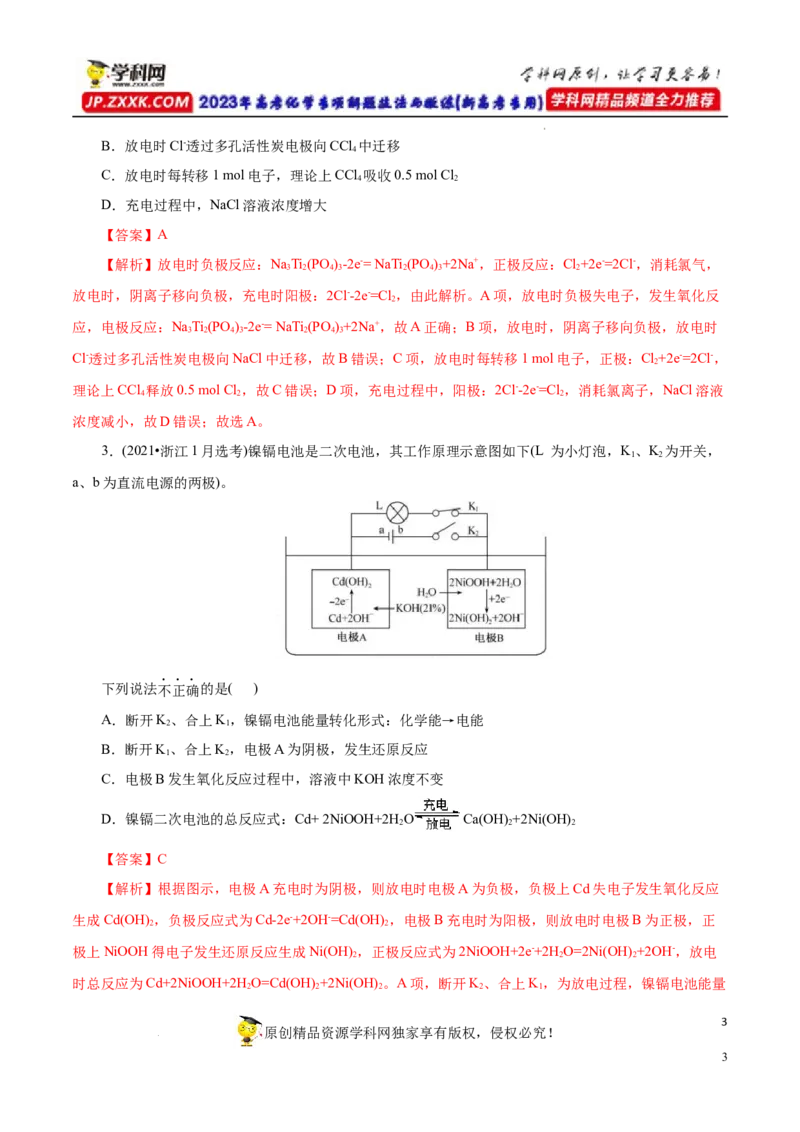
3.(2021•浙江1月选考)镍镉电池是二次电池,其工作原理示意图如下(L 为小灯泡,K、K 为开关,
1 2
a、b为直流电源的两极)。
下列说法不正确的是( )
A.断开K、合上K,镍镉电池能量转化形式:化学能→电能
2 1
B.断开K、合上K,电极A为阴极,发生还原反应
1 2
C.电极B发生氧化反应过程中,溶液中KOH浓度不变
D.镍镉二次电池的总反应式:Cd+ 2NiOOH+2H O Ca(OH) +2Ni(OH)
2 2 2
【答案】C
【解析】根据图示,电极A充电时为阴极,则放电时电极A为负极,负极上Cd失电子发生氧化反应
生成Cd(OH) ,负极反应式为Cd-2e-+2OH-=Cd(OH) ,电极B充电时为阳极,则放电时电极B为正极,正
2 2
极上NiOOH得电子发生还原反应生成Ni(OH) ,正极反应式为2NiOOH+2e-+2H O=2Ni(OH) +2OH-,放电
2 2 2
时总反应为Cd+2NiOOH+2H O=Cd(OH) +2Ni(OH) 。A项,断开K、合上K,为放电过程,镍镉电池能量
2 2 2 2 1
3
原创精品资源学科网独家享有版权,侵权必究!
3
学科网(北京)股份有限公司转化形式:化学能→电能,A正确;B项,断开K、合上K,为充电过程,电极A与直流电源的负极相连,
1 2
电极A为阴极,发生还原反应,电极反应式为Cd(OH) +2e-=Cd+2OH-,B正确;C项,电极B发生氧化反
2
应的电极反应式为2Ni(OH) -2e-+2OH-=2NiOOH+2H O,则电极A发生还原反应的电极反应式为
2 2
Cd(OH) +2e-=Cd+2OH-,此时为充电过程,总反应为Cd(OH) +2Ni(OH) Cd+2NiOOH+2H O,溶液中
2 2 2 2
KOH浓度减小,C错误;D项,根据分析,放电时总反应为Cd+2NiOOH+2H O=Cd(OH) +2Ni(OH) ,则镍
2 2 2
镉二次电池总反应式为Cd+2NiOOH+2H O Cd(OH) +2Ni(OH) ,D正确;故选C。
2 2 2
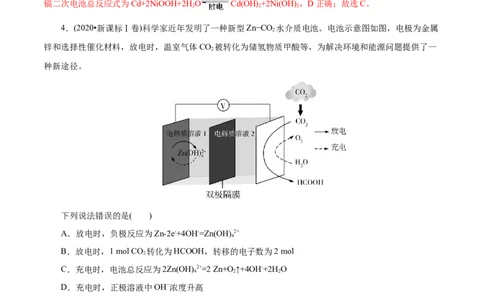
4.(2020•新课标Ⅰ卷)科学家近年发明了一种新型Zn−CO 水介质电池。电池示意图如图,电极为金属
2
锌和选择性催化材料,放电时,温室气体CO 被转化为储氢物质甲酸等,为解决环境和能源问题提供了一
2
种新途径。
下列说法错误的是( )
A.放电时,负极反应为Zn-2e-+4OH-=Zn(OH) 2+
4
B.放电时,1 mol CO 转化为HCOOH,转移的电子数为2 mol
2
C.充电时,电池总反应为2Zn(OH) 2+=2 Zn+O ↑+4OH-+2H O
4 2 2
D.充电时,正极溶液中OH−浓度升高
【答案】D
【解析】由题可知,放电时,CO 转化为HCOOH,即CO 发生还原反应,故放电时右侧电极为正极,
2 2
左侧电极为负极,Zn发生氧化反应生成Zn(OH) 2+;充电时,右侧为阳极,HO发生氧化反应生成O,左
4 2 2
侧为阴极,Zn(OH) 2+发生还原反应生成Zn。A项,放电时,负极上Zn发生氧化反应,电极反应式为:
4
Zn-2e-+4OH-=Zn(OH) 2+,故A正确,不选;B项,放电时,CO 转化为HCOOH,C元素化合价降低2,则
4 2
1molCO 转化为HCOOH时,转移电子数为2mol,故B正确,不选;C项,充电时,阳极上HO转化为
2 2
4
原创精品资源学科网独家享有版权,侵权必究!
4
学科网(北京)股份有限公司O,负极上Zn(OH) 2+转化为Zn,电池总反应为:2Zn(OH) 2+=2 Zn+O ↑+4OH-+2H O,故C正确,不选;D
2 4 4 2 2
项,充电时,正极即为阳极,电极反应式为:2HO-4e-=4H++O ↑,溶液中H+浓度增大,溶液中
2 2
c(H+)•c(OH-)=K ,温度不变时,K 不变,因此溶液中OH-浓度降低,故D错误,符合题意;故选D。
W W
1.二次电池的充放电规律
(1)放电时是原电池反应,充电时是电解池反应。
(2)充电时,可充电电池的正极连接外接电源的正极,可充电电池的负极连接外接电源的负极。[来源:
学科网]
(3)充、放电时电解质溶液中离子移动方向的判断:分析电池工作过程中电解质溶液的变化时,要结合
电池总反应进行分析。
①首先应分清电池是放电还是充电。
②再判断出正、负极或阴、阳极。
放电:阳离子→正极,阴离子→负极;
充电:阳离子→阴极,阴离子→阳极;
总之:阳离子→发生还原反应的电极;阴离子→发生氧化反应的电极。
2.二次电池的解题模板
3.可充电电池的思维模型
因此,充电时电极的连接可简记为“负接负后作阴极,正接正后作阳极”。
4.可充电电池题目的解答思路
5
原创精品资源学科网独家享有版权,侵权必究!
5
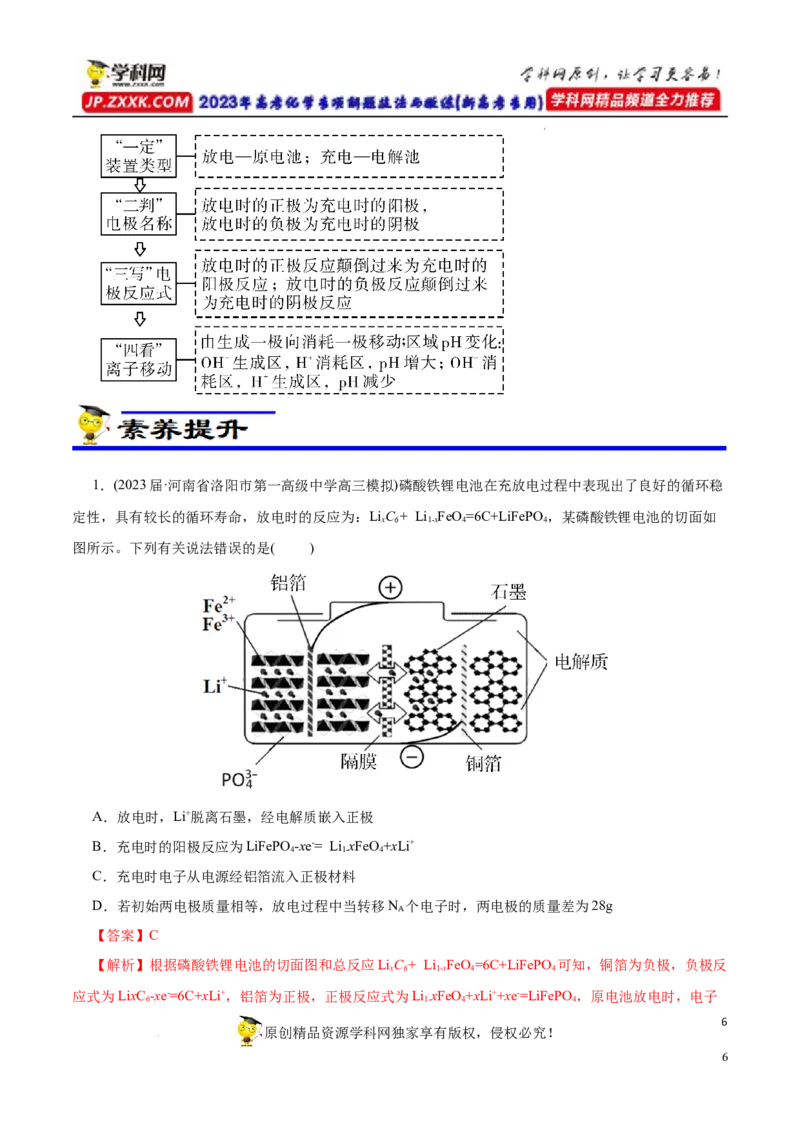
学科网(北京)股份有限公司1.(2023届·河南省洛阳市第一高级中学高三模拟)磷酸铁锂电池在充放电过程中表现出了良好的循环稳
定性,具有较长的循环寿命,放电时的反应为:LiC + Li FeO=6C+LiFePO ,某磷酸铁锂电池的切面如
x 6 1-x 4 4
图所示。下列有关说法错误的是( )
A.放电时,Li+脱离石墨,经电解质嵌入正极
B.充电时的阳极反应为LiFePO -xe-= Li xFeO+xLi+
4 1- 4
C.充电时电子从电源经铝箔流入正极材料
D.若初始两电极质量相等,放电过程中当转移N 个电子时,两电极的质量差为28g
A
【答案】C
【解析】根据磷酸铁锂电池的切面图和总反应LiC + Li FeO=6C+LiFePO 可知,铜箔为负极,负极反
x 6 1-x 4 4
应式为LixC -xe-=6C+xLi+,铝箔为正极,正极反应式为Li xFeO+xLi++xe-=LiFePO ,原电池放电时,电子
6 1- 4 4
6
原创精品资源学科网独家享有版权,侵权必究!
6
学科网(北京)股份有限公司从负极沿导线流向正极,内电路中阳离子移向正极,阴离子移向负极;充电时,装置为电解池,阴极、阳
极反应式与负极、正极反应式正好相反。A项,原电池放电时,电解质中阳离子移向正极,即Li+脱离石墨,
经电解质嵌入正极,A正确;B项,放电时,正极反应式为Li xFeO+xLi++xe-=LiFePO ,充电时,原电池
1- 4 4
的正极与外加电源正极相接,电极反应与原电池正极反应相反,即充电时电池正极上发生的反应为
LiFePO -xe-= Li xFeO+xLi+, B正确;C项,充电时电子从外电源负极→阴极、阳极→电源正极,即充电
4 1- 4
时电子从电源经铜箔流入负极材料,C错误; D项,根据电子守恒可知,放电过程中当转移2N 个电子时,
A
每个电极参与反应Li+的物质的量为2mol,若初始两电极质量相等,两电极的质量差为2mol
×7g/mol×2=28g, D正确;故选C。
2.(2023届·广东省惠州市(惠阳中山、龙门、仲恺中学)高三三校联考)某公司推出一款铁—空气燃料电
池,成本仅为锂电池的 ,其装置放电时的工作原理如图所示。下列说法错误的是( )
A.放电时,M为正极
B.放电一段时间,KOH溶液浓度不变
C.充电时,N极的电极反应式中包括:Fe O+H O+2e- = 2FeO+2OH-
2 3 2
D.放电时,K+从M移向N
【答案】D
【解析】由图可知,放电时,N极Fe失去电子作为负极,则M极为正极,充电时,N极为阴极,M极
为阳极。A项,Fe为活泼金属,放电时被氧化,所以N为负极,O 被还原,所以M为正极,A正确;B项,
2
放电过程中的总反应为Fe与O 反应得到Fe的氧化物,所以KOH溶液的浓度不变,B正确;C项,充电时,
2
N极为阴极,铁的氧化物被还原,包括Fe O+H O+2e- = 2FeO+2OH-,C正确;D项,原电池中阳离子移向
2 3 2
正极,则放电时,K+从N移向M,D错误;故选D。
3.(2023届·湖北省九师联盟高三开学考试)如图所示是一种可实现氢气循环利用的新型电池的放电工作
7
原创精品资源学科网独家享有版权,侵权必究!
7
学科网(北京)股份有限公司原理。下列说法正确的是( )
A.放电时,M电极的电势低于N电极
B.充电过程中Na+由右池通过交换膜向左池移动
C.放电时,N极电极反应式为H+2OH――2e-=2H O
2 2
D.若用铅蓄电池作为电源充电M电极连接铅蓄电池的铅电极
【答案】C
【解析】A项,由图可知,放电时N极作负极,氢气失电子,M极作负极,所以M极的电势高于N极,
A项错误;B项,充电时M电极为阳极,所以Na+由左池通过交换膜向右池移动,B项错误;C项,放电
时N极作负极,氢气失电子,碱性溶液中电极反应式为H+2OH――2e-=2H O,C项正确;D项,充电时,
2 2
M极为阳极,与电源正极相连,即与铅蓄电池的二氧化铅电极相连接,D项错误。故选C。
4.(2023届·河南省TOP二十名校高三摸底考试)刘天骠教授团队开发出一种锌-二茂铁氧化还原双极性
储能材料,应用于pH中性水系液流电池,将水系有机液流电池的性能推进到了一个新的高度。下列说法
正确的是( )
8
原创精品资源学科网独家享有版权,侵权必究!
8
学科网(北京)股份有限公司A.放电时,电极A作负极
B.放电时,Zn2+穿过离子交换膜向电极电极B迁移
C.充电时,阴极的电极反应为Zn2++2e-=Zn
D.充电时,1mol Zn2+过膜时,有2mol二茂铁被还原
【答案】C
【解析】放电时,电极A上得到电子,发生还原反应,则电极A为正极,电极B为负极;充电时,电
极A上失去电子,发生氧化反应,则电极A为阳极,电极B为阴极。A项,放电时,电极A发生还原反应,
作原电池正极,A项错误;B项,放电时,阳离子移向正极,Zn2+应向电极A迁移,B项错误;C项,充电
时,电极B作阴极,发生还原反应Zn2++2e-=Zn,C项正确;D项,1mol Zn2+过膜时,电路中转移2mol电
子,充电时有2mol二茂铁被氧化,D项错误;故选C。
5.(2023届·湖南省部分教育联盟高三模拟考试)我国科学家正在研究一种可充电Na-Zn双离子电池体
系(如图)。下列说法不正确的是( )
9
原创精品资源学科网独家享有版权,侵权必究!
9
学科网(北京)股份有限公司A.闭合K 时,锌电极为电池负极
1
B.闭合K 时,装置中的电能转化为化学能
2
C.放电时,每转移0.2 mol电子,负极区电解质溶液质量增加6.5 g
D.充电时,阳极反应式为Na MnO -xe-=Na MnO +xNa+
0.6 2 0.6-x 2
【答案】C
【解析】A项,闭合K 时,该装置为原电池,锌电极为负极,A正确;B项,闭合K 时,该装置为电
1 2
解池,电解池是将电能转化为化学能,B正确;C项,放电时,装置为原电池,负极发生反应:Zn-2e-
=Zn2+,每转移0.2 mol电子,负极区由Zn失去电子生成0.1 mol Zn2+,0.1 mol Zn2+与0.4 mol OH-结合生成
0.1 mol Na [Zn(OH) ],有0.2 mol Na+通过阳离子交换膜到正极,故负极区电解质溶液质量增重0.1 mol×65
2 4
g/mol-0.2 mol×23 g/mol=1.9 g,C错误;D项,充电时,阳极失电子,Mn的化合价升高,反应式为
Na MnO -xe-=Na MnO +xNa+,D正确;故选C。
0.6 2 0.6-x 2
6.(2022·广东省六校高三第六次联考)一种高达94.2%能效的可充电铝胺电池工作原理如图所示,用
Ph表示苯基,三苯基胺(Ph N)失去一个电子后形成的Ph N∙+结构较为稳定。下列说法不正确的是( )
3 3
10
原创精品资源学科网独家享有版权,侵权必究!
10
学科网(北京)股份有限公司A.与锂电池比,铝电池比能量略低,但铝含量丰富价格低廉
B.放电时,负极的电极反应式为Al-3e-+7AlCl -=4AlCl-
4 2 7
C.充电时,AlCl -向铝电极移动
4
D.理论上每生成1mol Ph N,外电路通过1mol电子
3
【答案】C
【解析】A项,铝电池比能量略低,且含量丰富价格低廉,A项错误;B项,放电时,负极上Al失电
子和AlCl -反应生成Al Cl-,电极反应式为Al-3e-+7AlCl -=4AlCl-,B项正确;C项,充电时Ph N失电子
4 2 7 4 2 7 3
生成Ph N+ , Ph N阳极、Al为阴极,阴离子向阳极移动,所以AlCl -向阳极Ph N移动,C项错误;D项,
3 3 4 3
充电时Ph N失电子生成Ph N+,则生成1个Ph N转移1个电子,所以理论上每生成1molPh N,外电路通
3 3 3 3
过1mol电子,D项正确。故选C。
7.(2022·湖北省部分重点中学高三第二次联考)我国科研团队以聚氨酯为电解液(合成路线如图)实现了
稳定高效且可逆循环的K-CO 电池。总反应为:4KSn+3CO 2KCO+4Sn,其中生成的KCO 附着在
2 2 2 3 2 3
正极上。下列说法错误的是( )
11
原创精品资源学科网独家享有版权,侵权必究!
11
学科网(北京)股份有限公司A.放电时,内电路中电流由KSn合金经酯基电解质流向羧基化碳纳米管
B.电池的正极反应式为4K++3CO +4e-=2K CO+C
2 2 3
C.羧基化碳纳米管中引入的羧基可促进电子的转移
D.充电时,电路中通过1mol电子,多壁碳纳米管减重36g
【答案】D
【解析】由总反应可知放电时KSn合金为负极,羧基化碳纳米管为正极;充电时KSn合金与电源负极
相连,为电解池阴极,羧基化碳纳米管为阳极。A项,放电时为原电池装置,内电路中电流是由负极流向
正极,即放电时,内电路中电流由KSn合金经酯基电解质流向羧基化碳纳米管,A正确;B项,根据总反
应式可知,负极反应式为:KSn-e-=Sn+K+,电池的正极反应式为4K++3CO +4e-=2K CO+C,B正确;C项,
2 2 3
电极材料为KSn和羧基化碳纳米管,KSn与水反应,-COOH与KOH反应,可促进电子的转移,C正确;
D项,充电时阳极反应为:C-4e-+ K CO=3 CO↑+4K+, 碳纳米管及附着的碳酸钾会减少,电路中通过
2 3 2
1mol电子,多壁碳纳米管减重3g,碳酸钾减少30g,D错误;故选D。
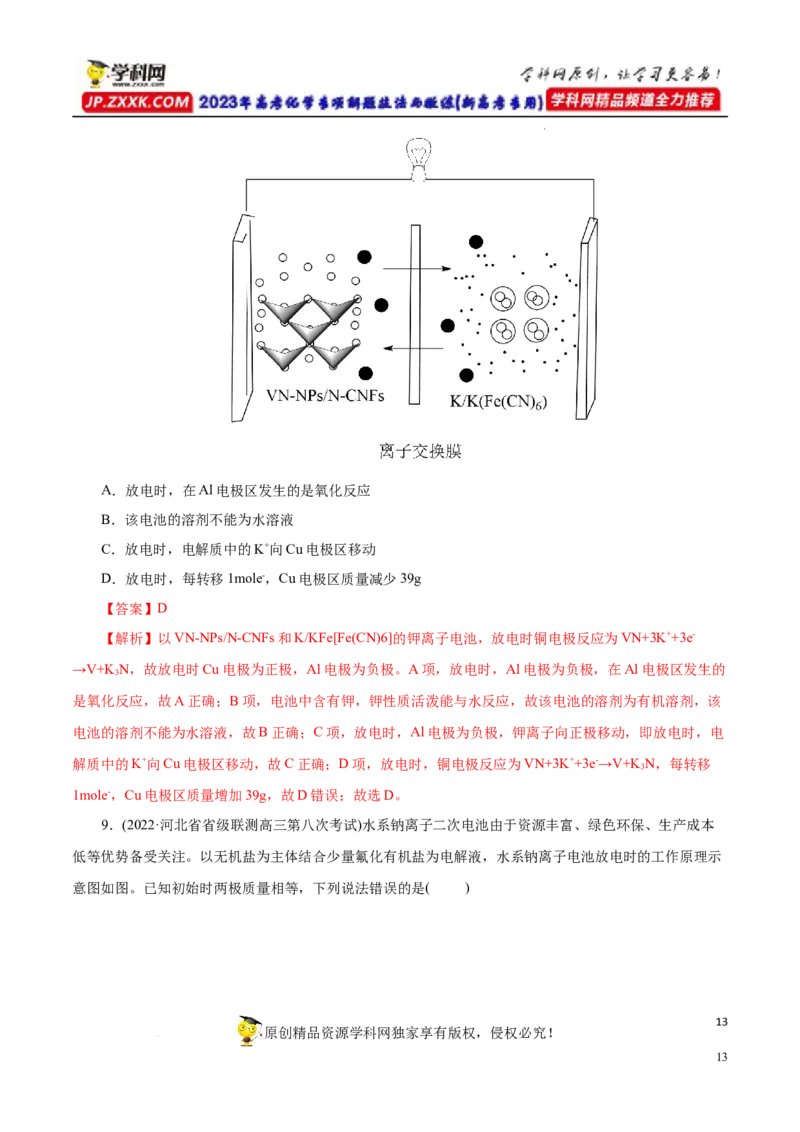
8.(2022·河北省石家庄市示范性高中高三调研考试)钾离子电池由于其低成本、电解液中快的离子传
导性以及高的工作电压等优点;近年来引起了科研工作者极大的关注。吉林大学杨春成教授课题组基于钾
离子电池特性,设计并合成了一种VN-NPs/N-CNFs复合材料,并将其应用于钾离子电池的电极,放电时
该电极反应为VN+3K++3e-→V+KN,下列有关说法中错误的是( )
3
12
原创精品资源学科网独家享有版权,侵权必究!
12
学科网(北京)股份有限公司A.放电时,在Al电极区发生的是氧化反应
B.该电池的溶剂不能为水溶液
C.放电时,电解质中的K+向Cu电极区移动
D.放电时,每转移1mole-,Cu电极区质量减少39g
【答案】D
【解析】以VN-NPs/N-CNFs和K/KFe[Fe(CN)6]的钾离子电池,放电时铜电极反应为VN+3K++3e-
→V+KN,故放电时Cu电极为正极,Al电极为负极。A项,放电时,Al电极为负极,在Al电极区发生的
3
是氧化反应,故A正确;B项,电池中含有钾,钾性质活泼能与水反应,故该电池的溶剂为有机溶剂,该
电池的溶剂不能为水溶液,故B正确;C项,放电时,Al电极为负极,钾离子向正极移动,即放电时,电
解质中的K+向Cu电极区移动,故C正确;D项,放电时,铜电极反应为VN+3K++3e-→V+KN,每转移
3
1mole-,Cu电极区质量增加39g,故D错误;故选D。
9.(2022·河北省省级联测高三第八次考试)水系钠离子二次电池由于资源丰富、绿色环保、生产成本
低等优势备受关注。以无机盐为主体结合少量氟化有机盐为电解液,水系钠离子电池放电时的工作原理示
意图如图。已知初始时两极质量相等,下列说法错误的是( )
13
原创精品资源学科网独家享有版权,侵权必究!
13
学科网(北京)股份有限公司A.电池总反应可表示为2NaV(PO ) 放电=充 NaV(PO )+NaV(PO )
3 2 4 3 == 电 5 2 4 3 2 4 3
B.充电时,阳极电极反应式为NaV(PO )-2e-=Na V(PO )+2Na+
5 2 4 3 3 2 4 3
C.充电时,电子由M极经导线流向N极;放电时,M极为负极
D.放电时,电路中通过0.005mol电子时,理论上两极质量差为0.23g
【答案】C
【解析】由题意知该电池属于二次电池,示意图为放电过程,M极NaV(PO ) 转化为NaV (PO ),发
3 2 4 3 2 4 3
生失电子的氧化反应,为负极,N极NaV(PO ) 转化为NaV(PO ),发生得电子的还原反应,为正极,充
3 2 4 3 5 2 4 3
电时为电解池,M极为阴极,N极为阳极。A项,根据上述分析电池总反应可表示为2NaV(PO ) 放电=充
3 2 4 3 == 电
NaV(PO )+NaV(PO ),A项正确;B项,充电时,N极为阳极,阳极电极反应式为NaV(PO )-2e-
5 2 4 3 2 4 3 5 2 4 3
=Na V(PO )+2Na+,B项正确;C项,放电时,M极为负极,但充电时,M极为阴极,是电子流入的一极,
3 2 4 3
C项错误;D项,由电池总反应知,放电时,电路中通过0.005mol电子时,负极减少0.005molNa+的质量,
正极增加0.005molNa+的质量,两极质量差为 ,D项正确。故选C。
10.(2022·河北省沧州市高三二模)火星大气约95%是CO,Li-CO 电池在未来的火星探测领域有着重
2 2
要的应用前景。科学家设计了一系列Ru/M-CPY@ CNT(碳纳米管)杂化材料(M = Co、Zn、Ni、Mn, CNTs
碳纳米管是一种电导率高、比表面积大、通道和孔隙率丰富的导电基底)作为电极。已知该电池放电时的反
应为4Li+3CO=2Li CO+C,下列说法错误的是( )
2 2 3
14
原创精品资源学科网独家享有版权,侵权必究!
14
学科网(北京)股份有限公司A.放电时,Li电极作电池负极,有电子经导线流出
B.充电时,每转移1mol电子,两电极的质量变化差值为7g
C.充电时,阳极的电极反应式为C-4e-+2Li CO =3CO ↑+4Li+
2 3 2
D.杂化材料中CNTs增多了CO 的吸附位点,可使该电池表现出优异的电化学性能
2
【答案】B
【解析】由电池放电时的反应可知,Li化合价由0价变成+1价,故是原电池的负极,复杂材料电极是
正极。A项,放电时,Li电极作电池负极,有电子经导线流出,A正确;B项,充电时,阳极C变成二氧
化碳,阴极Li+变成Li,故每转移1mol电子,消耗0.25molC质量为3g,生成1molLi质量为7g,故两电极
的质量变化差值为3g+7g=10g,B错误;C项,充电时,阳极上C失电子变成二氧化碳,故阳极的电极反
应式为C-4e-+2Li CO =3CO ↑+4Li+,C正确;D项,CNTs碳纳米管是一种电导率高、比表面积大、通道
2 3 2
和孔隙率丰富的导电基底,增加二氧化碳的吸收效率,故可使该电池表现出优异的电化学性能,D正确;
故选B。
11. 高电压水系锌—有机混合液流电池的装置如图所示。下列说法错误的是( )
A. 充电时,中性电解质NaCl的浓度增大
15
原创精品资源学科网独家享有版权,侵权必究!
15
学科网(北京)股份有限公司B. 放电时,负极反应式为Zn-2e-+4OH-=Zn(OH)
C. 充电时,1molFQH 转化为FQ转移2mol电子
2
D. 放电时,正极区溶液的pH增大
【答案】A
【解析】高电压水系锌-有机混合液流电池工作原理为:放电时为原电池,金属 Zn发生失电子的氧化
反应生成Zn2+,为负极,则FQ所在电极为正极,正极反应式为2FQ+2e-+2H+═FQH ,负极反应式为Zn-2e-
2
+4OH-=Zn(OH) 2-;充电时电解池,原电池的正负极连接电源的正负极,阴阳极的电极反应与原电池的负正
4
极的反应式相反,电解质中阳离子移向阴极、阴离子移向阳极。A项,充电时装置为电解池,电解质中阳
离子移向阴极、阴离子移向阳极,NaCl溶液中的钠离子和氯离子分别发生定向移动,即电解质NaCl的浓
度减小,故A错误;B项,放电时为原电池,金属Zn为负极,负极反应式为Zn-2e-+4OH-=Zn(OH) 2-,故
4
B正确;C项,充电时电解池,阳极反应为FQH -2e-=2FQ+2e-+2H+,则1molFQH 转化为FQ时转移2mol
2 2
电子,故C正确;D项,放电时为原电池,正极反应式为2FQ+2e-+2H+═FQH,即正极区溶液的pH增大,
2
故D正确;故选A。
16
原创精品资源学科网独家享有版权,侵权必究!
16
学科网(北京)股份有限公司17
原创精品资源学科网独家享有版权,侵权必究!
17
学科网(北京)股份有限公司