文档内容
专项训练 配位键的判断(解析版)
一、单选题
1.对HO+的说法正确的是
3
A.离子中无配位键 B.O原子采取sp3杂化
C.离子中配体为O原子 D.HO+中有2个σ键
3
【答案】B
【详解】A.水分子中氧提供孤电子对,1个氢离子提供空轨道,形成配位键,故A错
误;
B.O原子形成3个共价键,且还存在1对孤电子对,采取sp3杂化,故B正确;
C.离子中配体为HO,故C错误;
2
D.配位键也是σ键,故存在3个σ键,故D错误;
故选B。
2.在碱性镀铜中电镀液的主要成分是 ,其内界的电离与弱电解质类
似,仅部分解离为中心离子和配位体。设N 为阿伏加德罗常数的值,下列说法正确的
A
是
A.1mol/L 溶液中 数目小于N
A
B.22.4LNH 含有的质子数目为10N
3 A
C.1mol 的配位键数目为2N
A
D.N 和H 合成1molNH 转移电子数目为3N
2 2 3 A
【答案】D
【详解】A.未指明溶液体积,无法计算其含有的微粒数目,故A错误;
B.未给出氨气所处的温度和压强,无法计算其含有的微粒数目,故B错误;
C. 的配位键数目为 ,C项错误;
D.根据氧化还原原理可知, 和 合成 时转移电子数目为 ,D项正确;
故本题选D.
3.某种镁盐具有良好的电化学性能,其阴离子结构如图所示。W、X、Y、Z、Q是核
电荷数依次增大的短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是Q原
子价电子数的2倍。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.W与Y的化合物为极性分子 B.第一电离能Z>X>Y
C.Q的氧化物是两性氧化物 D.该阴离子中含有配位键
【答案】B
【详解】W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W形成1条单键且核
电荷数最小,W为H,X形成4条键,核电荷数大于H,且小于其他三种元素,X为
C,Y形成2条单键,核电荷数大于C,Y为O,W、Y原子序数之和等于Z,Z为F,
Y原子价电子数为Q原子价电子数的2倍,Q为Al;
A.W与Y的化合物为HO或HO,均为极性分子,A项正确;
2 2 2
B.同周期元素从左到右第一电离能呈增大趋势,则第一电离能F>O>C,B项错误;
C.Q为Al,Al O 为两性氧化物,C项正确;
2 3
D.该阴离子中L与Q之间含有1个配位键,D项正确;
答案选B。
4.下列有关 和 的说法错误的是
A. 能与 形成分子间氢键
B. 与 形成的 中 的配位数是4
C. 转化为 ,其键角变小
D. 中存在的配位键由氮原子提供孤电子对
【答案】C
【详解】A. 与 之间可以形成分子间氢键,故A正确;
B. 络离子中,一个锌离子周围与4个NH 形成配位键,Zn2+的配位数为
3
4,故B正确;
C.NH 变成 ,孤电子对变成了成键电子对,排斥力减小,键角变大,故C错误;
3
D.H+离子没有电子,孤对电子由N原子提供,故D正确;
答案选C。
资料收集整理【淘宝店铺:向阳百分百】5.下列化学用语正确的是
A. 的结构示意图:
B.基态 的价电子排布图为
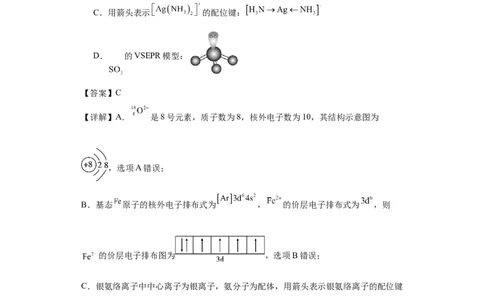
C.用箭头表示 的配位键:
D. 的VSEPR模型:
【答案】C
【详解】A. 是8号元素,质子数为8,核外电子数为10,其结构示意图为
,选项A错误;
B.基态 原子的核外电子排布式为 , 的价层电子排布式为 ,则
的价层电子排布图为 ,选项B错误;
C.银氨络离子中中心离子为银离子,氨分子为配体,用箭头表示银氨络离子的配位键
为 ,选项C正确;
D. 无孤电子对,价层电子对数为3,VSEPR模型是平面三角形,与图不相符,选
项D错误;
答案选C。
6.强酸 可由如下反应制备, 。下列说法正确的是
资料收集整理【淘宝店铺:向阳百分百】A. 的电子式为 B.相同条件下, 酸性弱于HF
C.BF 的空间结构是三角锥形 D. 中含有配位键
3
【答案】D
【详解】A.HBF 属于酸,属于共价化合物,故A错误;
4
B.HBF 属于强酸,HF为弱酸,因此相同条件下,HBF 酸性强于HF,故B错误;
4 4
C.BF 中心原子B的价层电子对数为3+ =3,因此空间构型为平面三角形,故
3
C错误;
D.B元素最外层有3个电子,BF 分子中B有空轨道,HF中F存在孤电子对,因此F
3
提供电子,B提供孤电子对,形成配位键,故D正确;
故答案为D。
7.向NaCl溶液中滴加几滴 溶液,产生白色沉淀AgCl;再滴入氨水,沉淀逐渐
溶解,得到澄清的 无色溶液,下列说法正确的是
A.AgCl属于弱电解质
B.键角:
C. 与 形成的 中有6个配位键
D.在 里, 中的N接受孤电子对, 给出孤对电子,以配位键
形成了
【答案】B
【详解】A.AgCl属于强电解质,A错误;
B.氨气为三角锥形分子,键角约为107°,水为V形分子,键角约为105°,故键角:
,B正确;
C. 与 形成的 中N原子提供孤对电子,有2个配位键,C错误;
D.在 里, 中的N提供孤电子对, 存在空轨道接受孤对电子,
资料收集整理【淘宝店铺:向阳百分百】以配位键形成了 ,D错误。
故选B。
8.广东是我国对外开放的窗口,有众多非物质文化遗产和特色产业,下列说法错误的
是
A.电白沉香是广东非物质文化遗产,点燃沉香房间充满香味,说明分子是运动的
B.东莞半导体产业发达,芯片的主要成分为二氧化硅
C.深圳鹏城实验室研究铝的化合物在有机催化方面取得了突破进展, 中含
有配位键
D.佛山铝材全国闻名,冰晶石助熔电解熔融氧化铝可冶炼铝
【答案】B
【详解】A.分子是不停运动的,点燃沉香,可以闻到散发的沉香香味,选项A正确;
B.芯片的主要成分是晶体硅,选项B错误;
C. 中含有配位键,选项C正确;
D.铝的冶炼是利用电解熔融氧化铝,但氧化铝熔点太高,采用冰晶石助熔可降低冶
炼成本,选项D正确;
答案选B。
9.在照相底片的定影过程中,未曝光的溴化银(AgBr)常用硫代硫酸钠(Na SO)溶解,
2 2 3
反应生成 。在废定影液中加入 使 中的银转化为
黑色沉淀,并使定影液再生。将黑色沉淀在高温下转化为Ag,以达到回收银的目的。
下列有关说法不正确的是
A. 与 的结构相似,中心硫原子杂化轨道类型均为
B. 中存在的作用力有离子键、共价键、配位键
C.废定影液中加入 的离子方程式为
D.黑色沉淀在空气中灼烧生成Ag与工业上氧化银分解制Ag均属于热分解法
【答案】D
【详解】A. 离子的中心硫原子的价层电子对数为4+ =4, 与
资料收集整理【淘宝店铺:向阳百分百】的结构相似, ,SO 离子的中心硫原子的价层电子对数也
2
为4,根据价层电子对互斥理论判断中心硫原子的杂化轨道类型为sp3,A正确;
B.Na[Ag(S O)]中阴阳离子之间存在离子键、Ag+和配体之间存在配位键、S-O原子
3 2 3 2
之间存在极性共价键,B正确;
C.根据题意,NaS与Na[Ag(S O)]反应生成Ag S,结合原子守恒还有NaSO 生成,
2 3 2 3 2 2 2 2 3
反应的化学方程式为NaS+ 2Na [Ag(S O)]=Ag S↓+4Na SO,离子方程式为
2 3 2 3 2 2 2 2 3
,C正确;
D.硫化银在空气中灼烧生成银和二氧化硫,工业上氧化银分解制得银和氧气,前者
有氧气参与,反应原理不相同,后者属于热分解法,D错误;
故选D。
10.在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的。
Be(OH) 和Al(OH) 均为两性氢氧化物,Be(OH) 溶于强碱形成 。BeO和
2 3 2
Al O 都具有难溶于水、高熔点等性质。BeCl 和AlCl 在气态时通常以二聚体的形式存
2 3 2 3
在,(AlCl )(的结构如图所示。B和Si均能溶于NaOH溶液生成盐和氢气。工业上用焦
3 2
炭和石英砂(主要成分为SiO)在高温条件下反应制得粗硅。硼酸(H BO)和硅酸都是弱
2 3 3
酸,硼酸晶体有类似于石墨的片层状结构,常用作医用消毒剂、润滑剂等。
下列说法正确的是
A.(AlCl ) 中含有配位键
3 2
B.可溶性铝盐净水原理:
C.SiO 中的O-Si-O键角为120°
2
D.HBO 晶体中存在的作用力只有共价键
3 3
【答案】A
资料收集整理【淘宝店铺:向阳百分百】【详解】A.(AlCl ) 中Al原子提供空轨道、Cl原子提供孤电子对以此来形成配位键,
3 2
所以(AlCl ) 中含有配位键,A正确;
3 2
B.可溶性铝盐净水原理为铝离子水解生成氢氧化铝胶体,B错误;
C.SiO 为原子晶体,每个O原子被两个Si原子共用,每个Si原子分别与4个O原子
2
相连,故Si原子采用sp3杂化,形成的应为正四面体结构,键角不为120°,C错误;
D.HBO 晶体中存在的作用力除了共价键还存在分子间作用力,D错误;
3 3
故选A。
11.我国科学家构建的NiO/ /Pt双组分催化剂,可实现氨硼烷( )与
高效产 的目的,发生反应的化学方程式为 。
下列说法正确的是
A.N核外有7种不同空间运动状态的电子
B.Ni位于周期表的d区,价电子排布式为
C.氨硼烷中B提供孤电子对和N提供的空轨道形成配位键
D.基态O原子核外电子占据的最高能级的电子云轮廓图为哑铃形
【答案】D
【详解】A.基态N原子核外电子排布式为1s22s22p3,占有5个原子轨道,即有5种不
同空间运动状态的电子,A错误;
B.Ni是28号元素,其价层电子排布式为3d84s2,B错误;
C.氨硼烷中B原子提供空轨道,与N原子提供的孤电子对形成配位键,C错误;
D.基态O原子核外电子排布式为1s22s22p4,占据的最高能级为2p,其电子云轮廓图
为哑铃形,D正确;
故选D。
12.硼酸 主要用于玻璃生产,能改善玻璃的耐热、透明性能,提高机械强度。
硼酸是一元弱酸,其电离方程式如下,常温下,其电离常数 。下列说
法正确的是
资料收集整理【淘宝店铺:向阳百分百】A. 电离常数的表达式为
B. 分子的空间构型为三角锥形
C. 的中心原子 的 模型为四面体形
D. 中普通共价键与配位键的个数之比为
【答案】C
【详解】A.根据硼酸的电离方程式,可知其电离常数表达式为:
,故A项错误;
B. 分子中,硼原子最外层有 个电子,分别与三个氧原子形成共价单键,无孤
电子对,因此硼原子采取 杂化, 分子的空间构型为平面三角形,故B项错
误;
C. 中,中心原子 原子无孤电子对,其成键数目为 ,采取 杂化,因此其
模型为四面体形,故C项正确;
D. 中,配位键数目为 ,普通共价键数目为 个 键加 个 键 ,
因此普通共价键与配位键的个数之比为 ,故D项错误。
答案为:C。
13.已知:BF 熔点-127°C,沸点-100°C,水解生成HBO(一元弱酸,结构如图所示)
3 3 3
和HBF ,与氨气相遇立即生成白色的BF·NH (氨合三氟化硼)固体。下列说法错误的
4 3 3
是
资料收集整理【淘宝店铺:向阳百分百】A.电负性:F>N>H>B
B. 的空间结构为三角锥形
C.HBO 中存在分子间氢键,BF·NH 中存在配位键
3 3 3 3
D.HBO 的电离方程式为:HBO+H O H+ +
3 3 3 3 2
【答案】B
【详解】A.元素的非金属性越强,其电负性就越大。元素的非金属性:F>N>H>
B,所以电负性大小关系为:F>N>H>B,A正确;
B. 的中心B原子价层电子对数是4+ =4,由于不含有孤电子对,所以其
空间结构为正四面体形,而不是呈三角锥形,B不正确;
C.HBO 的分子间存在分子间氢键,而BF·NH 中B原子与N原子之间存在配位键,
3 3 3 3
C正确;
D.HBO 分子中B原子上有空轨道,可以与水电离产生的OH-的O之间形成配位键,
3 3
导致溶液中c(OH-)>c(H+),因此溶液显酸性,则HBO 的电离方程式为:HBO+H O
3 3 3 3 2
H+ + ,D正确;
故合理想象是B。
14.氮化镓(GaN)硬度大、熔点高,在光电子、高温大功率器件上常用作半导体材料,
其制备方法之一为 。已知氮化镓的晶胞结构与金刚石相似,
下列说法正确的是
A.电负性: B.GaN中存在配位键
资料收集整理【淘宝店铺:向阳百分百】C. 的VSEPR模型名称为三角锥形 D.氮化镓晶胞中由氮、镓构成的最小的
环为十二元环
【答案】B
【详解】A.电负性: ,故A项错误;
B.Ga连有四条键,所以GaN中存在配位键,故B项正确;
C. 的VSEPR模型名称为四面体形,故C项错误;
D.氮化镓晶胞结构类似金刚石,其中由氮、镓构成的最小的环为六元环,故D项错
误;
答案选B。
15.氧杂环丁基叠氮聚合物制备反应原理如图:
下列说法错误的是
A.反应①属于开环聚合反应
B.反应①的催化剂中含有配位键
C.可用红外光谱仪检测叠氮聚合物的生成
D.生成1mol叠氮聚合物需要消耗2molNaN
3
【答案】D
【详解】A.根据反应①前后结构简式得到反应①属于开环且生成了高聚物,因此反
应属于开环聚合反应,故A正确;
B.反应①的催化剂中氧有孤对电子,B提供空轨道,因此催化剂中含有配位键,故B
正确;
C.可用红外光谱仪检测的大奥分子含有的化学键或官能团信息,因此可用红外光谱仪
检测叠氮聚合物的生成,故C正确;
D.生成1mol叠氮聚合物需要消耗2n mol NaN ,故D错误。
3
综上所述,答案为D。
16.下列关于超分子和配合物的叙述不正确的是
A.利用超分子的分子识别特征,可以分离 和
B.1mol 分子中含5 个配位键
资料收集整理【淘宝店铺:向阳百分百】C. 提供空轨道, 中氧原子提供孤对电子,从而形成配位键
D.配合物在半导体等尖端技术、医学科学、催化反应和材料化学等领域都有广泛
应用
【答案】B
【详解】A.利用超分子的分子识别特征,能够区分识别C 和C ,故可以分离C 和
60 70 60
C ,A正确;
70
B.CO分子存在1个配位键, 中存在5个Fe C配位键,故1mol
分子中含10 个配位键,B错误;
C.配离子中中心原子提供空轨道,配体提供孤电子对,所以[Cu(H O) ]2+中的Cu2+提
2 6
供空轨道,HO中的O原子提供孤对电子,两者结合形成配位键,C正确;
2
D.配合物的应用:①生命体中,许多酶与金属离子的配合物有关;②科学研究和生
产实践:进行溶解、沉淀或萃取等操作来达到分离提纯、分析检测等目的,D正确;
故选B。
17.在超分子化学中,常用Cu+模板合成各种拓扑结构分子,图1为诺贝尔得主
Auvage教授利用亚铜离子为模板合成的索烃结构。Cu也可与Zn、Sn及S构成四元半
导体化合物的四方晶胞,结构如图2所示,下列说法错误的是
A.索烃分子既有极性键又有非极性键
B.1mol索烃中所含的配位键的数量为8N
A
C.半导体化合物中Zn原子与Sn原子个数比为1:2
D.在四方晶胞中Sn位于S原子组成的四面体空隙中
【答案】C
【详解】A.索烃分子中C、N之间,C、H之间,C、O之间,形成极性键,C、C之
资料收集整理【淘宝店铺:向阳百分百】间形成非极性键,既有极性键又有非极性键,A正确;
B.索烃中每个Cu+形成4个配位键,1mol索烃中所含的配位键的数量为8N ,B正确;
A
C.根据均摊法,半导体化合物中Zn原子个数为 ,Sn原子个数为
,个数之比为1:1,C错误;
D.根据晶胞结构,在四方晶胞中Sn位于S原子组成的四面体空隙中,D正确;
故选C。
18.离子液体广泛应用于科研和生产中。某离子液体结构如下图,其中阳离子有类似
苯环的特殊稳定性,下列说法错误的是
A.阳离子中C有两种不同的杂化方式 B.阳离子中存在大π键
C.阳离子中所有C、N原子不可能共面 D.阴离子中含有配位键
【答案】C
【详解】A.由图可知,阳离子中的饱和碳原子的杂化方式为sp3杂化,双键碳原子的
的杂化方式为sp2杂化,共有2种,故A正确;
B.阳离子有类似苯环的特殊稳定性说明阳离子中环上的碳原子和氮原子杂化方式均为
sp2杂化,未参与杂化的p电子形成了π 大π键,故B正确;
C.阳离子有类似苯环的特殊稳定性说明环为平面结构,由三点成面可知,离子中所有
碳原子和氮原子可能共面,故C错误;
D.由化学式可知,四氯合铝离子中具有空轨道的铝离子与具有孤对电子的氯离子形
成了配位键,故D正确;
故选C。
19.“化学多米诺实验”(如图所示)即只需控制第一个反应,利用反应中气体产生的压
力和虹吸作用原理,使若干化学实验依次发生。已知:
(该反应产物可作为 的催化剂)。下列有
关分析错误的是
资料收集整理【淘宝店铺:向阳百分百】A.该实验成功的重要条件是整套装置气密性良好
B.H中出现浅黄色浑浊,证明O非金属性强于S
C. 中存在极性共价键和配位键,N原子的杂化类型为 杂化
D.若硫酸浓度及锌片大小表面积等均相同,则B中产生氢气速率大于D中速率
【答案】D
【分析】由装置及原理可知,实验中生成气体,应防止装置漏气,B中生成氢气,A
和B之间导管a可平衡气压,C中导管短进长出,氢气将C中溶液排入D中,B与D
两容器中比较,D中形成原电池后可以加快反应速率,生成的氢气将E中硫酸铜排入
F中发生Cu2++4NH•H O═4H O+[Cu(NH )]2+,然后进入G中,作HO 的催化剂可加快
3 2 2 3 4 2 2
反应进行,气流过快时H中过氧化氢与硫化氢反应生成S,I中NaOH溶液吸收尾气,
以此解答该题。
【详解】A.进行实验前必须进行的操作检验装置的气密性,一旦漏气实验失败,故A
正确;
B.氧气和硫化氢反应生成硫,H中出现浅黄色浑浊,可证明O非金属性强于S,故B
正确;
C. 中存在N-H极性共价键和配位键,NH 中N原子价层电子对数为3+
3
=4,N原子的杂化类型为 杂化,故C正确;
D.装置B与D中比较,D中形成原电池后可以加快反应速率,则若硫酸浓度及锌片
大小表面积等均相同,则B中产生氢气速率小于D中速率,故D错误;
故选D。
20.锌的某种配合物结构如图所示,已知该配合物中碳原子形成的环状结构均为平面
结构。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.该配合物中非金属元素电负性最小的是氢
B.1mol该配合物中通过螯合作用形成的配位键有4mol
C.该配合物受热时首先断裂的配位键是氮锌键
D.该配合物中存在 、 两种大π键
【答案】C
【详解】A.该配合物中含H、C、N、O、S五种非金属元素,同周期元素从左到右,
元素的电负性逐渐变大,同族元素从上到下,元素的电负性逐渐变小,则氢元素的电
负性最小,A正确;
B.由图可知,1mol该配合物中通过螯合作用成环形成的配位键(N→Zn)有4mol,B正
确;
C.由于电负性:O>N,因此氧锌键的成键电子对偏向于O,受热时容易断裂,同时由
于螯合作用形成的配位键氮锌键稳定性大于一般的配位键氧锌键,所以该配合物受热
时首先断裂的配位键是氧锌键,C错误;
D.该配合物中,每个N原子中的5个价层电子,2个用于形成共价键,2个用于形成
配位键,还有1个电子参与形成大π键。每个S原子中的6个价层电子,2个用于形成
共价键,2个填充在sp2杂化轨道中,还有2个电子参与形成大π键。因此在含硫五元
环中,共用6个电子,形成 大π键,在六元环中,共用6个电子,形成 大π键,
D正确;
故选C。
资料收集整理【淘宝店铺:向阳百分百】