文档内容
专题 10 大题突破——化学工艺流程
目录
01考情透视·目标导航........................................................................................................................
02知识导图·思维引航........................................................................................................................
03核心精讲·题型突破........................................................................................................................
题型一 工艺流程中的操作判断及操作步骤书写..........................................................................
【真题研析】..............................................................................................................................................................
【核心精讲】..............................................................................................................................................................
1.常考的化工术语....................................................................................................................................................
2.原料预处理的六种常用方法................................................................................................................................
3.常见的操作及目的................................................................................................................................................
4.物质分离的6种常用方法....................................................................................................................................
【命题预测】..............................................................................................................................................................
题型二 工艺流程中的条件控制及原因分析....................................................................................
【真题研析】..............................................................................................................................................................
【核心精讲】..............................................................................................................................................................
1.温度、浓度、压强的控制.................................................................
2.pH的控制...............................................................................
3.体系环境氛围及其它条件的控制...........................................................
【命题预测】..............................................................................................................................................................
题型三 产物或反应物推断、陌生方程式的书写............................................................................
【真题研析】..............................................................................................................................................................
【核心精讲】..............................................................................................................................................................
1.循环物质的确定....................................................................................................................................................
2.副产品的判断........................................................................................................................................................
【命题预测】..............................................................................................................................................................
题型四 数据的分析与处理................................................................................................................
【真题研析】..............................................................................................................................................................
【核心精讲】..............................................................................................................................................................
1.熟记常用计算公式................................................................................................................................................
2.利用“碘量法”进行物质含量测定....................................................................................................................
3.K 相关计算............................................................................................................................................................
sp
【命题预测】..............................................................................................................................................................考点
考题统计 考情分析
要求
2024·江苏卷,14,15分;2024· 海南卷,15,12分;2024·
贵州卷,16,14分;2024·江西卷,15,14分;2024·甘肃 化学工艺流程题是将元
卷,15,14分;2024·北京卷,18,15分;2024·福建卷, 素化合物和化学实验基
11,15分;2024·广西卷,15,14分;2024·山东卷,18, 础知识以真实工业流程
12;2024·辽吉黑卷,16,14分;2024·安徽卷,15,14分; 为载体来进行综合考
查,取代了传统的无机
2024·河北卷,16,14分;2024·湖北卷,16,13;2024·全国
框图题,是非选择题重
新课标卷,8,14分;2024·全国甲卷,8,14分;2024·浙江
要题型之一,试题知识
6月卷,18,10分;2023•全国甲卷26题,14分;2023•全国
融合、灵活性大,思维
乙卷27题,14分;22023•全国新课标卷27题,14分;2023•
空间大。预计2025年
山东卷17题,13分;2023•湖南卷17题,14分;2023•北京
化学 将化学工艺或化学工业
卷18题,13分;2023•广东卷18题,14分;2023•海南卷15
工艺 生产及最新科技成果融
题,10分;2023•江苏卷17题,17分;2023•江苏卷18题,
流程 入其中,来考查考生的
14分;2023•辽宁省选择性考试16题,14分;2023•湖北省选
综合能力。从命题趋势
择性考试16题,14分;2023•浙江省6月选考18题,10分; 来看,一般有三种题
2022•全国甲卷26题,14分;2022•全国乙卷27题,14分; 型:一是从实验设计和
2022•福建卷11题,13分;2022•重庆卷15题,15分;2022• 评价的角度对化工生产
北京卷18题,13分;2022•山东卷17题,13分;2022•江苏 进行模拟;二是根据一
卷题,12分;2022•湖北省选择性考试16题,14分;2022•辽 些化工生产的流程来考
宁省选择性考试16题,14分;2022•海南省选择性考试15 查考生的综合应用能
题,10分;2022•河北省选择性考试15题,14分;2022•湖南 力;三是关于化工生产
的相关计算。
选择性考试17题,14分;2022•广东选择性考试18题,14
分。题型一 工艺流程中的操作判断及操作步骤书写
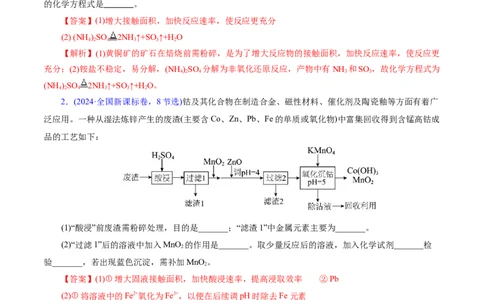
1.(2024·广西卷,15节选)广西盛产甘蔗,富藏锰矿。由软锰矿(MnO ,含SiO、Fe O、Al O 和CuO
2 2 2 3 2 3
等杂质)制备光电材料KMnF 的流程如下。回答下列问题:
3
(1)“甘蔗渣水解液”中含有还原性糖和HSO ,其主要作用是_______。为提高“浸取”速率,可采取
2 4
的措施是_______(任举一例)。
【答案】(1)①把二氧化锰还原为硫酸锰 ②把软锰矿粉碎、搅拌、加热等
【解析】(1)二氧化锰具有氧化性,“甘蔗渣水解液”中含有还原性糖和HSO ,其主要作用是把二氧
2 4
化锰还原为硫酸锰。根据影响反应速率的因素,为提高“浸取”速率,可采取的措施是把软锰矿粉碎、搅
拌、加热等。
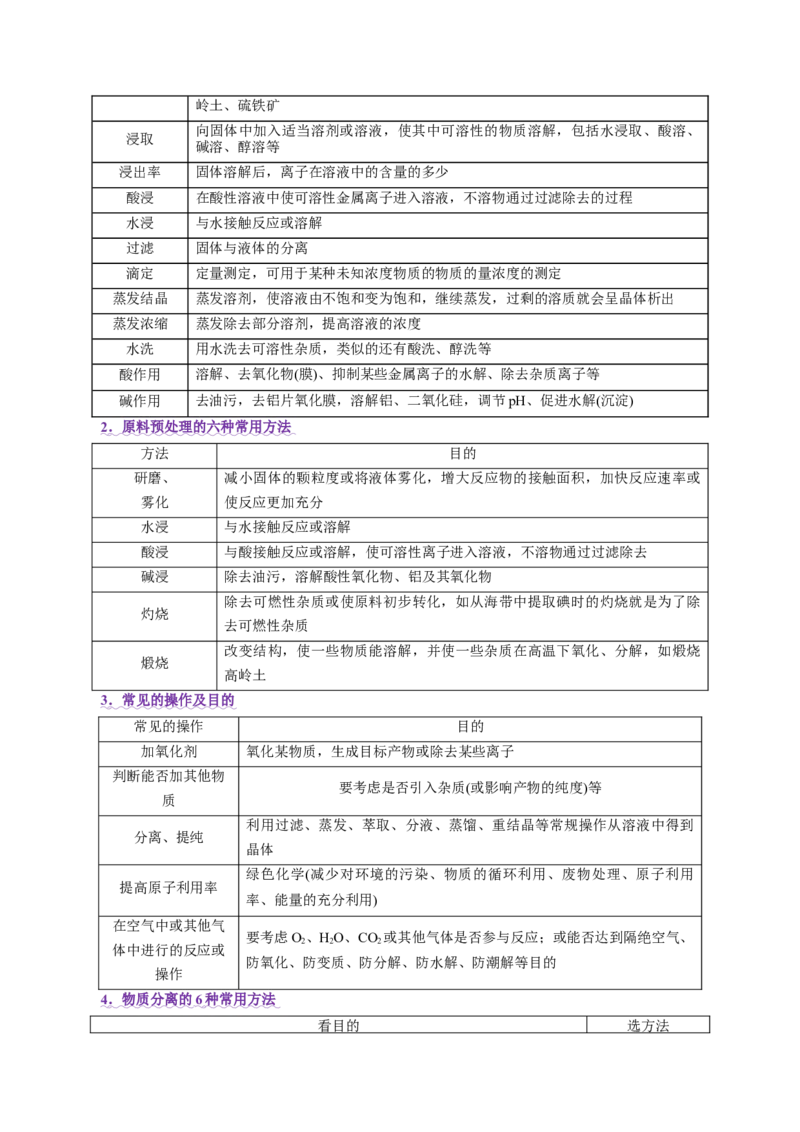
18.(2024·北京卷,18节选)利用黄铜矿(主要成分为CuFeS,含有SiO 等杂质)生产纯铜,流程示意图
2 2
如下。(1)矿石在焙烧前需粉碎,其作用是 。
(2) (NH )SO 的作用是利用其分解产生的SO 使矿石中的铜元素转化为CuSO 。(NH )SO 发生热分解
4 2 4 3 4 4 2 4
的化学方程式是 。
【答案】(1)增大接触面积,加快反应速率,使反应更充分
(2) (NH )SO 2NH ↑+SO↑+H O
4 2 4 3 3 2
【解析】(1)黄铜矿的矿石在焙烧前需粉碎,是为了增大反应物的接触面积,加快反应速率,使反应更
充分;(2)铵盐不稳定,易分解,(NH )SO 分解为非氧化还原反应,产物中有NH 和SO ,故化学方程式为
4 2 4 3 3
(NH )SO 2NH ↑+SO↑+H O。
4 2 4 3 3 2
2.(2024·全国新课标卷,8节选)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着广
泛应用。一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴成
品的工艺如下:
(1)“酸浸”前废渣需粉碎处理,目的是_______;“滤渣1”中金属元素主要为_______。
(2)“过滤1”后的溶液中加入MnO 的作用是_______。取少量反应后的溶液,加入化学试剂_______检
2
验_______,若出现蓝色沉淀,需补加MnO 。
2
【答案】(1)①增大固液接触面积,加快酸浸速率,提高浸取效率 ②Pb
(2)①将溶液中的Fe2+氧化为Fe3+,以便在后续调pH时除去Fe元素
【解析】(1)在原料预处理过程中,粉碎固体原料能增大固体与液体的接触面积,从而加快酸浸的反应
速率,提高浸取效率;由分析可知,“滤渣1”的主要成分为PbSO ,则“滤渣1”中金属元素主要为Pb;(2)酸
4
浸液中含有Co2+、Zn2+、Fe2+、Fe3+、SO 2-等离子。由题表中数据可知,当Fe3+完全沉淀时,Co2+未开始沉淀,
4
而当Fe2+完全沉淀时,Co2+已有一部分沉淀,因此为了除去溶液中的Fe元素且Co2+不沉淀,应先将Fe2+氧
化为Fe3+,然后调节溶液的pH使Fe3+完全水解转化为Fe(OH) 沉淀,因此,MnO 的作用是将Fe2+氧化为
3 2
Fe3+,以便在后续调pH时除去Fe元素。常用K[Fe(CN) ]溶液检验Fe2+,若生成蓝色沉淀,则说明溶液中仍
3 6
存在Fe2+,需补加MnO 。
23.(2022•河北省选择性考试,节选)以焙烧黄铁矿FeS(杂质为石英等)产生的红渣为原料制备铵铁蓝
2
Fe(NH )Fe(CN) 颜料。工艺流程如下:
4 6
(1)红渣的主要成分为_______(填化学式),滤渣①的主要成分为_______(填化学式)。
(2)黄铁矿研细的目的是_______。
(4)工序①的名称为_______,所得母液循环使用。
【答案】(1)Fe O SiO
2 3 2
(2)增大固液接触面积,加快反应速率,提高黄铁矿的利用率
(4)蒸发浓缩、冷却结晶、过滤洗涤
【解析】(1)已知黄铁矿高温煅烧生成Fe O,反应原理为:4FeS+11O 2Fe O+8SO,故产生的红
2 3 2 2 2 3 2
渣主要成分为Fe O 和SiO;(2)黄铁矿研细的主要目的是增大固液接触面积,加快反应速率,提高黄铁矿
2 3 2
的利用率;(4)工序①的名称为蒸发浓缩、冷却结晶、过滤洗涤,所得母液主要含有FeSO 溶液和HSO 可
4 2 4
以循环利用。
1 .常考的化工术语
关键词 释 义
将块状或颗粒状的物质磨成粉末或将液体雾化,增大反应物接触面积,以加快反
研磨、雾化
应速率或使反应更充分
灼烧(煅烧) 使固体在高温下分解或改变结构、使杂质高温氧化、分解等。如煅烧石灰石、高岭土、硫铁矿
向固体中加入适当溶剂或溶液,使其中可溶性的物质溶解,包括水浸取、酸溶、
浸取
碱溶、醇溶等
浸出率 固体溶解后,离子在溶液中的含量的多少
酸浸 在酸性溶液中使可溶性金属离子进入溶液,不溶物通过过滤除去的过程
水浸 与水接触反应或溶解
过滤 固体与液体的分离
滴定 定量测定,可用于某种未知浓度物质的物质的量浓度的测定
蒸发结晶 蒸发溶剂,使溶液由不饱和变为饱和,继续蒸发,过剩的溶质就会呈晶体析出
蒸发浓缩 蒸发除去部分溶剂,提高溶液的浓度
水洗 用水洗去可溶性杂质,类似的还有酸洗、醇洗等
酸作用 溶解、去氧化物(膜)、抑制某些金属离子的水解、除去杂质离子等
碱作用 去油污,去铝片氧化膜,溶解铝、二氧化硅,调节pH、促进水解(沉淀)
2 .原料预处理的六种常用方法
方法 目的
研磨、 减小固体的颗粒度或将液体雾化,增大反应物的接触面积,加快反应速率或
雾化 使反应更加充分
水浸 与水接触反应或溶解
酸浸 与酸接触反应或溶解,使可溶性离子进入溶液,不溶物通过过滤除去
碱浸 除去油污,溶解酸性氧化物、铝及其氧化物
除去可燃性杂质或使原料初步转化,如从海带中提取碘时的灼烧就是为了除
灼烧
去可燃性杂质
改变结构,使一些物质能溶解,并使一些杂质在高温下氧化、分解,如煅烧
煅烧
高岭土
3 .常见的操作及目的
常见的操作 目的
加氧化剂 氧化某物质,生成目标产物或除去某些离子
判断能否加其他物
要考虑是否引入杂质(或影响产物的纯度)等
质
利用过滤、蒸发、萃取、分液、蒸馏、重结晶等常规操作从溶液中得到
分离、提纯
晶体
绿色化学(减少对环境的污染、物质的循环利用、废物处理、原子利用
提高原子利用率
率、能量的充分利用)
在空气中或其他气
要考虑O、HO、CO 或其他气体是否参与反应;或能否达到隔绝空气、
2 2 2
体中进行的反应或
防氧化、防变质、防分解、防水解、防潮解等目的
操作
4 .物质分离的 6 种常用方法
看目的 选方法分离难溶物质和易溶物,根据特殊需要采用趁热过滤或者抽滤等方法 过滤(热滤或抽滤)
利用溶质在互不相溶的溶剂里的溶解度不同提纯分离物质,如用CCl 或苯萃
4
萃取和分液
取溴水中的溴
提纯溶解度随温度变化不大的溶质,如NaCl 蒸发结晶
提纯溶解度随温度变化较大的溶质,易水解的溶质或结晶水合物。如KNO、
3
冷却结晶
FeCl 、CuCl 、CuSO ·5H O、FeSO ·7H O等
3 2 4 2 4 2
分离沸点不同且互溶的液体混合物,如分离乙醇和甘油 蒸馏与分馏
利用气体易液化的特点分离气体,如合成氨工业采用冷却法分离氨气与N、
2
冷却法
H
2
1.(2025·四川省广安市期中,节选)利用废镍电池的金属电极芯(主要成分为Co、Ni,还含少量Fe、Al
等)生产醋酸钴晶体、硫酸镍晶体。
(1)用硫酸浸取金属电极芯时,提高浸取率的方法有 (写出一种合理方法即可)。
【答案】(1)将金属电极芯粉碎(合理即可)
【解析】(1)根据影响化学反应速率的因素可知,用硫酸浸取金属电极芯时,提高浸取率的方法有适当
升高温度、搅拌或将金属电极芯粉碎等。
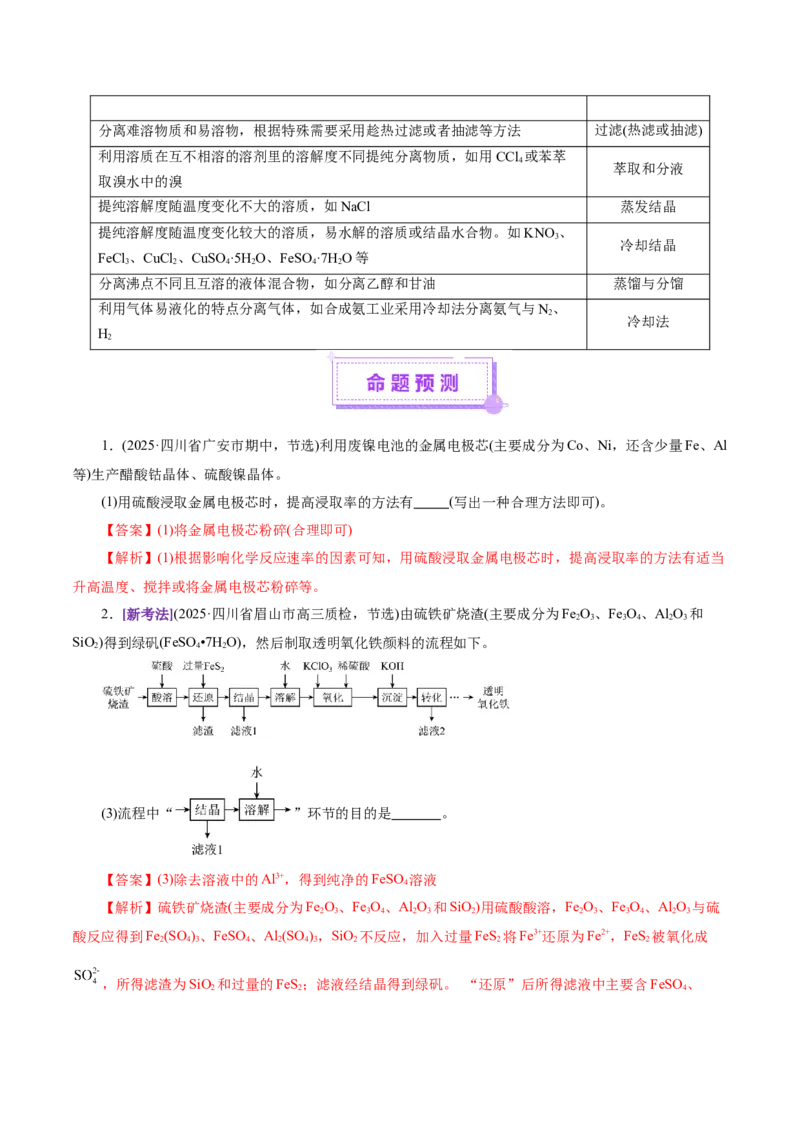
2.[新考法](2025·四川省眉山市高三质检,节选)由硫铁矿烧渣(主要成分为Fe O、Fe O、Al O 和
2 3 3 4 2 3
SiO)得到绿矾(FeSO •7H O),然后制取透明氧化铁颜料的流程如下。
2 4 2
(3)流程中“ ”环节的目的是 。
【答案】(3)除去溶液中的Al3+,得到纯净的FeSO 溶液
4
【解析】硫铁矿烧渣(主要成分为Fe O、Fe O、Al O 和SiO)用硫酸酸溶,Fe O、Fe O、Al O 与硫
2 3 3 4 2 3 2 2 3 3 4 2 3
酸反应得到Fe (SO )、FeSO 、Al (SO ),SiO 不反应,加入过量FeS 将Fe3+还原为Fe2+,FeS 被氧化成
2 4 3 4 2 4 3 2 2 2
,所得滤渣为SiO 和过量的FeS;滤液经结晶得到绿矾。 “还原”后所得滤液中主要含FeSO 、
2 2 4Al (SO ),“ ”环节的目的是除去溶液中的Al3+、得到纯净的FeSO 溶液。
2 4 3 4
3.高锰酸钾是中学常用的试剂,实验室模拟工业上用软锰矿制备高锰酸钾流程如图:
已知:KMnO 为墨绿色固体。
2 4
(1)操作I的名称是__________。
(2)通过某项操作可判断反应①完成,该操作具体为_____。
【答案】(1)过滤 (2)用洁净玻璃棒沾取溶液于滤纸上,若滤纸只有紫红色而无绿色痕迹,则反应完
成
【解析】(1)由流程图可知,通过操作I后得到滤液和滤渣,故操作I为的名称是过滤;(2)由信息可知
KMnO 为墨绿色,高锰酸钾为紫红色,反应①完成后,溶液就不存在KMnO ,则判断反应①完成的操作
2 4 2 4
为:用洁净玻璃棒沾取溶液于滤纸上,若滤纸只有紫红色而无绿色痕迹,则反应完成。
4.工业上用高硫铝土矿(主要成分为Fe O、Al O、SiO,少量FeS)为原料制备聚合硫酸铁的部分工
2 3 2 3 2 2
艺流程如下:
氧化过程中加入双氧水的目的为_______,实际生产过程中温度不宜过高且要控制HO 的投加速度,
2 2
其原因为_______。
【答案】将Fe2+氧化为Fe3+ 防止HO 受热分解,提高原料利用率
2 2
【解析】氧化过程中加入HO 的目的是将“酸浸”后溶液中的Fe2+氧化为Fe3+,离子方程式为2Fe2+
2 2
+H O+2H+=2Fe3++2H O,双氧水不稳定易分解,温度过高,双氧水分解速率加快,实际生产过程中温度不
2 2 2
宜过高且要控制HO 的投加速度,其原因为防止HO 受热分解,提高原料利用率。
2 2 2 25.(2025·四川省成都市期中,节选)金属锰的用途非常广泛,涉及人类生产生活的方方面面,用含锰
废料(主要成分为MnO ,含有少量Al O、Fe O、Fe O、MgO、SiO 等)制备锰的流程如图:
2 2 3 2 3 3 4 2
(2)“酸浸”前需将原料粉碎,目的是 ,“酸浸”时,充入的SO 作 (氧化/还原)剂。
2
【答案】(2)增大接触面积,提高反应速率 还原
【解析】接触面积越大,反应速率越快,则“酸浸”前需将原料粉碎,目的是增大接触面积,提高反
应速率,“酸浸”时,充入的SO 作还原剂。
2
题型二 工艺流程中的条件控制及原因分析
1.(2024·福建卷,11节选)锂云母的主要成分为K(Li Al )(AlSi O )(OH) F ,实验室探索一种碱浸分
1.5 1.5 3 10 x 2-X
解锂云母制备LiOH的工艺流程如下:
(4)“操作Z”为加热、趁热过滤和_______;趁热过滤的主要目的是_______。(LiOH分解温度约为
1000℃)
【答案】(4)①蒸发结晶 ②除去Ca(OH) 杂质
2
【解析】(4)滤液2中溶质主要为氢氧化锂,还有少量的氢氧化钙,由于氢氧化钙的溶解度随温度升高
而减小,加热升温会析出氢氧化钙晶体,故趁热过滤的主要目的是除去Ca(OH) 杂质;除杂后的滤液主要
2
含LiOH,通过蒸发结晶得到LiOH固体。
2.(2024·辽吉黑卷,16节选)中国是世界上最早利用细菌冶金的国家。已知金属硫化物在“细菌氧
化”时转化为硫酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中细小的Au颗粒被FeS、 包
2裹),以提高金的浸出率并冶炼金,工艺流程如下:
(5)“真金不拍火炼”,表明Au难被O 氧化,“浸金”中NaCN的作用为_______。
2
(6)“沉金”中Zn的作用为_______。
【答案】(5)做络合剂,将Au转化为[Au(CN) ]-从而浸出
2
(6)作还原剂,将[Au(CN) ]-还原为Au
2
【解析】(5)“浸金”中,Au作还原剂,O 作氧化剂,NaCN做络合剂,将Au转化为[Au(CN) ]-从而浸
2 2
出;(6)“沉金”中Zn作还原剂,将[Au(CN) ]-还原为Au。
2
3.(2024·湖南卷,16节选)铜阳极泥(含有Au、Ag Se、Cu Se、PbSO 等)是一种含贵金属的可再生资
2 2 4
源,回收贵金属的化工流程如下:
已知:①当某离子的浓度低于1.0×10−5 mol·L-1时,可忽略该离子的存在;
②AgCl(s)+Cl-(aq) [AgCl ]- (aq) K=2.0×10−5 ;
2
③NaSO 易从溶液中结晶析出;
2 3
(3)“氧化酸浸”和“除金”工序抣需加入一定量的NaCl:
①在“氧化酸浸”工序中,加入适量NaCl的原因是 。
②在“除金”工序溶液中, 浓度不能超过 。
【答案】(3) 使银元素转化为AgCl沉淀 0.5
【解析】(3)①在“氧化酸浸”工序中,加入适量NaCl的原因是使银元素转化为AgCl沉淀;②由题
目可知AgCl(s)+Cl-(aq) [AgCl ]- (aq),在“除金”工序溶液中,若Cl-加入过多,AgCl则会转化为
2
[AgCl ]-,当某离子的浓度低于1.0×10−5 mol·L-1时,可忽略该离子的存在,为了不让AgCl发生转化,则
2
另 ,由 ,可得c(Cl-)=0.5mol·L-1,即Cl-浓度不能超过0.5mol·L-1。
4.(2024·北京卷,18节选)利用黄铜矿(主要成分为CuFeS,含有SiO 等杂质)生产纯铜,流程示意图
2 2
如下。
(3)矿石和过量(NH )SO 按一定比例混合,取相同质量,在不同温度下焙烧相同时间,测得:“吸
4 2 4
收”过程氨吸收率和“浸铜”过程铜浸出率变化如图; 和 时,固体B中所含铜、铁的主要物质
如表。
温度/℃ B中所含铜、铁的主要物质
400 Fe O、CuSO 、CuFeS
2 3 4 2
500 Fe (SO )、CuSO 、CuO
2 4 3 4
①温度低于425℃,随焙烧温度升高,铜浸出率显著增大的原因是 。
②温度高于425℃,根据焙烧时可能发生的反应,解释铜浸出率随焙烧温度升高而降低的原因是
。
(4)用离子方程式表示置换过程中加入 的目的 。
(5)粗铜经酸浸处理,再进行电解精炼;电解时用酸化的CuSO 溶液做电解液,并维持一定的c(H+)和
4
c(Cu2+)。粗铜若未经酸浸处理,消耗相同电量时,会降低得到纯铜的量,原因是 。
【答案】(3) 温度低于425℃,随焙烧温度升高,(NH )SO 分解产生的SO 增多,可溶物CuSO 含量
4 2 4 3 4
增加,故铜浸出率显著增加 温度高于425℃,随焙烧温度升高发生反应:4CuFeS+17O +2CuSO
2 2 4
CuO+2Fe (SO )+4SO,CuFeS 和CuSO 转化成难溶于水的CuO,铜浸出率降低
2 4 3 3 2 4(4) Fe+Cu2+=Fe2++Cu
(5)粗铜若未经酸浸处理,其中杂质Fe会参与放电,则消耗相同电量时,会降低得到纯铜的量
【解析】(3)①由图,温度低于425℃,随焙烧温度升高,铜浸出率显著增大,是因为温度低于
425℃,随焙烧温度升高,(NH4)SO 分解产生的SO 增多,可溶物CuSO 含量增加,故铜浸出率显著增加;
2 4 3 4
②温度高于425℃,随焙烧温度升高,CuFeS 和CuSO 转化成难溶于水的CuO,发生反应
2 4
4CuFeS+17O +2CuSO CuO+2Fe (SO )+4SO,铜浸出率降低;(4)加入Fe置换硫酸铜溶液中的铜,反应
2 2 4 2 4 3 3
的离子方程式为Fe+Cu2+=Fe2++Cu;(5)粗铜中含有Fe杂质,加酸可以除Fe,但粗铜若未经酸浸处理,其中
杂质Fe会参与放电,则消耗相同电量时,会降低得到纯铜的量。
1.“操作或措施”
操作或措施 答题模板
从溶液中得到晶体
蒸发浓缩→冷却结晶→过滤→洗涤(包括水洗、冰水洗、热水洗、乙醇洗等)→干燥
的操作
将溶液转移到蒸发皿中加热,并用玻璃棒不断搅拌,待有大量晶体出现时停止加
蒸发结晶的操作
热,利用余热蒸干剩余水分
证明沉淀完全的操
静置,取上层清液,加入××试剂(沉淀剂),若没有沉淀生成,说明沉淀完全
作
沿玻璃棒向漏斗(过滤器)中的沉淀上加蒸馏水至没过沉淀,静置使水自然流干,重
洗涤沉淀的操作
复操作数次
2.“目的或原因”
目的或原因 答题模板
沉淀水洗的目的 除去××(可溶于水)杂质
a.减小固体的溶解度;b.除去固体表面吸附的杂质;c.乙醇挥发带走水
沉淀用乙醇洗涤的目的
分,使固体快速干燥
冷凝回流的作用及目的 防止××蒸气逸出脱离反应体系,提高××物质的转化率
防止××离子水解;防止××离子沉淀;确保××离子沉淀完全;防止××溶
控制溶液pH的目的
解等;促进/抑制××气体吸收/逸出
加过量A试剂的原因 使B物质反应完全(或提高B物质的转化率)等
温度过高××物质分解(如HO 、NH ·H O、浓硝酸、NH HCO 等)或××
2 2 3 2 4 3
温度不高于××℃的原因 物质挥发(如浓硝酸、浓盐酸)或××物质氧化(如NaSO 等)或促进××物
2 3
质水解(如AlCl 、FeCl 等)
3 3
减小压强,使液体沸点降低,防止××物质受热分解(如HO 、浓硝
2 2
减压蒸馏(减压蒸发)的原因
酸、NH HCO 等)
4 3
抑制××离子的水解(如加热蒸发AlCl 溶液时需在HCl气流中进行;加
3
蒸发、反应时的气体氛围
热MgCl ·6H O 得MgCl 时需在HCl气流中进行等)
2 2 2配制某溶液前先煮沸水的原因 除去溶解在水中的氧气,防止××物质被氧化
反应容器中和大气相通的玻璃
指示容器中压强大小,避免反应容器中压强过大
管的作用
1 .温度、浓度、压强的控制
术语 功能
温度 ①加快反应速率或溶解速率;②促进平衡向吸热方向移动;③除杂,除去热不
的控 升温 稳定的杂质,如NaHCO 、Ca(HCO )、KMnO 、I、NH Cl等物质。④使沸点
3 3 2 4 2 4
制 相对较低的原料气化
①防止某物质在高温时会溶解(或分解) ;② 使化学平衡向着题目要求的方向
降温 移动(放热方向);③使某个沸点较高的产物液化,使其与其他物质分离;④降
低晶体的溶解度,减少损失.
①防止某种物质温度过高时会分解或挥发;②为了使某物质达到沸点挥发出
控温(用 来;③使催化剂的活性达到最好;④防止副反应的发生;⑤降温或减压可以减
水浴或油 少能源成本,降低对设备的要求,达到绿色化学的要求;⑥如果题目中出现了
浴控温) 包括产物在内的各种物质的溶解度信息,则要根据它们的溶解度随温度升高而
改变的情况,寻找合适的结晶分离方法 ( 蒸发结晶或浓缩结晶) 。
增大反应 ①可加快反应速率 。对气体分子数减少的反应,加压使平衡向生成物方向移
物浓 动。但压强太大,动力消耗更多,设备要求更高,成本增加,故必须综合考
浓
度 、 加 虑;②加压一般是提高气体反应物浓度措施 ,在气体和固体、液体反应的体系
度、
压 中并不适宜;③生产中常使廉价易得的原料适当过量,以提高另一原料的利用
压强
率。
的控
制 减小压强,降低液体的沸点,防止(如浓HNO、NH .H O、HO、NH HCO 等)
减压蒸馏 3 3 2 2 2 4 3
物质分解;
2 . p H 的控制
术语 功能
(1)目的:调节pH值实质上是利用沉淀溶解平衡把某些离子转化成沉淀。(2)原则:不管是
调高还是调低,原则都是加过量的除杂剂而不引进新的杂质,这里分两种情况①如果要得
控制 到滤液,可加固体沉淀剂消耗H+或OH—,如除去含Cu2+溶液中混有的Fe3+,可通过加入
溶液 CuO、Cu(OH) 、Cu(OH) CO 等;②要得到滤渣,则需加入碱性溶液,如氨水或氢氧化钠溶
2 2 3
的PH 液。调低PH值的原则与调高PH的原则相同。(3)题目呈现方式:题中通常会以表格数据形
式,或“已知信息”给出需求的“适宜PH范围”的信息;(4)解题步骤:①判断溶液呈酸
(或碱)性; ②判断调高还是调低; ③选择合适的调节剂。
3 .体系环境氛围及其它条件的控制
术语 功能
酸 (1)蒸发或结晶时,加入相应的酸或碱,以抑制某些盐的水解;(2)需要在酸性气流中干燥
性、 FeCl 、AlCl 、MgCl 等含水晶体,以防止水解。如从海水中提取镁,从MgCl 的溶液里结
3 3 2 2
碱性 晶析出的是氯化镁结晶水合物,电解熔化氯化镁才能制得金属镁,要去除氯化镁晶体中的
或 结晶水"需要在氯化氢气流中加热,否则煅烧所得的最后固体不是 MgCl ,而是熔点更高的
2
某种 MgO, 具有相似情况的还有 FeCl AlCl 等;(3)营造还原性氛围:加热煮沸酸液后再冷
3 、 3
环境
却,其目的是排除酸溶液中的氧气,如用废铁制备绿矾晶体,需要把硫酸加热煮沸后再加
氛围
入,同时还不能加入过量,防止Fe2+被氧化;(4)营造氧化性氛围:加入氧化剂进行氧化,如加入绿色氧化剂 HO 将 Fe2+ 氧化转化为Fe3+ 。
2 2
1.(2025·河南省南阳市高三联考,节选)硝酸镉晶体[Cd(NO )·4H O]常用作玻璃和陶瓷的着色剂。以
3 2 2
镉黄废料(主要含CdS,含少量的FeO、Al O、SiO)为原料制备硝酸镉晶体的流程如下:
2 3 2
常温下,有关金属离子形成氢氧化物沉淀的相关pH如表。
Fe(OH) Al(OH) Cd(OH)
3 3 2
开始沉淀pH 2.3 4.0 8.2
沉淀完全pH 4.2 5.2 9.7
(1)“酸溶”时,反应温度不宜过高,原因是 。
(2)“滤渣1”的主要成分是 。
(4)“系列操作”步骤中,将滤液送入蒸发器浓缩至 ,然后送至结晶器进行冷却结晶,可得到硝
酸镉晶体。
【答案】(1)温度过高,硝酸会挥发和分解 (2)S、SiO
2
(4)出现晶膜(或有少量晶体析出)
【解析】(1)硝酸具有挥发性和不稳定性,加热时可挥发和分解,故酸溶时反应温度不宜过高的原因是:
温度过高,硝酸会挥发和分解。(2)酸溶时,硝酸有强氧化性,可把CdS中的S2-氧化生成S,SiO 不溶于硝
2
酸,因此滤渣1的主要成分是S、SiO。(4)“系列操作”步骤包括:蒸发浓缩、冷却结晶、过滤、洗涤、烘
2
干,在蒸发浓缩时,将滤液送入蒸发器浓缩至出现晶膜(或有少量晶体析出),然后送至结晶器进行冷却结
晶。
2.将净化液[(NH )VO ]中的钒转化为NH VO 固体,其流程如下。
4 3 4 4 3
向(NH )VO 溶液中加入NHCl溶液的目的:_______。
4 3 4 4
【答案】调节pH值,使(NH )VO 转化为NH VO
4 3 4 4 3【解析】向(NH )VO 溶液中加入NHCl溶液的目的是调节pH值,使(NH )VO 转化为NH VO ;
4 3 4 4 4 3 4 4 3
3.向铬铁矿(FeCrO)中通入O 进行焙烧,焙烧时气体与矿料逆流而行,目的是___________。
2 4 2
【答案】增大反应物接触面积,提高化学反应速率
4.将催化剂负载在玻璃棉上而不直接平铺在玻璃管中,目的是_____________________。
【答案】增大接触面积,提高催化效果,加快反应速率
5.向金属 Bi 中加入稀 HNO 酸浸,过程中分次加入稀 HNO 可降低反应剧烈程度,其原理是
3 3
_____________________________________________________。
【答案】减少稀HNO 的用量,降低反应剧烈程度,使HNO 充分反应防止挥发
3 3
【解析】强调分次加入对反应的影响:①控制用量,防止过量发生副反应;②降低反应剧烈程度;③
防止放热反应温度过高,造成副反应的发生,以及物质的挥发、分解。
6.TiO·xHO沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:
2 2
温度/℃ 30 35 40 45 50
TiO·xHO转化率/% 92 95 97 93 88
2 2
分析40 ℃时,TiO·xHO转化率最高的原因:______________________________。
2 2
【答案】低于40 ℃ TiO·xHO转化反应速率随温度的升高而增加;超过40 ℃,双氧水分解与氨气
2 2
逸出导致TiO·xHO转化率下降
2 2
7.科学合理地从污泥中提取铜、镍等有价金属,无论从经济利益还是环保利益上都有深远的意义。
常见的氨浸-沉淀法回收电镀污泥(主要金属元素及含量Ni:0.81%,Cu:0.94%,Fe:0.39%,Cr:1.14%,
Ca:1.49%,Mg:2.02%)中的铜。电镀污泥在氨浸以后,如果能提前进行化学除杂,将对后续分离铜、镍
有很大的帮助,通常我们用(NH )PO 溶液处理金属浸出液,查数据可知,此时Ni(NH )2+与(NH )PO 溶液
4 3 4 3 6 4 3 4
反应的离子方程式为3Ni(NH )2++2PO3-= Ni (PO )↓+18NH ,K=1.2×104,试回答可以用磷酸铵预处理浸出
3 6 4 3 4 2 3
液的原因:_______。
【答案】K值的大小并不代表反应进行的快慢,此外在其他金属配合物中,也有反应更大的可能性,
在相对强弱对比时,有可能是其他金属生成磷酸盐沉淀更容易
【解析】电镀污泥在氨浸以后,所得溶液中除去含有铜氨离子、镍氨离子外,可能还含有其它配离子,
用(NH )PO 溶液处理金属浸出液,可将其它配离子转化为沉淀,由反应3Ni(NH )2++2PO3-=
4 3 4 3 6 4
Ni (PO )↓+18NH,K=1.2×104可以看出,镍氨离子也有转化为沉淀的可能,若杂质离子更易转化为沉淀,
3 4 2 3
则可控制(NH )PO 溶液的用量,将杂质除尽,所以可以用磷酸铵预处理浸出液的原因:K值的大小并不代
4 3 4
表反应进行的快慢,此外在其他金属配合物中,也有反应更大的可能性,在相对强弱对比时,有可能是其
他金属生成磷酸盐沉淀更容易。
题型三 产物或反应物推断、陌生方程式的书写1.(2024·湖南卷,16节选)铜阳极泥(含有Au、Ag Se、Cu Se、PbSO 等)是一种含贵金属的可再生资
2 2 4
源,回收贵金属的化工流程如下:
(2)“滤液1”中含有Cu2+和HSeO,“氧化酸浸”时Cu Se反应的离子方程式为 ;
2 3 2
【答案】(2) Cu Se+4H O+4H+=2Cu2++HSeO+5H O
2 2 2 2 3 2
【解析】(2)滤液1中含有Cu2+和HSeO,氧化酸浸时Cu Se与HO、HSO 发生氧化还原反应,生成
2 3 2 2 2 2 4
CuSO 、HSeO 和HO,反应的离子方程式为:Cu Se+4H O+4H+=2Cu2++HSeO+5H O。
4 2 3 2 2 2 2 2 3 2
26.(2024·全国新课标卷,8节选)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着
广泛应用。一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴
成品的工艺如下:
(3)“氧化沉钴”中氧化还原反应的离子方程式为_______、_______。
【答案】(3)①3Co2++MnO - +7H O= 3Co(OH) ↓+MnO ↓+5H+
4 2 3 2
②2MnO - +3Mn2++2H O=5MnO ↓+4H+
4 2 2
【解析】(3)该过程发生两个氧化还原反应,根据分析中两个反应的反应物、产物与反应环境(pH=5),
结合得失电子守恒、电荷守恒和原子守恒可写出两个离子方程式:3Co2++MnO - +7H O= 3Co(OH) ↓
4 2 3
+MnO ↓+5H+、2MnO - +3Mn2++2H O=5MnO ↓+4H+。
2 4 2 2
2.(2024· 海南卷,15节选)锰锌铁氧体(MnZn Fe O)元件是电子线路中的基础组成部分。某实验室
x 1-y 2 4
利用废弃电子产品中的锰锌铁氧体制备MnO 、ZnO和FeC O·2H O,可用于电池,催化剂等行业,其工艺
2 2 4 2
流程如下:
(1)氨浸的作用是将 元素(填元素符号)有效转移到水溶液中。(2)煮沸含有配合物的溶液B,产生混合气体,经冷凝后所得溶液可循环用于氨浸,该溶液是 。
(4)沉铁时,选择KC O 是为了便于从滤液中回收有价值的钾盐 (填化学式)。该钾盐在种植业
2 2 4
中的一种用途是 。
【答案】(1)Zn (2)氨水 (4) K SO 钾肥或其他合理用途
2 4
【解析】(1)氨浸的作用是将Zn元素有效转移到水溶液中。(2)溶液B含有配合物,煮沸溶液B后生成
氢氧化锌沉淀,产生混合气体,经冷凝后的溶液可循环利用于氨浸,则生成的混合气体中含有氨气和水蒸
气,冷凝后的溶液为氨水。(4)用硫酸溶解固体A后,溶液中存在大量硫酸根,选择KC O 可以从滤液中
2 2 4
回收有价值的硫酸钾,该钾盐在种植业中可用作钾肥。
3.(2024· 贵州卷,16节选)煤气化渣属于大宗固废,主要成分为Fe O、Al O、SiO 及少量MgO等。
2 3 2 3 2
一种利用“酸浸—碱沉—充钠”工艺,制备钠基正极材料NaFePO 和回收Al O 的流程如下:
4 2 3
(3)“除杂”时需加入的试剂X是 。
(4)“水热合成”中,NH HPO 作为磷源,“滤液2”的作用是 ,水热合成NaFePO 的离子方程
4 2 4 4
式为 。
【答案】(3)NaOH溶液
(4)提供Na+和反应所需要的碱性环境
Fe2++NH++3OH-+Na++H PO -=NaFePO ↓+NH↑+3H O
4 2 4 4 3 2
【解析】(3)“除杂”时需要沉淀镁离子、得Na[Al(OH) ],所以加入的试剂X是NaOH溶液;(4)“水热
4
合成”中,NH HPO 作为磷源,“滤液2”为NaOH溶液,其既可以提供合成NaFePO 所需要的Na+,又可
4 2 4 4
以提供反应所需要的碱性环境,水热合成NaFePO 的离子方程式为Fe2++NH++3OH-+Na++H PO -
4 4 2 4
=NaFePO ↓+NH↑+3H O。
4 3 2
4.(2024·辽吉黑卷,16节选)中国是世界上最早利用细菌冶金的国家。已知金属硫化物在“细菌氧
化”时转化为硫酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中细小的Au颗粒被FeS、 包
2
裹),以提高金的浸出率并冶炼金,工艺流程如下:回答下列问题:
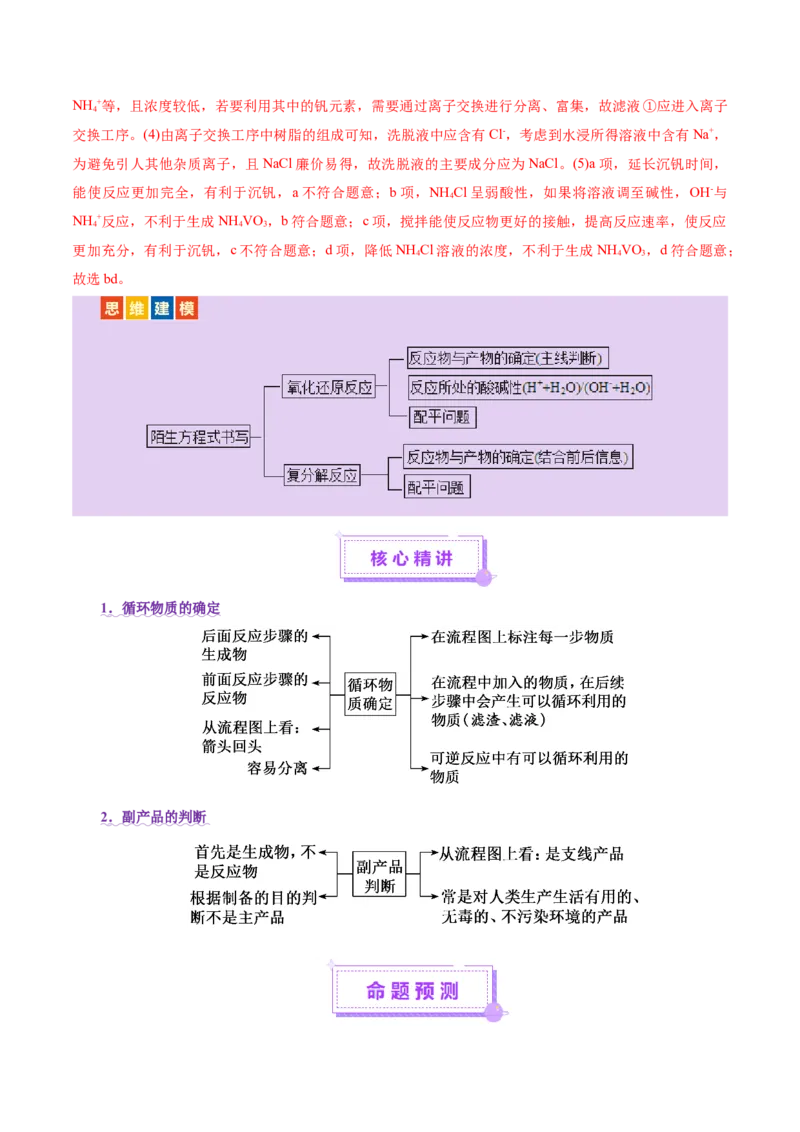
(1)北宋时期我国就有多处矿场利用细菌氧化形成的天然“胆水”冶炼铜,“胆水”的主要溶质为
_______(填化学式)。
(2)“细菌氧化”中,FeS 发生反应的离子方程式为_______。
2
(3)“沉铁砷”时需加碱调节pH,生成_______(填化学式)胶体起絮凝作用,促进了含As微粒的沉降。
(7)滤液②经HSO 酸化,[Zn(CN) ]2-转化为ZnSO 和HCN的化学方程式为_______。用碱中和HCN可
2 4 4 4
生成_______(填溶质化学式)溶液,从而实现循环利用。
【答案】(1)CuSO
4
(2)4FeS +15O +2H O 4Fe3++8SO2-+4H+
2 2 2 4
(3) Fe(OH)
3
(7) Na [Zn(CN) ] +2H SO =ZnSO +4HCN+ Na SO NaCN
2 4 2 4 4 2 4
【解析】(1)“胆水”冶炼铜,“胆水”的主要成分为CuSO ;(2)“细菌氧化”的过程中,FeS 在酸性环
4 2
境下被O 氧化为Fe3+和SO 2-,离子方程式为:4FeS+15O +2H O 4Fe3++8SO2-+4H+;(3)“沉铁砷”时,
2 4 2 2 2 4
加碱调节pH值,Fe3+转化为Fe(OH) 胶体,可起到絮凝作用,促进含As微粒的沉降;(7)滤液②含有
3
[Zn(CN) ]2-,经过HSO 的酸化,[Zn(CN) ]2-转化为ZnSO 和HCN,反应得化学方程式为:Na[Zn(CN) ]
4 2 4 4 4 2 4
+2H SO =ZnSO +4HCN+ Na SO ;用碱中和HCN得到的产物,可实现循环利用,即用NaOH中和HCN生
2 4 4 2 4
成NaCN,NaCN可用于“浸金”步骤,从而循环利用。
5.(2024·甘肃卷,15节选)我国科研人员以高炉渣(主要成分为CaO,MgO,Al O 和SiO 等)为原料,
2 3 2
对炼钢烟气(CO 和水蒸气)进行回收利用,有效减少了环境污染,主要流程如图所示:
2已知:K (CaSO)= 4.9×10-5,K (CaCO)= 3.4×10-9
sp 4 sp 3
(1)高炉渣与(NH )SO 经焙烧产生的“气体”是 。
4 2 4
(2)“滤渣”的主要成分是CaSO 和 。
4
(3)“水浸2”时主要反应的化学方程式为 ,该反应能进行的原因是 。
(4)铝产品NH Al(SO )·12H O可用于 。
4 4 2 2
【答案】(1)NH (2)SiO
3 2
(3)CaSO+(NH)CO= CaCO +(NH )SO K (CaSO)>K (CaCO),微溶的硫酸钙转化为更难溶的
4 4 2 3 3 4 2 4 sp 4 sp 3
碳酸钙
(4)净水
【解析】高炉渣(主要成分为CaO,MgO,Al O 和SiO 等)加入(NH )SO 在400℃下焙烧,生成硫酸钙、
2 3 2 4 2 4
硫酸镁、硫酸铝,同时产生气体,该气体与烟气(CO 和水蒸气)反应,生成(NH )CO ,所以该气体为
2 4 2 3
NH ;焙烧产物经过水浸1,然后过滤,滤渣为CaSO 以及未反应的SiO ,滤液溶质主要为硫酸镁、硫酸
3 4 2
铝及硫酸铵;滤液浓缩结晶,析出NH Al(SO )·12H O,剩余富镁溶液;滤渣加入(NH )CO 溶液,滤渣中
4 4 2 2 4 2 3
的CaSO 会转化为更难溶的碳酸钙。(1)高炉渣与(NH )SO 经焙烧产生的“气体”是NH ;(2)由分析可知,
4 4 2 4 3
“滤渣”的主要成分是CaSO 和未反应的SiO ;(3)“水浸2”时主要反应为硫酸钙与碳酸铵生成更难溶的碳
4 2
酸钙,反应方程式为 CaSO+(NH)CO= CaCO +(NH )SO ,该反应之所以能发生,是由于 K (CaSO)=
4 4 2 3 3 4 2 4 sp 4
4.9×10-5,K (CaCO)= 3.4×10-9,K (CaSO)>K (CaCO),微溶的硫酸钙转化为更难溶的碳酸钙;(4)铝产
sp 3 sp 4 sp 3
品NH Al(SO )·12H O溶于水后,会产生Al3+,Al3+水解生成Al(OH) 胶体,可用于净水。
4 4 2 2 3
6.(2024·河北卷,16) VO 是制造钒铁合金、金属钒的原料,也是重要的催化剂。以苛化泥为焙烧添
2 5
加剂从石煤中提取VO 的工艺,具有钒回收率高、副产物可回收和不产生气体污染物等优点。工艺流程如
2 5
下。
已知:i石煤是一种含VO 的矿物,杂质为大量Al O 和少量CaO等;苛化泥的主要成分为CaCO、
2 3 2 3 3
NaOH、NaCO 等。
2 3ⅱ高温下,苛化泥的主要成分可与Al O 反应生成偏铝酸盐;室温下,偏钒酸钙[Ca(VO )]和偏铝酸钙
2 3 3 2
均难溶于水。回答下列问题:
(1)钒原子的价层电子排布式为_______;焙烧生成的偏钒酸盐中钒的化合价为_______,产生的气体①
为_______(填化学式)。
(2)水浸工序得到滤渣①和滤液,滤渣①中含钒成分为偏钒酸钙,滤液中杂质的主要成分为_______(填
化学式)。
(3)在弱碱性环境下,偏钒酸钙经盐浸生成碳酸钙发生反应的离子方程式为_______;CO 加压导入盐
2
浸工序可提高浸出率的原因为_______;浸取后低浓度的滤液①进入_______(填工序名称),可实现钒元素
的充分利用。
(4)洗脱工序中洗脱液的主要成分为_______(填化学式)。
(5)下列不利于沉钒过程的两种操作为_______(填序号)。
a.延长沉钒时间 b.将溶液调至碱性 c.搅拌 d.降低NH Cl溶液的浓度
4
【答案】(1)①3d34s2 ②+5 ③CO
2
(2) NaAlO
2
(3)①Ca(VO )+HCO-+OH- CaCO+2VO -+H O
3 2 3 3 3 2
②提高溶液中HCO -浓度,促使偏钒酸钙转化为碳酸钙,释放VO - ③离子交换
3 3
(4) NaCl
(5)bd
【解析】石煤和苛化泥通入空气进行焙烧,反应生成 NaVO 、Ca(VO ) 、NaAlO 、Ca(AlO) 、CaO和
3 3 2 2 2 2
CO 等,水浸可分离焙烧后的可溶性物质(如NaVO )和不溶性物质[Ca(VO ) 、Ca(AlO) 等],过滤后滤液进
2 3 3 2 2 2
行离子交换、洗脱,用于富集和提纯 VO -,加入氯化铵溶液沉钒,生成NH VO ,经一系列处理后得到
3 4 3
VO ;滤渣①在 ,66~70℃的条件下加入3%NH HCO 溶液进行盐浸,滤渣①中含有钒元素,通过
2 3 4 3
盐浸,使滤渣①中的钒元素进入滤液①中,再将滤液①回流到离子交换工序,进行VO -的富集。(1)钒是
3
23号元素,其价层电子排布式为3d34s2 ;焙烧过程中,氧气被还原,VO 被氧化生成VO -,偏钒酸盐中
2 3 3
钒的化合价为+5价;CaCO 在 以上开始分解,生成的气体①为CO 。(2)由已知信息可知,高温下,
3 2
苛化泥的主要成分与Al O 反应生成偏铝酸钠和偏铝酸钙,偏铝酸钠溶于水,偏铝酸钙难溶于水,所以滤
2 3
液中杂质的主要成分是NaAlO 。(3)在弱碱性环境下,Ca(VO ) 与HCO -和OH-反应生成CaCO 、VO -和
2 3 2 3 3 3
HO,离子方程式为:Ca(VO )+HCO-+OH- CaCO+2VO -+H O; CO 加压导入盐浸工序可提高浸
2 3 2 3 3 3 2 2
出率,因为C可提高溶液中HCO -浓度,促使偏钒酸钙转化为碳酸钙,释放VO -;滤液①中含有VO -、
3 3 3NH +等,且浓度较低,若要利用其中的钒元素,需要通过离子交换进行分离、富集,故滤液①应进入离子
4
交换工序。(4)由离子交换工序中树脂的组成可知,洗脱液中应含有Cl-,考虑到水浸所得溶液中含有Na+,
为避免引人其他杂质离子,且NaCl廉价易得,故洗脱液的主要成分应为NaCl。(5)a项,延长沉钒时间,
能使反应更加完全,有利于沉钒,a不符合题意;b项,NH Cl呈弱酸性,如果将溶液调至碱性,OH-与
4
NH +反应,不利于生成NH VO ,b符合题意;c项,搅拌能使反应物更好的接触,提高反应速率,使反应
4 4 3
更加充分,有利于沉钒,c不符合题意;d项,降低NH Cl溶液的浓度,不利于生成NH VO ,d符合题意;
4 4 3
故选bd。
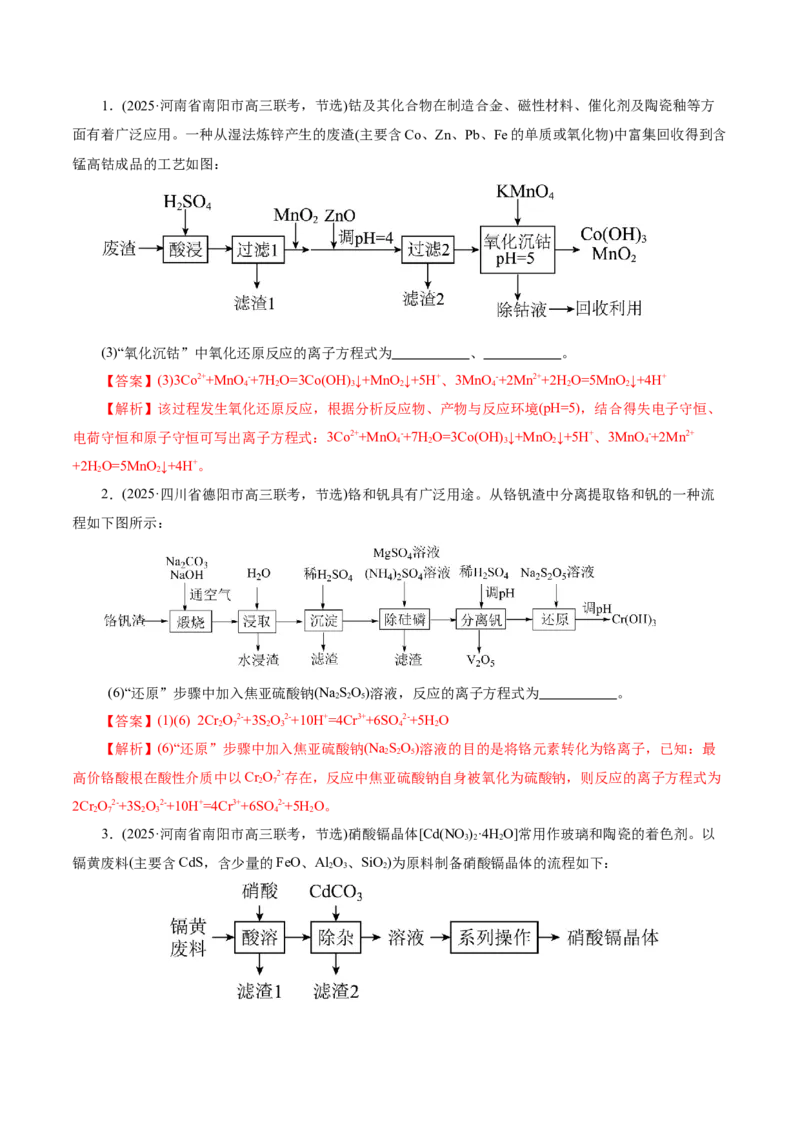
1 .循环物质的确定
2 .副产品的判断1.(2025·河南省南阳市高三联考,节选)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方
面有着广泛应用。一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含
锰高钴成品的工艺如图:
(3)“氧化沉钴”中氧化还原反应的离子方程式为 、 。
【答案】(3)3Co2++MnO-+7H O=3Co(OH) ↓+MnO↓+5H+、3MnO -+2Mn2++2H O=5MnO ↓+4H+
4 2 3 2 4 2 2
【解析】该过程发生氧化还原反应,根据分析反应物、产物与反应环境(pH=5),结合得失电子守恒、
电荷守恒和原子守恒可写出离子方程式:3Co2++MnO-+7H O=3Co(OH) ↓+MnO↓+5H+、3MnO -+2Mn2+
4 2 3 2 4
+2H O=5MnO ↓+4H+。
2 2
2.(2025·四川省德阳市高三联考,节选)铬和钒具有广泛用途。从铬钒渣中分离提取铬和钒的一种流
程如下图所示:
(6)“还原”步骤中加入焦亚硫酸钠(NaSO)溶液,反应的离子方程式为 。
2 2 5
【答案】(1)(6) 2Cr O2-+3S O2-+10H+=4Cr3++6SO2-+5H O
2 7 2 3 4 2
【解析】(6)“还原”步骤中加入焦亚硫酸钠(NaSO)溶液的目的是将铬元素转化为铬离子,已知:最
2 2 5
高价铬酸根在酸性介质中以Cr O2-存在,反应中焦亚硫酸钠自身被氧化为硫酸钠,则反应的离子方程式为
2 7
2Cr O2-+3S O2-+10H+=4Cr3++6SO2-+5H O。
2 7 2 3 4 2
3.(2025·河南省南阳市高三联考,节选)硝酸镉晶体[Cd(NO )·4H O]常用作玻璃和陶瓷的着色剂。以
3 2 2
镉黄废料(主要含CdS,含少量的FeO、Al O、SiO)为原料制备硝酸镉晶体的流程如下:
2 3 2常温下,有关金属离子形成氢氧化物沉淀的相关pH如表。
Fe(OH) Al(OH) Cd(OH)
3 3 2
开始沉淀pH 2.3 4.0 8.2
沉淀完全pH 4.2 5.2 9.7
(3)“除杂”步骤中,加入CdCO 的目的是调pH,范围为 。该过程中 发生反应的离子方程
3
式为 。
(5)硝酸镉晶体需在低温的条件下烘干。其在111.2℃时失去结晶水,217.3℃时分解产生CdO和红棕色
的混合气体,该混合气体可以使带火星的木条复燃,硝酸镉在217.3℃时分解的化学方程式为 。
【答案】(3) 5.2≤pH<8.2 2Fe3++3CdCO +3H O=2Fe(OH) +3CO ↑+3Cd2+
3 2 3 2
(5) 2Cd(NO ) 2CdO+4NO ↑+H O
3 2 2 2
【解析】(3)除杂步骤的目的是除去溶液中含有的H+、Fe3+、Al3+,根据Fe3+、Al3+形成氢氧化物沉淀的
相关pH数据,为使Fe3+、Al3+完全沉淀,而Cd2+不沉淀,溶液的pH可调范围是:5.2≤pH<8.2。Fe3+在水
溶液中存在水解平衡:Fe3++3H O Fe(OH) +3H+,加入的CdCO 能与H+反应,从而促进Fe3+的水解,
2 3 3
并调节溶液的pH,该过程中发生反应的离子方程式为:2Fe3++3CdCO +3H O=2 Fe(OH) +3CO ↑+3Cd2+。(5)
3 2 3 2
混合气体呈红棕色,说明含有NO ,可使带火星木条复燃,说明含O,因此硝酸镉在217.3℃时分解的产
2 2
物有CdO、NO 、O,反应中,N元素化合价变化为+5→+4,O元素化合价变化为-2→0,根据氧化还原反
2 2
应中元素化合升降总数相等得该反应的化学方程式为:2Cd(NO ) 2CdO+4NO ↑+H O。
3 2 2 2
4.(2025·山东省Eternal7社区高三模拟预测,节选)我国是稀土大国,储量大、矿种多。稀土元素的物
理性质和化学性质极为相似,常见化合价+3价其中钇(Y)元素是激光和超导的重要材料,工业上通过如下
工艺流程用钇矿石(Y FeBe Si O )制取氧化钇。
2 2 2 10
已知:
i.铍和铝符合元素周期表的对角线规则;
ii.草酸铵与稀土草酸盐可形成可溶性络合物;
(1)试写出“共熔”过程中的化学反应方程式: 。
【答案】(1)4Y FeBe Si O +32NaOH+O=8Y(OH) +2Fe O+8Na SiO+Na BeO+4H O
2 2 2 10 2 3 2 3 2 3 2 2 2
【解析】(1)钇矿石与氢氧化钠并通氧气共熔反应生成Y(OH) 、Fe O、NaSiO 和NaBeO,同时还会
3 2 3 2 3 2 2
生成水,则“共熔”过程中的化学反应方程式:
4YFeBe Si O +32NaOH+O=8Y(OH) +2Fe O+8Na SiO+Na BeO+4H O。
2 2 2 10 2 3 2 3 2 3 2 2 25.(2025·河南省郑州市高三联考,节选)砷的化合物可用于半导体领域。一种从酸性高浓度含砷废水
[砷主要以亚砷酸(H AsO )形式存在]中回收As O 的工艺流程如下:
3 3 2 3
已知:①6NaOH+AsS=Na AsO +Na AsS +3H O;
2 3 3 3 3 3 2
②As O(aq)+3S2-(aq) 2AsS 3-(aq)。
2 3 3
(4)写出“脱硫”时NaAsS 反应的离子方程式: ,相同条件下,单质硫在水、CCl 、酒精
3 3 4
三种溶剂中溶解度最小的是 。
(5)写出“还原”时反应的化学方程式: 。
(6) H AsO 是三元弱酸,第一步和第二步电离是通过和水中的OH-结合实现的,第三步则直接电离出
3 3
H+,第一步电离方程式为HAsO +H O [As(OH) ]-+H+,则第三步电离方程式为 。
3 4 2 4
【答案】(4)AsS 3-+4ClO-=AsO 3-+3S↓ +4Cl- 水
3 4
(5) 2H AsO +2SO=AsO+H SO +H O
3 4 2 2 3 2 4 2
(6) [As(OH) ]2- AsO 3-+H++2H O (写成[As(OH) ]2- [AsO(OH) ]3-+H+也可)
5 3 2 5 4
【解析】(4)“脱硫”时,NaAsS 与NaClO发生氧化还原反应,生成NaAsO 和S,在NaAsS 中,As
3 3 3 4 3 3
由+3价升高到+5价,S由-2价升高到0价,NaClO中Cl元素由+1价降低到-1价,依据得失电子守恒,可
得出二者的定量关系为:NaAsS (1个AsS 3-中As、S元素共升高8价)——4NaClO(1个ClO-中Cl元素共降
3 3 3
低2价),再依据电荷守恒、质量守恒,可得出发生反应的离子方程式:AsS 3-+4ClO-=AsO 3-+3S↓ +4Cl-,相
3 4
同条件下,单质硫、CCl 为非极性分子,酒精的极性较弱,水的极性较强,依据相似相溶原理,在水、
4
CCl 、酒精三种溶剂中溶解度最小的是水。(5)“还原”时,HAsO 被SO 还原,生成As O 和HSO ,依据
4 3 4 2 2 3 2 4
得失电子守恒,可建立关系式:2HAsO ——2SO ——As O,再依据质量守恒,便可得出反应的化学方程
3 4 2 2 3
式:2HAsO +2SO=AsO+H SO +H O。(6)H AsO 是三元弱酸,第一步和第二步电离是通过和水中的OH-
3 4 2 2 3 2 4 2 3 3
结合实现的,第三步则直接电离出H+,第一步电离方程式为HAsO +H O [As(OH) ]-+H+,第二步电
3 4 2 4
离方程式为[As(OH) ]-+ H O [As(OH) ]2-+H+,则第三步电离方程式为[As(OH) ]2- AsO 3-+H+
4 2 5 5 3
+2H O (写成[As(OH) ]2- [AsO(OH) ]3-+H+也可)。
2 5 4
6.[真题改编](2022•河北省选择性考试,节选)以焙烧黄铁矿FeS(杂质为石英等)产生的红渣为原料制
2
备铵铁蓝Fe(NH )Fe(CN) 颜料。工艺流程如下:
4 6(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(5)沉铁工序产生的白色沉淀Fe(NH )Fe(CN) 中 的化合价为_______,氧化工序发生反应的离子方程
4 2 6
式为_______。
【答案】(3)7Fe (SO )+FeS +8H O=15FeSO +8H SO
2 4 3 2 2 4 2 4
(5)+2; Fe(NH )Fe(CN) +ClO-+2H+=Fe(NH)Fe(CN) +H O+Cl-+NH+
4 2 6 4 6 2 4
【解析】(3)还原工序中,不产生S单质沉淀,则硫元素被氧化为SO 2-,反应原理为:14Fe3+
4
+FeS +8H O=15Fe2++2 SO 2-+16H+,故化学方程式为:7Fe (SO )+FeS +8H O=15FeSO +8H SO ;(5)沉铁工
2 2 4 2 4 3 2 2 4 2 4
序中产生的白色沉淀Fe(NH )Fe(CN) 中Fe的化合价为+2价和[Fe(CN) ]4-中的+3价,由分析可知,氧化工
4 2 6 6
序所发生的离子方程式为:6Fe(NH )Fe(CN) + ClO - +6H+=6Fe(NH)Fe(CN) +3H O+Cl-+6 NH +。
4 2 6 3 4 6 2 4
7.[真题改编](2022·湖南卷,17节选)以钛渣(主要成分为TiO,含少量V、Si和Al的氧化物杂质)为原
2
料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗TiCl 中含有的几种物质的沸点:
4
物质 TiCl VOCl SiCl AlCl
4 3 4 3
沸点/℃ 136 127 57 180
回答下列问题:
(3)“除钒”过程中的化学方程式为__________________;“除硅、铝”过程中,分离TiCl 中含Si、Al
4
杂质的方法是________________________________________________。
(4)“除钒”和“除硅、铝”的顺序______(填“能”或“不能”)交换,理由是
________________________________________________________________________。
【答案】(3)3VOCl +Al===3VOCl +AlCl 蒸馏
3 2 3
(4)不能 若先“除硅、铝”再“除钒”,“除钒”时需要加入Al,又引入Al杂质
【解析】(3)“降温收尘”后钒元素主要以VOCl 形式存在,加入Al得到VOCl 渣,根据得失电子守恒
3 2
和元素守恒配平化学方程式为3VOCl +Al===3VOCl +AlCl ;AlCl 、SiCl 与TiCl 沸点差异较大,“除硅、
3 2 3 3 4 4铝”过程中可采用蒸馏的方法分离AlCl 、SiCl 。
3 4
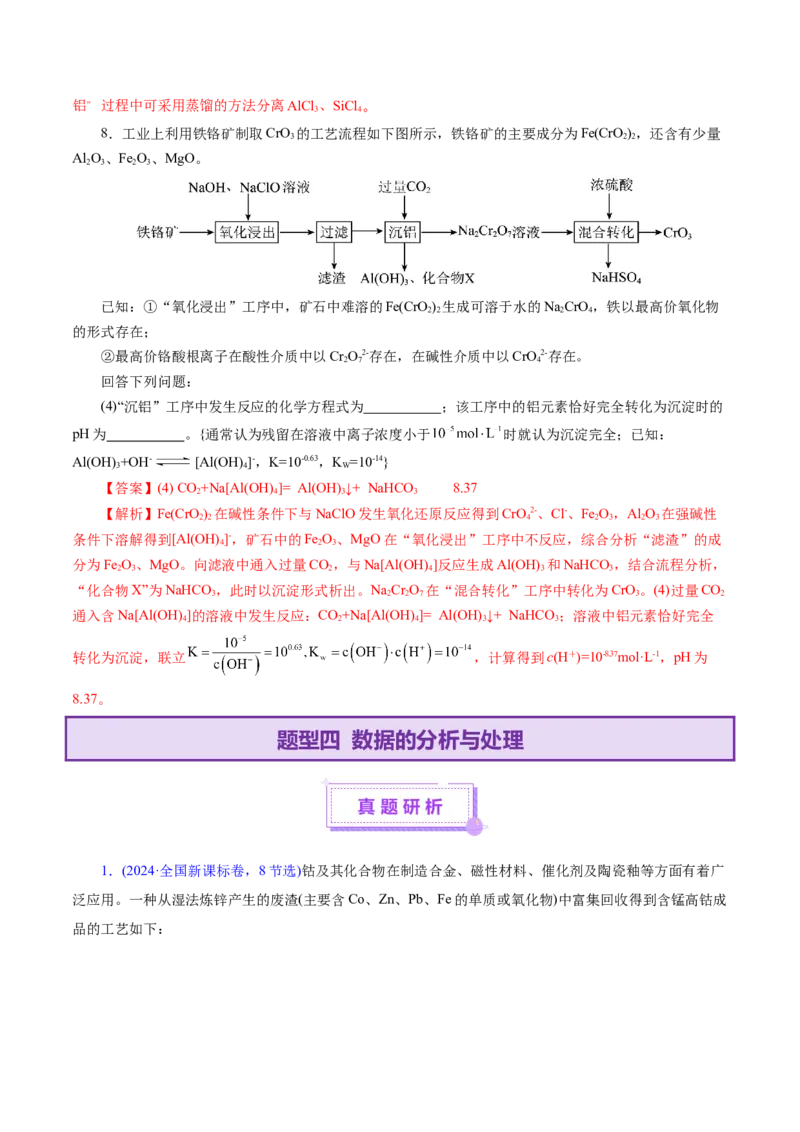
8.工业上利用铁铬矿制取CrO 的工艺流程如下图所示,铁铬矿的主要成分为Fe(CrO),还含有少量
3 2 2
Al O、Fe O、MgO。
2 3 2 3
已知:①“氧化浸出”工序中,矿石中难溶的Fe(CrO) 生成可溶于水的NaCrO,铁以最高价氧化物
2 2 2 4
的形式存在;
②最高价铬酸根离子在酸性介质中以Cr O2-存在,在碱性介质中以CrO2-存在。
2 7 4
回答下列问题:
(4)“沉铝”工序中发生反应的化学方程式为 ;该工序中的铝元素恰好完全转化为沉淀时的
pH为 。{通常认为残留在溶液中离子浓度小于 时就认为沉淀完全;已知:
Al(OH) +OH- [Al(OH) ]-,K=10-0.63,K =10-14}
3 4 W
【答案】(4) CO +Na[Al(OH)]= Al(OH) ↓+ NaHCO 8.37
2 4 3 3
【解析】Fe(CrO) 在碱性条件下与NaClO发生氧化还原反应得到CrO2-、Cl-、Fe O,Al O 在强碱性
2 2 4 2 3 2 3
条件下溶解得到[Al(OH) ]-,矿石中的Fe O、MgO在“氧化浸出”工序中不反应,综合分析“滤渣”的成
4 2 3
分为Fe O、MgO。向滤液中通入过量CO,与Na[Al(OH)]反应生成Al(OH) 和NaHCO ,结合流程分析,
2 3 2 4 3 3
“化合物X”为NaHCO ,此时以沉淀形式析出。NaCr O 在“混合转化”工序中转化为CrO。(4)过量CO
3 2 2 7 3 2
通入含Na[Al(OH)]的溶液中发生反应:CO+Na[Al(OH)]= Al(OH) ↓+ NaHCO ;溶液中铝元素恰好完全
4 2 4 3 3
转化为沉淀,联立 ,计算得到c(H+)=10-8.37mol·L-1,pH为
8.37。
题型四 数据的分析与处理
1.(2024·全国新课标卷,8节选)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方面有着广
泛应用。一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含锰高钴成
品的工艺如下:已知溶液中相关离子开始沉淀和沉淀完全( )时的pH:
Fe3+ Fe2+ Co3+ Co2+ Zn2+
.
开始沉淀的pH 15 6.9 — 7.4 6.2
沉淀完全的pH 2.8 8.4 1.1 9.4 8.2
(4)“除钴液”中主要的盐有_______(写化学式),残留的Co3+浓度为_______ mol·L-1。
【答案】(4)①ZnSO、KSO ②10-16.7
4 2 4
【解析】(4)最终得到的“除钴液”中含有的金属离子主要是最初“酸浸”时与加入ZnO调pH时引入的
Zn2+、加入KMnO “氧化沉钴”时引入的K+,而阴离子是在酸浸时引入的 SO 2-,因此其中主要的盐有
4 4
ZnSO 和KSO 。当溶液 pH=1.1时c(H+)=10-1.1mol·L-1,Co3+恰好完全沉淀,此时溶液中 c(Co3+)=1.0×10-
4 2 4
5mol·L-1,则 ,则 。“除
钴 液 ” 的 pH=5 , 即 c(H + )=10-5mol·L-1 , 则 , 此 时 溶 液 中
。
2.(2024·江苏卷,14节选)回收磁性合金钕铁硼(Nd Fe B)可制备半导体材料铁酸铋和光学材料氧化钕。
2 14
将8.84 mg Nd(OH)CO (摩尔质量为221 g·molˉ1)在氮气氛围中焙烧,剩余固体质量随温度变化曲线如图所
3
示。550~600℃时,所得固体产物可表示为NdO(CO),通过以上实验数据确定该产物中n(Nd3+):n(CO2-)
a b 3 c 3
的比值_______(写出计算过程)。【答案】(3) 2:1
【解析】8.84 mg Nd(OH)CO 的物质的量为 ,其在氮气氛围中焙烧后,金
3
属元素的质量和化合价均保持不变,因此,n(Nd3+)= ;550~600℃时剩余固体的质量为7.60
mg,固体减少的质量为1.24 mg,由于碱式盐在受热分解时易变为正盐,氢氧化物分解得到氧化物和
HO,碳酸盐分解得到氧化物和CO,因此,可以推测固体变为NdO(CO) 时失去的质量是生成HO和
2 2 a b 3 c 2
CO 的质量;根据H元素守恒可知,固体分解时生成HO的质量为
2 2
,则生成CO 的质量为1.24 mg-0.36mg=0.88mg,则生成
2
CO 的物质的量为 ,由C元素守恒可知,分解后剩余的CO2-的物质的量
2 3
为4×10-5mol- = ,因此可以确定该产物中n(Nd3+):n(CO2-)的比值为
3
。
3.(2024· 海南卷,15节选)锰锌铁氧体(MnZn Fe O)元件是电子线路中的基础组成部分。某实验室
x 1-y 2 4
利用废弃电子产品中的锰锌铁氧体制备MnO 、ZnO和FeC O·2H O,可用于电池,催化剂等行业,其工艺
2 2 4 2
流程如下:回答问题:
(3)沉锰反应的离子方程式为 。某次实验时,将原料中的Mn以MnO ·nH O形式定量沉淀完全,
2 2
消耗了2.0 mol KMnO ,并产出81gZnO (纯度为99.9%),则该原料MnZn Fe O 化学式中x = 。
4 x 1-y 2 4
(5)通过加入CaSO 固体,除去滤液中危害环境的SO 2-,已知K (CaSO)= 7.1×10-5,K (CaC O)=
4 4 sp 4 sp 2 4
2.3×10-9。反应CaSO(s)+C O2-(aq) CaC O(s))+SO 2-(aq)的平衡常数为 。
4 2 4 2 4 4
【答案】(3) 3Mn2+(aq) +2MnO-(aq) +(5n+2)H O=5MnO ·nH O(s)+4H+(aq)或不含结晶水形式 0.75
4 2 2 2
(5) 3.1×104
【解析】(3)根据沉锰前后物质可知,沉锰反应的离子反应式为3Mn2+(aq) +2MnO-(aq)
4
+(5n+2)H O=5MnO ·nH O(s)+4H+(aq) (便于后续计算)或不含结晶水;由离子反应式可知,消耗了2.0 mol
2 2 2
KMnO ,则锰锌铁氧体中 , ,由锰锌铁氧体化学式
4
可知, ,化合价代数和为0,则 ,解的 。(5)平衡常
数 。
利用关系式法解题思维流程:
1 .熟记常用计算公式
(1)物质的质量分数(或纯度)=×100%。
(2)反应物的转化率=×100%。(3)生成物的产率=×100%。其中理论产量是根据方程式计算出的数值。
2 .利用“碘量法”进行物质含量测定
(1)直接碘量法:直接碘量法是用碘滴定液直接滴定还原性物质的方法。在滴定过程中,I 被还原为I
2
-。
淀粉:淀粉遇碘显蓝色,反应极为灵敏。化学计量点稍后,溶液中有过量的
指示剂 碘,碘与淀粉结合显蓝色而指示终点到达。碘自身的颜色指示终点,化学计
量点后,溶液中稍过量的碘显黄色而指示终点。
适用对 I 是较弱的氧化剂,强还原性的S2-、SO、SO、As O 、Vc等都可直接滴
2 2 2 3
象 定。
(2)间接碘量法
①剩余碘量法:剩余碘量法是在供试品(还原性物质)溶液中先加入定量、过
量的碘滴定液,待I 与测定组分反应完全后,然后用硫代硫酸钠滴定液滴
2
定剩余的碘,以求出待测组分含量的方法。滴定反应为:
I(定量过量)+还原性物质→2I-+I(剩余)
2 2
I(剩余)+2SO2-→SO2-+2I-
2 2 3 4 6
分类
②置换碘量法:置换碘量法是先在供试品(氧化性物质)溶液中加入碘化钾,
供试品将碘化钾氧化析出定量的碘,碘再用硫代硫酸钠滴定液滴定,从而
可求出待测组分含量。滴定反应为:
氧化性物质+2I-→I
2
I+2SO2-→SO2-+2I-。
2 2 3 4 6
淀粉,淀粉指示剂应在近终点时加入,因为当溶液中有大量碘存在时,碘
指示剂
易吸附在淀粉表面,影响终点的正确判断。
适 用 对 I-是中等强度的还原剂。主要用来测氧化态物质:CrO2-、Cr O2-、HO 、
4 2 7 2 2
象 KMnO 、IO -、Cu2+、NO -、NO -等。
4 3 3 2
3 . K 相关计算
sp
考查角度 思路分析
①根据离子浓度数据求得Q,若Q>K ,则有沉淀生成;
sp
判断沉淀的生成或沉淀
②利用K 的数值计算某一离子浓度,若该离子浓度小于10-5
sp
是否完全
mol·L-1,则该离子沉淀完全
①根据氢氧化物的K 以及开始沉淀时金属阳离子的初始浓度,计
sp
常温下,计算氢氧化物
算溶液中c(OH-),再求得溶液的pH;
沉淀开始和沉淀完全时
②金属阳离子沉淀完全时的离子浓度为10-5 mol·L-1,根据K 可
sp
的pH
计算金属阳离子沉淀完全时溶液中的c(OH-),进而求得pH
计算沉淀转化反应的平
根据沉淀的转化反应和K
sp
,计算该反应的平衡常数,K的值越大,
衡常数,并判断沉淀转 转化反应越易进行,转化程度越大化的程度
①沉淀类型相同,则K 小的化合物先沉淀;
sp
沉淀先后的计算与判断 ②沉淀类型不同,则需要根据K 计算出沉淀时所需离子浓度,所
sp
需离子浓度小的先沉淀
1.(2025·河南省南阳市高三联考,节选)钴及其化合物在制造合金、磁性材料、催化剂及陶瓷釉等方
面有着广泛应用。一种从湿法炼锌产生的废渣(主要含Co、Zn、Pb、Fe的单质或氧化物)中富集回收得到含
锰高钴成品的工艺如图:
已知溶液中相关离子开始沉淀和沉淀完全(c≤1.0×10-5mol·L-1)时的pH:
Zn
Fe3+ Fe2+ Co3+ Co2+
2+
开始沉淀的pH 1.5 6.9 — 7.4 6.2
沉淀完全的pH 2.8 8.4 1.1 9.4 8.2
(4)“除钴液”中主要的盐有 (写化学式),残留的Co3+浓度为 mol·L-1。
(5)CoC O 是制备钴的氧化物的重要原料。如图为二水合草酸钴(CoC O·2H O)在空气中受热的质量变
2 4 2 4 2
化曲线,曲线中300℃及以上所得固体均为钴的氧化物。
通过计算确定C点剩余固体的化学成分为 (填化学式)。写出B点对应的物质与O 在
2
225~300℃发生反应的化学方程式: 。【答案】(4) ZnSO 、KSO 10-16.7
4 2 4
(5) Co O 3CoC O+2O Co O+6CO
3 4 2 4 2 3 4 2
【解析】(4)由流程分析可知,“除钴液”中含有的金属阳离子主要是Zn2+和K+,而阴离子主要是“酸
浸”步骤引入的SO 2-,因此其中主要的盐有ZnSO 和KSO 。当Co3+恰好完全沉淀时,溶液中,
4 4 2 4
c(Co3+)=1.0×10-5mol•L-1,此时溶液pH=1.1,即c(H+ )=10-1.1mol•L-1,则 ,则
,“除钴液”的pH=5,即c(H+)=10-5mol•L-1,则
,此时溶液中 。(5)由图
可知,CoC O·2H O的质量为18.3g,其物质的量为0.1mol,Co元素质量为5.9g,C点钴氧化物质量为
2 4 2
8.03g,氧化物中氧元素质量为8.03g-5.9g=2.13g,则氧化物中Co原子与O原子物质的量之比为0.1mol:
=3:4,故C点剩余固体的化学成分为Co O;B点对应物质的质量为14.7g,与其起始物质的质量
3 4
相比减少18.3g-14.7g=3.6g,为结晶水的质量,故B点物质为CoC O,与氧气反应生成Co O 与二氧化碳,
2 4 3 4
反应方程式为:3CoC O+2O Co O+6CO 。
2 4 2 3 4 2
2.黏土钒矿中,钒以+3价、+4价、+5价的化合物存在,还包括SiO、Fe O 和铝硅酸盐(Al O·SiO)
2 2 3 2 3 2
等。采用以下流程可由黏土钒矿制备VO、Fe O 和硫酸铝铵。
2 5 2 3
已知:ⅰ.有机酸性萃取剂HR的萃取原理为: ;org表
示有机溶液。
ⅱ.酸性溶液中,HR对 价钒萃取能力强,而对 价钒的萃取能力较弱。
ⅲ.HR能萃取Fe3+而不能萃取Fe2+。
(6)测定VO 产品的纯度。称取VO 产品ag,先加入硫酸将VO 转化为VO +,加入指示剂后,用
2 5 2 5 2 5 2cmol/L (NH )Fe(SO ) 溶液滴定将VO +转化为VO2+至终点,消耗(NH )Fe(SO ) 溶液的体积为VmL。假设
4 2 4 2 2 4 2 4 2
杂质不参与反应,则VO 产品中VO 的质量分数是 (V O 的摩尔质量为Mg/mol)。
2 5 2 5 2 5
【答案】(6)
【解析】黏土钒矿中,钒以+3价、+4价、+5价的化合物存在,还包括SiO、Fe O 和铝硅酸盐
2 2 3
(Al O·SiO)等,加入浓硫酸且通入空气,SiO 不反应成为滤渣;浸出液中加入氨水调节pH,生成硫酸铝
2 3 2 2
铵沉淀;滤液中加入铁粉将Fe3+转化为Fe2+,并将五价钒还原为四价钒;使用HR萃取钒到有机层,有机层
加入硫酸、氯酸钾可将四价钒转化为五价钒,加入氨水得到NH VO ,煅烧得到VO;水层加入氨水、通
4 3 2 5
入空气得到氢氧化铁,煅烧可得到氧化铁。(6)加入硫酸将VO 转化为VO +,加入指示剂后,再用
2 5 2
(NH )Fe(SO ) 溶液滴定将VO +转化为VO2+,则根据得失电子守恒和原子守恒可得:VO~2VO+~2Fe3+,
4 2 4 2 2 2 5 2
则 ,质量分数为 。
3.红矾钠( )可用于制备制革产业中的铬鞣剂。对含铬污泥进行酸浸处理后,得到浸出
液(主要含 ),经过如下主要流程,可制得红矾钠,实现铬资源的有效
循环利用。
已知:i.Cr(VI)在溶液中存在以下平衡:
ⅱ。溶液1条件下,相关金属离子形成氢氧化物沉淀的 范围:
金属离子 开始沉淀的 沉淀完全的
4.3 5.6
7.1 9.2
(6)为了测定红矾钠的纯度,称取上述流程的产品ag配成 溶液,取出 于锥形瓶中,加入稀
硫酸和足量的KI溶液,置于暗处充分反应至全部 转化为 后,滴入2~3滴淀粉溶液,最后用浓度
为 的 标准溶液滴定,共消耗 。
已知:
①滴定终点的现象为 。
②该产品中,红矾钠(摩尔质量为 )的质量分数为 (列出计算式)。
【答案】
(6)溶液蓝色褪去,且30s不变色
【解析】浸出液(主要含 ),根据流程图,先加入NaHSO、
3NaOH, 与NaHSO 发生氧化还原反应后得到 与氢氧化钠反应Cr(OH) ,Cr(OH) ,Cr(OH) 与
3 3 3 3
NaOH和HO 反应生成NaCrO,NaCrO 酸化后生成NaCr O 溶液,加热蒸发结晶,趁热过滤后冷却结晶
2 2 2 4 2 4 2 2 7
得到红矾钠 ( ),据此回答。
(6)①本实验指示剂为淀粉溶液,I 遇到淀粉溶液显蓝色,故滴定终点的现象为滴入最后半滴NaSO
2 2 2 3
标准溶液后,溶液由蓝色变为无色,且半分钟内不恢复蓝色;
②根据得失电子总数相等可知, ,故有
,所得红矾钠
(摩尔质量为 )的质量分数为 。
4.镍的氧化物M是蓄电池材料。某小组用含镍废料(成分为NiO、Ni O 、FeO、MgO和SiO 等)制备
2 3 2
M的工艺流程如图所示。
回答下列问题:
(3)已知25℃时: , 。若浸出液中 ,当离
子浓度≤1×10-5mol·L-1时认为已完全沉淀。用NaCO 调节pH范围为 。
2 3
【答案】(3)3.2 ≤ pH<6.65
【解析】(3)根据溶度积数据计算,沉淀完全时, , ,则可
推得, ,pH=3.2;同理可知,Ni(OH) 开始沉淀时, ,pH=6.65,故应控
2
制溶液的pH为:3.2≤pH<6.65。
5.以锌浸出渣(主要成分为PbSO ,还含有PbO和ZnFe O)为原料制备金属Pb,其工艺流程如下:
4 2 4
已知:①“碱浸”时,ZnFe O 与NaOH反应生成NaZnO 和HO,还有一种氧化物;
2 4 2 2 2
②“碱浸”后,铅主要以[Pb(OH) ]-的形式存在溶液中。
3
“碱浸”液经处理后所得溶液[ 、 ]用于“沉铅”。(1)“沉铅”时,理论上,当PbS完全沉淀时 ,ZnS_________(是或否)开始沉淀,通
过计算说明_________[已知: 、 ]。
(2)“滤液”中主要含有的金属阳离子有_________。
【答案】(1)是 (2)当PbS完全沉淀时,S2-的浓度为 ,
> ,所以ZnS开始沉淀 Na+、Zn2+
【解析】“沉铅”时,当PbS完全沉淀时 ,S2-的浓度为 ,
> ,所以存在ZnS沉淀;②“滤液”中主要含有的金属
阳离子有Na+、Zn2+。
6.FeFe O 复合物是一种高密度磁记录材料,磁记录材料有记录和存储信息的功能。制备该材料的一
/ 3 4
种流程如下:
已知:I.①3Fe(OH) =Fe+2Fe(OH) ;②Fe(OH) +2Fe(OH) =Fe O+4H O。
2 3 2 3 3 4 2
II. 时, 。
(1)用 溶液和KOH溶液制备FeFe O 反应的化学方程式为: 。该“反应”中通入氩气的
/ 3 4
原因 。
(2)取少量反应后溶液于试管中,可证明FeCl 溶液已反应完全的试剂和现象是 。在隔绝空气条
2
件下,向浓度均为 的FeCl 和FeCl 混合溶液中滴加稀NaOH溶液,当开始出现第二种沉淀时,
2 3
溶液中比值c(Fe2+):c(Fe3+)= 。
【答案】(1) 4FeCl+8KOH Fe↓+Fe O↓+8KCl+4H O 防止亚铁离子被空气中的氧气氧化
2 3 4 2
(2)铁氰化钾溶液 不产生蓝色沉淀 5×1017:6
【解析】氯化亚铁溶液和氢氧化钾溶液在“反应”中发生反应Fe2++2OH-=Fe(OH) ↓、3Fe(OH) =
2 2
Fe+2Fe(OH) 、Fe(OH) +2Fe(OH) =Fe O+4H O,经过过滤、洗涤、干燥得到FeFe O 复合物。(1)用氯化亚
3 2 3 3 4 2 / 3 4
铁溶液和氢氧化钾溶液反应制备FeFe O,根据原子守恒和电荷守恒可知其方程式为4FeCl+8KOH Fe↓
/ 3 4 2
+Fe O↓+8KCl+4H O;亚铁离子具有较强的还原性,可以被氧气氧化,在反应中通入氩气可以防止亚铁离
3 4 2子和氧气反应;(2)检验FeCl 溶液已反应完就是检验溶液中没有二价铁离子,选择的试剂为铁氰化钾溶液,
2
现象为不出现蓝色沉淀;当开始出现第二种沉淀时,即氢氧化亚铁开始沉淀,当氢氧化亚铁开始沉淀时,
溶液中氢氧根离子的浓度为 ,此时溶液
中Fe3+的浓度为 ,则溶液中比值
。