文档内容
表格型实验方案的评价
(选择题1~10题,每小题5分,共50分)
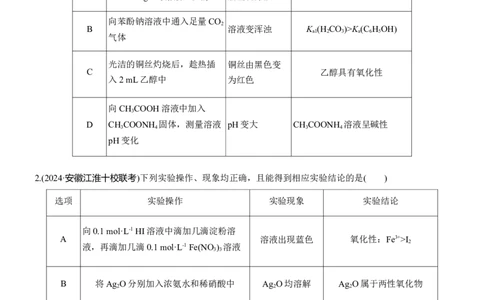
1.(2024·合肥高三检测)下列由实验操作及现象所得的结论正确的是( )
选项 实验操作 现象 结论
向0.5 mL溴乙烷中加入约2 溶液分层,上 溴乙烷是电解质,能电离出
A
mL 2% AgNO 溶液,振荡 层出现浑浊 Br-
3
向苯酚钠溶液中通入足量CO
2
B 溶液变浑浊 K (H CO )>K(C H OH)
a1 2 3 a 6 5
气体
光洁的铜丝灼烧后,趁热插 铜丝由黑色变
C 乙醇具有氧化性
入2 mL乙醇中 为红色
向CH COOH溶液中加入
3
D CH COONH 固体,测量溶液 pH变大 CH COONH 溶液呈碱性
3 4 3 4
pH变化
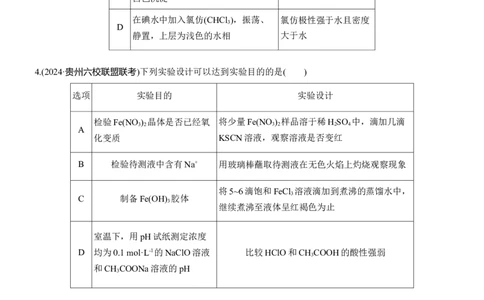
2.(2024·安徽江淮十校联考)下列实验操作、现象均正确,且能得到相应实验结论的是( )
选项 实验操作 实验现象 实验结论
向0.1 mol·L-1 HI溶液中滴加几滴淀粉溶
A 溶液出现蓝色 氧化性:Fe3+>I
2
液,再滴加几滴0.1 mol·L-1 Fe(NO ) 溶液
3 3
B 将Ag O分别加入浓氨水和稀硝酸中 Ag O均溶解 Ag O属于两性氧化物
2 2 2
向蔗糖溶液中加入稀硫酸并加热一段时
C 无银镜产生 蔗糖未水解
间,然后滴加银氨溶液
向浓度均为0.1 mol·L-1的MgSO 和CuSO
4 4
先观察到有蓝色
D 的混合溶液中逐滴加入0.01 mol·L-1的 K [Cu(OH) ]K [Cu(OH) ]
4 sp 2 sp 2
蓝色沉淀
向Na S O 溶液中滴加稀硫酸,产生浅黄色沉淀
2 2 3
D 稀硫酸仅表现酸性
和刺激性气味的气体
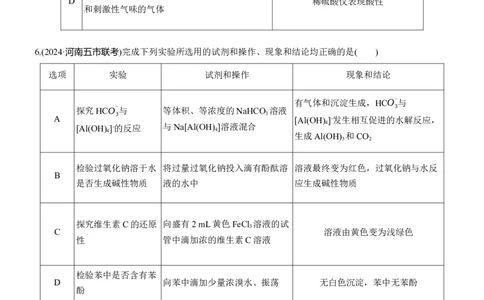
6.(2024·河南五市联考)完成下列实验所选用的试剂和操作、现象和结论均正确的是( )
选项 实验 试剂和操作 现象和结论
有气体和沉淀生成,HCO-
与
探究HCO-
与 等体积、等浓度的NaHCO 溶液
3
3 3
A [Al(OH) ]-发生相互促进的水解反应,
[Al(OH) 4 ]-的反应 与Na[Al(OH) 4 ]溶液混合 4
生成Al(OH) 和CO
3 2
检验过氧化钠溶于水 将过量过氧化钠投入滴有酚酞溶 溶液最终变为红色,过氧化钠与水反
B
是否生成碱性物质 液的水中 应生成碱性物质
探究维生素C的还原 向盛有2 mL黄色FeCl 溶液的试
3
C 溶液由黄色变为浅绿色
性 管中滴加浓的维生素C溶液
检验苯中是否含有苯
D 向苯中滴加少量浓溴水、振荡 无白色沉淀,苯中无苯酚
酚
7.下列实验中,依据实验操作及现象得出的结论正确的是( )
选项 操作 现象 结论
常温下,向盛有硅酸钠溶液的试管中滴加 试管中溶液的红色褪
A 非金属性:Cl>Si
1滴酚酞,然后逐滴加入稀盐酸 去,试管里出现凝胶
B 常温下,向[Ag(NH ) ]OH溶液中加入稀 有白色沉淀产生 Cl-与Ag+结合的能
3 2力强于NH 分子与
3
盐酸
Ag+的配位能力
C 向CaCO 固体中加入稀硫酸 固体不溶解 CaCO 不能溶于酸
3 3
反应中生成的碘单
常温下,向含碘食盐中加入KI⁃ 淀粉溶液
D 溶液由无色变为蓝色 质既是氧化产物,
和醋酸溶液
又是还原产物
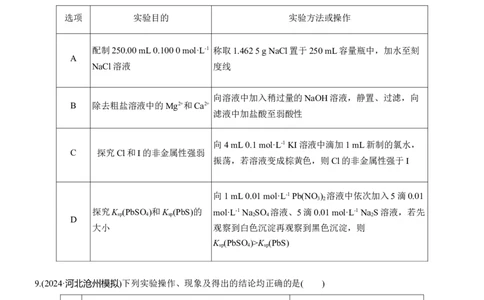
8.(2024·广西1月适应性测试)为达到实验目的,下列对应的实验方法正确或操作规范的是( )
选项 实验目的 实验方法或操作
配制250.00 mL 0.100 0 mol·L-1 称取1.462 5 g NaCl置于250 mL容量瓶中,加水至刻
A
NaCl溶液 度线
向溶液中加入稍过量的NaOH溶液,静置、过滤,向
B 除去粗盐溶液中的Mg2+和Ca2+
滤液中加盐酸至弱酸性
向4 mL 0.1 mol·L-1 KI溶液中滴加1 mL新制的氯水,
C 探究Cl和I的非金属性强弱
振荡,若溶液变成棕黄色,则Cl的非金属性强于I
向1 mL 0.01 mol·L-1 Pb(NO ) 溶液中依次加入5滴0.01
3 2
探究K (PbSO )和K (PbS)的 mol·L-1 Na SO 溶液、5滴0.01 mol·L-1 Na S溶液,若先
sp 4 sp 2 4 2
D
大小 观察到白色沉淀再观察到黑色沉淀,则
K (PbSO )>K (PbS)
sp 4 sp
9.(2024·河北沧州模拟)下列实验操作、现象及得出的结论均正确的是( )
选项 实验操作、现象 实验结论
0.1 mol·L-1的NaHCO 溶液与0.1 mol·L-1的
A 3 结合H+能力:[Al(OH) ]->CO2-
4 3
Na[Al(OH) ]溶液等体积混合,产生白色沉淀
4
将补铁口服液(含维生素C)滴入酸性KMnO 溶液,
4
B 补铁口服液中含有Fe2+
紫红色褪去
C 将久置的Na O 加入稀盐酸中,产生气泡 Na O 已经变质
2 2 2 2取两份新制氯水,分别滴加AgNO
3
溶液和淀粉 ⁃KI溶
D 氯气与水的反应存在限度
液,前者有白色沉淀,后者溶液变蓝
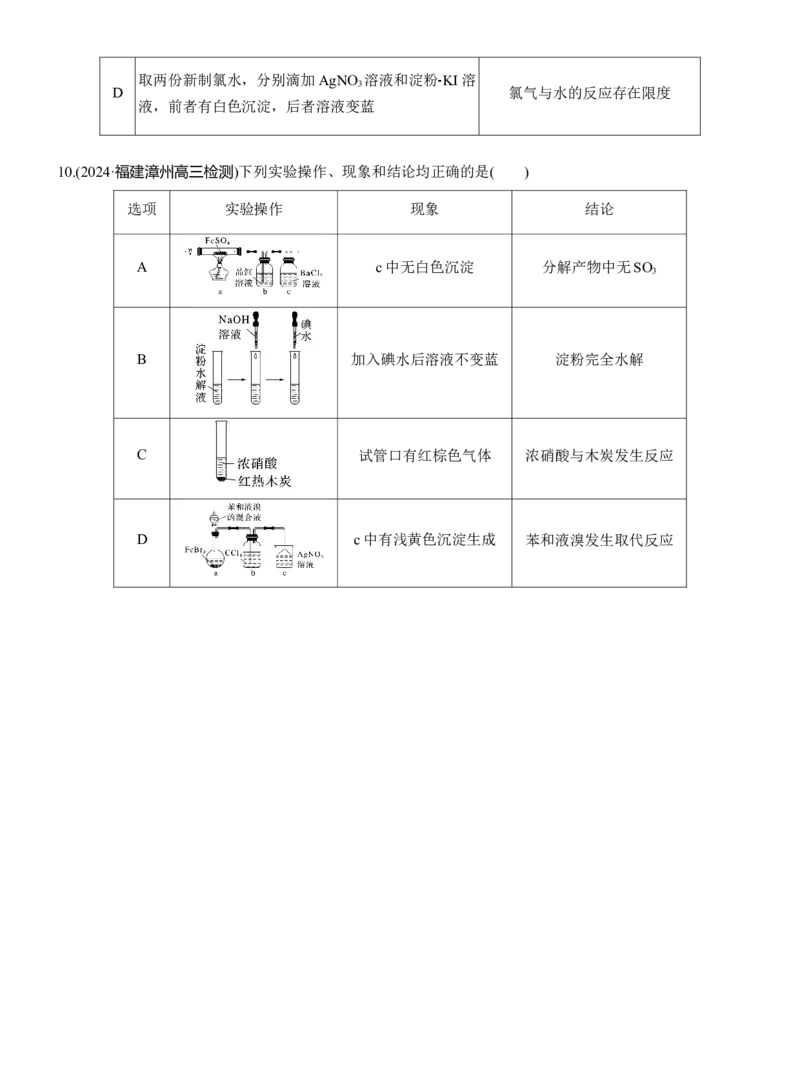
10.(2024·福建漳州高三检测)下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
A c中无白色沉淀 分解产物中无SO
3
B 加入碘水后溶液不变蓝 淀粉完全水解
C 试管口有红棕色气体 浓硝酸与木炭发生反应
D c中有浅黄色沉淀生成 苯和液溴发生取代反应答案精析
1.B [溴乙烷不能电离出Br-,与硝酸银溶液不反应,溶液分层,上层为无色溶液,A错误;铜与氧气反应
生成氧化铜,氧化铜可氧化乙醇生成乙醛,则乙醇具有还原性,C错误;CH COONH 溶液为中性,
3 4
CH COONH 固体溶于水电离出的醋酸根离子可抑制醋酸的电离,溶液的pH变大,D错误。]
3 4
2.D [硝酸根离子与氢离子也可以氧化碘离子,A错误;Ag O溶于氨水形成配合物,因此Ag O不属于两
2 2
性氧化物,B错误;滴加银氨溶液之前应先将溶液调至碱性,C错误;同类型物质K 小的先生成沉淀,因
sp
此K [Cu(OH) ]硅酸,但盐酸不是氯
元素最高价氧化物的水化物,不能判断非金属性的强弱,故A错误;[Ag(NH ) ]OH溶液中加入盐酸产生
3 2
AgCl沉淀,离子方程式:[Ag(NH ) ]++OH-+3H++Cl-===AgCl↓+2N H+ +H O,滴加盐酸过程中只要
3 2 4 2
Q>K (AgCl)即可产生沉淀,而氯化银沉淀的产生会促使配离子进一步解离,故不能说明Cl-与Ag+结合的能
sp
力强于NH 分子与Ag+的配位能力,故B错误;碳酸钙和稀硫酸反应生成的硫酸钙是微溶物,附着在
3
CaCO 表面,阻止稀硫酸与碳酸钙进一步反应,故C错误;含碘食盐含KIO ,在酸性溶液中KI与KIO 发
3 3 3
生归中反应生成I ,碘单质既是氧化产物,又是还原产物,故D正确。]
2
8.C [配制250.00 mL 0.100 0 mol·L-1NaCl溶液时,称取的氯化钠固体应先在烧杯中溶解,再转移至容量瓶
中定容,A错误;向溶液中加入稍过量的NaOH溶液,除去粗盐溶液中的Mg2+,还需向溶液中加入
Na CO 溶液除去Ca2+,过滤后再向滤液中加入适量盐酸除去过量的NaOH和Na CO ,B错误;向1 mL
2 3 2 3
0.01 mol·L-1 Pb(NO ) 溶液中依次加入5滴0.01 mol·L-1 Na SO 溶液、5滴0.01 mol·L-1Na S溶液,Pb(NO )
3 2 2 4 2 3 2
过量,若先观察到白色沉淀PbSO ,再观察到黑色沉淀PbS,则不能确定发生了沉淀转化,无法得到
4
K (PbSO )>K (PbS),D错误。]
sp 4 sp9.A [等物质的量浓度、等体积的NaHCO 溶液与Na[Al(OH) ]溶液混合,产生白色沉淀,发生反应:
3 4
[Al(OH) ]-+HCO- ===Al(OH) ↓+CO2- +H O,说明结合H+能力:[Al(OH) ]->CO2- ,A正确;维生素C也
4 3 3 3 2 4 3
能使酸性KMnO 溶液褪色,B错误;盐酸可与Na O 反应,反应的化学方程式为
4 2 2
2Na O +4HCl===4NaCl+2H O+O ↑,C错误;新制氯水中的Cl 和HClO都能与KI反应生成使淀粉变蓝色
2 2 2 2 2
的碘,则溶液变蓝色不能说明溶液中存在氯气分子,无法证明氯气与水的反应存在限度,D错误。]
10.D [三氧化硫可与水反应生成硫酸,因此SO 在装置b中可被吸收,即使生成了三氧化硫,也不会进入
3
装置c生成白色沉淀,所以无法证明分解产物中是否含有三氧化硫,故A错误;碘水中的I 可与NaOH反
2
应,所以加入碘水后溶液不变蓝不能说明淀粉完全水解,故B错误;试管口红棕色的二氧化氮气体可能是
浓硝酸在加热条件下与木炭反应生成的,也可能是浓硝酸受热分解生成的,故C错误;装置b中四氯化碳
可除去挥发出来的Br ,所以c中出现的浅黄色沉淀是苯和液溴发生取代反应生成的HBr和硝酸银反应生
2
成的,即可证明苯和液溴发生了取代反应,故D正确。]