文档内容
专题三 能力提升检测卷
一、选择题(本题共12小题,每小题5分,共60分)
1.下列生活用品中主要由黑色金属材料制造的是( )
A.塑钢门窗 B.不锈钢刀
C.纯铜导线 D.18K金首饰
2.《本草图经》描述:“绿矾形似朴消(Na SO ·10H O)而绿色,取此物置于铁板上,聚炭,封之囊袋,吹
2 4 2
令火炽,其矾即沸,流出,色赤如融金汁者是真也。”下述说明中正确的是( )
①绿矾又称胆矾,化学式为CuSO ·5H O
4 2
②绿矾的分解过程中发生了氧化还原反应
③“色赤”物质可能是铜单质
④流出的液体中可能含有硫酸
A.①③ B.②④
C.②③ D.①④
3.露置于空气不易因氧化而变质的是
A.NaOH B.NaSO C.KI D.FeCl
2 3 2
4.已知甲是一种金属单质,乙是淡黄色的固体,其转化关系如图所示,下列说法不正确的是
A.甲能与水发生剧烈的反应,熔成小球,生成氢气
B.乙可用作潜水艇中的氧气的来源
C.丙的焰色反应的火焰呈淡紫色(透过蓝色钴玻璃)
D.丁固体暴露在空气中易潮解
5.某同学利用如图所示装置探究 Na与CO 反应的还原产物,已知PdCl +CO+HO===Pd(黑色)↓+CO +
2 2 2 2
2HCl,下列相关分析错误的是( )
A.装置Ⅰ中发生的反应可以是NaCO+HSO ===Na SO +HO+CO↑
2 3 2 4 2 4 2 2B.装置Ⅱ中浓硫酸的作用是干燥CO
2
C.实验时,装置Ⅲ中石英玻璃管容易受到腐蚀
D.装置Ⅳ的目的是证明还原产物中是否有CO
6.化合物X在一定条件下可发生如图转化,有关叙述错误的是
A.溶液C到溶液D中发生的离子方程式为:Fe3++3SCN— Fe(SCN)
3
B.E为CO,物质的量为0.05mol
C.X为Fe(CO)
4
D.过量的稀硫酸若换成盐酸,会造成环境污染
7.为测定碳酸钠的质量分数(设含杂质碳酸氢钠),某学生设计了如下实验方案,下列对实验方案的叙述正
确的是( )
A.称量所需要的仪器是托盘天平
B.样品放在蒸发皿中灼烧
C.样品中碳酸钠的质量分数为76%
D.如果灼烧后的样品放在空气中冷却,会造成实验结果偏大
8.下列实验过程中产生的现象与对应的图像不相符的是( )9.下列实验操作正确的是
实验 操作
用镊子从煤油中取出钠,切下豆绿大小的钠,放入装满水
A 观察钠与水反应的现象
的烧杯中
B 检验NaHCO 与NaCO 溶液 用小试管分别取少量溶液,然后滴加澄清石灰水
3 2 3
棉花包裹的NaO 放入充满CO 的集气瓶中,棉花燃烧说明
C 证明NaO 与CO 反应是放热反应 2 2 2
2 2 2 是放热反应
用铂丝分别蘸取溶液,在酒精灯外焰上灼烧,直接观察火
D 检验NaCO 与KCO 溶液
2 3 2 3 焰的颜色
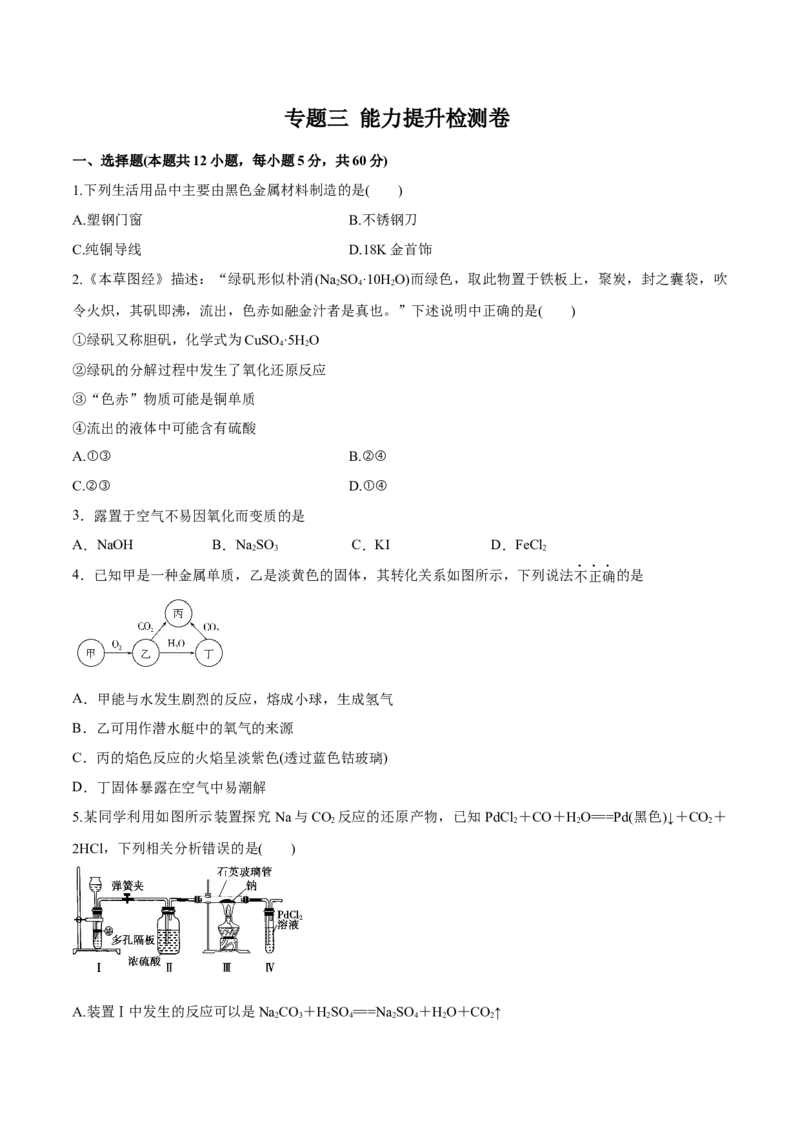
10.以CO 和NaO 为原料制取纯净干燥的O 实验装置如图:
2 2 2 2
下列说法不正确的是
A.装置②中试剂可以是NaOH溶液
B.装置③的作用是干燥O
2
C.收集氧气应选择装置a
D.装置②、③之间应增加盛澄清石灰水的洗气瓶
11.为测定某NaO 试样(含少量NaO)中NaO 的质量分数,设计如下实验:
2 2 2 2 2下列分析错误的是
A.操作Ⅰ和Ⅱ都需要玻璃棒 B.需称量样品和NaCl的质量
C.操作Ⅱ若损失部分固体,测定结果偏大 D.若溶液转移不完全,测定结果偏小
12.某稀溶液中含有Fe(NO ) 、Cu(NO ) 、HNO ,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的
3 3 3 2 3
物质的量之间的关系如图所示。则稀溶液中Fe(NO )、Cu(NO )、HNO 物质的量浓度之比为( )
3 3 3 2 3
A.1∶1∶1 B.1∶3∶1
C.3∶3∶8 D.1∶1∶4
二、非选择题(本题共2小题,每小题10分,共20分)
13.(10分)NaO 是种淡黄色固体,可作为深潜等工作时的供氧剂。
2 2
(1)Na O 的电子式为___________
2 2
(2)某化学课外活动小组为探究此反应的产物,设计了如下表所示的实验,请协助该组同学对部分现象进行
记录,并对相关现象作出合理的解释(结论)。
试验编号 实验操作 实验现象 结论
取少许NaO 置于一试管中,往此试 NaO 表面_____(填现 据此,NaO 与水反应
2 2 2 2 2 2
1 管中加过量的水;将带火星的木条伸 象,下同);带火星的 生成了____(填分子
入试管中。 木条_____。 式)。
实验1的试管中无明显现象后,用胶 无色透明溶液______。 据实验1、2,NaO 与
2 2
2 头滴管向所得无色透明溶液中滴加几 随后,溶液又恢复成无 水反应的反应式为
滴酚酞试液。 色透明溶液。 ____。
用药匙向实验2最后所得的无色透明 加入少量MnO 粉末时
2
3 溶液中加入少量MnO 粉末;又将带 现象是____。 反应的化学方程式为
2
火星的木条伸入试管中。 ____。
(3)取实验1所得溶液少许于试管中,加稀硫酸酸化后,再滴加高锰酸钾溶液,高锰酸钾溶液褪色并有气泡
冒出,所发生反应的离子反应方程式是___________。根据题目信息,有的物质___________(填“可以”或
“不可以”)既具有氧化性,又具有还原性。
14.(10分)工业上以碳酸锰矿(主要成分为MnCO ,另含FeO、Fe O、CaO等杂质)为主要原料生产锰酸
3 2 3锂(LiMn O)的工艺流程如下:
2 4
(1)为了提高碳酸锰矿浸出的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③____等。
(2)“除铁”时,加入CaO的目的是_______。
(3)“合成MnO ”的化学方程式为_______。
2
(4)“锂化”是将MnO 和LiCO 按4∶1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温
2 2 3
24h,自然冷却至室温得产品。
①升温到515℃时,开始有CO 产生,比预计碳酸锂的分解温度(723℃)低得多。可能的原因是_______。
2
②写出该反应的化学方程式:_______。
15.(10分)实验室以绿矾(FeSO ·7H O)制备补血剂甘氨酸亚铁[(NH CHCOO) Fe],有关物质性质如下
4 2 2 2 2
表:
甘氨酸(NH CHCOOH) 柠檬酸 甘氨酸亚铁
2 2
易溶于水和乙醇,有强酸性和还原
易溶于水,微溶于乙醇,两性化合物 易溶于水,难溶于乙醇
性
实验过程:
Ⅰ.配制含0.10mol FeSO 的绿矾溶液。
4
Ⅱ.制备FeCO:将配制好的绿矾溶液与200mL 1.1mol·L-1NH HCO 溶液混合,反应结束后过滤并洗涤沉
3 4 3
淀。
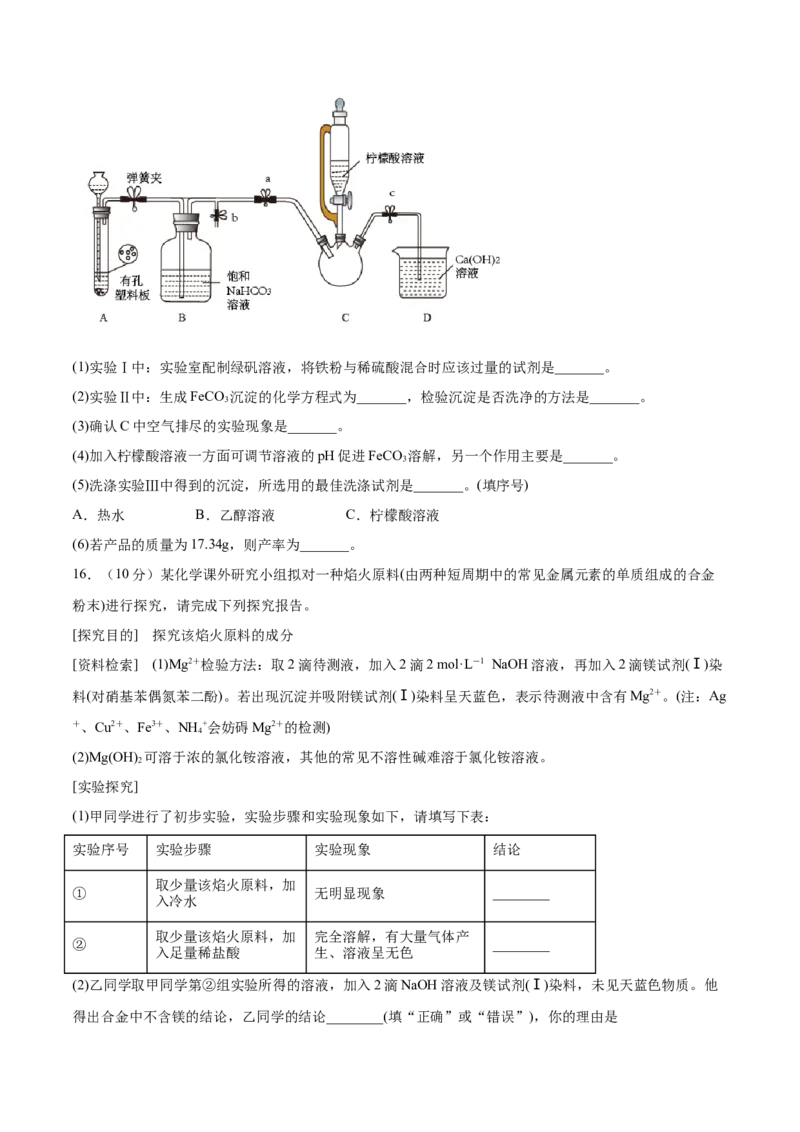
Ⅲ.制备(NH CHCOO) Fe:实验装置如图(夹持和加热仪器已省略),将实验Ⅱ得到的沉淀和含0.20 mol甘氨
2 2 2
酸的水溶液混合后加入C中,然后利用A中的反应将C中空气排净,接着滴入柠檬酸溶液并加热。反应结
束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。回答下列问题:(1)实验Ⅰ中:实验室配制绿矾溶液,将铁粉与稀硫酸混合时应该过量的试剂是_______。
(2)实验Ⅱ中:生成FeCO 沉淀的化学方程式为_______,检验沉淀是否洗净的方法是_______。
3
(3)确认C中空气排尽的实验现象是_______。
(4)加入柠檬酸溶液一方面可调节溶液的pH促进FeCO 溶解,另一个作用主要是_______。
3
(5)洗涤实验Ⅲ中得到的沉淀,所选用的最佳洗涤试剂是_______。(填序号)
A.热水 B.乙醇溶液 C.柠檬酸溶液
(6)若产品的质量为17.34g,则产率为_______。
16.(10分)某化学课外研究小组拟对一种焰火原料(由两种短周期中的常见金属元素的单质组成的合金
粉末)进行探究,请完成下列探究报告。
[探究目的] 探究该焰火原料的成分
[资料检索] (1)Mg2+检验方法:取2滴待测液,加入2滴2 mol·L-1 NaOH溶液,再加入2滴镁试剂(Ⅰ)染
料(对硝基苯偶氮苯二酚)。若出现沉淀并吸附镁试剂(Ⅰ)染料呈天蓝色,表示待测液中含有Mg2+。(注:Ag
+、Cu2+、Fe3+、NH +会妨碍Mg2+的检测)
4
(2)Mg(OH) 可溶于浓的氯化铵溶液,其他的常见不溶性碱难溶于氯化铵溶液。
2
[实验探究]
(1)甲同学进行了初步实验,实验步骤和实验现象如下,请填写下表:
实验序号 实验步骤 实验现象 结论
取少量该焰火原料,加
① 无明显现象 ________
入冷水
取少量该焰火原料,加 完全溶解,有大量气体产
② ________
入足量稀盐酸 生、溶液呈无色
(2)乙同学取甲同学第②组实验所得的溶液,加入2滴NaOH溶液及镁试剂(Ⅰ)染料,未见天蓝色物质。他
得出合金中不含镁的结论,乙同学的结论________(填“正确”或“错误”),你的理由是_______________________________________________________。
(3)丙同学设计实验方案,确定焰火原料中的金属种类,实验记录如下:
由丙同学的实验记录可知该焰火原料是由________和________两种金属组成的合金;实验中滤液加入足量
氢氧化钠溶液后需煮沸的理由是_______________________________。