文档内容
溶液中的离子浓度关系与滴定曲线分析
(一)溶液中的离子浓度关系
1.解题模型——分清主次,抓主要矛盾
例1 单一溶液
(1)0.1 mol·L-1 H S溶液中离子浓度大小关系: 。
2
(2)NaHS溶液中离子浓度大小关系: 。
例2 物质的量浓度1∶1的缓冲溶液
等浓度的NaOH和CH COOH按1∶2体积比混合后pH<7,离子浓度大小顺序为 。
3
解题策略 溶液中物质间若能发生化学反应,则优先考虑化学反应。
2.溶液中部分粒子浓度之和(差)的大小比较
解题模型
(1)先确定溶液中粒子的构成。
(2)从守恒出发,根据溶液中存在的元素守恒或电荷守恒进行分析比较。
(3)三大守恒式的书写
①电荷守恒
电解质溶液中,无论存在多少种离子,溶液都呈电中性,故存在电荷守恒,即阳离子所带正电荷总数=
阴离子所带负电荷总数。
如Na S与NaHS的混合溶液中存在电荷守恒: 。
2
②元素守恒
电解质溶液中,由于某些离子能够水解,离子种类增多,但元素总是守恒的,即元素守恒的特征:元
素写两边、系数交叉配。
如0.1 mol·L-1 Na CO 溶液中存在的元素守恒关系: 。
2 3
物质的量浓度1∶1的HA、 NaA的混合溶液中存在元素守恒: 。
③质子守恒
酸碱质子理论认为,酸碱反应实质是质子(H+)的转移。失质子总数=游离质子数+得质子总数。
如写出Na CO 的质子守恒: 。
2 3(二)滴定图像分析应用
类型一 中和滴定反应“突跃”曲线的分析应用
1.强碱滴定强酸
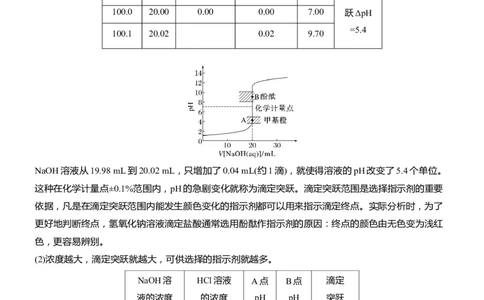
(1)0.10 mol·L-1 NaOH标准液滴定20 mL 0.10 mol·L-1 HCl溶液(如图)
加入NaOH溶液
剩余HCl溶液 过量NaOH溶
pH
体积/mL 液体积/mL
滴定/% V/mL
99.9 19.98 0.02 4.30
滴定突
100.0 20.00 0.00 0.00 7.00 跃ΔpH
=5.4
100.1 20.02 0.02 9.70
NaOH溶液从19.98 mL到20.02 mL,只增加了0.04 mL(约1滴),就使得溶液的pH改变了5.4个单位。
这种在化学计量点±0.1%范围内,pH的急剧变化就称为滴定突跃。滴定突跃范围是选择指示剂的重要
依据,凡是在滴定突跃范围内能发生颜色变化的指示剂都可以用来指示滴定终点。实际分析时,为了
更好地判断终点,氢氧化钠溶液滴定盐酸通常选用酚酞作指示剂的原因:终点的颜色由无色变为浅红
色,更容易辨别。
(2)浓度越大,滴定突跃就越大,可供选择的指示剂就越多。
NaOH溶 HCl溶液 A点 B点 滴定
液的浓度 的浓度 pH pH 突跃
1.00 mol·L-1 1.00 mol·L-1 3.30 10.70 ΔpH=7.4
0.10 mol·L-1 0.10 mol·L-1 4.30 9.70 ΔpH=5.4
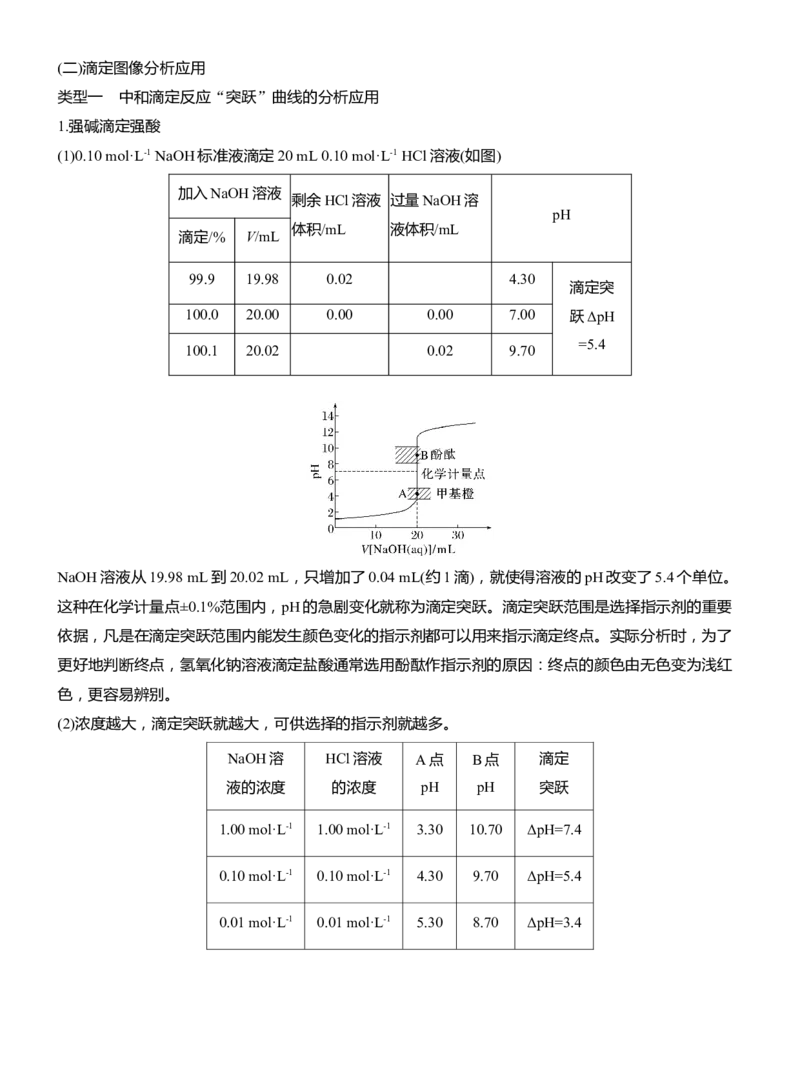
0.01 mol·L-1 0.01 mol·L-1 5.30 8.70 ΔpH=3.42.强碱滴定弱酸曲线
由图可知:酸性越弱,K 越小,滴定突跃范围就越小。
a
3.巧抓“四点”,突破溶液中的粒子浓度关系
(1)抓反应“一半”点,判断是什么溶质的等量混合。
(2)抓“恰好”反应点,生成的溶质是什么?判断溶液的酸碱性。
(3)抓溶液的“中性”点,生成什么溶质,哪种物质过量或不足。
(4)抓反应的“过量”点,溶液中的溶质是什么?判断哪种物质过量。
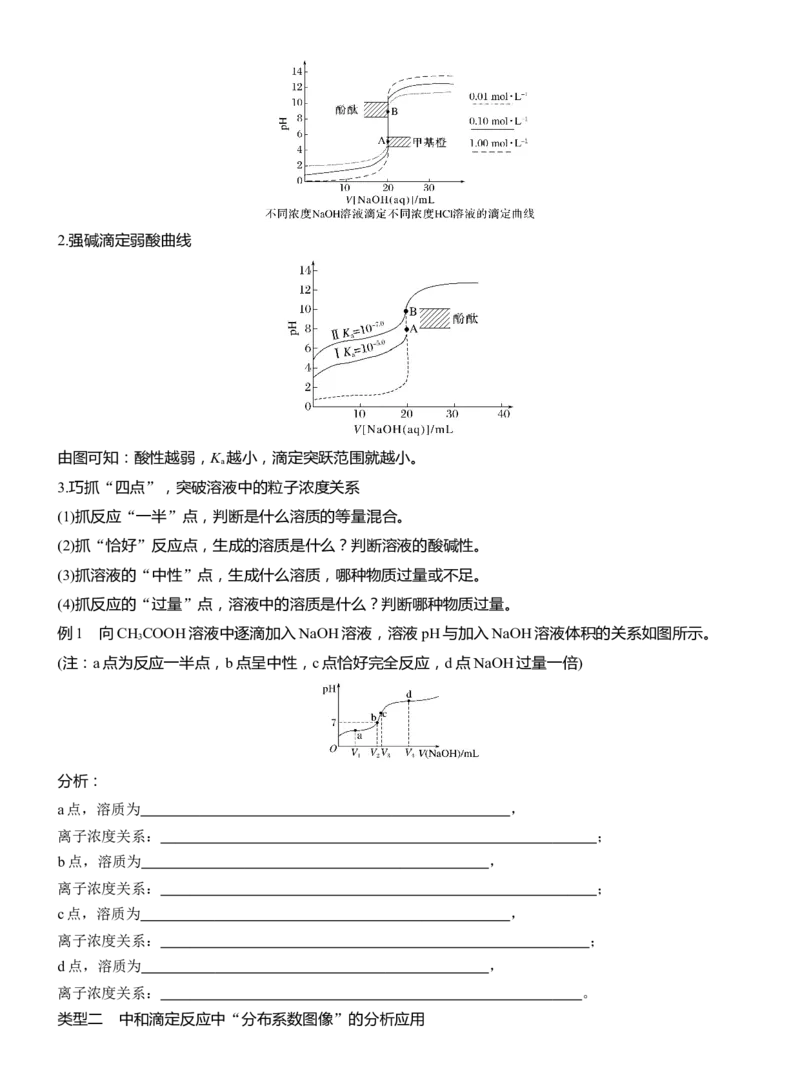
例1 向CH COOH溶液中逐滴加入NaOH溶液,溶液pH与加入NaOH溶液体积的关系如图所示。
3
(注:a点为反应一半点,b点呈中性,c点恰好完全反应,d点NaOH过量一倍)
分析:
a点,溶质为 ,
离子浓度关系: ;
b点,溶质为 ,
离子浓度关系: ;
c点,溶质为 ,
离子浓度关系: ;
d点,溶质为 ,
离子浓度关系: 。
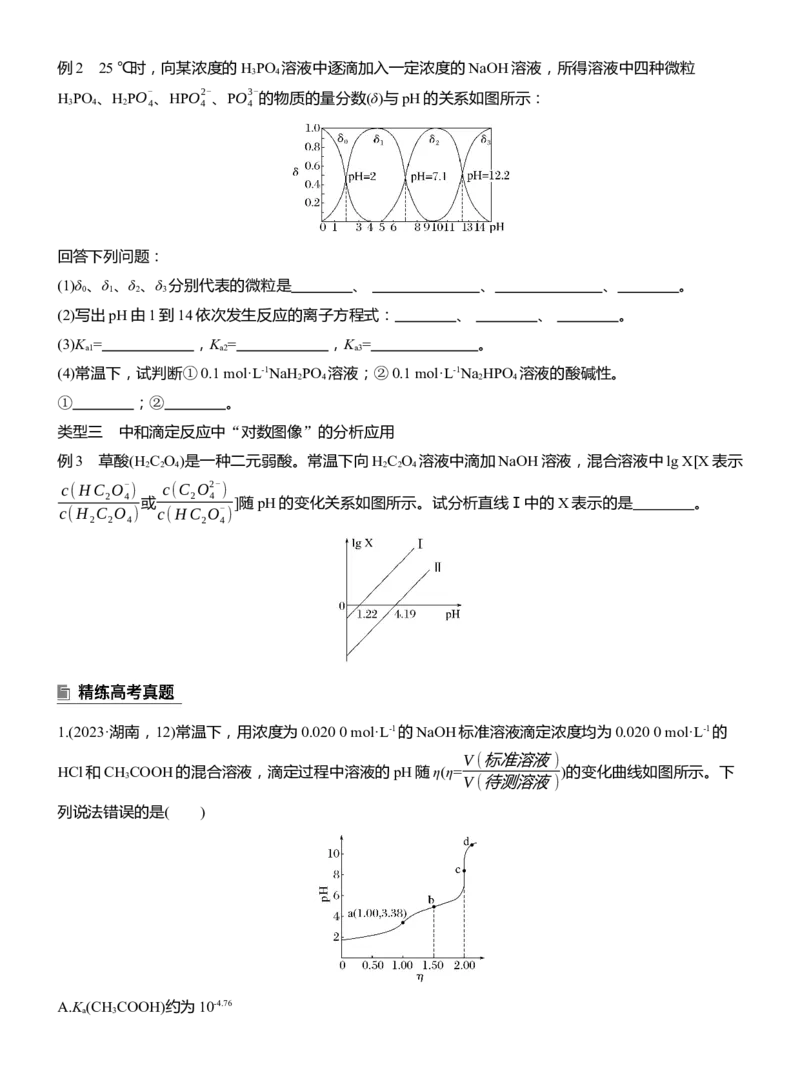
类型二 中和滴定反应中“分布系数图像”的分析应用例2 25 ℃时,向某浓度的H PO 溶液中逐滴加入一定浓度的NaOH溶液,所得溶液中四种微粒
3 4
H PO 、H
PO- 、HPO2- 、PO3-
的物质的量分数(δ)与pH的关系如图所示:
3 4 2 4 4 4
回答下列问题:
(1)δ 、δ 、δ 、δ 分别代表的微粒是 、 、 、 。
0 1 2 3
(2)写出pH由1到14依次发生反应的离子方程式: 、 、 。
(3)K = ,K = ,K = 。
a1 a2 a3
(4)常温下,试判断①0.1 mol·L-1NaH PO 溶液;②0.1 mol·L-1Na HPO 溶液的酸碱性。
2 4 2 4
① ;② 。
类型三 中和滴定反应中“对数图像”的分析应用
例3 草酸(H C O )是一种二元弱酸。常温下向H C O 溶液中滴加NaOH溶液,混合溶液中lg X[X表示
2 2 4 2 2 4
c(HC O- ) c(C O2- )
2 4 2 4
或 ]随pH的变化关系如图所示。试分析直线Ⅰ中的X表示的是 。
c(H C O ) c(HC O- )
2 2 4 2 4
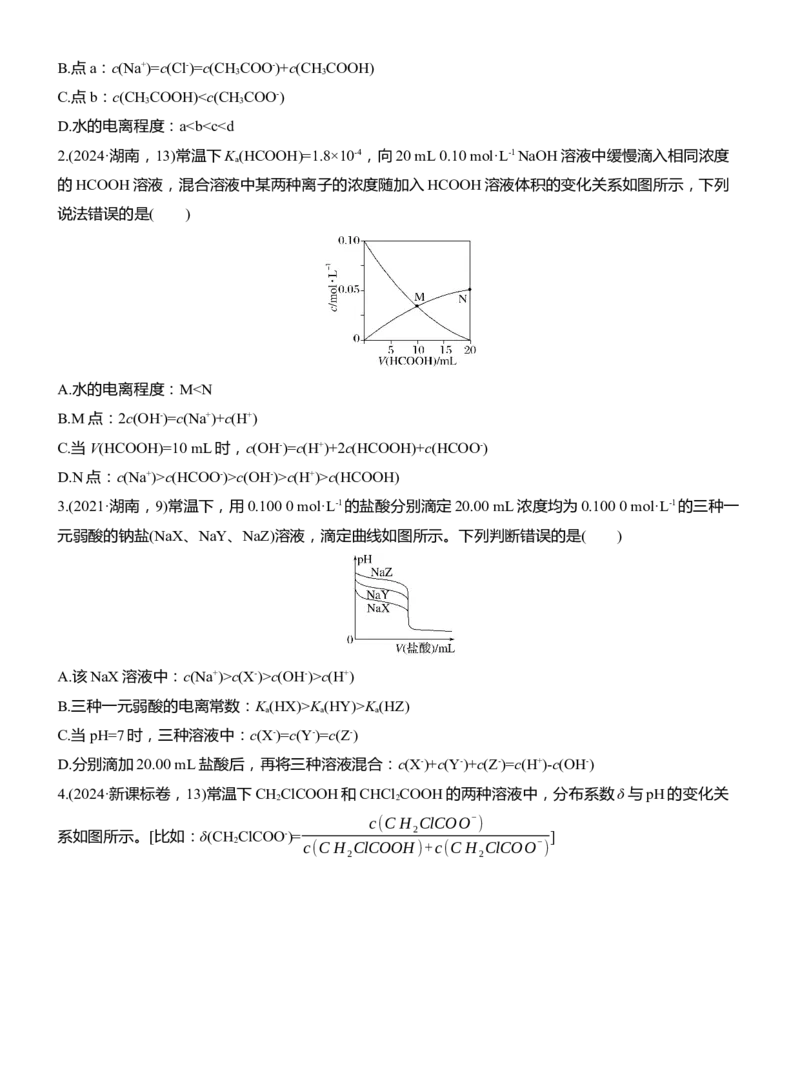
1.(2023·湖南,12)常温下,用浓度为0.020 0 mol·L-1的NaOH标准溶液滴定浓度均为0.020 0 mol·L-1的
V(标准溶液)
HCl和CH COOH的混合溶液,滴定过程中溶液的pH随η(η= )的变化曲线如图所示。下
3 V(待测溶液)
列说法错误的是( )
A.K(CH COOH)约为10-4.76
a 3B.点a:c(Na+)=c(Cl-)=c(CH COO-)+c(CH COOH)
3 3
C.点b:c(CH COOH)c(HCOO-)>c(OH-)>c(H+)>c(HCOOH)
3.(2021·湖南,9)常温下,用0.100 0 mol·L-1的盐酸分别滴定20.00 mL浓度均为0.100 0 mol·L-1的三种一
元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是( )
A.该NaX溶液中:c(Na+)>c(X-)>c(OH-)>c(H+)
B.三种一元弱酸的电离常数:K(HX)>K(HY)>K(HZ)
a a a
C.当pH=7时,三种溶液中:c(X-)=c(Y-)=c(Z-)
D.分别滴加20.00 mL盐酸后,再将三种溶液混合:c(X-)+c(Y-)+c(Z-)=c(H+)-c(OH-)
4.(2024·新课标卷,13)常温下CH ClCOOH和CHCl COOH的两种溶液中,分布系数δ与pH的变化关
2 2
c(CH ClCOO- )
2
系如图所示。[比如:δ(CH ClCOO-)= ]
2 c(CH ClCOOH)+c(CH ClCOO- )
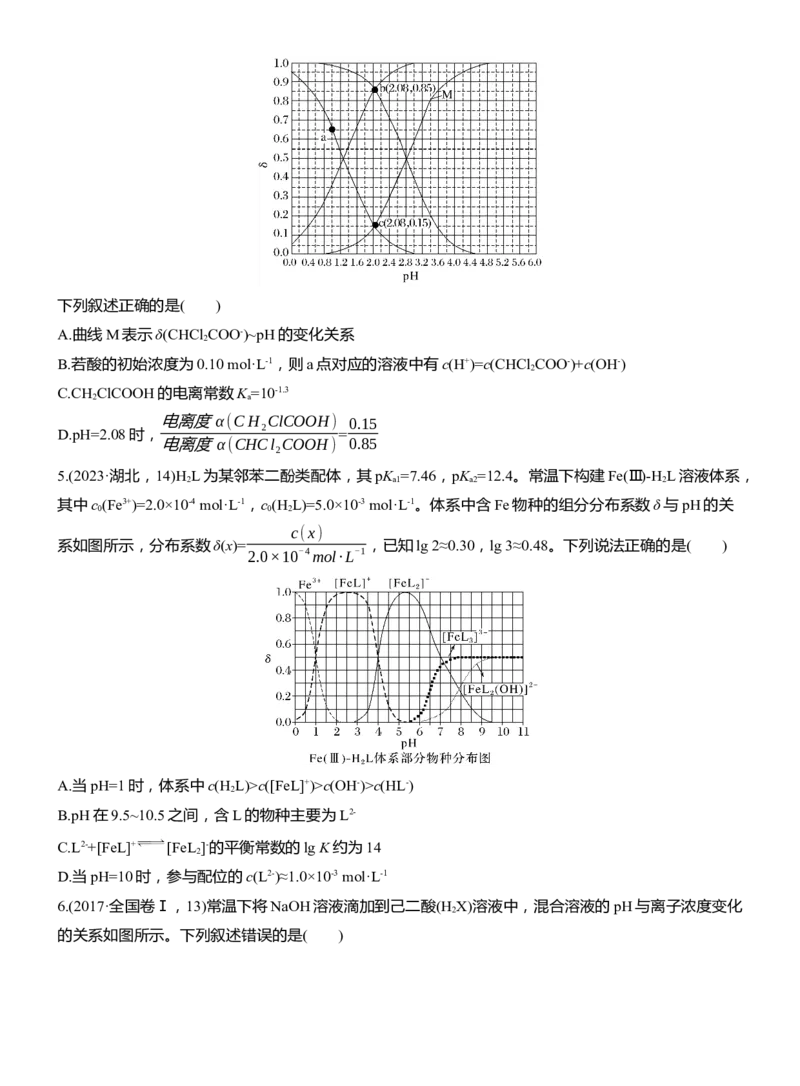
2 2下列叙述正确的是( )
A.曲线M表示δ(CHCl COO-)~pH的变化关系
2
B.若酸的初始浓度为0.10 mol·L-1,则a点对应的溶液中有c(H+)=c(CHCl COO-)+c(OH-)
2
C.CH ClCOOH的电离常数K=10-1.3
2 a
电离度α(CH ClCOOH) 0.15
2
D.pH=2.08时, =
电离度α(CHCl COOH) 0.85
2
5.(2023·湖北,14)H L为某邻苯二酚类配体,其pK =7.46,pK =12.4。常温下构建Fe(Ⅲ)-H L溶液体系,
2 a1 a2 2
其中c (Fe3+)=2.0×10-4 mol·L-1,c (H L)=5.0×10-3 mol·L-1。体系中含Fe物种的组分分布系数δ与pH的关
0 0 2
c(x)
系如图所示,分布系数δ(x)= ,已知lg 2≈0.30,lg 3≈0.48。下列说法正确的是( )
2.0×10-4mol·L-1
A.当pH=1时,体系中c(H L)>c([FeL]+)>c(OH-)>c(HL-)
2
B.pH在9.5~10.5之间,含L的物种主要为L2-
C.L2-+[FeL]+ [FeL ]-的平衡常数的lg K约为14
2
D.当pH=10时,参与配位的c(L2-)≈1.0×10-3 mol·L-1
6.(2017·全国卷Ⅰ,13)常温下将NaOH溶液滴加到己二酸(H X)溶液中,混合溶液的pH与离子浓度变化
2
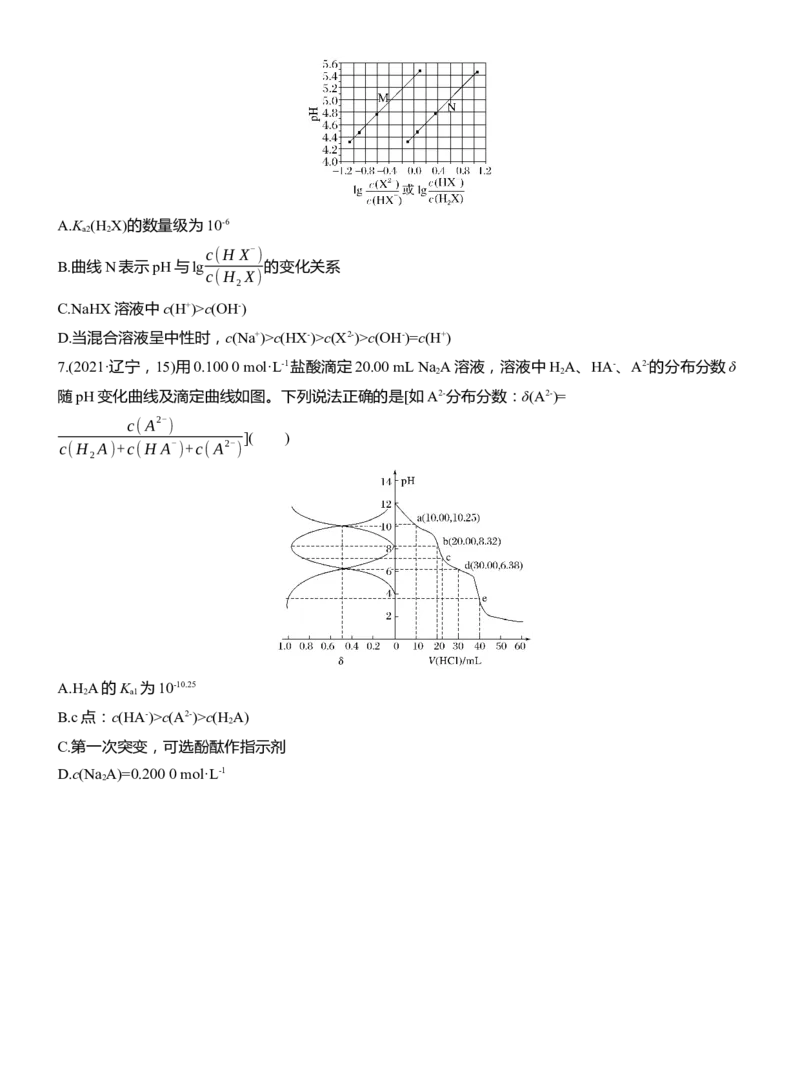
的关系如图所示。下列叙述错误的是( )A.K (H X)的数量级为10-6
a2 2
c(H X- )
B.曲线N表示pH与lg 的变化关系
c(H X)
2
C.NaHX溶液中c(H+)>c(OH-)
D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(OH-)=c(H+)
7.(2021·辽宁,15)用0.100 0 mol·L-1盐酸滴定20.00 mL Na A溶液,溶液中H A、HA-、A2-的分布分数δ
2 2
随pH变化曲线及滴定曲线如图。下列说法正确的是[如A2-分布分数:δ(A2-)=
c(A2-
)
]( )
c(H A)+c(H A- )+c(A2- )
2
A.H A的K 为10-10.25
2 a1
B.c点:c(HA-)>c(A2-)>c(H A)
2
C.第一次突变,可选酚酞作指示剂
D.c(Na A)=0.200 0 mol·L-1
2答案精析
盘点核心知识
(一)
1.例1 (1)c(H+)>c(HS-)>c(S2-)>c(OH-)
(2)c(Na+)>c(HS-)>c(OH-)>c(H+)>c(S2-)
例2 c(CH COO-)>c(Na+)>c(H+)>c(OH-)
3
2.(3)①c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-)
②c(Na+)=2c(HCO- )+2c(CO2-
)+2c(H CO )
3 3 2 3
2c(Na+)=c(A-)+c(HA)
③c(OH-)=c(H+)+c(HCO-
)+2c(H CO )
3 2 3
解析 ③方法一:由电荷守恒式和元素守恒式联立消去阳离子(Na+)得到。
方法二:框图法快速求Na CO 的质子守恒。
2 3
(二)
例1 CH COONa、CH COOH c(CH COO-)>c(Na+)>c(H+)>c(OH-) CH COONa、CH COOH
3 3 3 3 3
c(CH COO-)=c(Na+)>c(H+)=c(OH-) CH COONa c(Na+)>c(CH COO-)>c(OH-)>c(H+) CH COONa、NaOH
3 3 3 3
c(Na+)>c(OH-)>c(CH COO-)>c(H+)
3
例2 (1)H PO H
PO- HPO2- PO3-
3 4 2 4 4 4
(2)H PO +OH-===H PO- +H O
3 4 2 4 2
H
PO- +OH-===HPO2-
+H O
2 4 4 2
HPO2- +OH-===PO3-
+H O
4 4 2
(3)10-2 10-7.1 10-12.2 (4)①酸性 ②碱性
K 10-14 K 10-14
解析 (4)①K (H
PO-
)=
w
= =10-12<10-7.1,溶液呈酸性。②K
(HPO2-
)=
w
= =10-6.9>10-12.2,溶
h 2 4 K 10-2 h 4 K 10-7.1
a1 a2
液呈碱性。
c(HC O- )
例3
2 4
c(H C O )
2 2 4解析 当lg X=0时,c(HC
O-
)=c(H C O ),c(C
O2-
)=c(HC
O-
),直线Ⅰ中pH=1.22,直线Ⅱ中pH=4.19,
2 4 2 2 4 2 4 2 4
c(HC O- )
则直线Ⅰ中X表示的是 2 4 。
c(H C O )
2 2 4
精练高考真题
1.D [a点时溶质成分为NaCl和CH COOH,c(CH COOH)≈0.010 0 mol·L-1,c(H+)=10-3.38 mol·L-1,
3 3
c(H+ )·c(CH COO- ) 10-3.38×10-3.38
K(CH COOH)= 3 ≈ =10-4.76,故A正确;a点溶液为等浓度的NaCl和
a 3
c(CH COOH) 0.01
3
CH COOH混合溶液,存在元素守恒:c(Na+)=c(Cl-)=c(CH COOH)+c(CH COO-),故B正确;点b溶液中含
3 3 3
有NaCl及等浓度的CH COOH和CH COONa,由于pH<7,溶液显酸性,说明CH COOH的电离程度大于
3 3 3
CH COO-的水解程度,则c(CH COOH)d,故D错误。]
2.D [向20 mL 0.10 mol·L-1 NaOH溶液中滴入相同浓度的HCOOH溶液,Na+、OH-逐渐下降,HCOO-浓度
上升,当V(HCOOH)=20 mL时,c(Na+)=0.05 mol·L-1,由图可知,经过M点在下降的曲线表示的是OH-浓
度变化的曲线,经过M点、N点的上升曲线表示的是HCOO-浓度变化的曲线。M点时,V(HCOOH)=10
mL,溶液中的溶质为等物质的量的NaOH和HCOONa,NaOH抑制水的电离,N点HCOOH溶液与NaOH
溶液恰好反应生成HCOONa,只存在HCOONa水解,水的电离程度最大,故A正确;M点时,
V(HCOOH)=10 mL,根据电荷守恒有c(Na+)+c(H+)=c(HCOO-)+c(OH-),又因M点c(HCOO-)=c(OH-),联立
可得2c(OH-)=c(Na+)+c(H+),根据元素守恒有c(Na+)=2c(HCOO-)+2c(HCOOH),联立电荷守恒可得
c(OH-)=c(H+)+2c(HCOOH)+c(HCOO-),故B、C正确;N点是HCOONa溶液,甲酸根离子发生水解,因此
c(Na+)>c(HCOO-)、c(OH-)>c(H+),由图中N点可知,c(HCOO-)≈0.05 mol·L-1,根据K(HCOOH)=
a
c(H+ )·c(HCOO-
)
=1.8×10-4,可知c(HCOOH)>c(H+),故D错误。]
c(HCOOH)
3.C [NaX为强碱弱酸盐,在溶液中水解使溶液呈碱性,则溶液中离子浓度的大小顺序为
c(Na+)>c(X-)>c(OH-)>c(H+),故A正确;弱酸的酸性越弱,电离常数越小,分析可知,HX、HY、HZ三种
一元弱酸的酸性依次减弱,则三种一元弱酸的电离常数的大小顺序为K(HX)>K(HY)>K(HZ),故B正确;
a a a
当溶液pH为7时,酸越弱,向盐溶液中加入盐酸的体积越大,酸根离子的浓度越小,则三种盐溶液中酸
根离子的浓度大小顺序为c(X-)>c(Y-)>c(Z-),故C错误;向三种盐溶液中分别滴加20.00 mL盐酸,三种盐
都完全反应,溶液中钠离子浓度等于氯离子浓度,将三种溶液混合后溶液中存在电荷守恒关系c(Na+)
+c(H+)=c(X-)+c(Y-)+c(Z-)+c(Cl-)+c(OH-),由c(Na+)=c(Cl-)可得:c(X-)+c(Y-)+c(Z-)=c(H+)-c(OH-),故D正确。]
4.D [—Cl为吸电子基团,则酸性:CHCl COOH>CH ClCOOH,即K(CHCl COOH)>K(CH ClCOOH)。随
2 2 a 2 a 2
着pH的增大,c(CH ClCOOH)、c(CHCl COOH)减小,c(CH ClCOO-)、c(CHCl COO-)增大。δ(酸分子)=δ(酸
2 2 2 2
根离子)=0.5时的pH分别约为1.3、2.8,故两种酸的电离常数分别为K(CHCl COOH)≈10-1.3,
a 2
K(CH ClCOOH)≈10-2.8。根据分析,曲线M表示δ(CH ClCOO-)~pH的变化关系,A错误;CHCl COOH为
a 2 2 2弱酸,若c (CHCl COOH)=0.1 mol·L-1,且溶液中溶质只有CHCl COOH时,c(H+)<0.1 mol·L-1,a点对应的
0 2 2
c(H+)=0.1 mol·L-1,说明此时溶液中加入了酸性更强的酸,根据电荷守恒,c(H+)>c(CHCl COO-)+c(OH-),B
2
n
错误;CH ClCOOH的电离常数K=10-2.8,C错误;电离度α= 电离 ,n =n +n ,则
2 a n 始 电离 未电离
始
α(CH ClCOOH)=δ(CH ClCOO-),α(CHCl COOH)=δ(CHCl COO-),pH=2.08时,δ(CH ClCOO-)=0.15,
2 2 2 2 2
δ(CHCl COO-)=0.85,D正确。]
2
5.C [由图可知,pH=1,即c(H+)=0.1 mol·L-1时c([FeL]+)=1.0×10-4 mol·L-1,又c (H L)=5.0×10-3 mol·L-1,根
0 2
据Fe3++H L [FeL]++2H+知,此时c(H L)=(5.0-0.1)×10-3 mol·L-1=4.9×10-3 mol·L-1,结合K =
2 2 a1
c(H+ )·c(H L- )
=10-7.46知,此时c(HL-)=10-7.46×4.9×10-3×10=4.9×10-9.46 mol·L-1,又pH=1时,c(OH-)=10-13
c(H L)
2
mol·L-1,故A错误;pH在9.5~10.5之间时c([FeL ]3-)=c([FeL (OH)]2-)=10-4 mol·L-1,其中两种离子共含
3 2
c(L2-)=3×10-4 mol·L-1+2×10-4 mol·L-1=5×10-4 mol·L-1,当pH=10时,c(H+)=10-10 mol·L-1,根据K =
a1
c(H+ )·c(H L- ) 10-10c(H L- ) c(H+ )·c(L2- )
= =10-7.46,c(HL-)=102.54c(H L),即c(HL-)>c(H L),由K = =10-
c(H L) c(H L) 2 2 a2 c(H L- )
2 2
c([FeL ] - )
12.4,得c(HL-)=102.4c(L2-),即c(HL-)>c(L2-),B、D错误;该反应的平衡常数K= 2 ,由题图
c(L2- )·c([FeL] + )
c2 (H+ )·c(L2-
)
知,当c([FeL ]-)=c([FeL]+)时,pH=4,由K ·K =10-19.86= ,得①式:10-19.86×c(H L)=10-
2 a1 a2 c(H L) 2
2
4.7×10-22.86
8c(L2-),此时c(H L)=5.0×10-3 mol·L-1-3×10-4 mol·L-1=4.7×10-3 mol·L-1,代入①式,c(L2-)=
2 10-8
1
=4.7×10-14.86 mol·L-1,则K= ≈2.1×1013.86,故lg K=13.86+lg 2.1≈14,C正确。]
4.7×10-14.86
6.D [横坐标取0时,曲线M对应pH约为5.4,曲线N对应pH约为4.4,因为是NaOH滴定H X溶液,所
2
c(H X- )
以在酸性较强的溶液中会存在c(HX-)=c(H X),所以曲线N表示pH与lg 的变化关系,B正确;
2 c(H X)
2
c(X2-
)
c(X2-
)
c(H+ )·c(X2-
)
=1时,即lg =0,pH≈5.4,c(H+)=1×10-5.4 mol·L-1,K (H X)= =1×10-5.4,A
c(H X- ) c(H X- ) a2 2 c(H X- )
c(H X- )
正确;由图像可知,当lg =0时,pH≈4.4,则K (H X)=10-4.4,NaHX溶液中,HX-的电离常数
c(H X) a1 2
2
K
w
K (H X)大于其水解常数[ ],此时溶液呈酸性,C正确;当溶液呈中性时,由曲线M可知lg
a2 2 K (H X)
a1 2
c(X2-
)
c(X2-
)
>0, >1,即c(X2-)>c(HX-),D错误。]
c(H X- ) c(H X- )
7.Cc(H+ )·c(H A- )
[H A的K = ,根据上图交点1计算可知K =10-6.38,A错误;根据图像可知c点
2 a1 c(H A) a1
2
c(HA-)>c(H A)>c(A2-),B错误;根据图像可知第一次滴定突变溶液呈碱性,所以可以选择酚酞作指示剂,
2
C正确;根据图像e点可知,当加入盐酸40 mL时,全部生成H A,根据Na A+2HCl===2NaCl+H A计算
2 2 2
可知c(Na A)=0.100 0 mol·L-1,D错误。]
2