文档内容
专题十六 沉淀溶解平衡 基础过关检测
考试时间:70分钟 卷面分值:100分
学校:___________姓名:___________班级:___________考号:___________
注意事项:
1.答题前,务必将自己的姓名、考号填写在答题卡规定的位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦擦干净后,再选涂其它答案标号。
3.答非选择题时,必须将答案书写在专设答题页规定的位置上。
4.所有题目必须在答题卡上作答。在试题卷上答题无效。
5.考试结束后,只交试卷答题页。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
一、选择题(本题含20小题,每题5分,共100分。每题只有一个选项符合题意)
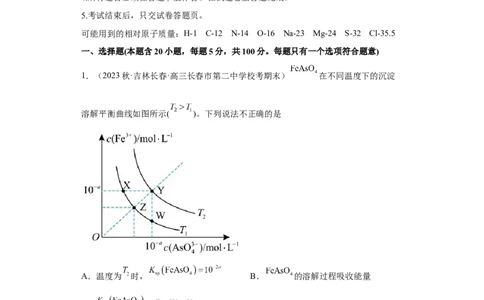
1.(2023秋·吉林长春·高三长春市第二中学校考期末) 在不同温度下的沉淀
溶解平衡曲线如图所示( )。下列说法不正确的是
A.温度为 时, B. 的溶解过程吸收能量
C. : D.将Z的悬浊液升温可以得到Y溶液
【答案】C
【详解】A.温度为T 时, =10-a×10-a=10-2a,故A正确;
2
B.由图可知,K (T ) ,不利于 沉淀溶解,从而析出 沉淀,而相对于
c
来说,相当于减少 ,则Q< ,促进 溶解,从而
c
不析出 沉淀,B正确;
C.向b点溶液中加入少量 固体, 不变, 增加则
减小 增大,b点沿着直线①向下移动,不会变到a点,C错误;
D.逐渐升高温度, 增大,直线①向左下方移动, 、 都
增大,D错误;
答案选B。
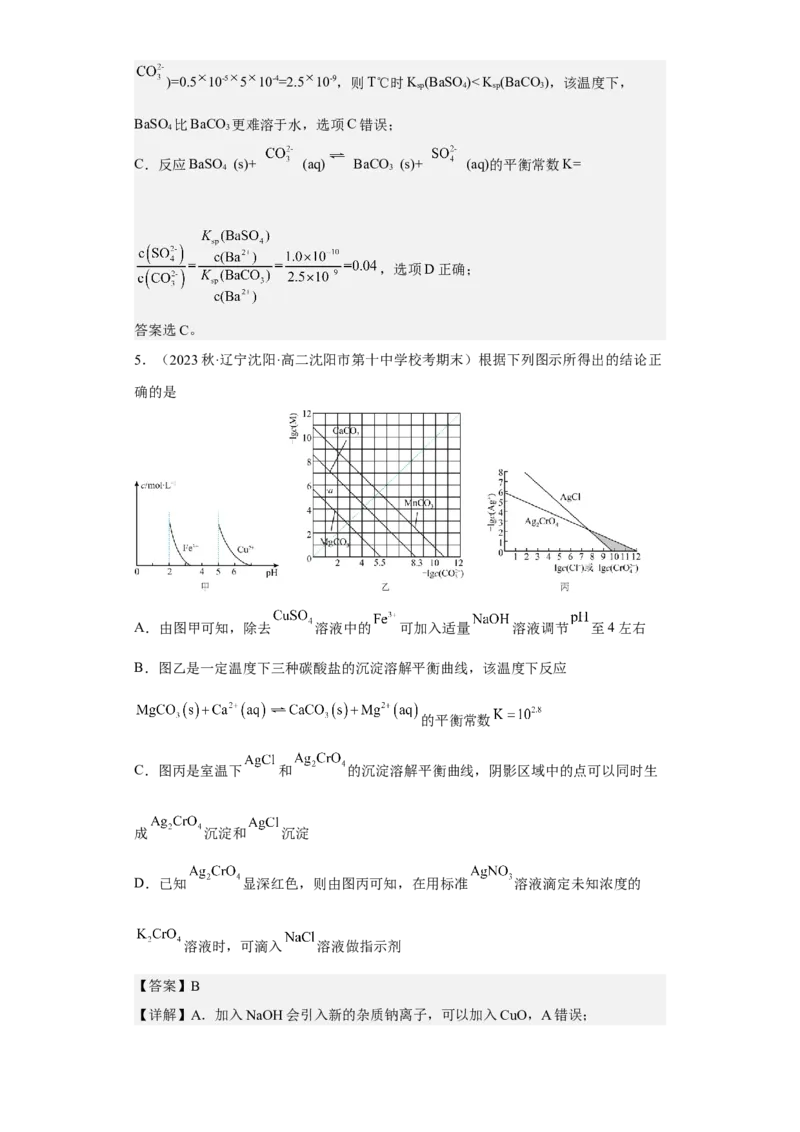
7.(2023秋·河北石家庄·高三统考期末)25℃时,向20mL0.01mol/L的RCl 溶液中通
2
入氨气,测得溶液的pH与p(R2+)之间的变化曲线如图所示[已知:
, ,忽略反应过程中溶液体积的变化]。下
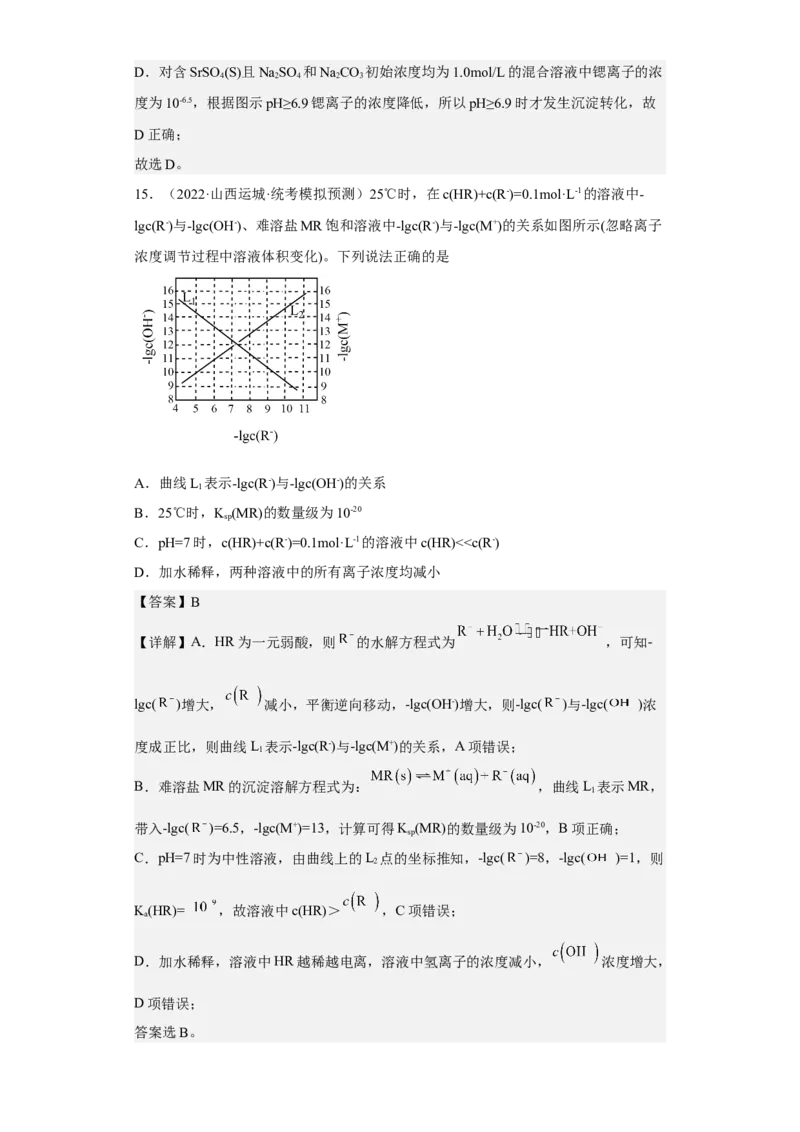
列说法正确的是A. 的数量级是
B.a点溶液中会产生 沉淀
C.b点溶液存在:
D.c点溶液存在:
【答案】C
【详解】A.由题干图示信息点(2,8.3)可知,K [R(OH) ]=c(R2+)c2(OH-)=10-2×(
sp 2
)2=10-13.4,故K [R(OH) ]的数量级是10-14,A错误;
sp 2
B.由题干图示信息可知,a点对应的溶解平衡点为b点或者c点,则可知a点对应的
c(R2+)c2(OH-)小于其Ksp[R(OH) ],故a点溶液中不会产生 沉淀,B错误;
2
C.由A项分析可知,K [R(OH) ]=10-13.4,则有b点时c(R2+)= =10-
sp 2
3.4mol/L,根据 ,即 =1.8×10-5,则有
=1.8,即有c( )>c(NH ·H O),且题干告知是通入NH ,使
3 2 3
R2+沉淀,故b点溶液存在: ,C正确;
D.c点溶液中电荷守恒式为: ,又知c点溶液呈
碱性,即c(OH-)>c(H+),故c点溶液中存在: ,D错误;
试卷第8页,共22页故答案为:C。
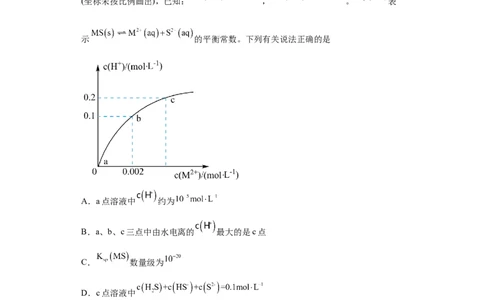
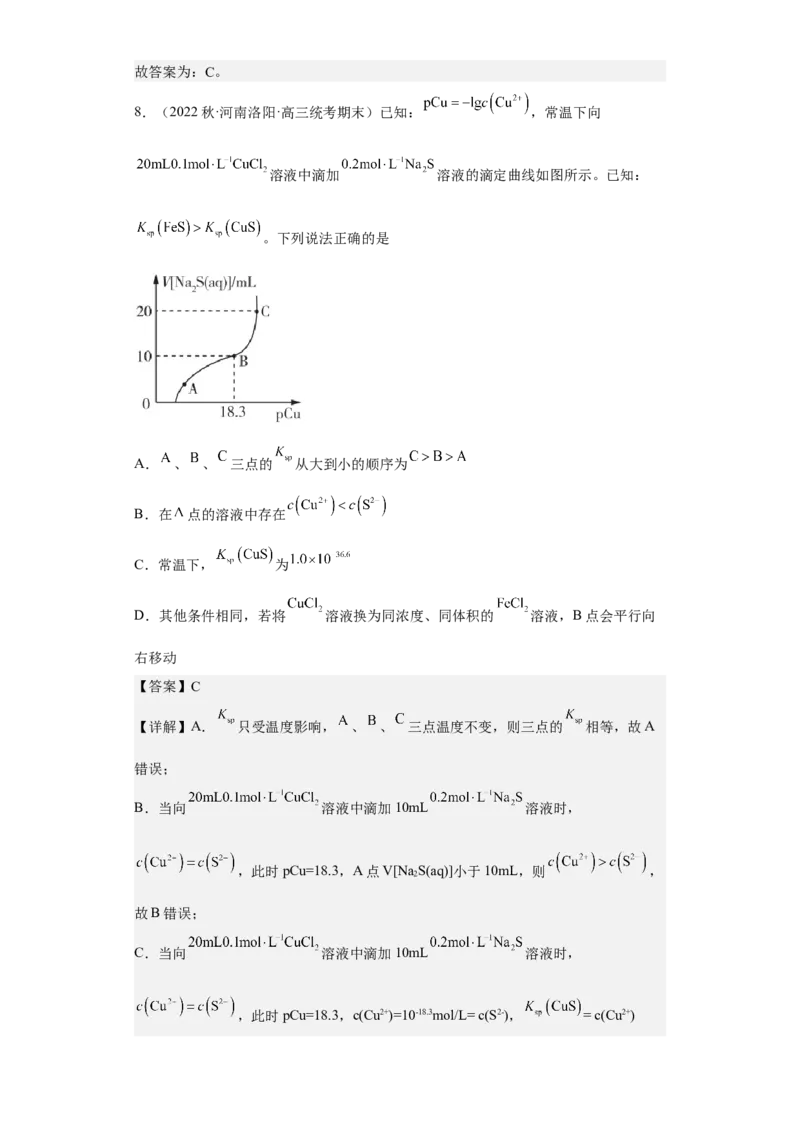
8.(2022秋·河南洛阳·高三统考期末)已知: ,常温下向
溶液中滴加 溶液的滴定曲线如图所示。已知:
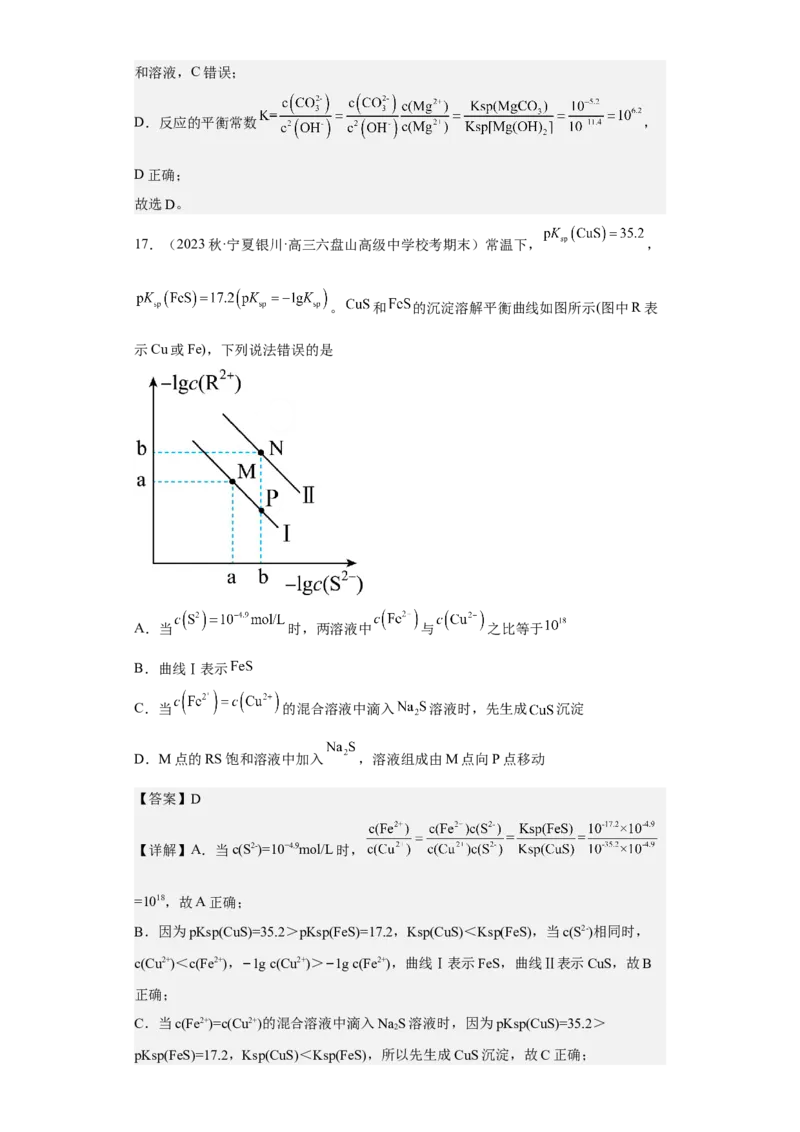
。下列说法正确的是
A. 、 、 三点的 从大到小的顺序为
B.在 点的溶液中存在
C.常温下, 为
D.其他条件相同,若将 溶液换为同浓度、同体积的 溶液,B点会平行向
右移动
【答案】C
【详解】A. 只受温度影响, 、 、 三点温度不变,则三点的 相等,故A
错误;
B.当向 溶液中滴加10mL 溶液时,
,此时pCu=18.3,A点V[Na S(aq)]小于10mL,则 ,
2
故B错误;
C.当向 溶液中滴加10mL 溶液时,
,此时pCu=18.3,c(Cu2+)=10-18.3mol/L= c(S2-), = c(Cu2+)c(S2-)= ,故C正确;
D.其他条件相同,若将 溶液换为同浓度、同体积的 溶液,滴加10mL
溶液时, ,由于 ,
则pFe会向左移动,故D错误;
故选C。
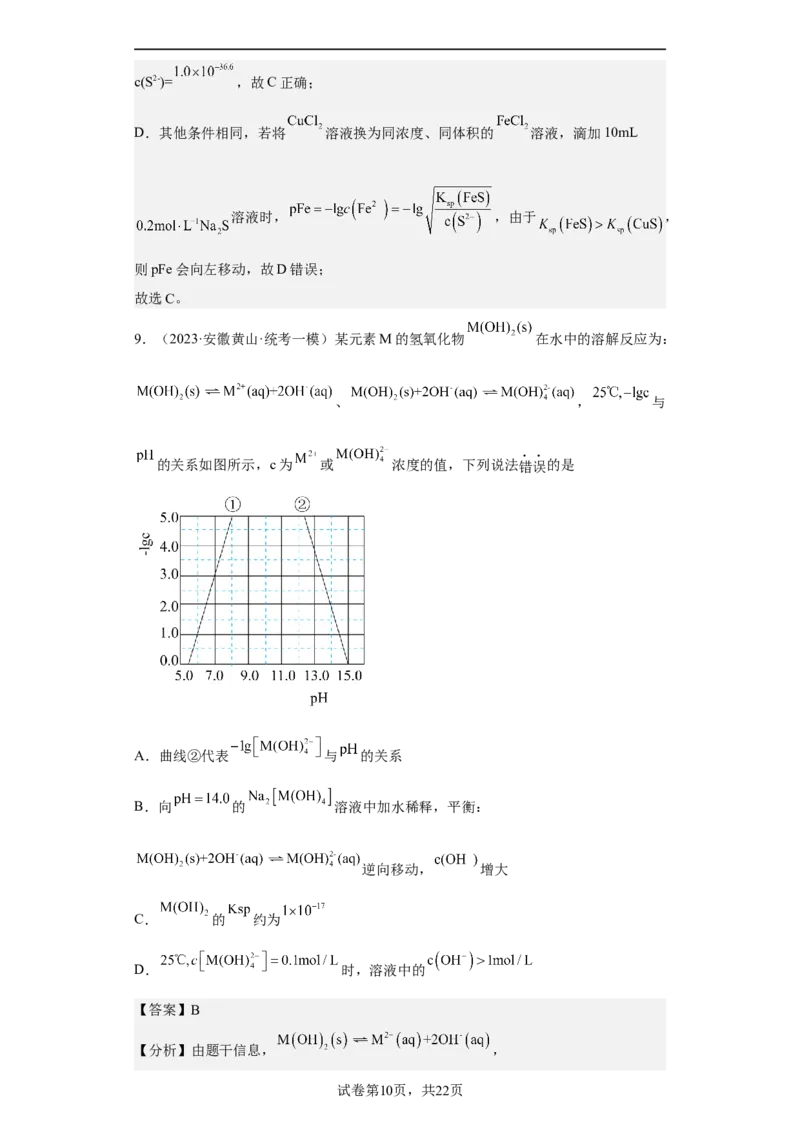
9.(2023·安徽黄山·统考一模)某元素M的氢氧化物 在水中的溶解反应为:
、 , 与
的关系如图所示,c为 或 浓度的值,下列说法错误的是
A.曲线②代表 与 的关系
B.向 的 溶液中加水稀释,平衡:
逆向移动, 增大
C. 的 约为
D. 时,溶液中的
【答案】B
【分析】由题干信息, ,
试卷第10页,共22页,随着pH增大,c(OH-)增大,则c(M2+)减小,
c[ ]增大,即-lg c(M2+)增大,-lg c[ ]减小,因此曲线①代表-lg c(M2+)与
pH的关系,曲线②代表-lg c[ ]与pH的关系。
【详解】A.由分析可知,曲线②代表-lg c[ ]与pH的关系,选项A正确;
B.向 的 溶液中加水稀释, 减小,平衡:
逆向移动, 选项B错误;
C.由图像,pH=7.0时,-lg c(M2+)=3.0,则M(OH) 的K =c(M2+)·c2(OH-)=1×10-17,选项
2 sp
C正确;
D.根据图中曲线可知, 时,-lg c[ ]=1,溶液的
pH>14, ,选项D正确;
答案选B。
10.(2023秋·山东烟台·高三统考期末)以硫铁矿(主要成分是 ,含少量
和 )为原料制备磷酸铁的工艺流程如下,可能用到的数据见下表。下
列说法错误的是
开始沉淀 2.3 7.6 4.0
沉淀完全 4.1 9.7 5.2A.滤渣A的主要成分为 B.操作I加入 目的是除去过量的硫
酸
C.调 的范围为5.2~7.6 D.沉淀时, 过高或者过低均不利于
生成磷酸铁
【答案】B
【分析】以硫铁矿主要成分是 ,含少量 、 和 通入空气后 被
氧气氧化生成二氧化硫,铁元素被氧化为三价铁,在酸浸后二氧化硅不反应到滤渣A
中,三氧化铝和氧化铁与硫酸反应,生成硫酸铝和硫酸铁,在还原时硫化铁加入后将
三价铁还原为二价铁,在除铝过程中加入碳酸铁调节pH值将铝元素转化为氢氧化铝沉
淀,在氧化过程中双氧水将二价铁氧化为三价铁,在沉铁过程中将三价铁转化为磷酸
铁;
【详解】A.根据分析,酸浸后二氧化硅不反应到,滤渣A的主要成分为 ,故A
正确;
B.根据分析,操作I加入 目的是将三价铁还原为二价铁,故B错误;
C.用 调节pH根据除去氢氧化铝,故pH调节大于5.2,而不能将二价铁沉淀,
故pH小于7.6,故pH为5.2~7.6,故C正确;
D.沉淀时, 过高会使Fe3+生成Fe(OH) ,过低无法生成磷酸铁沉淀,D正确;
3
故选B。
11.(2022·浙江·统考一模)室温下,用0.100 的标准AgNO 溶液滴定20.00mL
3
浓度相等的NaCl、NaBr和NaI的混合溶液,通过电位滴定法获得lgc(Ag+)与V(AgNO)
3
的关系曲线如图所示(忽略沉淀对离子的吸附作用。若溶液中离子浓度小于
时,认为该离子沉淀完全。 , ,
)。下列说法不正确的是
试卷第12页,共22页A.a点溶液中有黄色沉淀生成
B.原溶液中NaCl、NaBr和NaI的浓度为0.0500mol·L−1
C.当Br−沉淀完全时,已经有部分Cl−沉淀,故第二个突跃不明显
D.b点溶液中:
【答案】D
【分析】根据溶度积的含义,对于阴阳离子组成比例相同的难溶物,溶度积越小,越
难溶,因为 ,所以三种难溶物中,AgI最难熔;用
0.100 的标准AgNO 溶液滴定20.00mL浓度相等的NaCl、NaBr和NaI的混合溶
3
液,先生成AgI,最后生成AgCl,如图滴定曲线,完全反应时消耗0.100 的标
准AgNO 溶液30mL,NaCl、NaBr和NaI的混合溶液中三种物质浓度相等,为
3
;
【详解】A.根据溶度积的相关信息,三种难溶物中,AgI最难溶,滴定时先生成AgI
淡黄色沉淀,故A正确;
B.如图滴定曲线,完全反应时消耗0.100 的标准AgNO 溶液30mL,NaCl、
3
NaBr和NaI的混合溶液中三种物质浓度相等,为 ,
故B正确;
C.当Br−沉淀完全时, ,
;此时若氯离子开始沉淀,此时氯离子浓度为< ,所以当
Br−沉淀完全时,已经有部分Cl−沉淀,故第二个突跃不明显,故C正确;
D.由NaCl、NaBr和NaI的浓度均为 可知,
,刚好滴定到终点时,溶质为 ,
,b点时硝酸银过量,所以b点时 ,
因为 ,所以溶液中 ,因为硝
酸银过量,抑制AgI、AgBr、AgCl溶解,所以 ,综上
所述, ,故D错误;
故选D。
12.(2022·浙江·模拟预测)T℃时, 和 的沉淀溶解平衡曲线如图所
示。已知 为 浓度的负对数,pN为阴离子浓度的负对数。下列说法不正确的
是
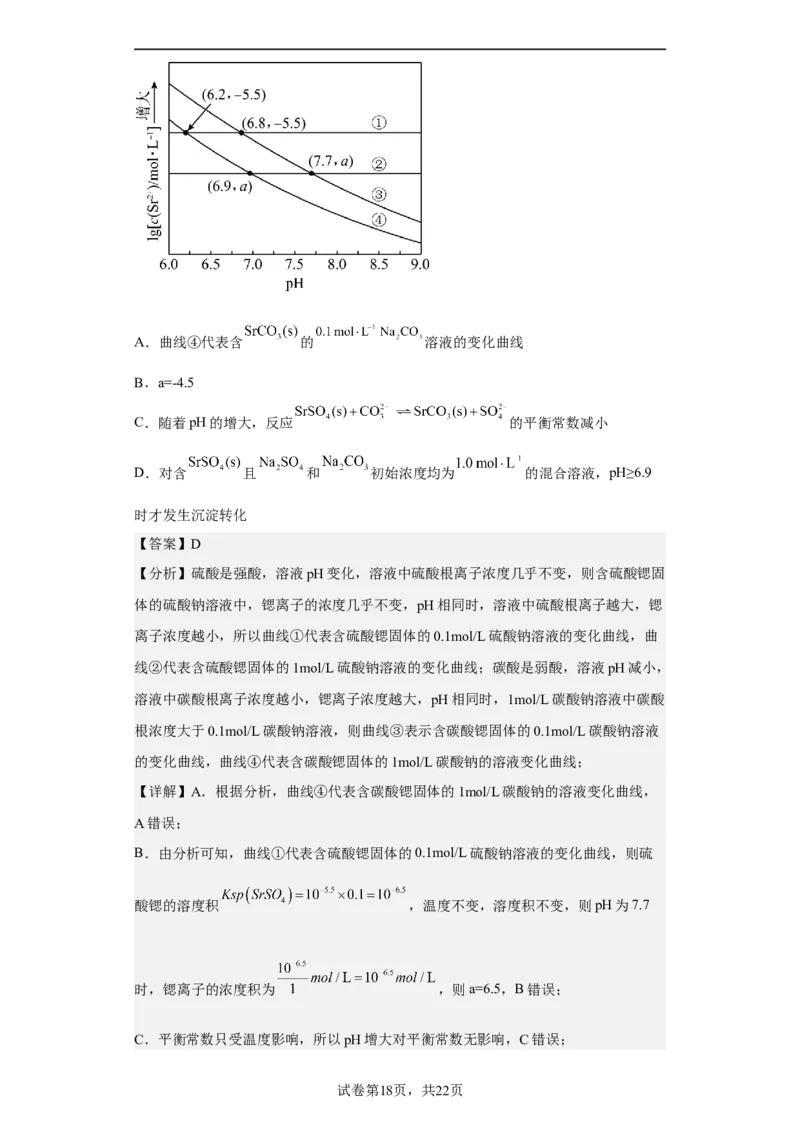
A.曲线Ⅰ是 ,的沉淀溶解平衡曲线
B.加热可使溶液由X点变到Z点
C.Y点对应的可能为 的过饱和溶液
试卷第14页,共22页D.T℃时, 的平衡常数
【答案】B
【分析】 的沉淀溶解平衡为 ,即
,则 ; 的沉淀
溶解平衡为 ,即
,则 ,结合题图中
曲线Ⅰ、Ⅱ的斜率可知,曲线I为 的沉淀溶解平衡曲线,曲线Ⅱ为 的
沉淀溶解平衡曲线, ,即
;而 ,即 。
【详解】A.根据分析,A正确;
B.曲线Ⅰ为 的沉淀溶解平衡曲线,若加热, 的沉淀溶解平衡正向
移动,溶液中的 和 浓度会同时增大,阴、阳离子浓度的负对数均会减小,B
错误;
C.Y点在 的沉淀溶解平衡曲线的下方,该点 为4,即
, 为6,即 ,则
,故Y点对应的为 的过饱和溶液,C正确;
D.由反应 可知,,D正确;
故答案为:B。
13.(2023·湖南岳阳·统考一模)室温时,用 的标准 溶液滴定
浓度相等的 、 和 混合溶液,通过电位滴定法获得 与
的关系曲线如图所示(忽略沉淀对离子的吸附作用。若溶液中离子浓度小于
时,认为该离子沉淀完全。 ,
, )。下列说法错误的是
A.a点:
B.原溶液中 的浓度为
C.当 沉淀完全时, 已部分沉淀
D. 时,
【答案】C
【分析】阴阳离子相同类型的难溶物,溶度积越小,越难溶,根据溶度积相关数值,
溶解性:AgId,a>e
1
D.降低温度a点可移动至c点
【答案】C
【分析】K (CaSO)=9.0×10-6则饱和CaSO 溶液中
sp 4 4
。K (CaCO)=2.8×10-9,则
sp 3
。计算得知 ,则L2
为CaSO,L1为CaCO 。
4 3
【详解】A.由以上分析L 为CaSO,L 为CaCO ,A项错误;
2 4 1 3
B.c、c 分别为饱和溶液中的离子浓度,则c 的数量级为10-5而c=3×10-3,B项错误;
1 2 1 2
C.a→d点溶液中Ca2+增加而 减少,说明向该溶液中加入了Ca2+溶解平衡
试卷第22页,共22页逆向,所有CaCO 溶解度降低。所有溶解度a>d。a→e
3
点溶液中 增加而Ca2+减少,说明向该溶液中加入了 溶解平衡
逆向,所有CaCO 溶解度降低。所有溶解度a>e。C项正
3
确;
D.降低温度,CaCO 溶解平衡逆向,饱和溶液中离子浓度降低,a不会移向c点,D
3
项错误;
故选C。
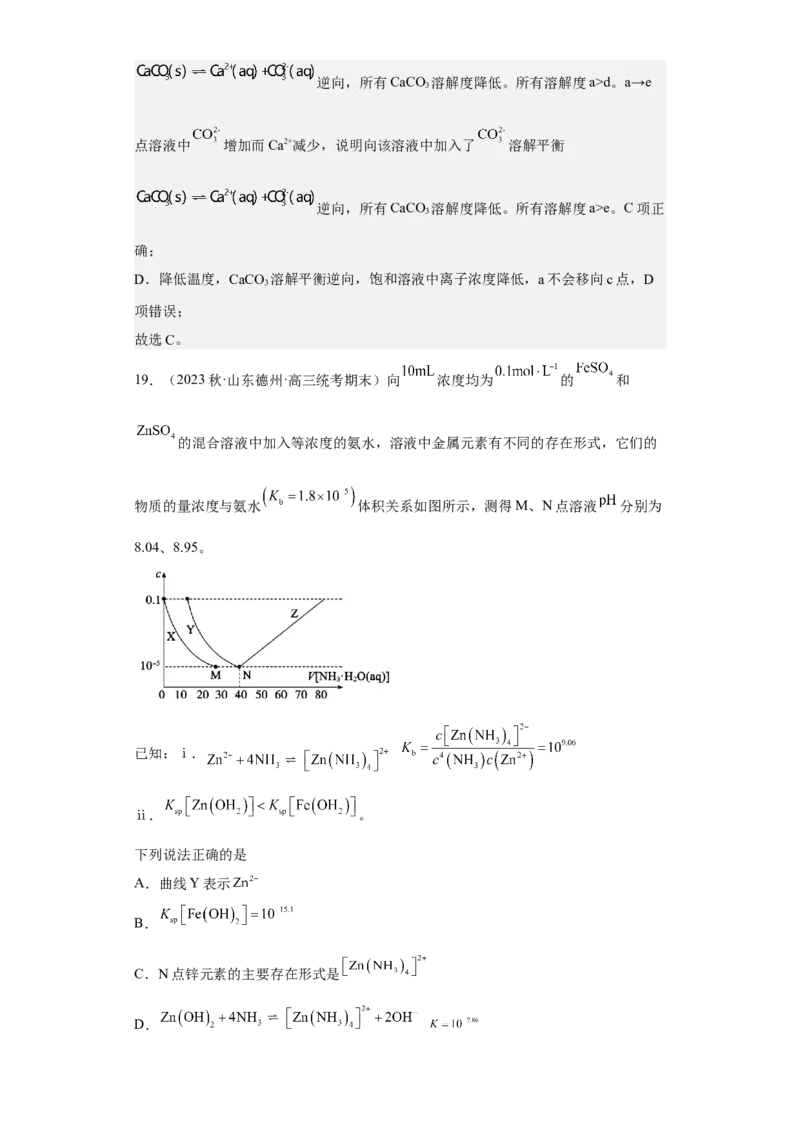
19.(2023秋·山东德州·高三统考期末)向 浓度均为 的 和
的混合溶液中加入等浓度的氨水,溶液中金属元素有不同的存在形式,它们的
物质的量浓度与氨水 体积关系如图所示,测得M、N点溶液 分别为
8.04、8.95。
已知:ⅰ.
ⅱ. 。
下列说法正确的是
A.曲线Y表示
B.
C.N点锌元素的主要存在形式是
D.【答案】BD
【详解】A. ,加入氨水先生成Zn(OH) 沉淀,所以X
2
表示 ,故A错误;
B.N点表示Fe2+完全沉淀的点,pH=8.95,
,故B正确;
C.N点锌元素沉淀完全,主要存在形式是 ,故C错误;
D.M点表示Fe2+完全沉淀的点,pH=8.04,
,
, ,故D正确;
选BD。
20.(2023秋·山东潍坊·高三统考期末)常温下,天然水体中的HCO 与空气中的
2 3
CO 保持平衡,pH变化对HCO 的浓度基本无影响。已知K (CaCO)=2.8×10-9,常温
2 2 3 sp 3
时测得某溶洞水体中-lgc(X)(X为HCO、HCO 、CO 或Ca2+)与pH的关系如图所示。
2 3
下列说法正确的是
试卷第24页,共22页A.随pH增大,c(HCO )与c(Ca2+)的变化趋势相同
B.HCO 的二级电离常数K =10-8.3
2 3 a2
C.N点对应溶液中,c(Ca2+)=0.0028mol·L-1
D.pH=7时,lgc(CO )-2lgc(HCO )=1
【答案】BD
【分析】因为pH变化对HCO 的浓度基本无影响,所以④为HCO;根据图象可知,
2 3 2 3
随着pH的的增大,溶液碱性增强,HCO 、CO 浓度都增大,而曲线①在pH很小时
也产生,因此曲线①代表HCO ,②代表CO ,③代表Ca2+,曲线①与HCO 曲线的
2 3
交点处c(HCO )=c(H CO), ,曲线①与曲线②的
2 3
交点cc(HCO )=c(CO ), 。
【详解】A.由上述分析可知①代表HCO ,③代表Ca2+,c(HCO )与c(Ca2+)的变化趋
势不相同,A错误;
B.由上述分析可知 ,B正确;C.由分析可知 ,N点处c(H+)=10-8.3mol·L-1,
c(HCO)=10-5mol·L-1,代入 ,得c(CO )=10-
2 3
4.7mol·L-1,根据K (CaCO)=2.8×10-9,得c(Ca2+)=2.8×10-4.3mol·L-1,C错误;
sp 3
D.直线①方程为: ;直线②方程为:
, 得lgc(CO )-2lgc(HCO )=1,D正确;
试卷第26页,共22页