文档内容
绝密★启用前
2025 年高考考前信息必刷卷 01(广东专用)
化 学
考情速递
高考·新动向:包含高考命题趋势变化,题目呈现方式的变化等
题目呈现方式新变化,先是以传统文字描述为主,流程图和图表题占比约30%;然后引入动态图表(如
反应速率随温度变化曲线);再到新增三维晶体结构图、分子空间填充模型,图文结合题占比超50%。
2025年可能引入“动态模拟图”(如粒子碰撞动画截图)或“多模态信息组合”(文字+图表+公
式)。
高考·新考法:对常规考点的新设问或知识融合,对非常规考点的创新糅合等
考点新设问,从常规计算题为主,如溶液浓度计算;到知识融合题涌现,如将"化学平衡"与"电化学"结
合;再到逆向思维考查(如通过异常现象反推反应机理)和开放性实验设计。2025年可能要求"多角度论
证”(如从热力学和动力学双视角分析工业条件选择)。
高考·新情境:可涉及情境题目的创新性、实时性、开放性以及跨学科的融合性等
重视创新性与实时性,从传统工业情境(如合成氨、海水提镁);到结合科技热点(核酸检测荧光探针、
钠离子电池);再到紧扣国家战略(碳中和背景的CO制甲醇、钠离子电池量产化)。2025年可能聚焦"氢
能储运""核废水处理""固态电解质"等新兴领域。
命题·大预测:基于本卷的题目进行具体分析,给出趋势性预测,也可提出备考方向等
2025年必考热点:新能源材料(钠/锂/固态电池、光伏制氢);绿色化学(催化反应路径优化、生物降解塑
料);资源循环(废旧电池回收、海水提锂)。题型创新:可能设计“科研论文片段分析",要求提取关键数
据并推导结论。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16
一、选择题:本题共16个小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在
每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列物质使用的材料属于有机高分子材料的是
A.航空发动机——碳 B.人造骨骼——镍 C.量子计算机——铁基超 D.滑雪服面料
化硅纤维 钛合金 导材料 ——聚酰胺纤维
2.生活离不开化学。下列说法不正确的是
A.食盐的主要成分是 ,用电子式表示其形成过程为:
B.食醋的溶质是醋酸,醋酸的分子结构模型:
C.天然气是一种清洁的化石燃料,主要成分 的空间结构为正四面体形
D.蔗糖和核糖都是二糖,它们的水解产物都是葡萄糖
3.湛江市历史悠久,文化底蕴浓厚。下列说法不正确的是
A.“廉江乌龙茶”讲究独特,沏泡过程涉及溶解、过滤、蒸馏等
B.“湛江木偶”栩栩如生,木偶的主要成分是纤维素,纤维素属于多糖
C.“雷州石狗”千姿百态,雕刻石狗的石头属于无机非金属材料
D.“吴川泥塑”惟妙惟肖,制作工艺中的“烧胚”属于化学变化
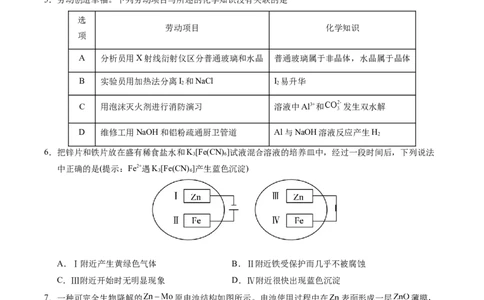
4.下列实验装置或操作能达到实验目的的是A.提纯乙酸乙酯 B.吸收氨气 C.除去 中的少量 D.制取少量
5.劳动创造幸福。下列劳动项目与所述的化学知识没有关联的是
选
劳动项目 化学知识
项
A 分析员用X射线衍射仪区分普通玻璃和水晶 普通玻璃属于非晶体,水晶属于晶体
B 实验员用加热法分离I 和NaCl I 易升华
2 2
C 用泡沫灭火剂进行消防演习 溶液中Al3+和 发生双水解
D 维修工用NaOH和铝粉疏通厨卫管道 Al与NaOH溶液反应产生H
2
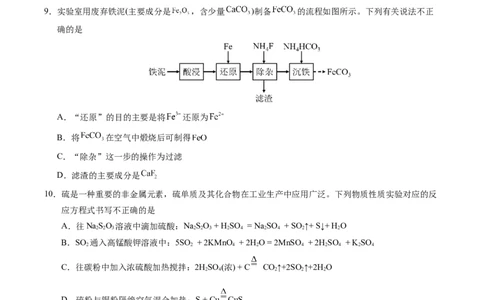
6.把锌片和铁片放在盛有稀食盐水和K[Fe(CN) ]试液混合溶液的培养皿中,经过一段时间后,下列说法
3 6
中正确的是(提示:Fe2+遇K[Fe(CN) ]产生蓝色沉淀)
3 6
A.Ⅰ附近产生黄绿色气体 B.Ⅱ附近铁受保护而几乎不被腐蚀
C.Ⅲ附近开始时无明显现象 D.Ⅳ附近很快出现蓝色沉淀
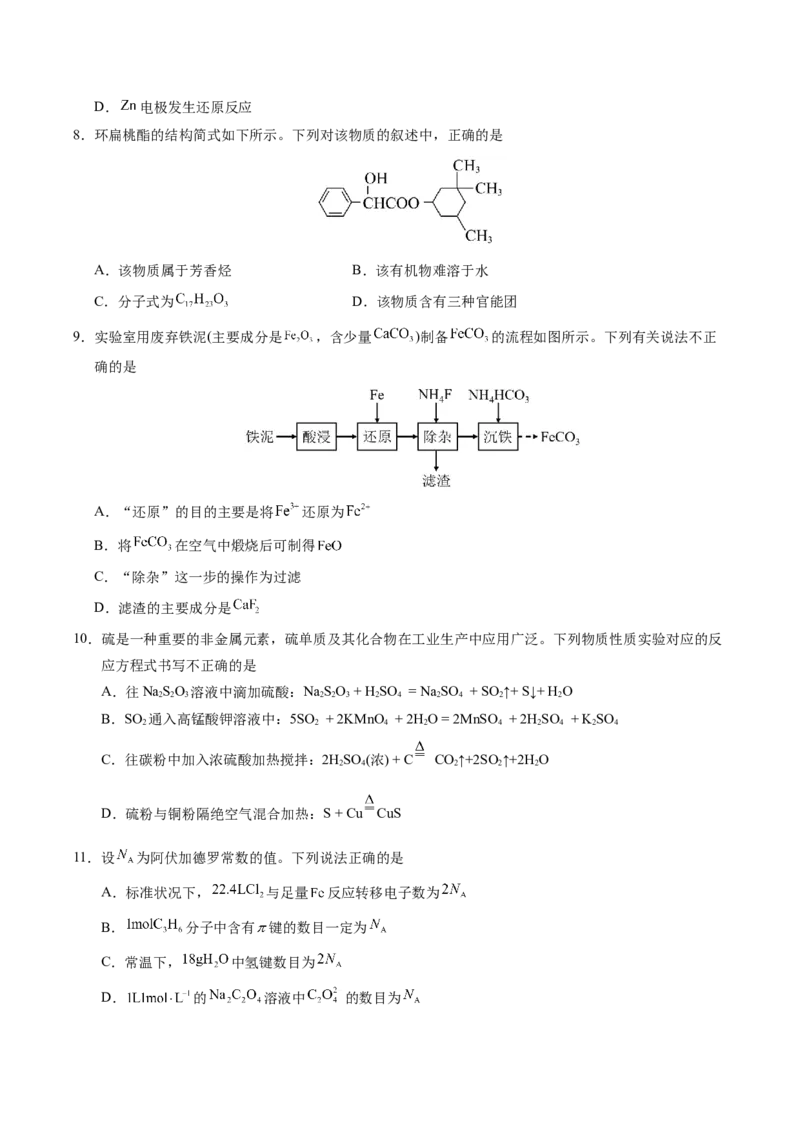
7.一种可完全生物降解的 原电池结构如图所示。电池使用过程中在 表面形成一层 薄膜,
下列说法正确的是
水凝胶掺杂
A. 作原电池负极
B.电子由 经电解质流向
C. 表面发生的电极反应:D. 电极发生还原反应
8.环扁桃酯的结构简式如下所示。下列对该物质的叙述中,正确的是
A.该物质属于芳香烃 B.该有机物难溶于水
C.分子式为 D.该物质含有三种官能团
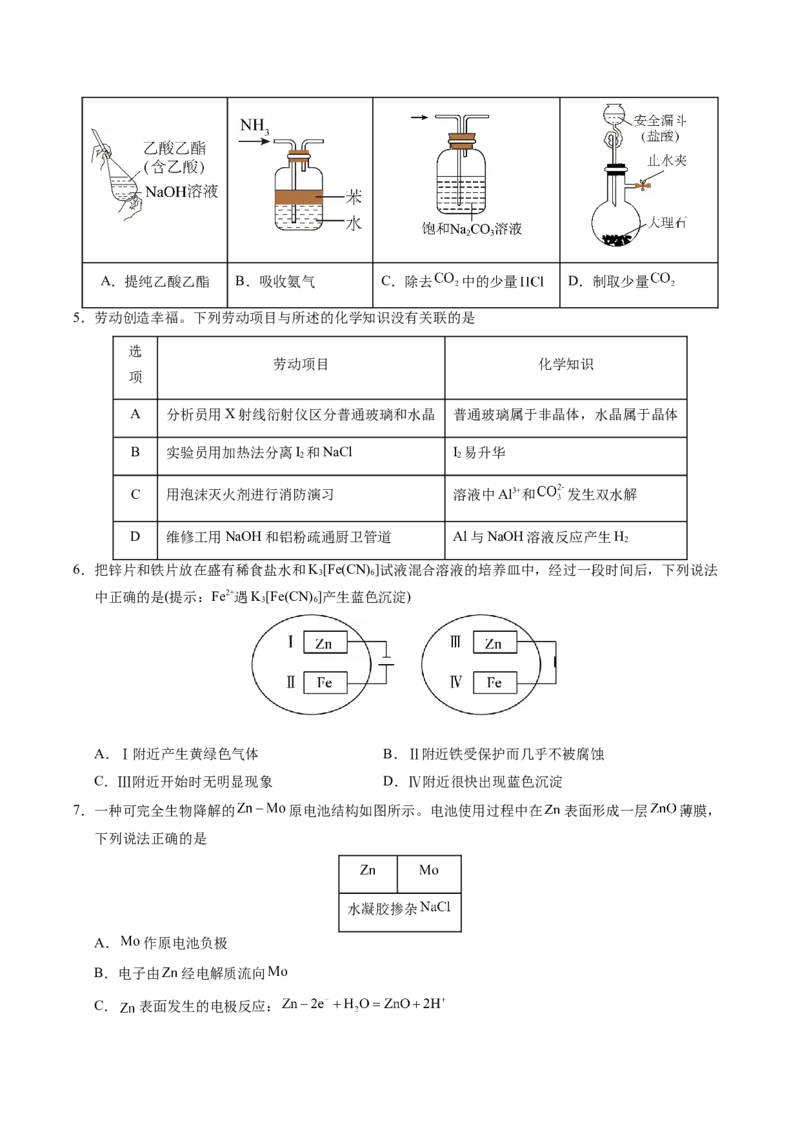
9.实验室用废弃铁泥(主要成分是 ,含少量 )制备 的流程如图所示。下列有关说法不正
确的是
A.“还原”的目的主要是将 还原为
B.将 在空气中煅烧后可制得
C.“除杂”这一步的操作为过滤
D.滤渣的主要成分是
10.硫是一种重要的非金属元素,硫单质及其化合物在工业生产中应用广泛。下列物质性质实验对应的反
应方程式书写不正确的是
A.往NaSO 溶液中滴加硫酸:NaSO + H SO = Na SO + SO ↑+ S↓+ H O
2 2 3 2 2 3 2 4 2 4 2 2
B.SO 通入高锰酸钾溶液中:5SO + 2KMnO + 2H O = 2MnSO + 2H SO + K SO
2 2 4 2 4 2 4 2 4
C.往碳粉中加入浓硫酸加热搅拌:2HSO (浓) + C CO↑+2SO↑+2H O
2 4 2 2 2
D.硫粉与铜粉隔绝空气混合加热:S+ Cu CuS
11.设 为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下, 与足量 反应转移电子数为
B. 分子中含有 键的数目一定为
C.常温下, 中氢键数目为
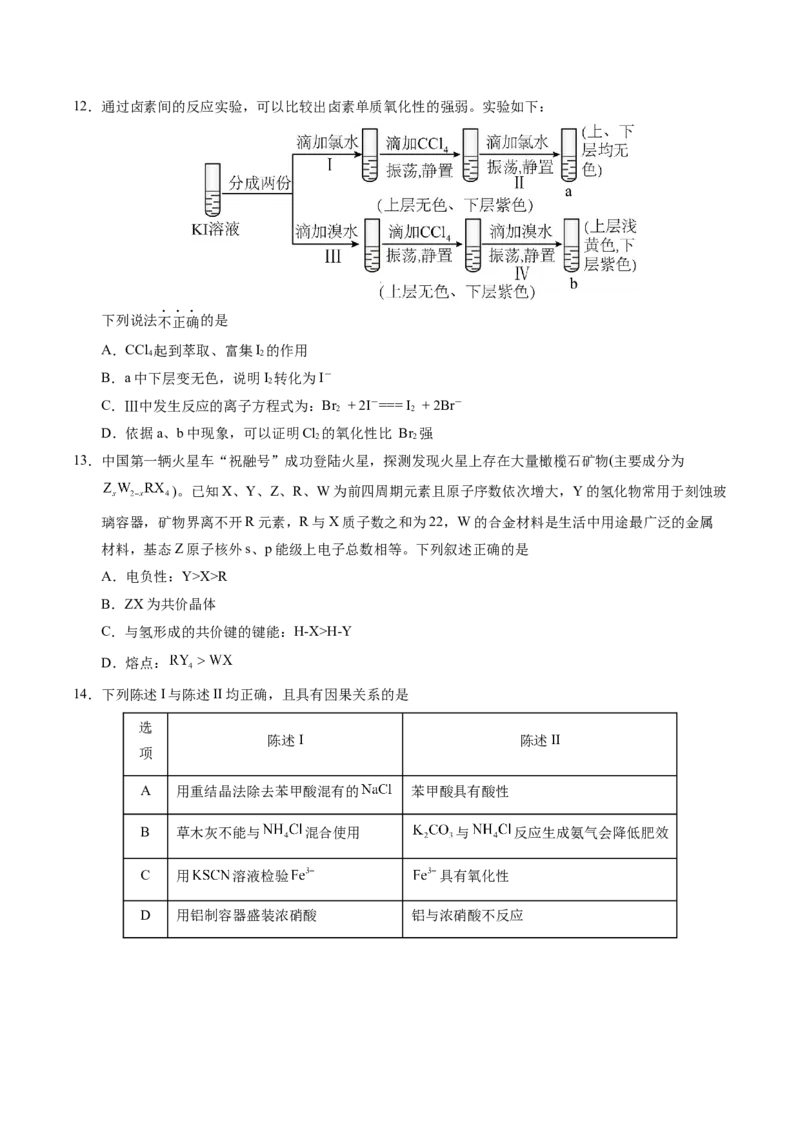
D. 的 溶液中 的数目为12.通过卤素间的反应实验,可以比较出卤素单质氧化性的强弱。实验如下:
下列说法不正确的是
A.CCl 起到萃取、富集I 的作用
4 2
B.a中下层变无色,说明I 转化为I-
2
C.Ⅲ中发生反应的离子方程式为:Br + 2I-=== I + 2Br-
2 2
D.依据a、b中现象,可以证明Cl 的氧化性比 Br 强
2 2
13.中国第一辆火星车“祝融号”成功登陆火星,探测发现火星上存在大量橄榄石矿物(主要成分为
)。已知X、Y、Z、R、W为前四周期元素且原子序数依次增大,Y的氢化物常用于刻蚀玻
璃容器,矿物界离不开R元素,R与X质子数之和为22,W的合金材料是生活中用途最广泛的金属
材料,基态Z原子核外s、p能级上电子总数相等。下列叙述正确的是
A.电负性:Y>X>R
B.ZX为共价晶体
C.与氢形成的共价键的键能:H-X>H-Y
D.熔点:
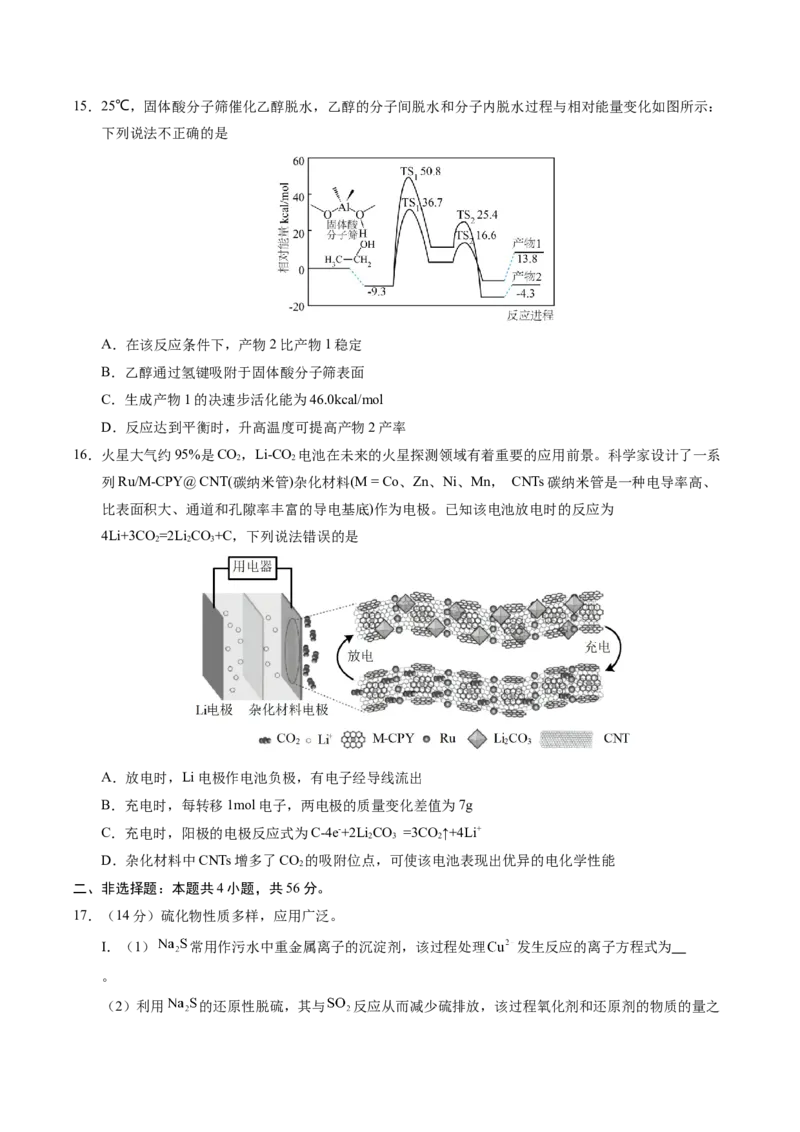
14.下列陈述I与陈述II均正确,且具有因果关系的是
选
陈述I 陈述II
项
A 用重结晶法除去苯甲酸混有的 苯甲酸具有酸性
B 草木灰不能与 混合使用 与 反应生成氨气会降低肥效
C 用 溶液检验 具有氧化性
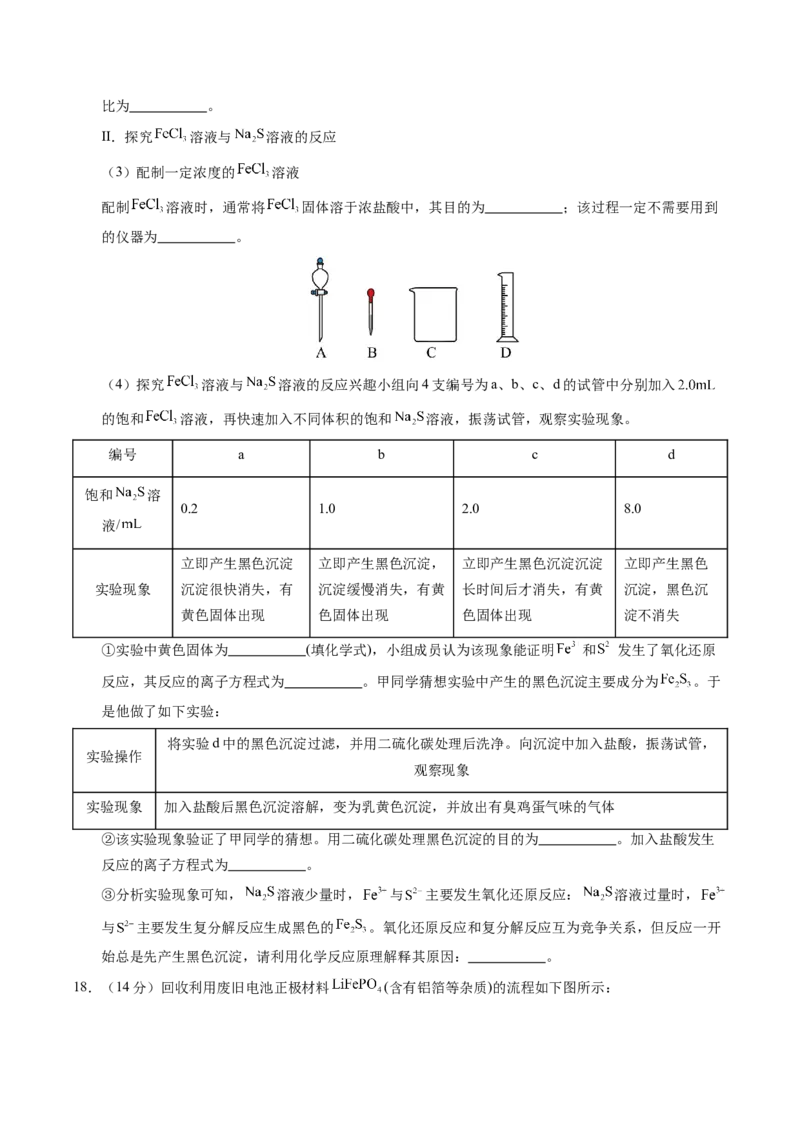
D 用铝制容器盛装浓硝酸 铝与浓硝酸不反应15.25℃,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对能量变化如图所示:
下列说法不正确的是
A.在该反应条件下,产物2比产物1稳定
B.乙醇通过氢键吸附于固体酸分子筛表面
C.生成产物1的决速步活化能为46.0kcal/mol
D.反应达到平衡时,升高温度可提高产物2产率
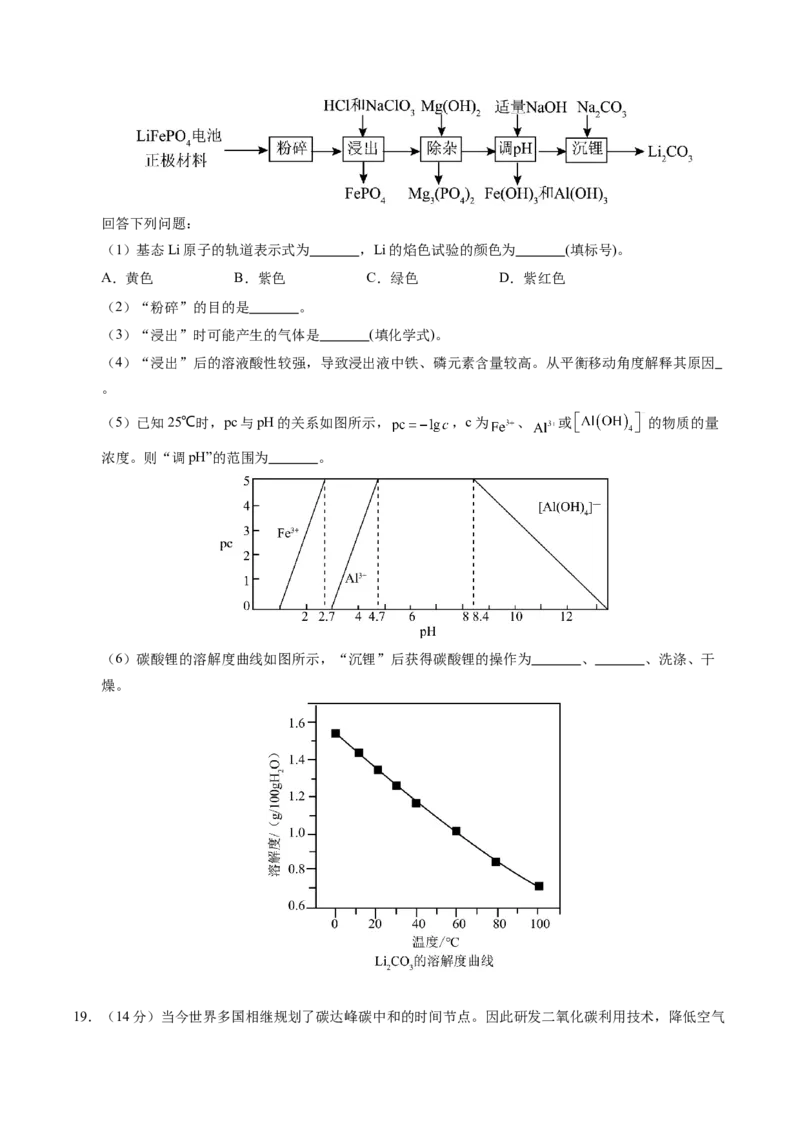
16.火星大气约95%是CO,Li-CO 电池在未来的火星探测领域有着重要的应用前景。科学家设计了一系
2 2
列Ru/M-CPY@ CNT(碳纳米管)杂化材料(M = Co、Zn、Ni、Mn, CNTs碳纳米管是一种电导率高、
比表面积大、通道和孔隙率丰富的导电基底)作为电极。已知该电池放电时的反应为
4Li+3CO=2Li CO+C,下列说法错误的是
2 2 3
A.放电时,Li电极作电池负极,有电子经导线流出
B.充电时,每转移1mol电子,两电极的质量变化差值为7g
C.充电时,阳极的电极反应式为C-4e-+2Li CO =3CO ↑+4Li+
2 3 2
D.杂化材料中CNTs增多了CO 的吸附位点,可使该电池表现出优异的电化学性能
2
二、非选择题:本题共4小题,共56分。
17.(14分)硫化物性质多样,应用广泛。
I.(1) 常用作污水中重金属离子的沉淀剂,该过程处理 发生反应的离子方程式为
。
(2)利用 的还原性脱硫,其与 反应从而减少硫排放,该过程氧化剂和还原剂的物质的量之比为 。
II.探究 溶液与 溶液的反应
(3)配制一定浓度的 溶液
配制 溶液时,通常将 固体溶于浓盐酸中,其目的为 ;该过程一定不需要用到
的仪器为 。
(4)探究 溶液与 溶液的反应兴趣小组向4支编号为a、b、c、d的试管中分别加入
的饱和 溶液,再快速加入不同体积的饱和 溶液,振荡试管,观察实验现象。
编号 a b c d
饱和 溶
0.2 1.0 2.0 8.0
液/
立即产生黑色沉淀 立即产生黑色沉淀, 立即产生黑色沉淀沉淀 立即产生黑色
实验现象 沉淀很快消失,有 沉淀缓慢消失,有黄 长时间后才消失,有黄 沉淀,黑色沉
黄色固体出现 色固体出现 色固体出现 淀不消失
①实验中黄色固体为 (填化学式),小组成员认为该现象能证明 和 发生了氧化还原
反应,其反应的离子方程式为 。甲同学猜想实验中产生的黑色沉淀主要成分为 。于
是他做了如下实验:
将实验d中的黑色沉淀过滤,并用二硫化碳处理后洗净。向沉淀中加入盐酸,振荡试管,
实验操作
观察现象
实验现象 加入盐酸后黑色沉淀溶解,变为乳黄色沉淀,并放出有臭鸡蛋气味的气体
②该实验现象验证了甲同学的猜想。用二硫化碳处理黑色沉淀的目的为 。加入盐酸发生
反应的离子方程式为 。
③分析实验现象可知, 溶液少量时, 与 主要发生氧化还原反应: 溶液过量时,
与 主要发生复分解反应生成黑色的 。氧化还原反应和复分解反应互为竞争关系,但反应一开
始总是先产生黑色沉淀,请利用化学反应原理解释其原因: 。
18.(14分)回收利用废旧电池正极材料 (含有铝箔等杂质)的流程如下图所示:回答下列问题:
(1)基态Li原子的轨道表示式为 ,Li的焰色试验的颜色为 (填标号)。
A.黄色 B.紫色 C.绿色 D.紫红色
(2)“粉碎”的目的是 。
(3)“浸出”时可能产生的气体是 (填化学式)。
(4)“浸出”后的溶液酸性较强,导致浸出液中铁、磷元素含量较高。从平衡移动角度解释其原因
。
(5)已知25℃时,pc与pH的关系如图所示, ,c为 、 或 的物质的量
浓度。则“调pH”的范围为 。
(6)碳酸锂的溶解度曲线如图所示,“沉锂”后获得碳酸锂的操作为 、 、洗涤、干
燥。
19.(14分)当今世界多国相继规划了碳达峰碳中和的时间节点。因此研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二二氧化碳。已知:
①
②
③
回答下列问题:
(1) 。
(2)在300℃恒压密闭容器中,加入2mol 和6mol ,发生上述反应。反应达平衡时, 的
转化率为75%,容器体积减小25%, 的物质的量为 mol。CO的物质的量为
mol。反应①的平衡常数 。
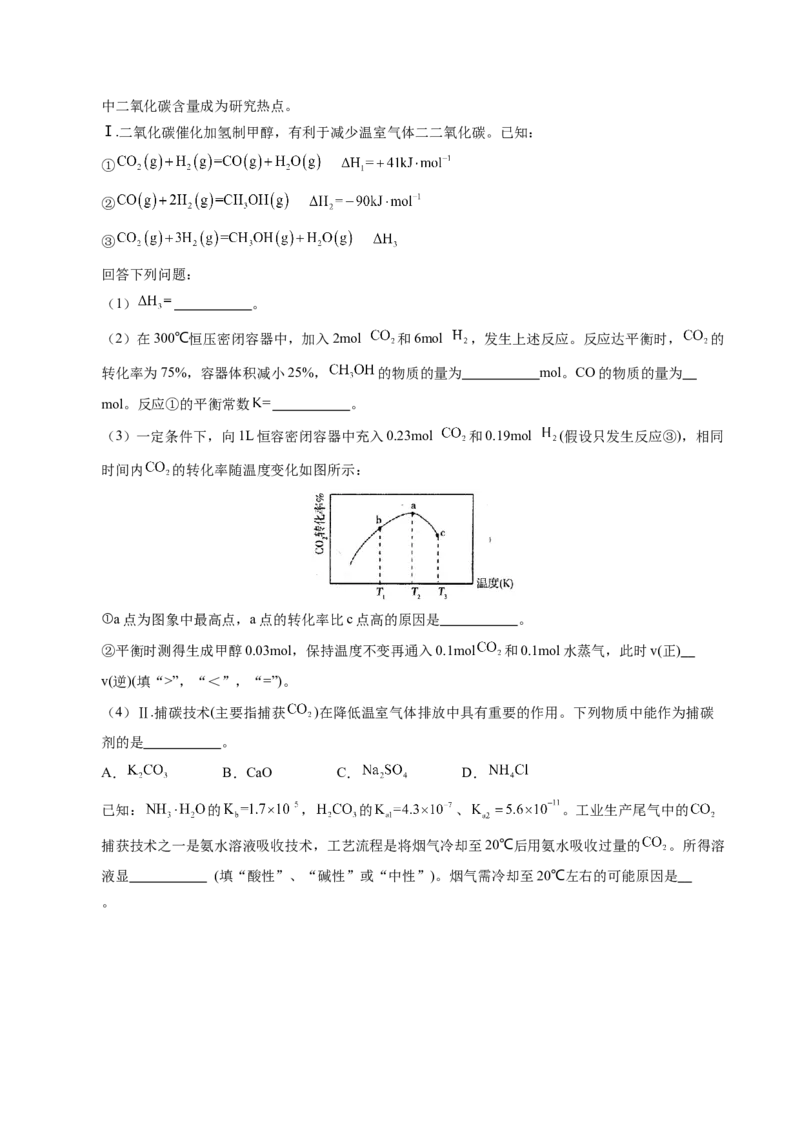
(3)一定条件下,向1L恒容密闭容器中充入0.23mol 和0.19mol (假设只发生反应③),相同
时间内 的转化率随温度变化如图所示:
①a点为图象中最高点,a点的转化率比c点高的原因是 。
②平衡时测得生成甲醇0.03mol,保持温度不变再通入0.1mol 和0.1mol水蒸气,此时v(正)
v(逆)(填“>”,“<”,“=”)。
(4)Ⅱ.捕碳技术(主要指捕获 )在降低温室气体排放中具有重要的作用。下列物质中能作为捕碳
剂的是 。
A. B.CaO C. D.
已知: 的 , 的 、 。工业生产尾气中的
捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至20℃后用氨水吸收过量的 。所得溶
液显 (填“酸性”、“碱性”或“中性”)。烟气需冷却至20℃左右的可能原因是
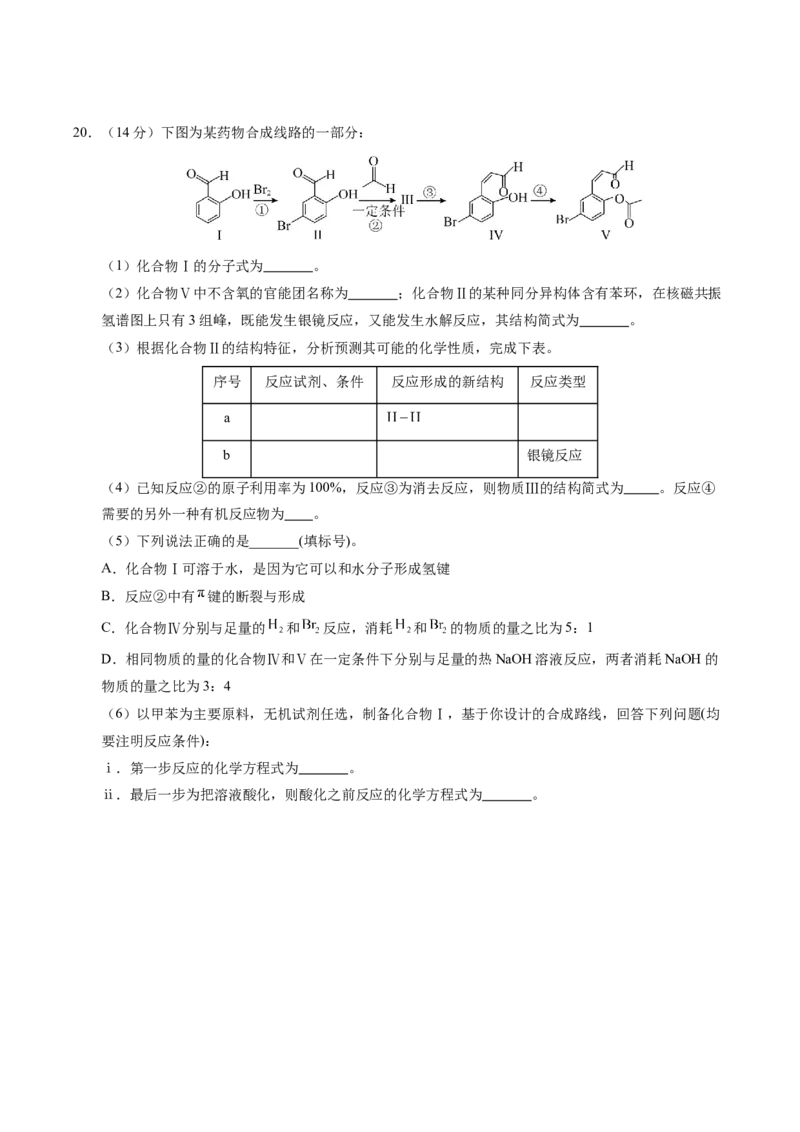
。20.(14分)下图为某药物合成线路的一部分:
(1)化合物Ⅰ的分子式为 。
(2)化合物Ⅴ中不含氧的官能团名称为 ;化合物Ⅱ的某种同分异构体含有苯环,在核磁共振
氢谱图上只有3组峰,既能发生银镜反应,又能发生水解反应,其结构简式为 。
(3)根据化合物Ⅱ的结构特征,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
a
b 银镜反应
(4)已知反应②的原子利用率为100%,反应③为消去反应,则物质Ⅲ的结构简式为 。反应④
需要的另外一种有机反应物为 。
(5)下列说法正确的是_______(填标号)。
A.化合物Ⅰ可溶于水,是因为它可以和水分子形成氢键
B.反应②中有 键的断裂与形成
C.化合物Ⅳ分别与足量的 和 反应,消耗 和 的物质的量之比为5:1
D.相同物质的量的化合物Ⅳ和Ⅴ在一定条件下分别与足量的热NaOH溶液反应,两者消耗NaOH的
物质的量之比为3:4
(6)以甲苯为主要原料,无机试剂任选,制备化合物Ⅰ,基于你设计的合成路线,回答下列问题(均
要注明反应条件):
ⅰ.第一步反应的化学方程式为 。
ⅱ.最后一步为把溶液酸化,则酸化之前反应的化学方程式为 。