文档内容
绝密★启用前
2025 年高考考前信息必刷卷 03(黑吉辽蒙专用)
化 学
考情速递
高考·新动向:2025年由吉林省自主命题,黑吉辽蒙使用相同试卷。参照2024年高考真题,单项选择
题有15小题,每小题3分,共45分;非选择题4小题,共55分。
高考·新考法:2025年高考化学题型丰富,每道题的不同选项考察不同方向的内容,要求考生做到厚积
薄发,全面学习。
高考·新情境:以教材的方程式或拓展等内容作为情境,要求学生熟悉教材中的信息,比如:水合离子
的图片、三价铁与碘离子的反应、硫酸工艺等,都是以必修教材中常见物质的制备、流程、实验探究
等相关内容为情境,考察学生温故知新的能力。
命题·大预测:基于2025年2月全国各地市最新模考题,预测黑吉辽蒙高考试题信息会出现教材常见的
反应。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Cl 35.5
一、选择题:本题共15小题,每小题3分,共45分。每小题只有一个选项符合题目要求。
1.化学与职业息息相关,下列对于化学相关职业的理解不正确的是
A.电池研发与生产、生活和军事等领域的发展密切相关,研发人员的工作只需要研究电池的材料构成
B.现代高分子三大合成材料为塑料、合成纤维和合成橡胶,此外黏合剂、涂料、高吸水性树脂、高分
子膜等也属于高分子材料
C.化工工程师的主要工作是设计化工生产的工艺流程,并监控生产过程,及时解决生产中遇到的技术
问题
D.环境保护工程师的主要工作是预防和治理环境污染;原子利用率100%符合绿色化学思想
2.下列化学用语或图示正确的是
A.甲醛的电子式为B.NaCl溶液中的水合离子为
C.苯胺 的所有原子共平面
D.乙烯分子中π键的形成过程
3.已知反应:①l0lkPa时,2C(s)+O(g)=2CO(g) △H=-221kJ/mol
2
②稀溶液中,H+(aq)+OH-(aq)=H O(1) △H=-57.3kJ/mol
2
③红磷的化学式为P,白磷的化学式为P,已知
4
P(s)+5O(g)=P O (s) △H=-3093.5kJ/mol
4 2 4 10
4P(s)+5O (g)=P O (s) △H=-2954.0kJ/mol。下列结论正确的是
2 4 10
A.由于红磷转化为白磷是放热反应,等质量的红磷能量比白磷低
B.36.5gHCl的稀溶液与含N 个NH 的稀溶液反应放出的热量为57.3kJ
A 3
C.lmol稀硫酸与足量浓NaOH溶液反应的中和热为57.3kJ
D.碳的燃烧热大于110.5kJ/mol
4.高铜酸钾( )是一种难溶于水的黑色粉末状固体(其中氧元素的化合价为 价),与高铁酸钾(
)性质相似,可以由四羟基合铜酸钾和次溴酸在冰水浴中合成:①
(未配平)。高铜酸钾在酸性条件下不稳定:②
(未配平)。下列说法错误的是
A.①中还原剂和氧化剂的数量之比为
B.①反应中,HBrO过量更有利于反应发生
C.②中 既表现氧化性,又表现还原性
D.由①、②可知氧化性强弱顺序为
5.下列各组溶液中的两个反应,可用同一个离子反应表示的是
A.NaOH和 NaOH和HCl B. 和 、 和
C. 和 和 D. 和 和
6.白色固体样品X,可能含 和 之中的一种或两种。在
三个烧杯中各加入适量X,进行实验(必要时微热,使之充分反应),实验记录如下:
编
操作 现象
号加水溶解,用洁净的铂丝蘸取少许溶液,在煤气灯外焰上灼
I 焰色呈黄色
烧
Ⅱ 加入蒸馏水 固体全部溶解,得到透明溶液
产生浅黄色沉淀和刺激性气味的气
Ⅲ 加入稀硫酸
体
依据实验现象,下列说法错误的是
A.X可能是
B.X不可能含 或
C.X可能是 和 的混合物
D.X可能是 和 的混合物
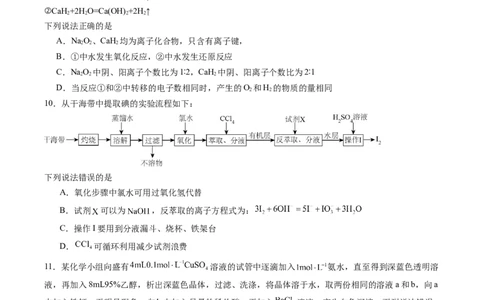
7.为探讨化学平衡移动的影响因素,某同学通过改变浓度研究“2Fe3+ +2I- 2Fe2+ +I ”反应中Fe3+和
2
Fe2+的相互转化。实验过程中的主要现象如图所示:
下列相关的说法不正确的是
A.待实验I溶液颜色不再改变时,才能进行实验II
B.实验③是实验②的对比实验
C.实验①和实验②中平衡都向Fe2+转化成Fe3+方向移动
D.上述实验表明,实验I所得溶液颜色主要是由Fe3+引起的
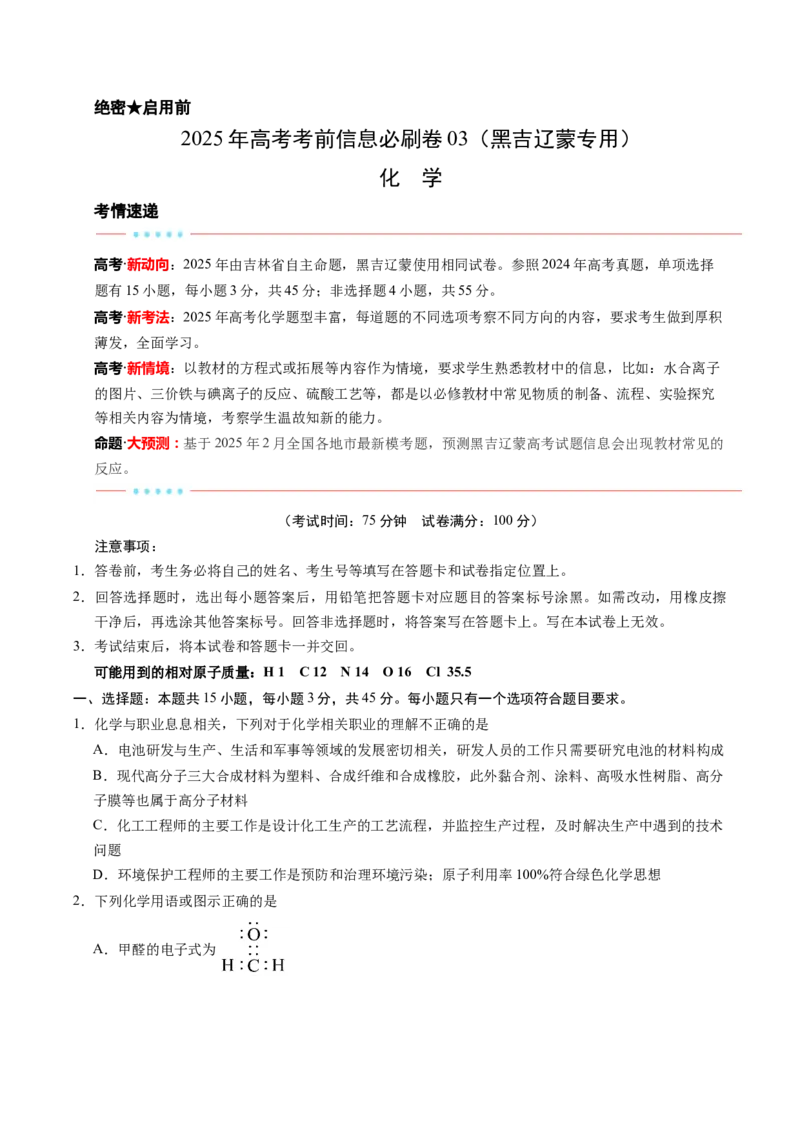
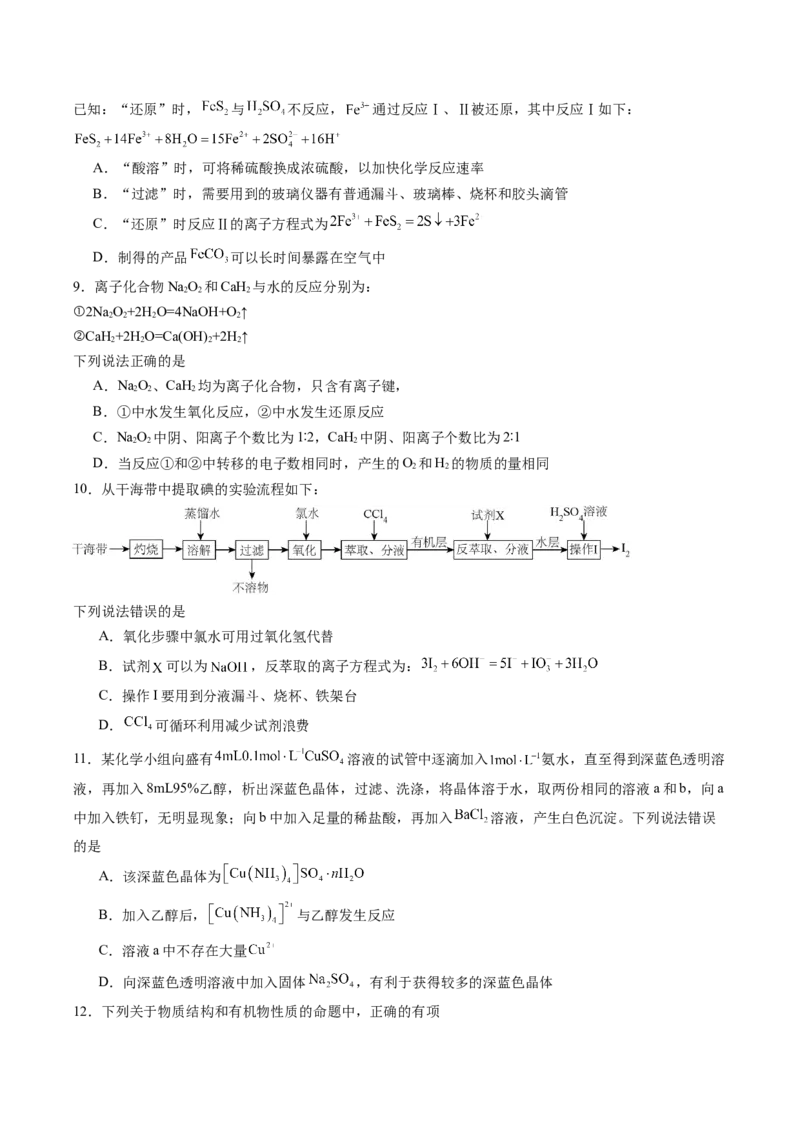
8.工业上可以利用硫酸厂产生的烧渣(主要成分含 、FeO还有一定量的 )制备碳酸亚铁的工艺流
程如图所示,下列说法正确的是已知:“还原”时, 与 不反应, 通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ如下:
A.“酸溶”时,可将稀硫酸换成浓硫酸,以加快化学反应速率
B.“过滤”时,需要用到的玻璃仪器有普通漏斗、玻璃棒、烧杯和胶头滴管
C.“还原”时反应Ⅱ的离子方程式为
D.制得的产品 可以长时间暴露在空气中
9.离子化合物NaO 和CaH 与水的反应分别为:
2 2 2
①2Na O+2H O=4NaOH+O ↑
2 2 2 2
②CaH+2H O=Ca(OH) +2H ↑
2 2 2 2
下列说法正确的是
A.NaO、CaH 均为离子化合物,只含有离子键,
2 2 2
B.①中水发生氧化反应,②中水发生还原反应
C.NaO 中阴、阳离子个数比为1∶2,CaH 中阴、阳离子个数比为2∶1
2 2 2
D.当反应①和②中转移的电子数相同时,产生的O 和H 的物质的量相同
2 2
10.从干海带中提取碘的实验流程如下:
下列说法错误的是
A.氧化步骤中氯水可用过氧化氢代替
B.试剂 可以为 ,反萃取的离子方程式为:
C.操作I要用到分液漏斗、烧杯、铁架台
D. 可循环利用减少试剂浪费
11.某化学小组向盛有 溶液的试管中逐滴加入 氨水,直至得到深蓝色透明溶
液,再加入8mL95%乙醇,析出深蓝色晶体,过滤、洗涤,将晶体溶于水,取两份相同的溶液a和b,向a
中加入铁钉,无明显现象;向b中加入足量的稀盐酸,再加入 溶液,产生白色沉淀。下列说法错误
的是
A.该深蓝色晶体为
B.加入乙醇后, 与乙醇发生反应
C.溶液a中不存在大量
D.向深蓝色透明溶液中加入固体 ,有利于获得较多的深蓝色晶体
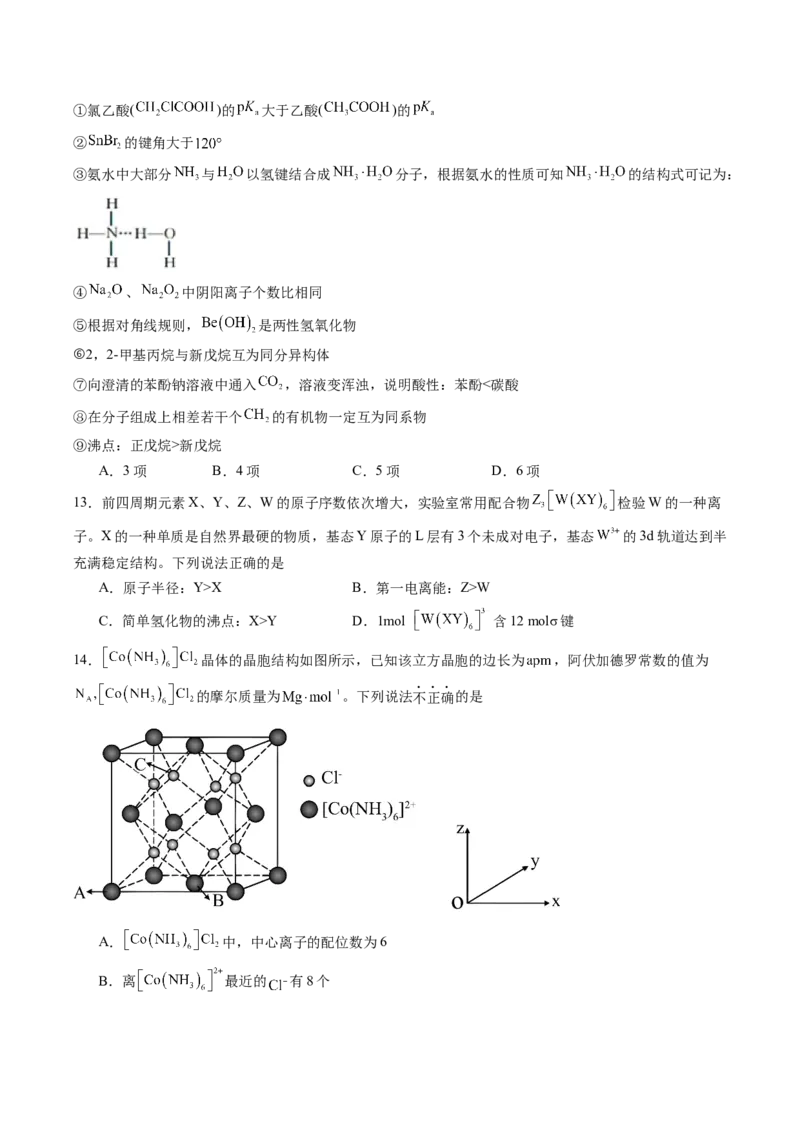
12.下列关于物质结构和有机物性质的命题中,正确的有项①氯乙酸( )的 大于乙酸( )的
② 的键角大于
③氨水中大部分 与 以氢键结合成 分子,根据氨水的性质可知 的结构式可记为:
④ 、 中阴阳离子个数比相同
⑤根据对角线规则, 是两性氢氧化物
⑥2,2-甲基丙烷与新戊烷互为同分异构体
⑦向澄清的苯酚钠溶液中通入 ,溶液变浑浊,说明酸性:苯酚<碳酸
⑧在分子组成上相差若干个 的有机物一定互为同系物
⑨沸点:正戊烷>新戊烷
A.3项 B.4项 C.5项 D.6项
13.前四周期元素X、Y、Z、W的原子序数依次增大,实验室常用配合物 检验W的一种离
子。X的一种单质是自然界最硬的物质,基态Y原子的L层有3个未成对电子,基态 的3d轨道达到半
充满稳定结构。下列说法正确的是
A.原子半径:Y>X B.第一电离能:Z>W
C.简单氢化物的沸点:X>Y D.1mol 含12 molσ键
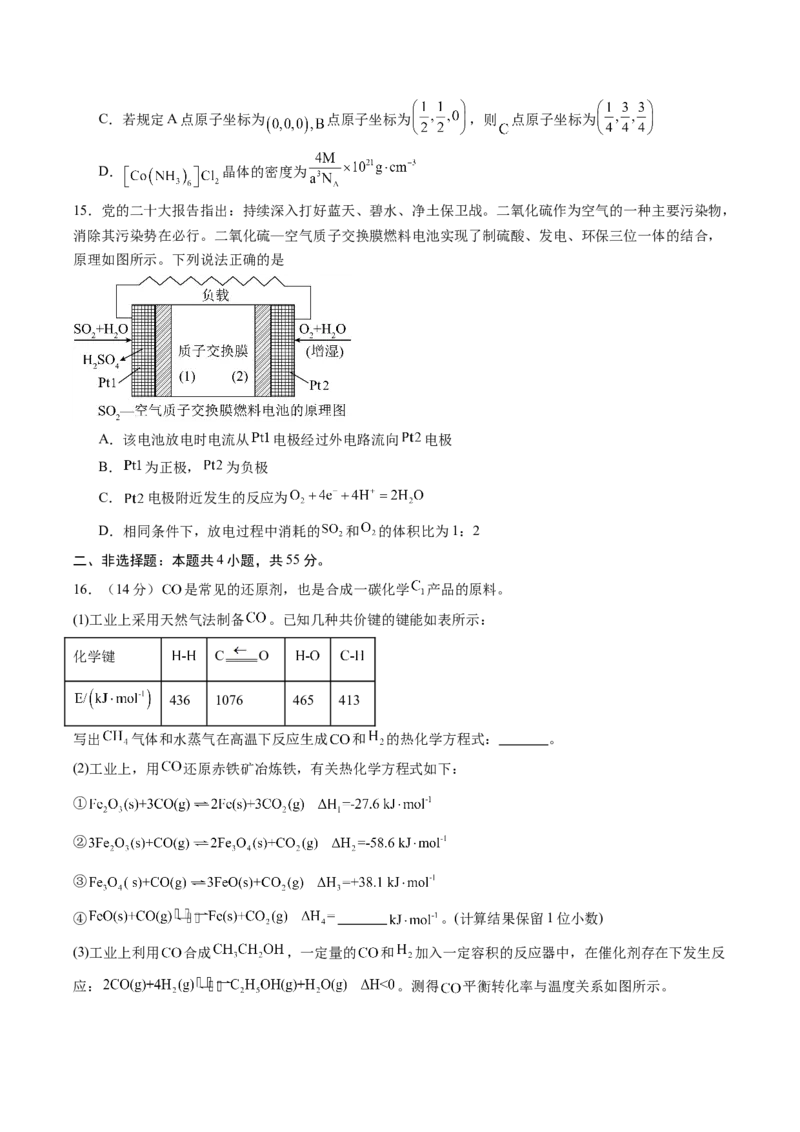
14. 晶体的晶胞结构如图所示,已知该立方晶胞的边长为 ,阿伏加德罗常数的值为
的摩尔质量为 。下列说法不正确的是
A. 中,中心离子的配位数为6
B.离 最近的 有8个C.若规定A点原子坐标为 点原子坐标为 ,则 点原子坐标为
D. 晶体的密度为
15.党的二十大报告指出:持续深入打好蓝天、碧水、净土保卫战。二氧化硫作为空气的一种主要污染物,
消除其污染势在必行。二氧化硫—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,
原理如图所示。下列说法正确的是
A.该电池放电时电流从 电极经过外电路流向 电极
B. 为正极, 为负极
C. 电极附近发生的反应为
D.相同条件下,放电过程中消耗的 和 的体积比为1:2
二、非选择题:本题共4小题,共55分。
16.(14分) 是常见的还原剂,也是合成一碳化学 产品的原料。
(1)工业上采用天然气法制备 。已知几种共价键的键能如表所示:
化学键 C O
436 1076 465 413
写出 气体和水蒸气在高温下反应生成 和 的热化学方程式: 。
(2)工业上,用 还原赤铁矿冶炼铁,有关热化学方程式如下:
①
②
③
④ 。(计算结果保留1位小数)
(3)工业上利用 合成 ,一定量的 和 加入一定容积的反应器中,在催化剂存在下发生反
应: 。测得 平衡转化率与温度关系如图所示。①温度升高, 平衡转化率降低,其主要原因是 。
② (填“>”、“<”或“=”)。
(4)工业上,常用 处理 ,在催化剂存在条件下发生反应:2 。
在体积相等的甲、乙两个密闭容器中分别充入 、 气体,在恒温恒容、绝热恒容下分别
发生上述反应。测得气体压强与时间关系如图所示。
①容器 (填“甲”或“乙”)在恒温恒容条件下反应。
②气体总物质的量:a b(填“>”“<”或“=”)。
③b点平衡常数 (填“>”“<”或“=”) 。提示:用分压计算的平衡常数为 ,分压等于总
压×物质的量分数。
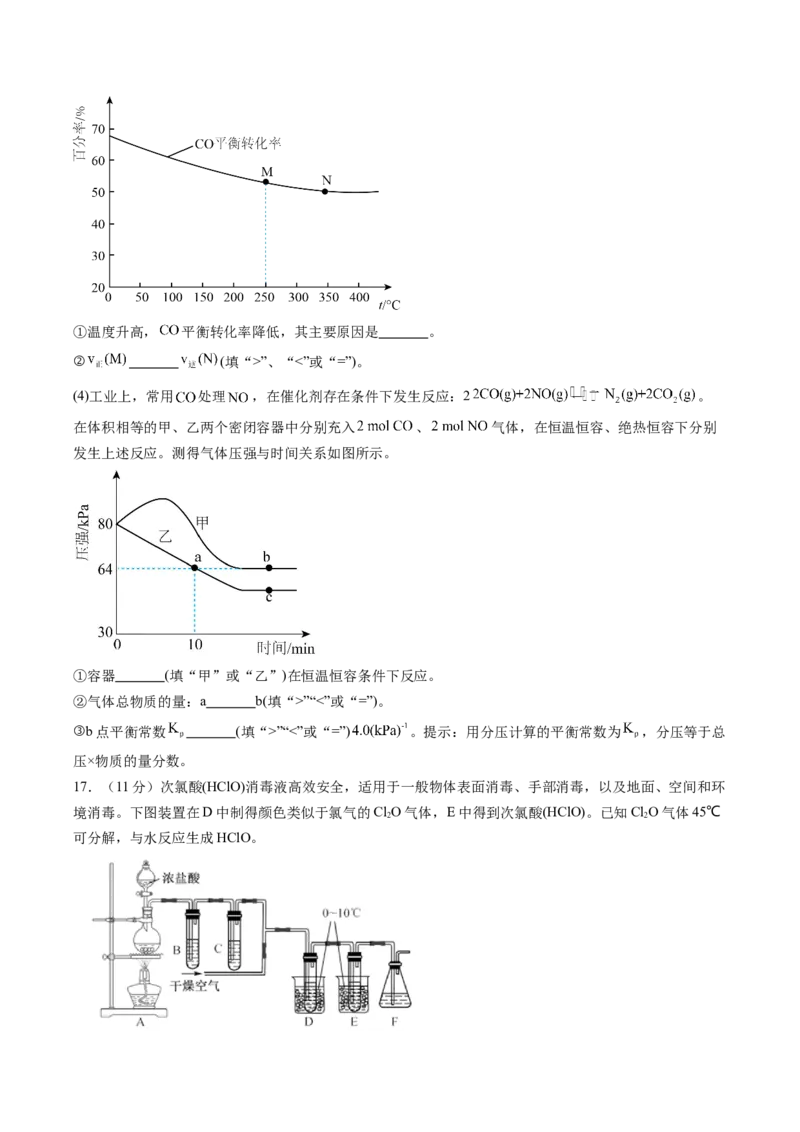
17.(11分)次氯酸(HClO)消毒液高效安全,适用于一般物体表面消毒、手部消毒,以及地面、空间和环
境消毒。下图装置在D中制得颜色类似于氯气的ClO气体,E中得到次氯酸(HClO)。已知ClO气体45℃
2 2
可分解,与水反应生成HClO。(1)A装置中发生的反应为 。
(2)B装置、F装置中分别盛装 、 ;C的作用是 。
(3)实验时,一直要通入干燥的空气,其体积大约是氯气的3倍,主要作用是 ,同时还可以抑
制ClO的分解,保证实验安全。
2
(4)D中盛装含水碳酸钠(即NaCO 与水按照质量106:9调制而成),用来吸收氯气制备ClO。
2 3 2
①如果用NaCO·xH O表示含水碳酸钠,则x为 。
2 3 2
②D中生成的气体中含有CO,则生成ClO的化学方程式为 。
2 2
18.(16分)某化学实验小组用酸性KMnO 溶液与草酸(H C O)溶液反应,研究外界条件对反应速率的影
4 2 2 4
响,实验操作及现象如下:
编
实验操作 实验现象
号
向一支试管中先加入1 mL0.01 mol/L酸性KMnO 溶液,再 前10 min内溶液紫色无明显变化,
4
Ⅰ 加入1滴3 mol/L硫酸和9滴蒸馏水,最后加入1 mL0.1 后颜色逐渐变浅,30 min后几乎变
mol/L草酸溶液 为无色
向另一支试管中先加入1 mL0.01 mol/L酸性KMnO 溶液, 1 min内溶液紫色无明显变化,后
4
Ⅱ 再加入10滴3mol/L硫酸,最后加入1 mL0.1 mol/L草酸溶 颜色迅速变浅,约3 min后几乎变
液 为无色
(1)写出高锰酸钾与草酸反应的离子方程式: 。
(2)由实验Ⅰ、Ⅱ可得出的结论是 。
(3)关于实验Ⅱ中3 min后溶液颜色迅速变浅的原因,该小组提出猜想: 。并设计实验Ⅲ,验证
猜想:向试管中先加入1 mL0.01 mol/L酸性KMnO 溶液,再加10滴3mol/L硫酸,加入少量MnSO 固体,
4 4
最后加入1 mL0.1 mol/L草酸溶液。
(4)草酸是乙二酸的俗称,在工业上有重要用途。下图流程表示其部分转化关系。
已知:
①X是具有六元环状结构的碳氧化合物,C、O原子均满足8电子结构。写出X的结构式 。
②下列说法正确的是 。
A.X是一种酸性氧化物B.由途径Ⅱ可知,草酸钙不溶于稀盐酸
C.乙二酸的酸性比乙酸强D.乙二酸跟足量乙醇反应生成乙二酸乙二酯
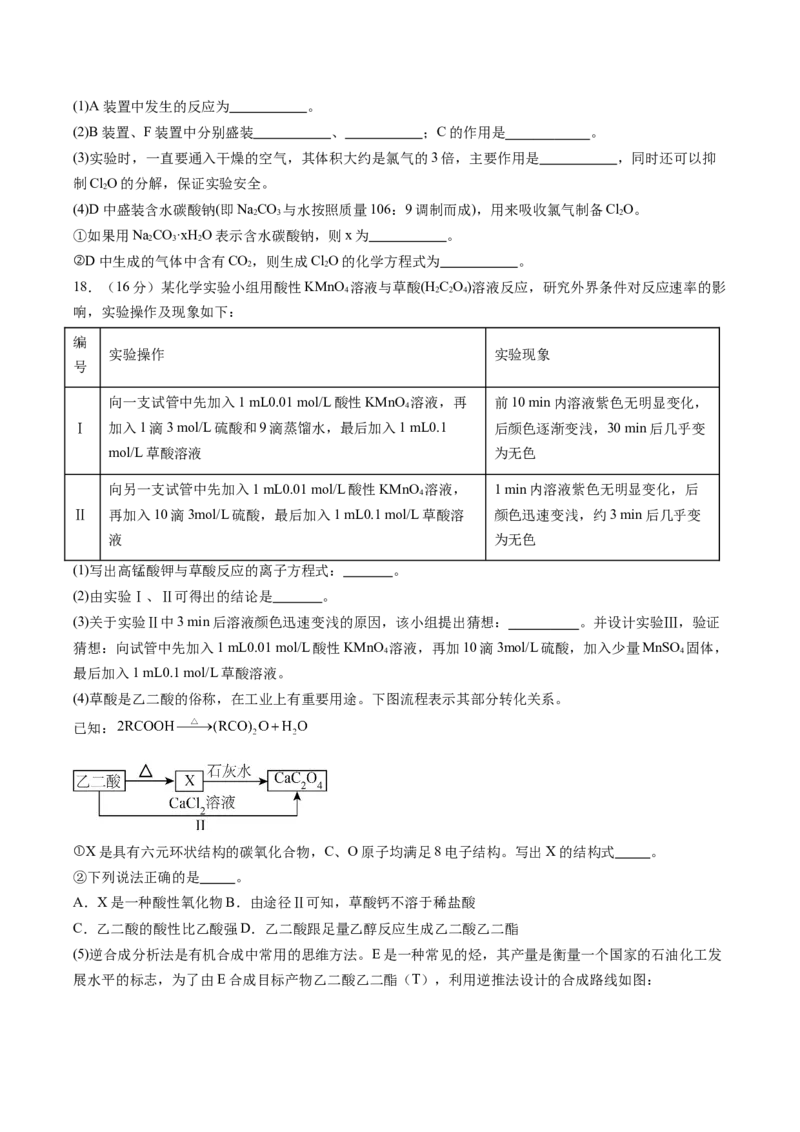
(5)逆合成分析法是有机合成中常用的思维方法。E是一种常见的烃,其产量是衡量一个国家的石油化工发
展水平的标志,为了由E合成目标产物乙二酸乙二酯(T),利用逆推法设计的合成路线如图:。
已知:①图1所示为有机物B的质谱图;
②有机物B的核磁共振氢谱图如图2所示,其面积比为1:2。
请回答下列问题:
①A与B反应生成T的化学方程式为 。
②C分子中的官能团名称为 ,由D生成B的反应类型为 。
③设计由原料E合成草酸的路线(其他试剂任选)。
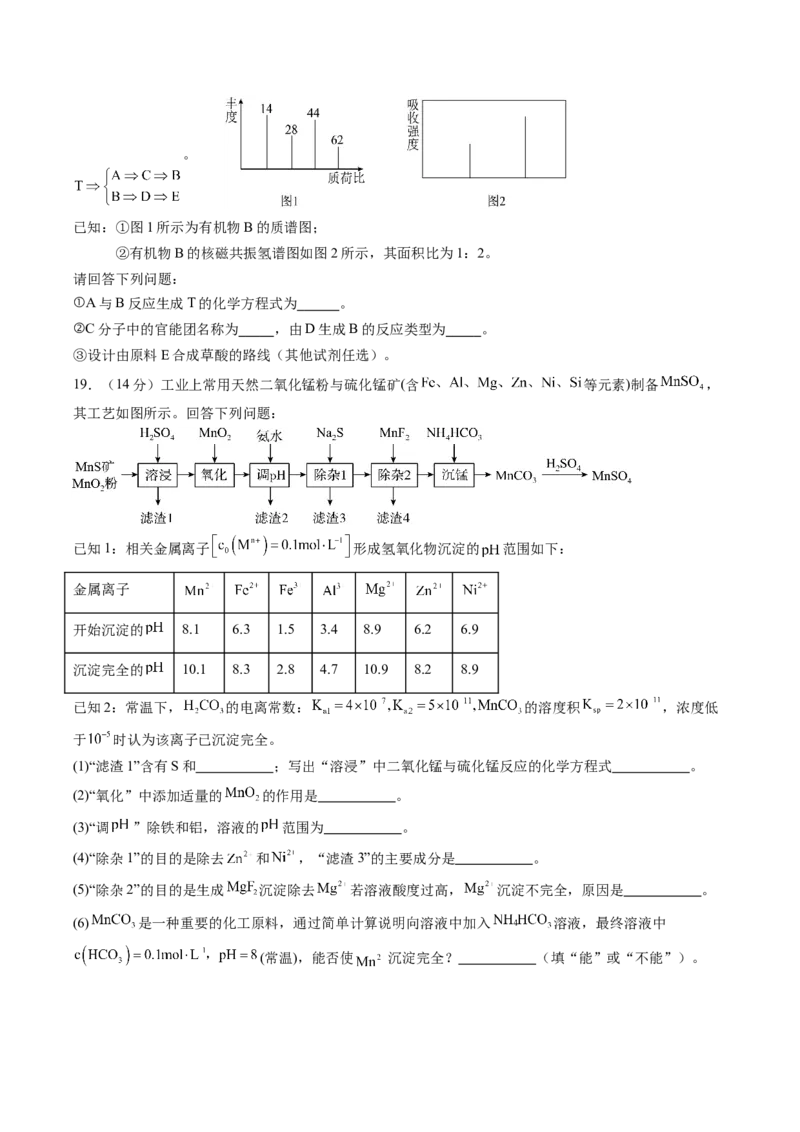
19.(14分)工业上常用天然二氧化锰粉与硫化锰矿(含 等元素)制备 ,
其工艺如图所示。回答下列问题:
已知1:相关金属离子 形成氢氧化物沉淀的 范围如下:
金属离子
开始沉淀的 8.1 6.3 1.5 3.4 8.9 6.2 6.9
沉淀完全的 10.1 8.3 2.8 4.7 10.9 8.2 8.9
已知2:常温下, 的电离常数: 的溶度积 ,浓度低
于 时认为该离子已沉淀完全。
(1)“滤渣1”含有S和 ;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式 。
(2)“氧化”中添加适量的 的作用是 。
(3)“调 ”除铁和铝,溶液的 范围为 。
(4)“除杂1”的目的是除去 和 ,“滤渣3”的主要成分是 。
(5)“除杂2”的目的是生成 沉淀除去 若溶液酸度过高, 沉淀不完全,原因是 。
(6) 是一种重要的化工原料,通过简单计算说明向溶液中加入 溶液,最终溶液中
(常温),能否使 沉淀完全? (填“能”或“不能”)。