文档内容
选择题标准练(九)
1.(2024·陕西渭南质检一)2023年10月26日11时14分,神舟十七号载人飞船点火升空成功发射,我
国航天航空事业再次迎来飞速发展。下列有关说法错误的是( )
A.太阳电池翼采用的碳纤维框架和玻璃纤维框架均为无机非金属材料
B.返回舱降落回收过程中使用了芳纶制作的降落伞,芳纶是有机高分子材料
C.飞船舱体外壳部件材料是铝合金材料制成的,主要是利用了其密度大、硬度大的特性
D.新型火箭燃料煤基航天煤油主要由不同馏分的烷烃、芳香烃和烯烃类的碳氢化合物组成
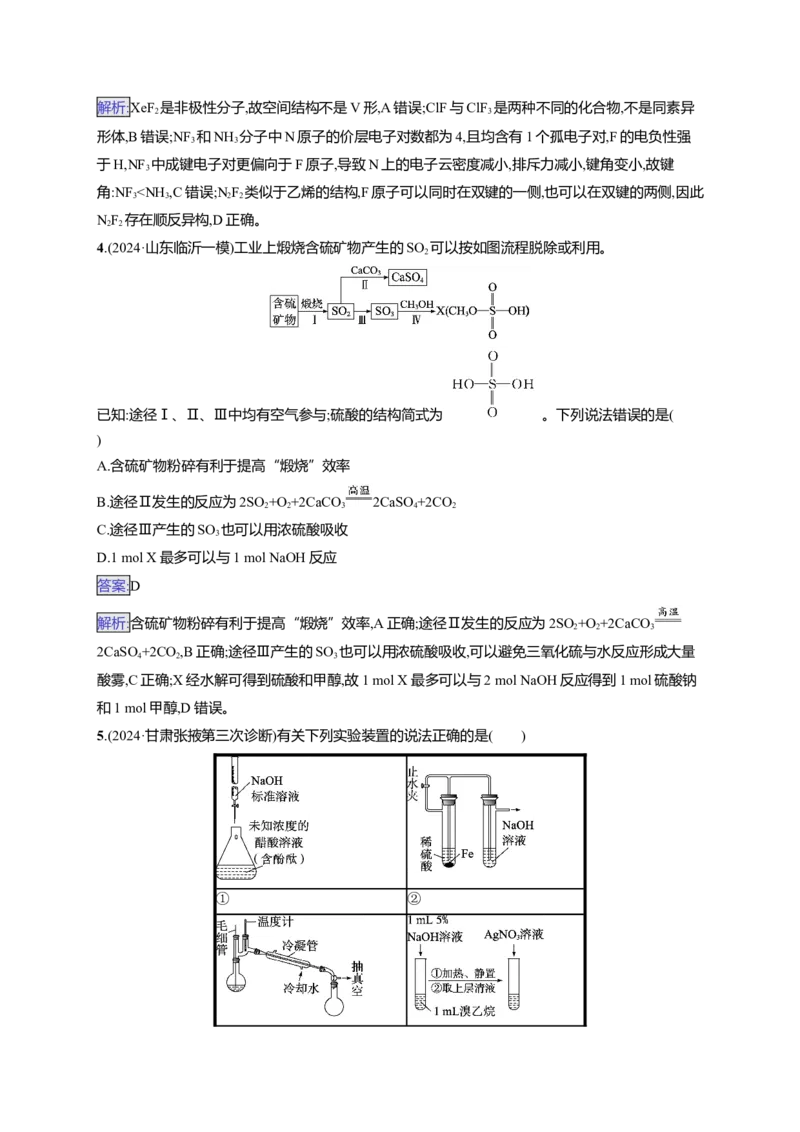
2.(2024·甘肃张掖第三次诊断)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.10 g立方氮化硼晶体所含原子数目为N
A
B.1 L pH=1的HSO 与(NH )SO 混合溶液中,H+数目为0.1N
2 4 4 2 4 A
C.含4 mol Si—O键的SiO 晶体中氧原子数目为N
2 A
D.标准状况下,22.4 L NO 的分子数目为N
2 A
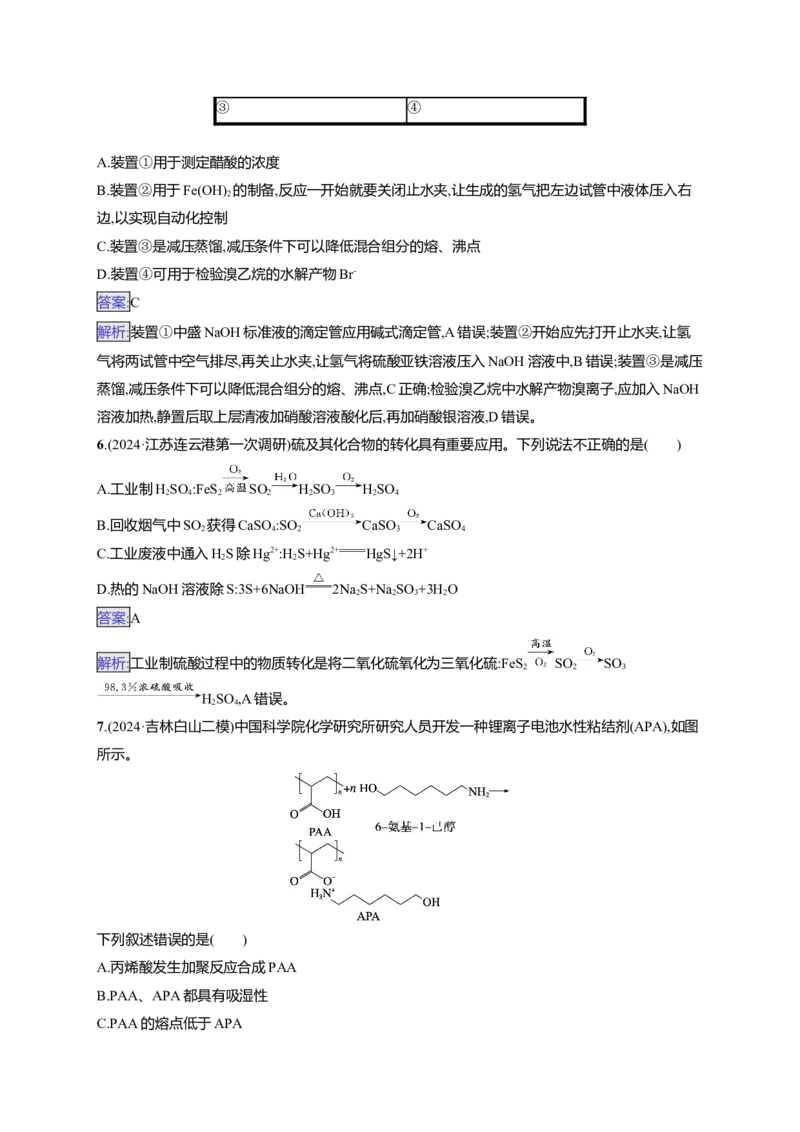
3.(2024·江苏泰州一模)氟是已知元素中电负性最大、单质氧化性最强的元素,与稀有气体Xe形成的
XeF 分子是非极性分子,与其他卤素形成的卤素互化物(如ClF、ClF )具有与Cl 相似的化学性质,与
2 3 2
氮形成的NF 可与NH 反应生成NF(结构式:
3 3 2 2
F—N N—F)。自然界中,含氟矿石有萤石(CaF )、冰晶石(Na AlF)等,萤石可与浓硫酸共热制取HF
2 3 6
气体。工业上,可通过电解KF的无水HF溶液(含F-和HF-
)制取F。下列有关说法正确的是( )
2 2
A.XeF 的空间结构为V形
2
B.ClF与ClF 互为同素异形体
3
C.键角:NF>NH
3 3
D.NF 存在顺反异构现象
2 2
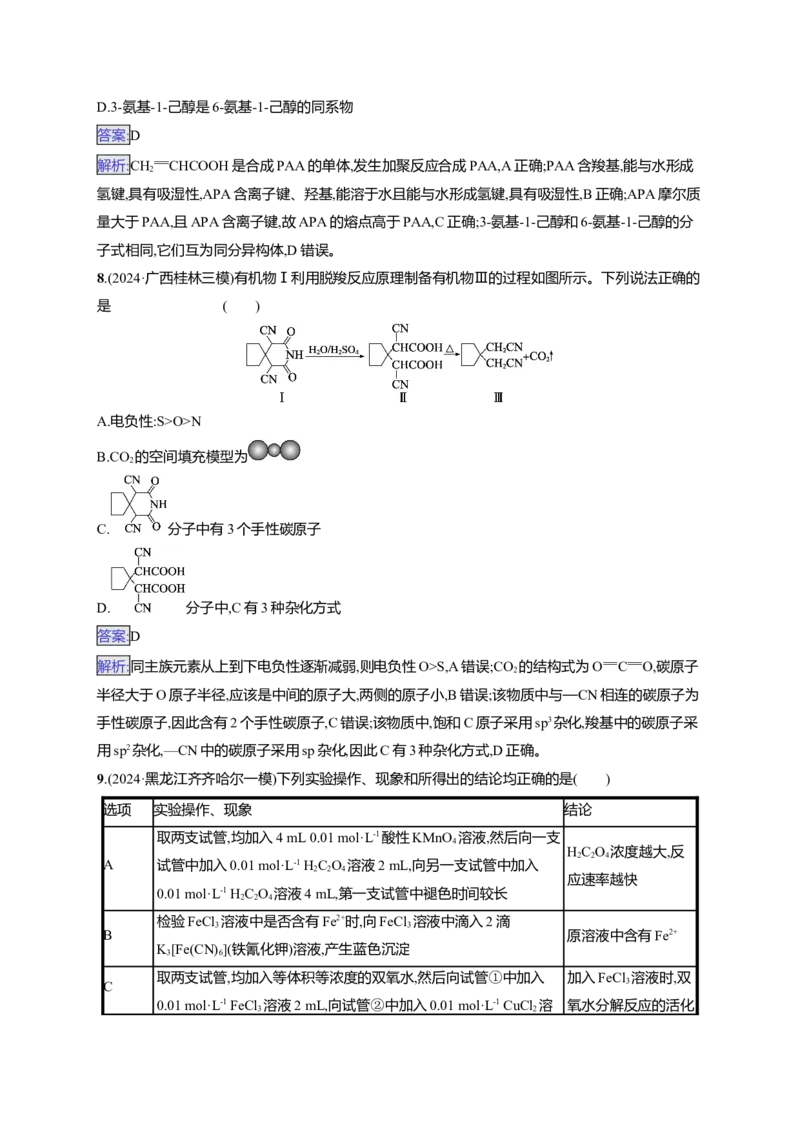
4.(2024·山东临沂一模)工业上煅烧含硫矿物产生的SO 可以按如图流程脱除或利用。
2已知:途径Ⅰ、Ⅱ、Ⅲ中均有空气参与;硫酸的结构简式为 。下列说法错误的是(
)
A.含硫矿物粉碎有利于提高“煅烧”效率
B.途径Ⅱ发生的反应为2SO +O +2CaCO 2CaSO+2CO
2 2 3 4 2
C.途径Ⅲ产生的SO 也可以用浓硫酸吸收
3
D.1 mol X最多可以与1 mol NaOH反应
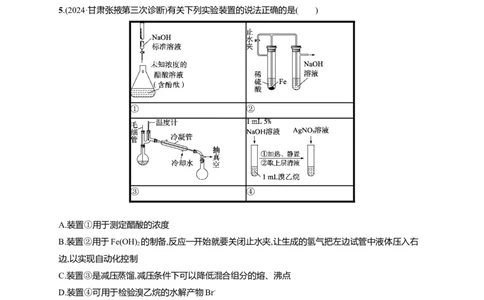
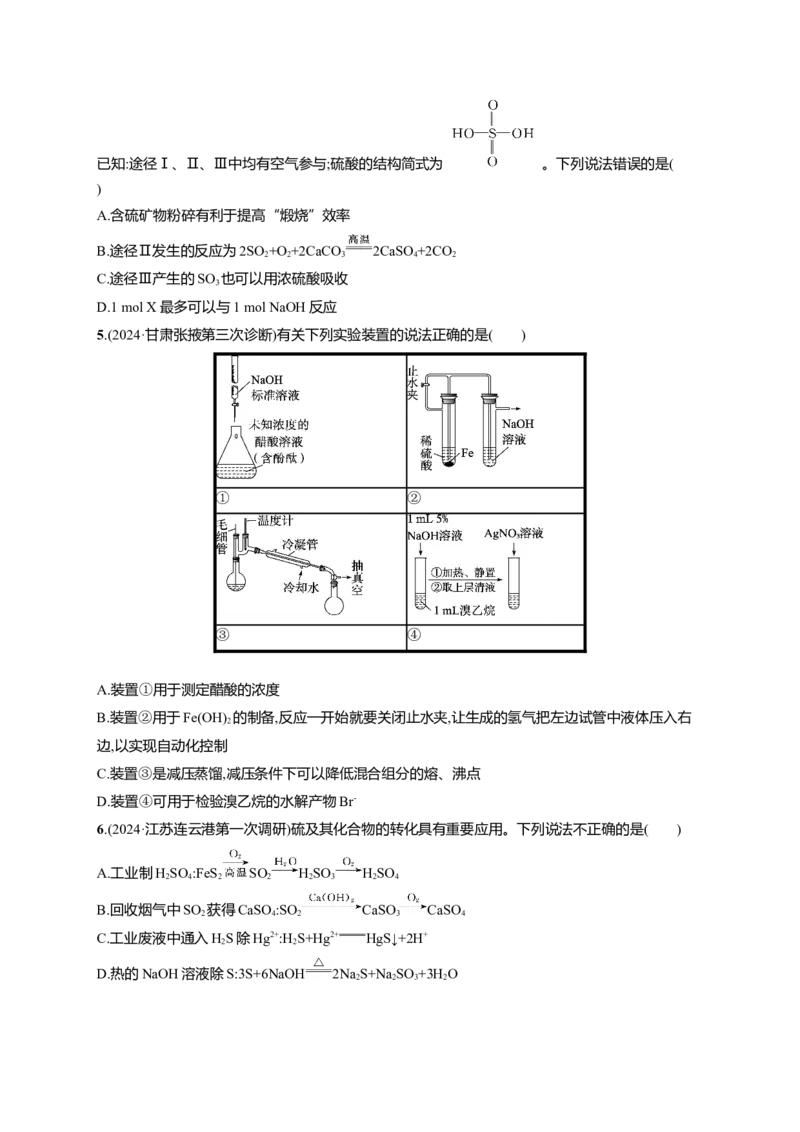
5.(2024·甘肃张掖第三次诊断)有关下列实验装置的说法正确的是( )
① ②
③ ④
A.装置①用于测定醋酸的浓度
B.装置②用于Fe(OH) 的制备,反应一开始就要关闭止水夹,让生成的氢气把左边试管中液体压入右
2
边,以实现自动化控制
C.装置③是减压蒸馏,减压条件下可以降低混合组分的熔、沸点
D.装置④可用于检验溴乙烷的水解产物Br-
6.(2024·江苏连云港第一次调研)硫及其化合物的转化具有重要应用。下列说法不正确的是( )
A.工业制HSO :FeS SO HSO HSO
2 4 2 2 2 3 2 4
B.回收烟气中SO 获得CaSO:SO CaSO CaSO
2 4 2 3 4
C.工业废液中通入HS除Hg2+:H S+Hg2+ HgS↓+2H+
2 2
D.热的NaOH溶液除S:3S+6NaOH 2NaS+Na SO +3H O
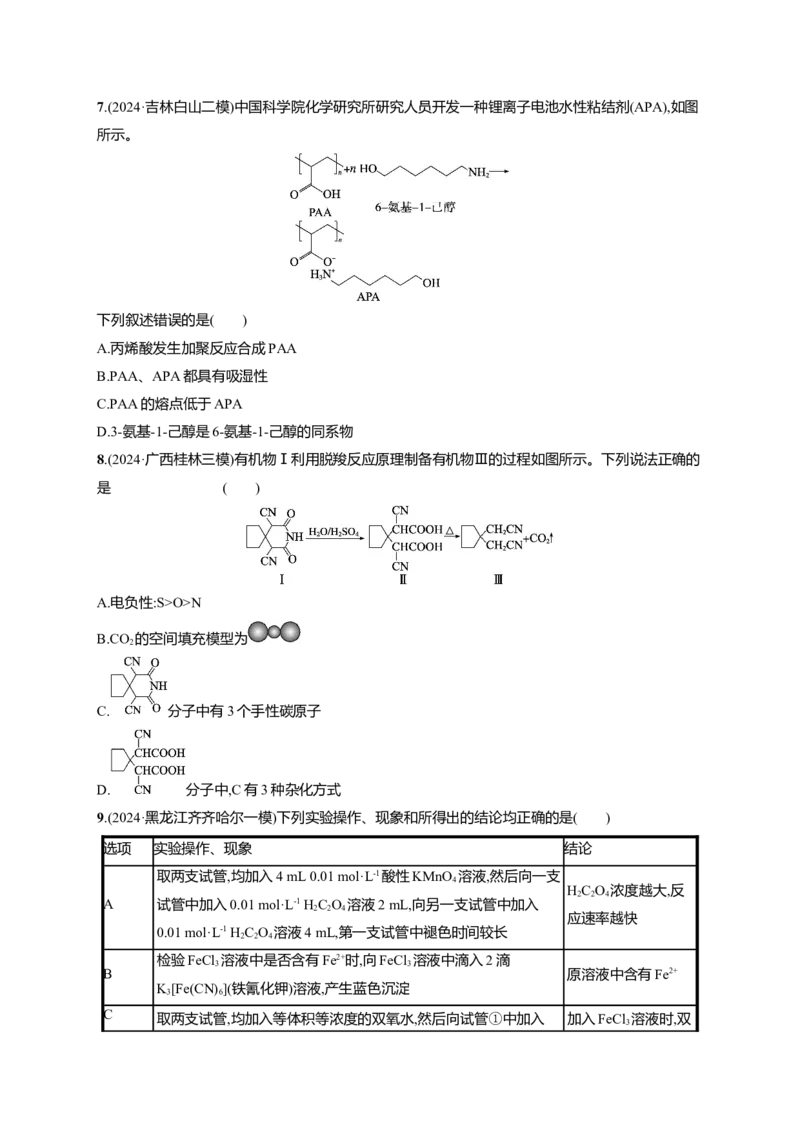
2 2 3 27.(2024·吉林白山二模)中国科学院化学研究所研究人员开发一种锂离子电池水性粘结剂(APA),如图
所示。
下列叙述错误的是( )
A.丙烯酸发生加聚反应合成PAA
B.PAA、APA都具有吸湿性
C.PAA的熔点低于APA
D.3-氨基-1-己醇是6-氨基-1-己醇的同系物
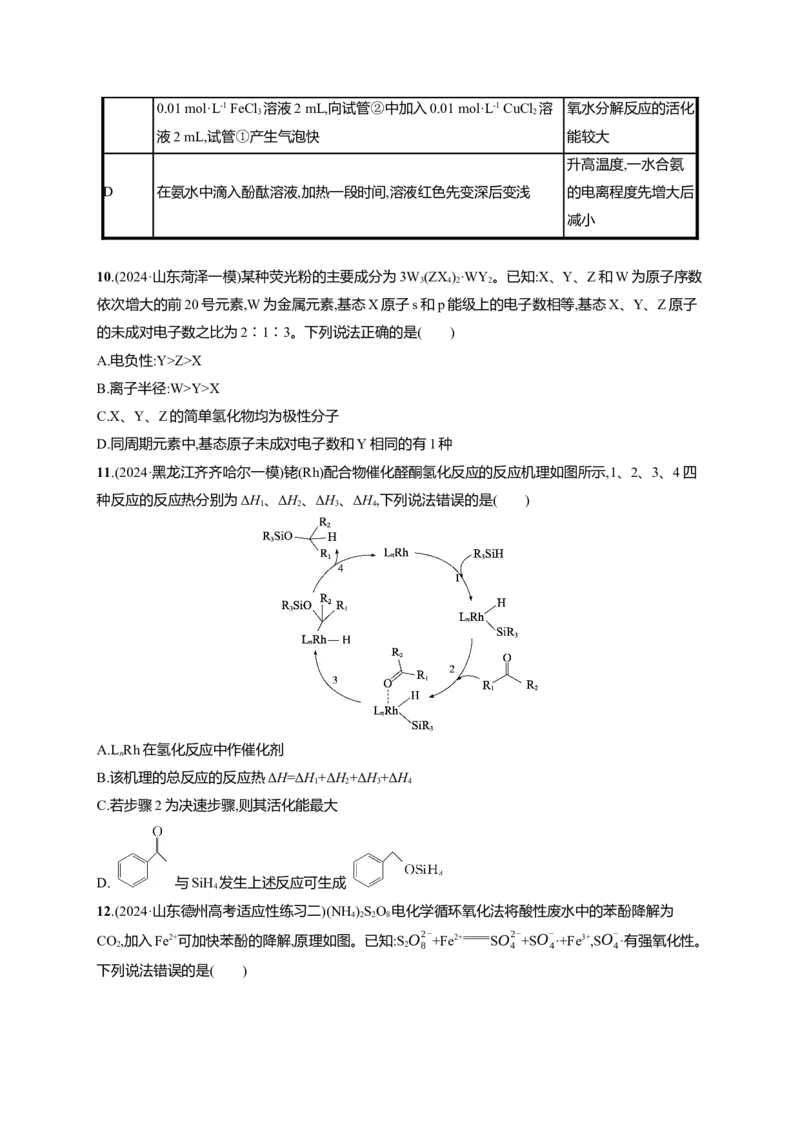
8.(2024·广西桂林三模)有机物Ⅰ利用脱羧反应原理制备有机物Ⅲ的过程如图所示。下列说法正确的
是 ( )
A.电负性:S>O>N
B.CO 的空间填充模型为
2
C. 分子中有3个手性碳原子
D. 分子中,C有3种杂化方式
9.(2024·黑龙江齐齐哈尔一模)下列实验操作、现象和所得出的结论均正确的是( )
选项 实验操作、现象 结论
取两支试管,均加入4 mL 0.01 mol·L-1酸性KMnO 溶液,然后向一支
4
HC O 浓度越大,反
2 2 4
A 试管中加入0.01 mol·L-1 H C O 溶液2 mL,向另一支试管中加入
2 2 4
应速率越快
0.01 mol·L-1 H C O 溶液4 mL,第一支试管中褪色时间较长
2 2 4
检验FeCl 溶液中是否含有Fe2+时,向FeCl 溶液中滴入2滴
3 3
B 原溶液中含有Fe2+
K[Fe(CN) ](铁氰化钾)溶液,产生蓝色沉淀
3 6
C 取两支试管,均加入等体积等浓度的双氧水,然后向试管①中加入 加入FeCl 溶液时,双
30.01 mol·L-1 FeCl 溶液2 mL,向试管②中加入0.01 mol·L-1 CuCl 溶 氧水分解反应的活化
3 2
液2 mL,试管①产生气泡快 能较大
升高温度,一水合氨
D 在氨水中滴入酚酞溶液,加热一段时间,溶液红色先变深后变浅 的电离程度先增大后
减小
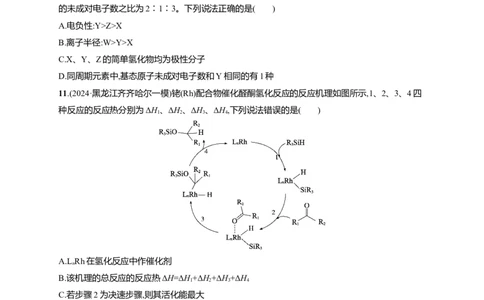
10.(2024·山东菏泽一模)某种荧光粉的主要成分为3W(ZX)·WY。已知:X、Y、Z和W为原子序数
3 4 2 2
依次增大的前20号元素,W为金属元素,基态X原子s和p能级上的电子数相等,基态X、Y、Z原子
的未成对电子数之比为2∶1∶3。下列说法正确的是( )
A.电负性:Y>Z>X
B.离子半径:W>Y>X
C.X、Y、Z的简单氢化物均为极性分子
D.同周期元素中,基态原子未成对电子数和Y相同的有1种
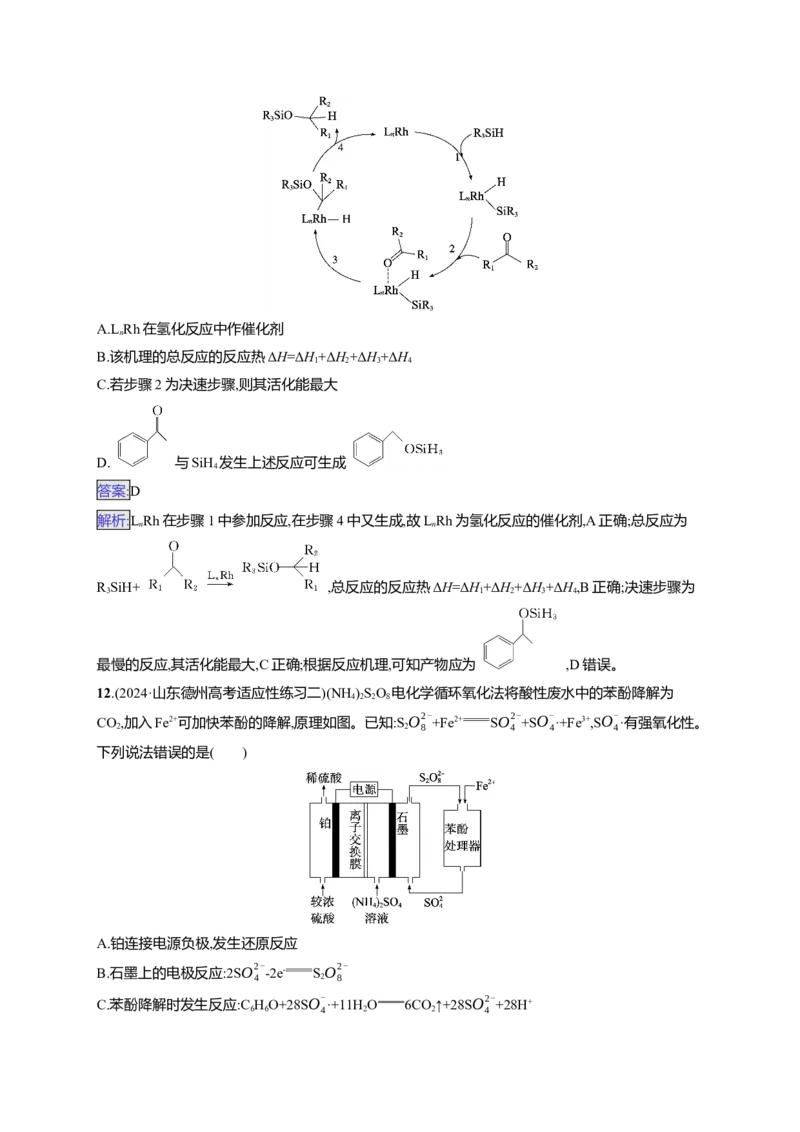
11.(2024·黑龙江齐齐哈尔一模)铑(Rh)配合物催化醛酮氢化反应的反应机理如图所示,1、2、3、4四
种反应的反应热分别为ΔH、ΔH、ΔH、ΔH,下列说法错误的是( )
1 2 3 4
A.L Rh在氢化反应中作催化剂
n
B.该机理的总反应的反应热ΔH=ΔH+ΔH+ΔH+ΔH
1 2 3 4
C.若步骤2为决速步骤,则其活化能最大
D. 与SiH 发生上述反应可生成
4
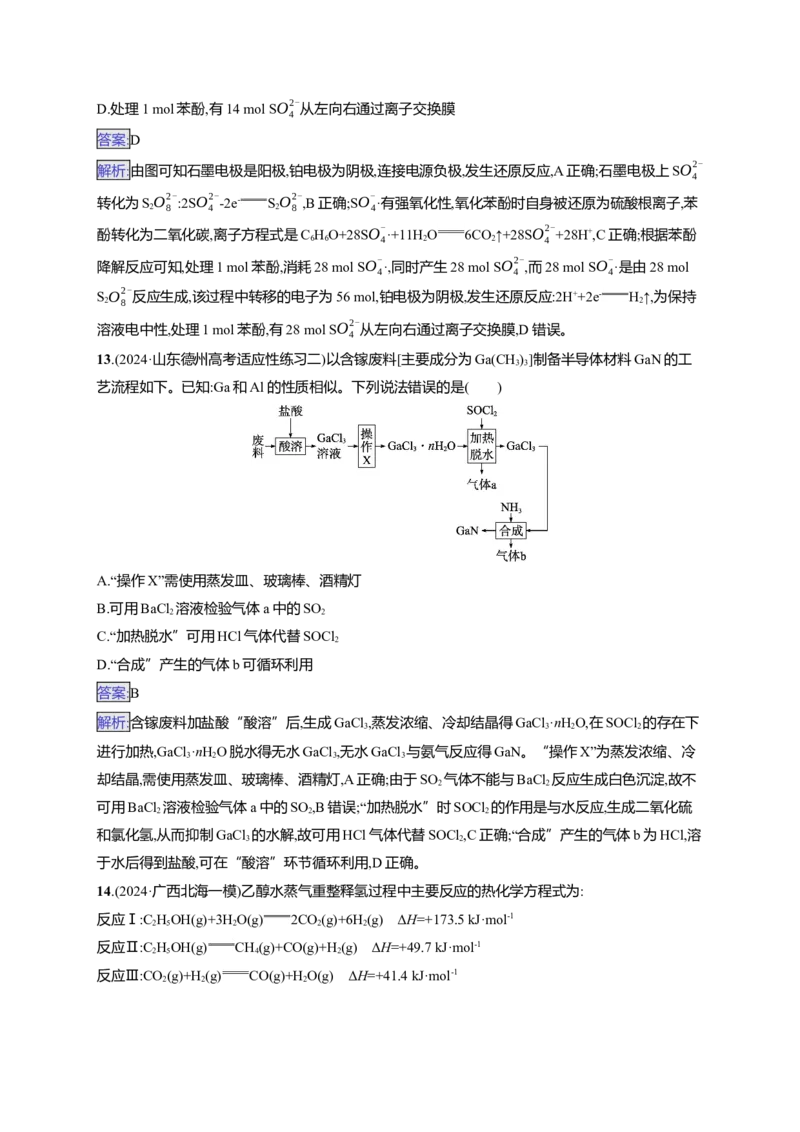
12.(2024·山东德州高考适应性练习二)(NH )SO 电化学循环氧化法将酸性废水中的苯酚降解为
4 2 2 8
CO,加入Fe2+可加快苯酚的降解,原理如图。已知:SO2-
+Fe2+
SO2- +SO- ·+Fe3+,SO-
·有强氧化性。
2 2 8 4 4 4
下列说法错误的是( )A.铂连接电源负极,发生还原反应
B.石墨上的电极反应:2SO2-
-2e-
SO2-
4 2 8
C.苯酚降解时发生反应:C
HO+28SO-
·+11H O
6CO↑+28SO2-
+28H+
6 6 4 2 2 4
D.处理1 mol苯酚,有14 mol
SO2-
从左向右通过离子交换膜
4
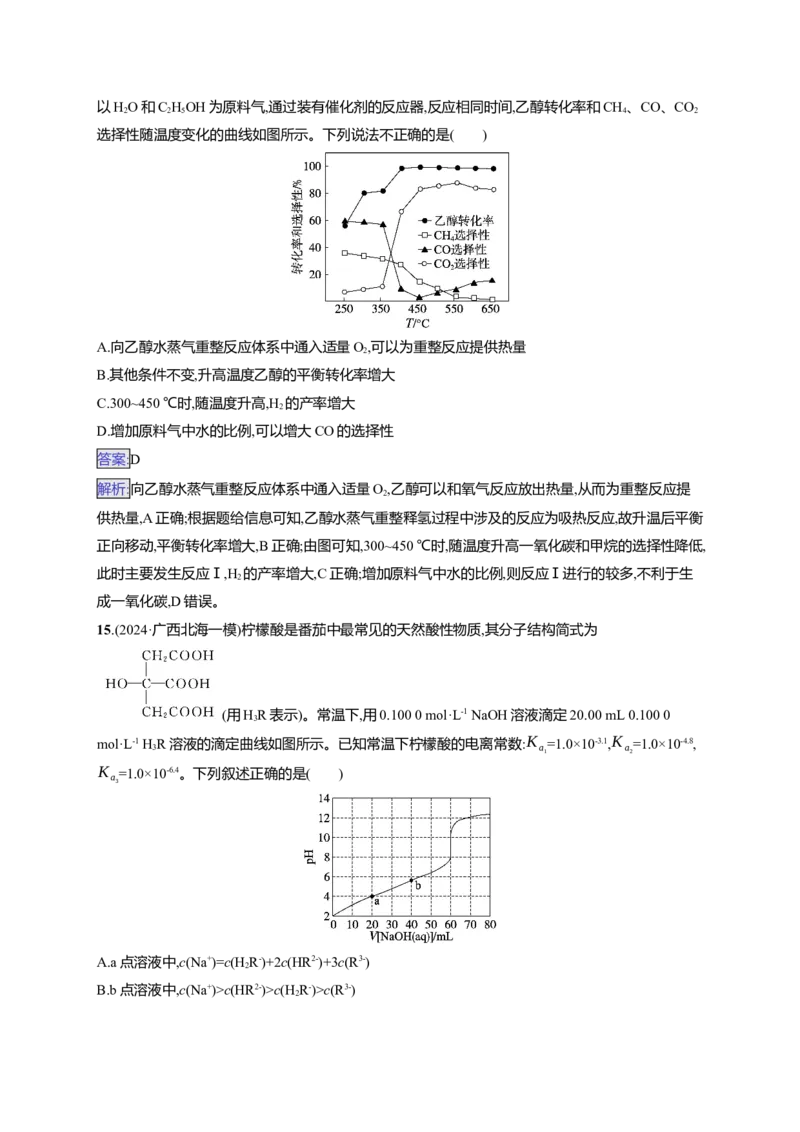
13.(2024·山东德州高考适应性练习二)以含镓废料[主要成分为Ga(CH )]制备半导体材料GaN的工
3 3
艺流程如下。已知:Ga和Al的性质相似。下列说法错误的是( )
A.“操作X”需使用蒸发皿、玻璃棒、酒精灯
B.可用BaCl 溶液检验气体a中的SO
2 2
C.“加热脱水”可用HCl气体代替SOCl
2
D.“合成”产生的气体b可循环利用
14.(2024·广西北海一模)乙醇水蒸气重整释氢过程中主要反应的热化学方程式为:
反应Ⅰ:C HOH(g)+3H O(g) 2CO(g)+6H(g) ΔH=+173.5 kJ·mol-1
2 5 2 2 2
反应Ⅱ:C HOH(g) CH(g)+CO(g)+H(g) ΔH=+49.7 kJ·mol-1
2 5 4 2
反应Ⅲ:CO (g)+H(g) CO(g)+HO(g) ΔH=+41.4 kJ·mol-1
2 2 2
以HO和C HOH为原料气,通过装有催化剂的反应器,反应相同时间,乙醇转化率和CH、CO、CO
2 2 5 4 2
选择性随温度变化的曲线如图所示。下列说法不正确的是( )A.向乙醇水蒸气重整反应体系中通入适量O,可以为重整反应提供热量
2
B.其他条件不变,升高温度乙醇的平衡转化率增大
C.300~450 ℃时,随温度升高,H 的产率增大
2
D.增加原料气中水的比例,可以增大CO的选择性
15.(2024·广西北海一模)柠檬酸是番茄中最常见的天然酸性物质,其分子结构简式为
(用HR表示)。常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0
3
mol·L-1 H R溶液的滴定曲线如图所示。已知常温下柠檬酸的电离常数:K =1.0×10-3.1,K =1.0×10-4.8,
3 a a
1 2
K =1.0×10-6.4。下列叙述正确的是( )
a
3
A.a点溶液中,c(Na+)=c(H R-)+2c(HR2-)+3c(R3-)
2
B.b点溶液中,c(Na+)>c(HR2-)>c(H R-)>c(R3-)
2
c(H R-)
2
C.常温下NaHR溶液加水稀释过程中, 减小
2 c(H R2-)
D.常温下R3-的水解常数为1.0×10-9.2
选择题标准练(九)1.(2024·陕西渭南质检一)2023年10月26日11时14分,神舟十七号载人飞船点火升空成功发射,我
国航天航空事业再次迎来飞速发展。下列有关说法错误的是( )
A.太阳电池翼采用的碳纤维框架和玻璃纤维框架均为无机非金属材料
B.返回舱降落回收过程中使用了芳纶制作的降落伞,芳纶是有机高分子材料
C.飞船舱体外壳部件材料是铝合金材料制成的,主要是利用了其密度大、硬度大的特性
D.新型火箭燃料煤基航天煤油主要由不同馏分的烷烃、芳香烃和烯烃类的碳氢化合物组成
答案:C
解析:飞船舱体外壳部件材料是铝合金材料制成的,主要是利用了其密度小、硬度大的特性,C错误。
2.(2024·甘肃张掖第三次诊断)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.10 g立方氮化硼晶体所含原子数目为N
A
B.1 L pH=1的HSO 与(NH )SO 混合溶液中,H+数目为0.1N
2 4 4 2 4 A
C.含4 mol Si—O键的SiO 晶体中氧原子数目为N
2 A
D.标准状况下,22.4 L NO 的分子数目为N
2 A
答案:B
1 1
解析:立方氮化硼晶胞中B原子在面心和顶角,个数为8× +6× =4,N原子在体内,个数为4,化学式为
8 2
BN,10 g立方氮化硼物质的量为0.4 mol,所含原子数为0.8N ,A错误;1 L pH=1的HSO 与(NH )SO
A 2 4 4 2 4
混合溶液中,H+数目为0.1 mol·L-1×1 L×N mol-1=0.1N ,B正确;含4 mol Si—O键的SiO 晶体中有1
A A 2
mol SiO ,氧原子数目为2N ,C错误;标准状况下,NO 不是气体,22.4 L NO 的分子数目大于N ,D错误。
2 A 2 2 A
3.(2024·江苏泰州一模)氟是已知元素中电负性最大、单质氧化性最强的元素,与稀有气体Xe形成的
XeF 分子是非极性分子,与其他卤素形成的卤素互化物(如ClF、ClF )具有与Cl 相似的化学性质,与
2 3 2
氮形成的NF 可与NH 反应生成NF(结构式:
3 3 2 2
F—N N—F)。自然界中,含氟矿石有萤石(CaF )、冰晶石(Na AlF)等,萤石可与浓硫酸共热制取HF
2 3 6
气体。工业上,可通过电解KF的无水HF溶液(含F-和HF-
)制取F。下列有关说法正确的是( )
2 2
A.XeF 的空间结构为V形
2
B.ClF与ClF 互为同素异形体
3
C.键角:NF>NH
3 3
D.NF 存在顺反异构现象
2 2
答案:D解析:XeF 是非极性分子,故空间结构不是V形,A错误;ClF与ClF 是两种不同的化合物,不是同素异
2 3
形体,B错误;NF 和NH 分子中N原子的价层电子对数都为4,且均含有1个孤电子对,F的电负性强
3 3
于H,NF 中成键电子对更偏向于F原子,导致N上的电子云密度减小,排斥力减小,键角变小,故键
3
角:NFO>N
B.CO 的空间填充模型为
2
C. 分子中有3个手性碳原子
D. 分子中,C有3种杂化方式
答案:D
解析:同主族元素从上到下电负性逐渐减弱,则电负性O>S,A错误;CO 的结构式为O C O,碳原子
2
半径大于O原子半径,应该是中间的原子大,两侧的原子小,B错误;该物质中与—CN相连的碳原子为
手性碳原子,因此含有2个手性碳原子,C错误;该物质中,饱和C原子采用sp3杂化,羧基中的碳原子采
用sp2杂化,—CN中的碳原子采用sp杂化,因此C有3种杂化方式,D正确。
9.(2024·黑龙江齐齐哈尔一模)下列实验操作、现象和所得出的结论均正确的是( )
选项 实验操作、现象 结论
取两支试管,均加入4 mL 0.01 mol·L-1酸性KMnO 溶液,然后向一支
4
HC O 浓度越大,反
2 2 4
A 试管中加入0.01 mol·L-1 H C O 溶液2 mL,向另一支试管中加入
2 2 4
应速率越快
0.01 mol·L-1 H C O 溶液4 mL,第一支试管中褪色时间较长
2 2 4
检验FeCl 溶液中是否含有Fe2+时,向FeCl 溶液中滴入2滴
3 3
B 原溶液中含有Fe2+
K[Fe(CN) ](铁氰化钾)溶液,产生蓝色沉淀
3 6
取两支试管,均加入等体积等浓度的双氧水,然后向试管①中加入 加入FeCl 溶液时,双
C 3
0.01 mol·L-1 FeCl 溶液2 mL,向试管②中加入0.01 mol·L-1 CuCl 溶 氧水分解反应的活化
3 2液2 mL,试管①产生气泡快 能较大
升高温度,一水合氨
D 在氨水中滴入酚酞溶液,加热一段时间,溶液红色先变深后变浅 的电离程度先增大后
减小
答案:B
解析:两支试管中KMnO 均有剩余,溶液均不会褪色,A错误;Fe2+与K[Fe(CN) ]溶液反应生成
4 3 6
KFe[Fe(CN) ]蓝色沉淀,实验现象说明原溶液中含有Fe2+,B正确;试管①加入FeCl 溶液时产生气泡快,
6 3
说明双氧水分解反应的活化能较小,C错误;在氨水中滴入酚酞溶液,加热一段时间,一开始温度升高,
一水合氨的电离程度增大,溶液中c(OH-)增大,溶液红色变深,随着温度的继续升高,一水合氨分解,氨
气逸出,溶液碱性减弱,溶液红色变浅,D错误。
10.(2024·山东菏泽一模)某种荧光粉的主要成分为3W(ZX)·WY。已知:X、Y、Z和W为原子序数
3 4 2 2
依次增大的前20号元素,W为金属元素,基态X原子s和p能级上的电子数相等,基态X、Y、Z原子
的未成对电子数之比为2∶1∶3。下列说法正确的是( )
A.电负性:Y>Z>X
B.离子半径:W>Y>X
C.X、Y、Z的简单氢化物均为极性分子
D.同周期元素中,基态原子未成对电子数和Y相同的有1种
答案:C
解析:从荧光粉的化学式可以看出W为+2价元素,故其为Ca元素;结合其他信息可知,X、Y、Z元素
分别为O、F、P。X、Y、Z分别为O、F、P,电负性:Y>X>Z,A错误;W、Y、X的离子分别为Ca2+、
F-、O2-,电子层数相同,核电荷数越大的,粒子半径越小,即离子半径O2->F-,B错误;X、Y、Z的简单氢
化物分别为HO、HF、PH ,均为极性分子,C正确;Y的基态原子未成对电子数为1,同周期元素中,基
2 3
态原子未成对电子数和Y相同的有Li(1s22s1)和B(1s22s22p1),D错误。
11.(2024·黑龙江齐齐哈尔一模)铑(Rh)配合物催化醛酮氢化反应的反应机理如图所示,1、2、3、4四
种反应的反应热分别为ΔH、ΔH、ΔH、ΔH,下列说法错误的是( )
1 2 3 4A.L Rh在氢化反应中作催化剂
n
B.该机理的总反应的反应热ΔH=ΔH+ΔH+ΔH+ΔH
1 2 3 4
C.若步骤2为决速步骤,则其活化能最大
D. 与SiH 发生上述反应可生成
4
答案:D
解析:LRh在步骤1中参加反应,在步骤4中又生成,故LRh为氢化反应的催化剂,A正确;总反应为
n n
R SiH+ ,总反应的反应热ΔH=ΔH+ΔH+ΔH+ΔH,B正确;决速步骤为
3 1 2 3 4
最慢的反应,其活化能最大,C正确;根据反应机理,可知产物应为 ,D错误。
12.(2024·山东德州高考适应性练习二)(NH )SO 电化学循环氧化法将酸性废水中的苯酚降解为
4 2 2 8
CO,加入Fe2+可加快苯酚的降解,原理如图。已知:SO2-
+Fe2+
SO2- +SO- ·+Fe3+,SO-
·有强氧化性。
2 2 8 4 4 4
下列说法错误的是( )
A.铂连接电源负极,发生还原反应
B.石墨上的电极反应:2SO2-
-2e-
SO2-
4 2 8
C.苯酚降解时发生反应:C
HO+28SO-
·+11H O
6CO↑+28SO2-
+28H+
6 6 4 2 2 4D.处理1 mol苯酚,有14 mol
SO2-
从左向右通过离子交换膜
4
答案:D
解析:由图可知石墨电极是阳极,铂电极为阴极,连接电源负极,发生还原反应,A正确;石墨电极上SO2-
4
转化为SO2- :2SO2-
-2e-
SO2- ,B正确;SO-
·有强氧化性,氧化苯酚时自身被还原为硫酸根离子,苯
2 8 4 2 8 4
酚转化为二氧化碳,离子方程式是C
HO+28SO-
·+11H O
6CO↑+28SO2-
+28H+,C正确;根据苯酚
6 6 4 2 2 4
降解反应可知,处理1 mol苯酚,消耗28 mol
SO-
·,同时产生28 mol
SO2-
,而28 mol
SO-
·是由28 mol
4 4 4
SO2- 反应生成,该过程中转移的电子为56 mol,铂电极为阴极,发生还原反应:2H++2e- H↑,为保持
2 8 2
溶液电中性,处理1 mol苯酚,有28 mol
SO2-
从左向右通过离子交换膜,D错误。
4
13.(2024·山东德州高考适应性练习二)以含镓废料[主要成分为Ga(CH )]制备半导体材料GaN的工
3 3
艺流程如下。已知:Ga和Al的性质相似。下列说法错误的是( )
A.“操作X”需使用蒸发皿、玻璃棒、酒精灯
B.可用BaCl 溶液检验气体a中的SO
2 2
C.“加热脱水”可用HCl气体代替SOCl
2
D.“合成”产生的气体b可循环利用
答案:B
解析:含镓废料加盐酸“酸溶”后,生成GaCl ,蒸发浓缩、冷却结晶得GaCl ·nHO,在SOCl 的存在下
3 3 2 2
进行加热,GaCl ·nHO脱水得无水GaCl ,无水GaCl 与氨气反应得GaN。“操作X”为蒸发浓缩、冷
3 2 3 3
却结晶,需使用蒸发皿、玻璃棒、酒精灯,A正确;由于SO 气体不能与BaCl 反应生成白色沉淀,故不
2 2
可用BaCl 溶液检验气体a中的SO ,B错误;“加热脱水”时SOCl 的作用是与水反应,生成二氧化硫
2 2 2
和氯化氢,从而抑制GaCl 的水解,故可用HCl气体代替SOCl ,C正确;“合成”产生的气体b为HCl,溶
3 2
于水后得到盐酸,可在“酸溶”环节循环利用,D正确。
14.(2024·广西北海一模)乙醇水蒸气重整释氢过程中主要反应的热化学方程式为:
反应Ⅰ:C HOH(g)+3H O(g) 2CO(g)+6H(g) ΔH=+173.5 kJ·mol-1
2 5 2 2 2
反应Ⅱ:C HOH(g) CH(g)+CO(g)+H(g) ΔH=+49.7 kJ·mol-1
2 5 4 2
反应Ⅲ:CO (g)+H(g) CO(g)+HO(g) ΔH=+41.4 kJ·mol-1
2 2 2以HO和C HOH为原料气,通过装有催化剂的反应器,反应相同时间,乙醇转化率和CH、CO、CO
2 2 5 4 2
选择性随温度变化的曲线如图所示。下列说法不正确的是( )
A.向乙醇水蒸气重整反应体系中通入适量O,可以为重整反应提供热量
2
B.其他条件不变,升高温度乙醇的平衡转化率增大
C.300~450 ℃时,随温度升高,H 的产率增大
2
D.增加原料气中水的比例,可以增大CO的选择性
答案:D
解析:向乙醇水蒸气重整反应体系中通入适量O,乙醇可以和氧气反应放出热量,从而为重整反应提
2
供热量,A正确;根据题给信息可知,乙醇水蒸气重整释氢过程中涉及的反应为吸热反应,故升温后平衡
正向移动,平衡转化率增大,B正确;由图可知,300~450 ℃时,随温度升高一氧化碳和甲烷的选择性降低,
此时主要发生反应Ⅰ,H 的产率增大,C正确;增加原料气中水的比例,则反应Ⅰ进行的较多,不利于生
2
成一氧化碳,D错误。
15.(2024·广西北海一模)柠檬酸是番茄中最常见的天然酸性物质,其分子结构简式为
(用HR表示)。常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0
3
mol·L-1 H R溶液的滴定曲线如图所示。已知常温下柠檬酸的电离常数:K =1.0×10-3.1,K =1.0×10-4.8,
3 a a
1 2
K =1.0×10-6.4。下列叙述正确的是( )
a
3
A.a点溶液中,c(Na+)=c(H R-)+2c(HR2-)+3c(R3-)
2
B.b点溶液中,c(Na+)>c(HR2-)>c(H R-)>c(R3-)
2c(H R-)
2
C.常温下NaHR溶液加水稀释过程中, 减小
2 c(H R2-)
D.常温下R3-的水解常数为1.0×10-9.2
答案:C
解析:a点溶液为NaH R溶液,溶液呈酸性,电荷守恒为c(Na+)+c(H+)=c(OH-)+c(H R-)+2c(HR2-)
2 2
+3c(R3-),A错误;b点溶液为NaHR溶液,溶液呈酸性,HR2-的电离程度大于HR2-的水解程度,故离子浓
2
度大小为c(Na+)>c(HR2-)>c(R3-)>c(H R-),B错误;Na HR溶液呈酸性,加水稀释过程中,溶液中c(H+)减小,
2 2
则溶液中c(OH-)增大。常温下加水稀释过程中,HR2-的水解常数保持不变,加水稀释过程中c(OH-)增
c(H R-) c(H R-)·c(OH-) K c(H R-)
大, 2 = 2 = h ,则 2 减小,C正确;常温下,R3-的水解
c(H R2-) c(H R2-)·c(OH-) c(OH-) c(H R2-)
K 1.0×10-14
常数= W = =1.0×10-7.6, D错误。
K 1.0×10-6.4
a
3