文档内容
3.化学实验操作及装置分析
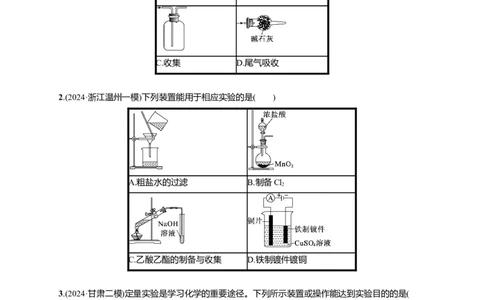
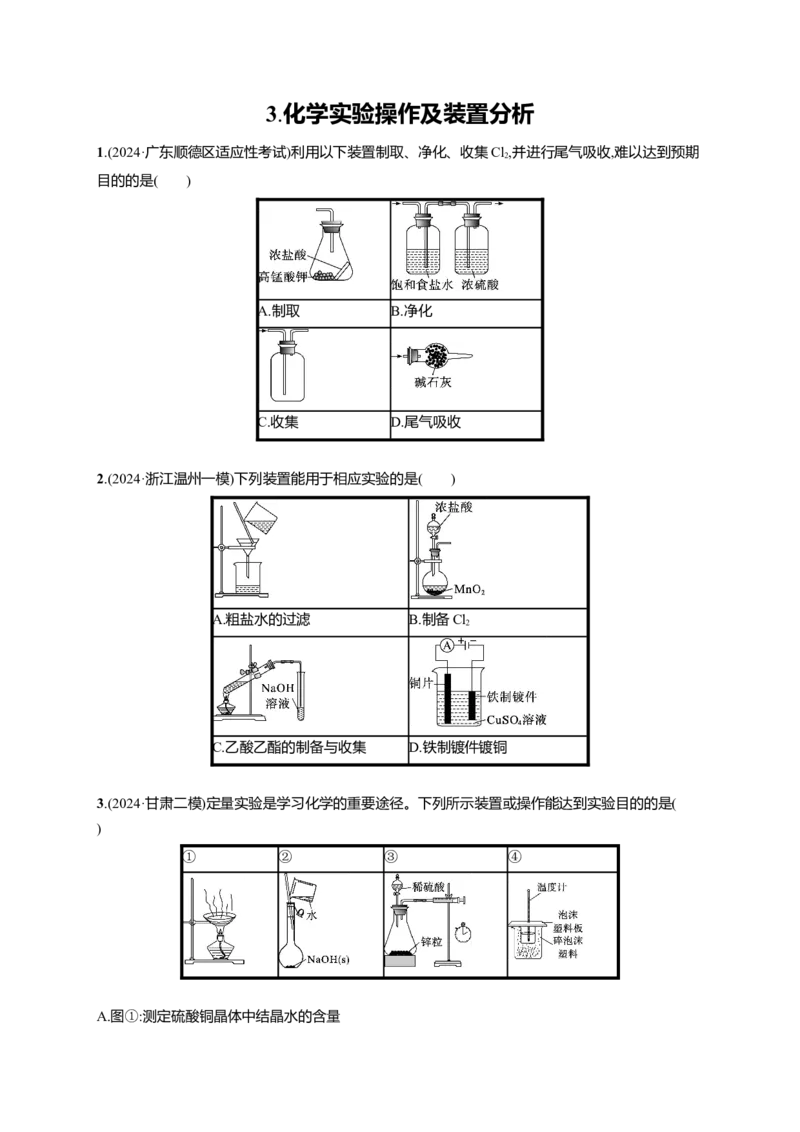
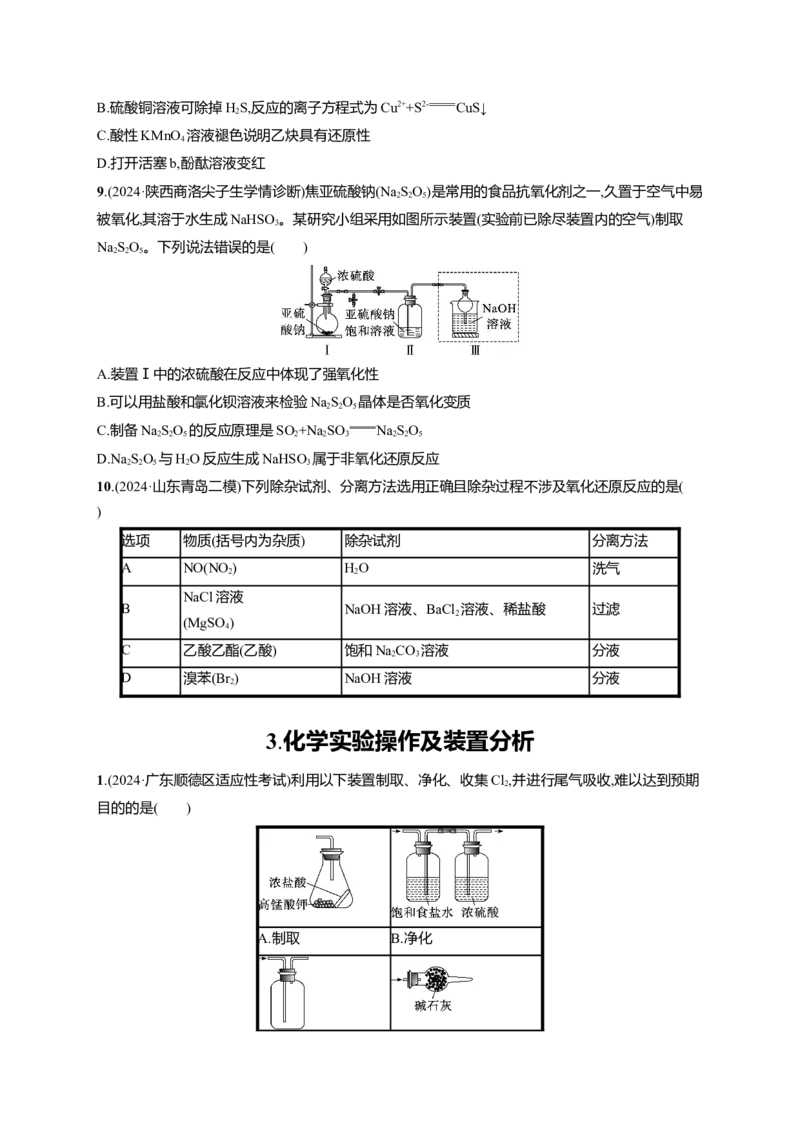
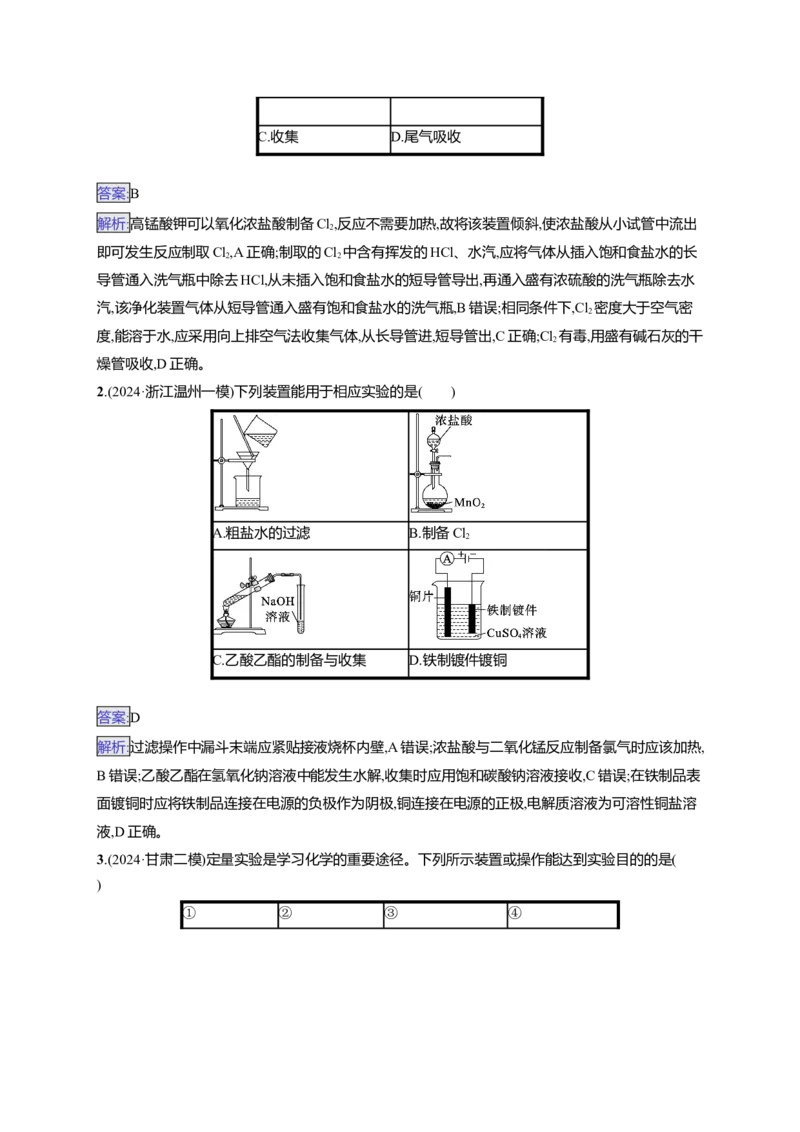
1.(2024·广东顺德区适应性考试)利用以下装置制取、净化、收集Cl,并进行尾气吸收,难以达到预期
2
目的的是( )
A.制取 B.净化
C.收集 D.尾气吸收
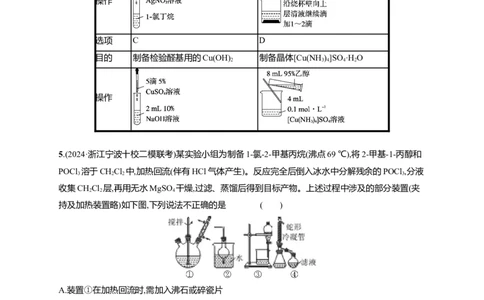
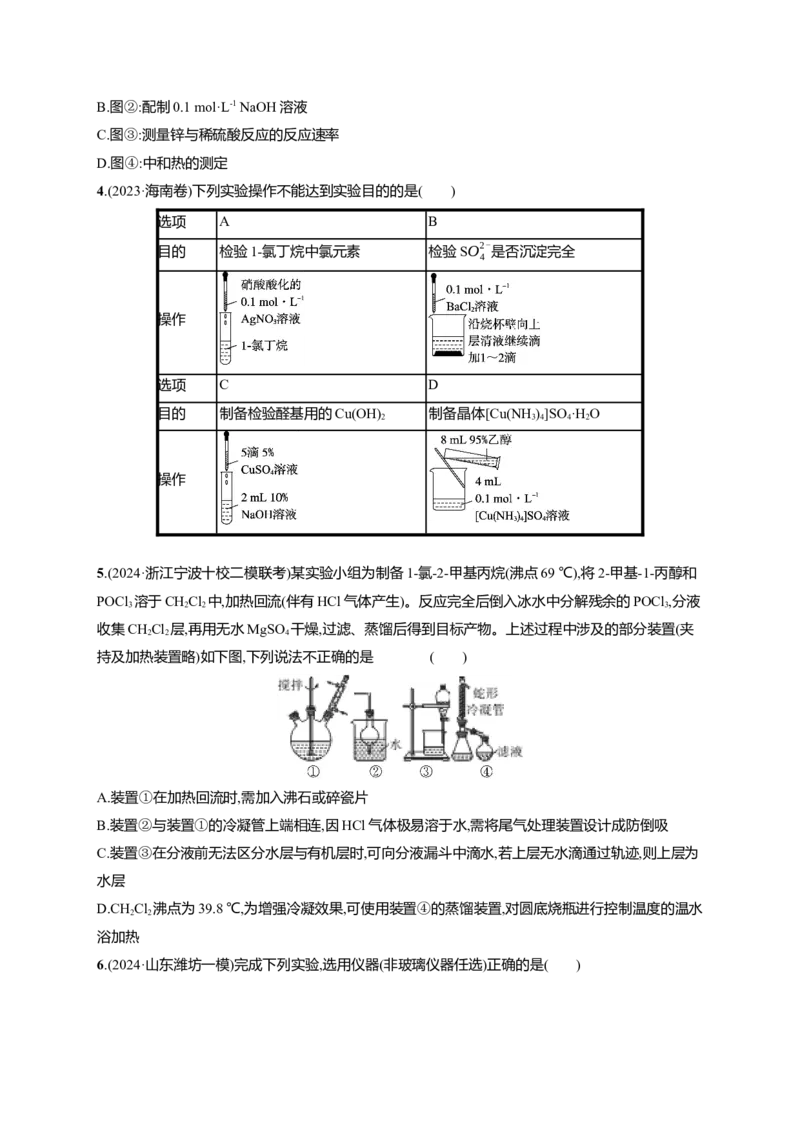
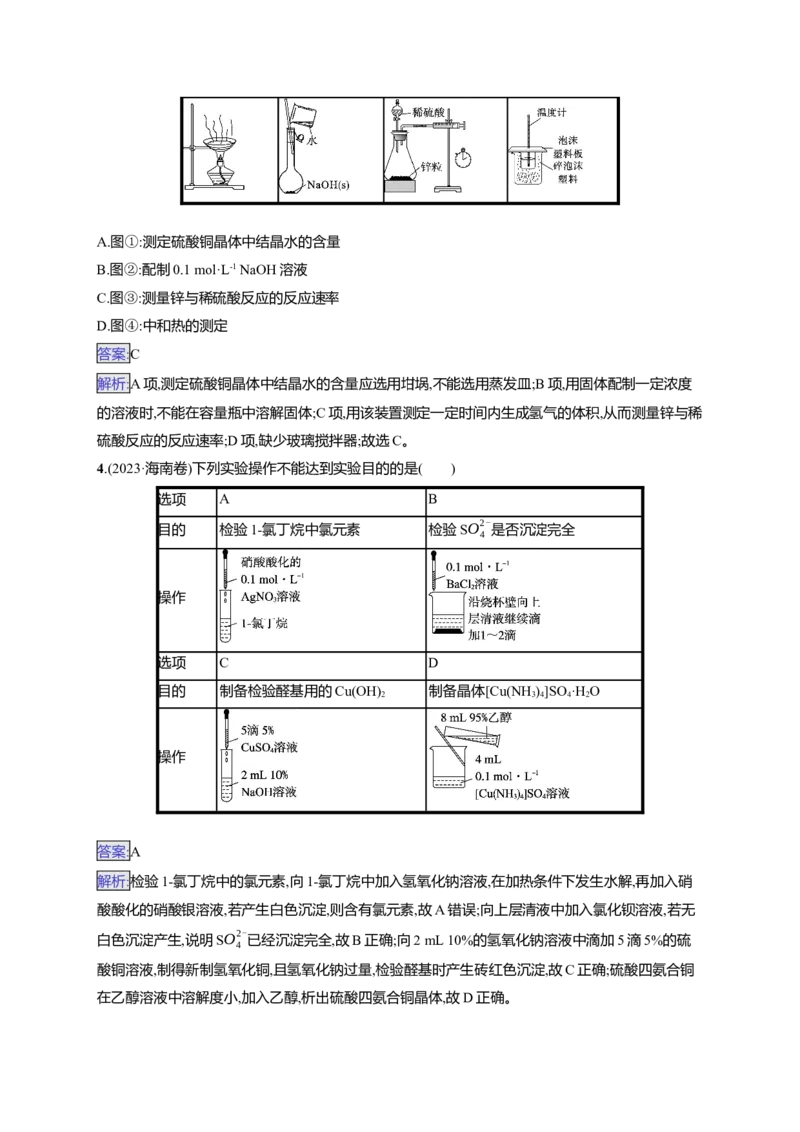
2.(2024·浙江温州一模)下列装置能用于相应实验的是( )
A.粗盐水的过滤 B.制备Cl
2
C.乙酸乙酯的制备与收集 D.铁制镀件镀铜
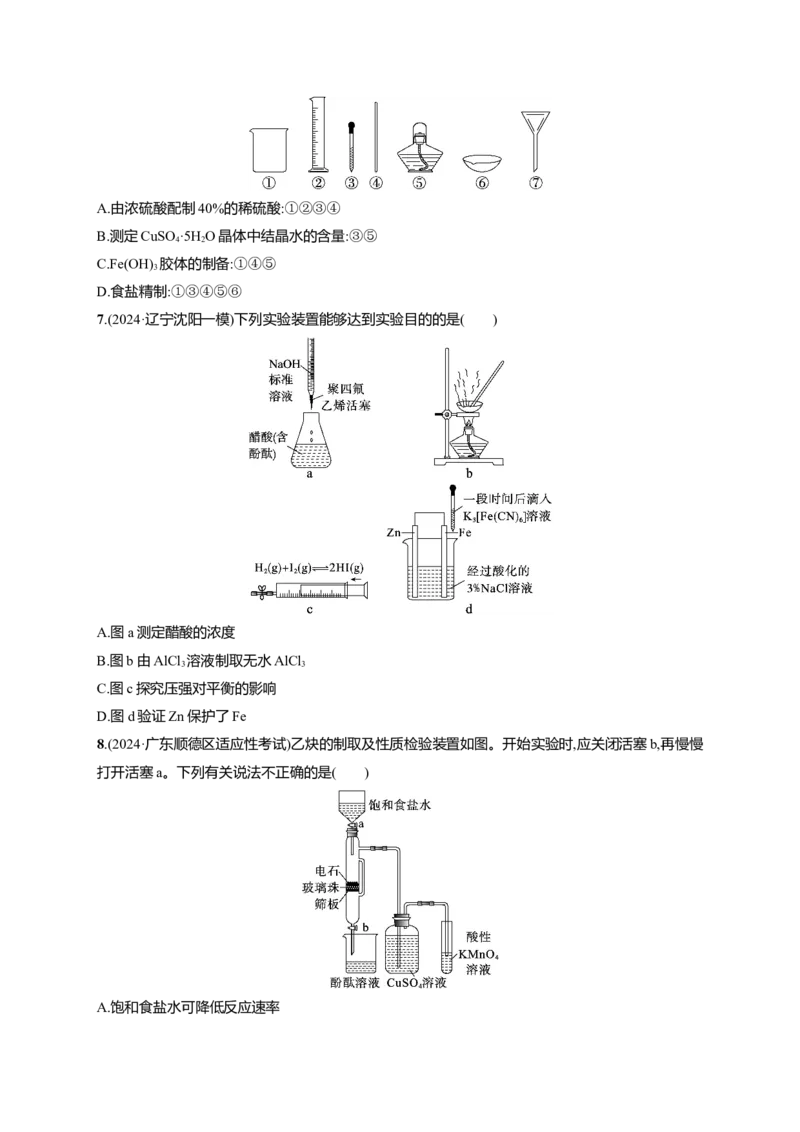
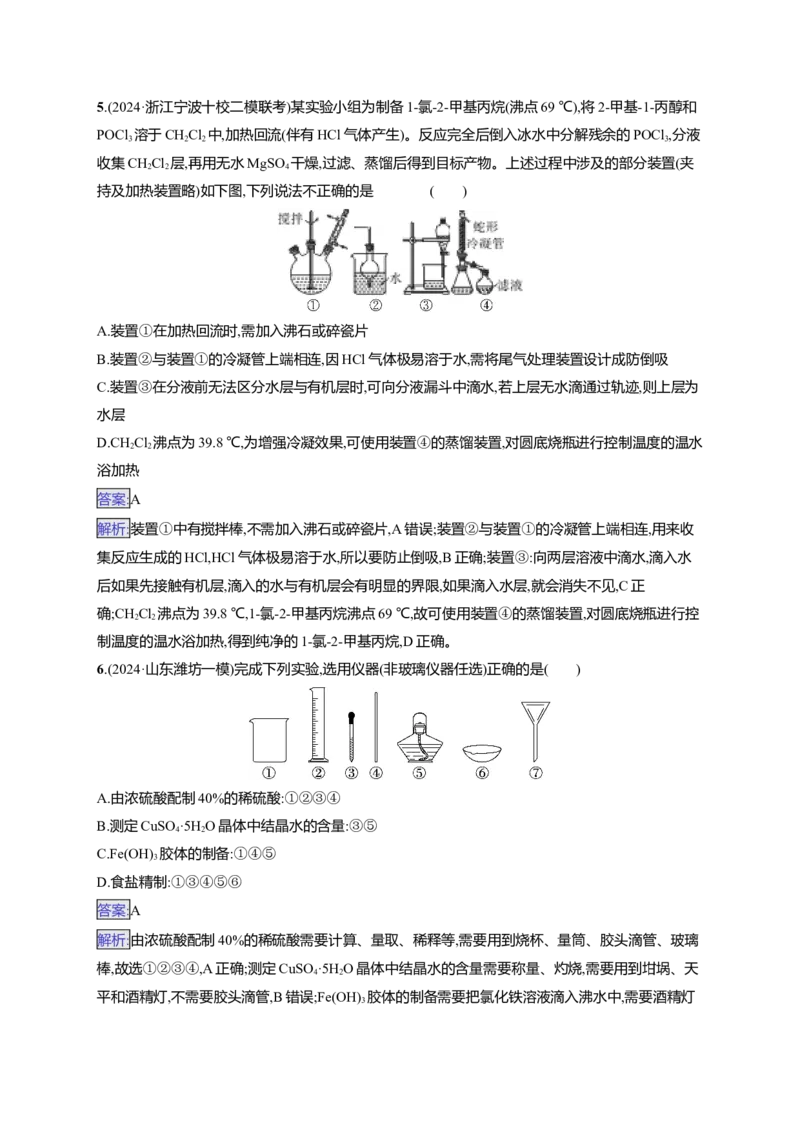
3.(2024·甘肃二模)定量实验是学习化学的重要途径。下列所示装置或操作能达到实验目的的是(
)
① ② ③ ④
A.图①:测定硫酸铜晶体中结晶水的含量B.图②:配制0.1 mol·L-1 NaOH溶液
C.图③:测量锌与稀硫酸反应的反应速率
D.图④:中和热的测定
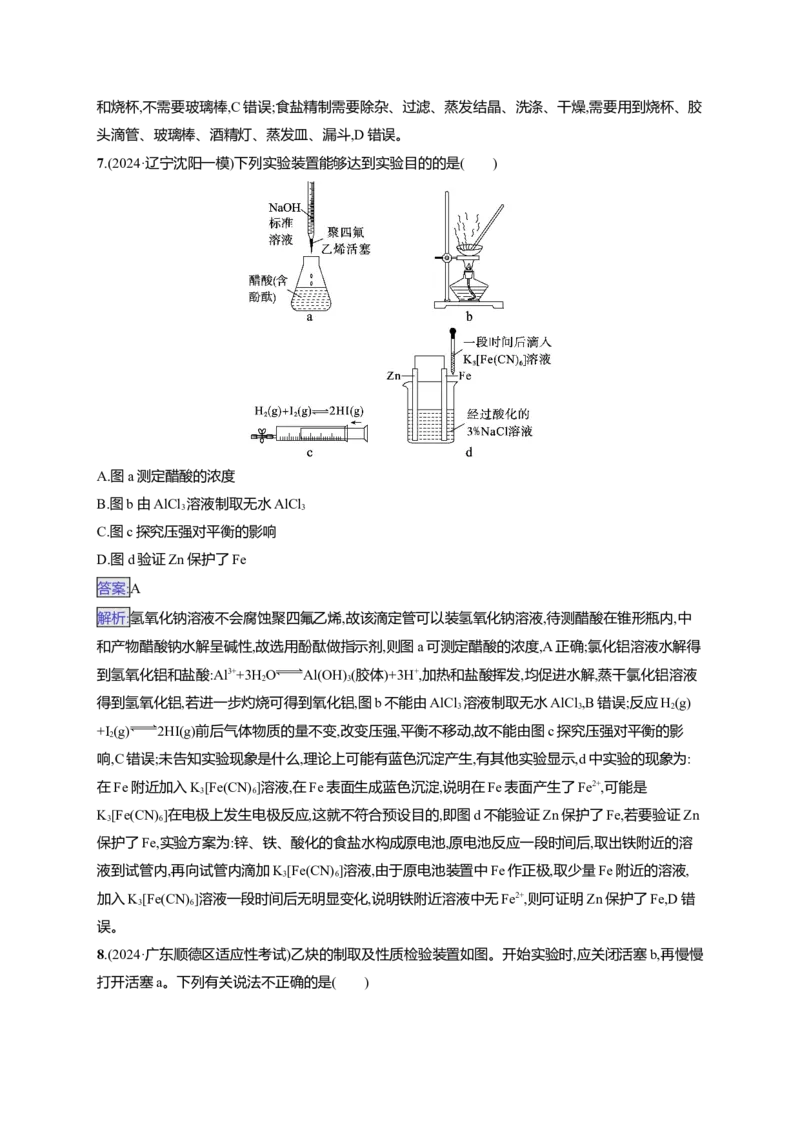
4.(2023·海南卷)下列实验操作不能达到实验目的的是( )
选项 A B
目的 检验1-氯丁烷中氯元素
检验SO2-
是否沉淀完全
4
操作
选项 C D
目的 制备检验醛基用的Cu(OH) 制备晶体[Cu(NH )]SO ·H O
2 3 4 4 2
操作
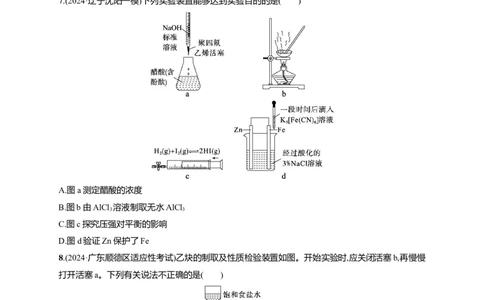
5.(2024·浙江宁波十校二模联考)某实验小组为制备1-氯-2-甲基丙烷(沸点69 ℃),将2-甲基-1-丙醇和
POCl 溶于CHCl 中,加热回流(伴有HCl气体产生)。反应完全后倒入冰水中分解残余的POCl ,分液
3 2 2 3
收集CHCl 层,再用无水MgSO 干燥,过滤、蒸馏后得到目标产物。上述过程中涉及的部分装置(夹
2 2 4
持及加热装置略)如下图,下列说法不正确的是 ( )
A.装置①在加热回流时,需加入沸石或碎瓷片
B.装置②与装置①的冷凝管上端相连,因HCl气体极易溶于水,需将尾气处理装置设计成防倒吸
C.装置③在分液前无法区分水层与有机层时,可向分液漏斗中滴水,若上层无水滴通过轨迹,则上层为
水层
D.CHCl 沸点为39.8 ℃,为增强冷凝效果,可使用装置④的蒸馏装置,对圆底烧瓶进行控制温度的温水
2 2
浴加热
6.(2024·山东潍坊一模)完成下列实验,选用仪器(非玻璃仪器任选)正确的是( )A.由浓硫酸配制40%的稀硫酸:①②③④
B.测定CuSO ·5H O晶体中结晶水的含量:③⑤
4 2
C.Fe(OH) 胶体的制备:①④⑤
3
D.食盐精制:①③④⑤⑥
7.(2024·辽宁沈阳一模)下列实验装置能够达到实验目的的是( )
A.图a测定醋酸的浓度
B.图b由AlCl 溶液制取无水AlCl
3 3
C.图c探究压强对平衡的影响
D.图d验证Zn保护了Fe
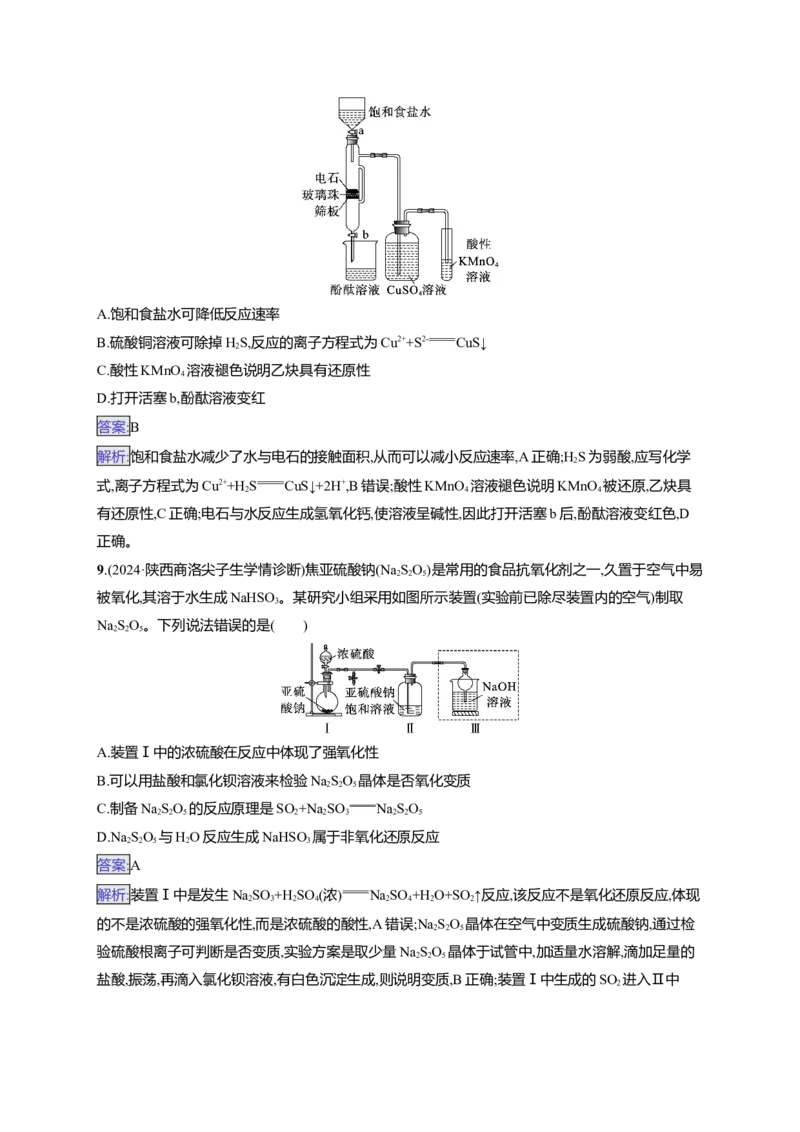
8.(2024·广东顺德区适应性考试)乙炔的制取及性质检验装置如图。开始实验时,应关闭活塞b,再慢慢
打开活塞a。下列有关说法不正确的是( )
A.饱和食盐水可降低反应速率B.硫酸铜溶液可除掉HS,反应的离子方程式为Cu2++S2- CuS↓
2
C.酸性KMnO 溶液褪色说明乙炔具有还原性
4
D.打开活塞b,酚酞溶液变红
9.(2024·陕西商洛尖子生学情诊断)焦亚硫酸钠(Na SO)是常用的食品抗氧化剂之一,久置于空气中易
2 2 5
被氧化,其溶于水生成NaHSO。某研究小组采用如图所示装置(实验前已除尽装置内的空气)制取
3
NaSO。下列说法错误的是( )
2 2 5
A.装置Ⅰ中的浓硫酸在反应中体现了强氧化性
B.可以用盐酸和氯化钡溶液来检验NaSO 晶体是否氧化变质
2 2 5
C.制备NaSO 的反应原理是SO +Na SO NaSO
2 2 5 2 2 3 2 2 5
D.Na SO 与HO反应生成NaHSO 属于非氧化还原反应
2 2 5 2 3
10.(2024·山东青岛二模)下列除杂试剂、分离方法选用正确且除杂过程不涉及氧化还原反应的是(
)
选项 物质(括号内为杂质) 除杂试剂 分离方法
A NO(NO ) HO 洗气
2 2
NaCl溶液
B NaOH溶液、BaCl 溶液、稀盐酸 过滤
2
(MgSO )
4
C 乙酸乙酯(乙酸) 饱和NaCO 溶液 分液
2 3
D 溴苯(Br) NaOH溶液 分液
2
3.化学实验操作及装置分析
1.(2024·广东顺德区适应性考试)利用以下装置制取、净化、收集Cl,并进行尾气吸收,难以达到预期
2
目的的是( )
A.制取 B.净化C.收集 D.尾气吸收
答案:B
解析:高锰酸钾可以氧化浓盐酸制备Cl,反应不需要加热,故将该装置倾斜,使浓盐酸从小试管中流出
2
即可发生反应制取Cl,A正确;制取的Cl 中含有挥发的HCl、水汽,应将气体从插入饱和食盐水的长
2 2
导管通入洗气瓶中除去HCl,从未插入饱和食盐水的短导管导出,再通入盛有浓硫酸的洗气瓶除去水
汽,该净化装置气体从短导管通入盛有饱和食盐水的洗气瓶,B错误;相同条件下,Cl 密度大于空气密
2
度,能溶于水,应采用向上排空气法收集气体,从长导管进,短导管出,C正确;Cl 有毒,用盛有碱石灰的干
2
燥管吸收,D正确。
2.(2024·浙江温州一模)下列装置能用于相应实验的是( )
A.粗盐水的过滤 B.制备Cl
2
C.乙酸乙酯的制备与收集 D.铁制镀件镀铜
答案:D
解析:过滤操作中漏斗末端应紧贴接液烧杯内壁,A错误;浓盐酸与二氧化锰反应制备氯气时应该加热,
B错误;乙酸乙酯在氢氧化钠溶液中能发生水解,收集时应用饱和碳酸钠溶液接收,C错误;在铁制品表
面镀铜时应将铁制品连接在电源的负极作为阴极,铜连接在电源的正极,电解质溶液为可溶性铜盐溶
液,D正确。
3.(2024·甘肃二模)定量实验是学习化学的重要途径。下列所示装置或操作能达到实验目的的是(
)
① ② ③ ④A.图①:测定硫酸铜晶体中结晶水的含量
B.图②:配制0.1 mol·L-1 NaOH溶液
C.图③:测量锌与稀硫酸反应的反应速率
D.图④:中和热的测定
答案:C
解析:A项,测定硫酸铜晶体中结晶水的含量应选用坩埚,不能选用蒸发皿;B项,用固体配制一定浓度
的溶液时,不能在容量瓶中溶解固体;C项,用该装置测定一定时间内生成氢气的体积,从而测量锌与稀
硫酸反应的反应速率;D项,缺少玻璃搅拌器;故选C。
4.(2023·海南卷)下列实验操作不能达到实验目的的是( )
选项 A B
目的 检验1-氯丁烷中氯元素
检验SO2-
是否沉淀完全
4
操作
选项 C D
目的 制备检验醛基用的Cu(OH) 制备晶体[Cu(NH )]SO ·H O
2 3 4 4 2
操作
答案:A
解析:检验1-氯丁烷中的氯元素,向1-氯丁烷中加入氢氧化钠溶液,在加热条件下发生水解,再加入硝
酸酸化的硝酸银溶液,若产生白色沉淀,则含有氯元素,故A错误;向上层清液中加入氯化钡溶液,若无
白色沉淀产生,说明SO2-
已经沉淀完全,故B正确;向2 mL 10%的氢氧化钠溶液中滴加5滴5%的硫
4
酸铜溶液,制得新制氢氧化铜,且氢氧化钠过量,检验醛基时产生砖红色沉淀,故C正确;硫酸四氨合铜
在乙醇溶液中溶解度小,加入乙醇,析出硫酸四氨合铜晶体,故D正确。5.(2024·浙江宁波十校二模联考)某实验小组为制备1-氯-2-甲基丙烷(沸点69 ℃),将2-甲基-1-丙醇和
POCl 溶于CHCl 中,加热回流(伴有HCl气体产生)。反应完全后倒入冰水中分解残余的POCl ,分液
3 2 2 3
收集CHCl 层,再用无水MgSO 干燥,过滤、蒸馏后得到目标产物。上述过程中涉及的部分装置(夹
2 2 4
持及加热装置略)如下图,下列说法不正确的是 ( )
A.装置①在加热回流时,需加入沸石或碎瓷片
B.装置②与装置①的冷凝管上端相连,因HCl气体极易溶于水,需将尾气处理装置设计成防倒吸
C.装置③在分液前无法区分水层与有机层时,可向分液漏斗中滴水,若上层无水滴通过轨迹,则上层为
水层
D.CHCl 沸点为39.8 ℃,为增强冷凝效果,可使用装置④的蒸馏装置,对圆底烧瓶进行控制温度的温水
2 2
浴加热
答案:A
解析:装置①中有搅拌棒,不需加入沸石或碎瓷片,A错误;装置②与装置①的冷凝管上端相连,用来收
集反应生成的HCl,HCl气体极易溶于水,所以要防止倒吸,B正确;装置③:向两层溶液中滴水,滴入水
后如果先接触有机层,滴入的水与有机层会有明显的界限,如果滴入水层,就会消失不见,C正
确;CH Cl 沸点为39.8 ℃,1-氯-2-甲基丙烷沸点69 ℃,故可使用装置④的蒸馏装置,对圆底烧瓶进行控
2 2
制温度的温水浴加热,得到纯净的1-氯-2-甲基丙烷,D正确。
6.(2024·山东潍坊一模)完成下列实验,选用仪器(非玻璃仪器任选)正确的是( )
A.由浓硫酸配制40%的稀硫酸:①②③④
B.测定CuSO ·5H O晶体中结晶水的含量:③⑤
4 2
C.Fe(OH) 胶体的制备:①④⑤
3
D.食盐精制:①③④⑤⑥
答案:A
解析:由浓硫酸配制40%的稀硫酸需要计算、量取、稀释等,需要用到烧杯、量筒、胶头滴管、玻璃
棒,故选①②③④,A正确;测定CuSO ·5H O晶体中结晶水的含量需要称量、灼烧,需要用到坩埚、天
4 2
平和酒精灯,不需要胶头滴管,B错误;Fe(OH) 胶体的制备需要把氯化铁溶液滴入沸水中,需要酒精灯
3和烧杯,不需要玻璃棒,C错误;食盐精制需要除杂、过滤、蒸发结晶、洗涤、干燥,需要用到烧杯、胶
头滴管、玻璃棒、酒精灯、蒸发皿、漏斗,D错误。
7.(2024·辽宁沈阳一模)下列实验装置能够达到实验目的的是( )
A.图a测定醋酸的浓度
B.图b由AlCl 溶液制取无水AlCl
3 3
C.图c探究压强对平衡的影响
D.图d验证Zn保护了Fe
答案:A
解析:氢氧化钠溶液不会腐蚀聚四氟乙烯,故该滴定管可以装氢氧化钠溶液,待测醋酸在锥形瓶内,中
和产物醋酸钠水解呈碱性,故选用酚酞做指示剂,则图a可测定醋酸的浓度,A正确;氯化铝溶液水解得
到氢氧化铝和盐酸:Al3++3H O Al(OH) (胶体)+3H+,加热和盐酸挥发,均促进水解,蒸干氯化铝溶液
2 3
得到氢氧化铝,若进一步灼烧可得到氧化铝,图b不能由AlCl 溶液制取无水AlCl ,B错误;反应H(g)
3 3 2
+I (g) 2HI(g)前后气体物质的量不变,改变压强,平衡不移动,故不能由图c探究压强对平衡的影
2
响,C错误;未告知实验现象是什么,理论上可能有蓝色沉淀产生,有其他实验显示,d中实验的现象为:
在Fe附近加入K[Fe(CN) ]溶液,在Fe表面生成蓝色沉淀,说明在Fe表面产生了Fe2+,可能是
3 6
K[Fe(CN) ]在电极上发生电极反应,这就不符合预设目的,即图d不能验证Zn保护了Fe,若要验证Zn
3 6
保护了Fe,实验方案为:锌、铁、酸化的食盐水构成原电池,原电池反应一段时间后,取出铁附近的溶
液到试管内,再向试管内滴加K[Fe(CN) ]溶液,由于原电池装置中Fe作正极,取少量Fe附近的溶液,
3 6
加入K[Fe(CN) ]溶液一段时间后无明显变化,说明铁附近溶液中无Fe2+,则可证明Zn保护了Fe,D错
3 6
误。
8.(2024·广东顺德区适应性考试)乙炔的制取及性质检验装置如图。开始实验时,应关闭活塞b,再慢慢
打开活塞a。下列有关说法不正确的是( )A.饱和食盐水可降低反应速率
B.硫酸铜溶液可除掉HS,反应的离子方程式为Cu2++S2- CuS↓
2
C.酸性KMnO 溶液褪色说明乙炔具有还原性
4
D.打开活塞b,酚酞溶液变红
答案:B
解析:饱和食盐水减少了水与电石的接触面积,从而可以减小反应速率,A正确;H S为弱酸,应写化学
2
式,离子方程式为Cu2++H S CuS↓+2H+,B错误;酸性KMnO 溶液褪色说明KMnO 被还原,乙炔具
2 4 4
有还原性,C正确;电石与水反应生成氢氧化钙,使溶液呈碱性,因此打开活塞b后,酚酞溶液变红色,D
正确。
9.(2024·陕西商洛尖子生学情诊断)焦亚硫酸钠(Na SO)是常用的食品抗氧化剂之一,久置于空气中易
2 2 5
被氧化,其溶于水生成NaHSO。某研究小组采用如图所示装置(实验前已除尽装置内的空气)制取
3
NaSO。下列说法错误的是( )
2 2 5
A.装置Ⅰ中的浓硫酸在反应中体现了强氧化性
B.可以用盐酸和氯化钡溶液来检验NaSO 晶体是否氧化变质
2 2 5
C.制备NaSO 的反应原理是SO +Na SO NaSO
2 2 5 2 2 3 2 2 5
D.Na SO 与HO反应生成NaHSO 属于非氧化还原反应
2 2 5 2 3
答案:A
解析:装置Ⅰ中是发生NaSO +H SO (浓) NaSO +H O+SO ↑反应,该反应不是氧化还原反应,体现
2 3 2 4 2 4 2 2
的不是浓硫酸的强氧化性,而是浓硫酸的酸性,A错误;Na SO 晶体在空气中变质生成硫酸钠,通过检
2 2 5
验硫酸根离子可判断是否变质,实验方案是取少量NaSO 晶体于试管中,加适量水溶解,滴加足量的
2 2 5
盐酸,振荡,再滴入氯化钡溶液,有白色沉淀生成,则说明变质,B正确;装置Ⅰ中生成的SO 进入Ⅱ中
2NaSO 饱和溶液发生反应生成NaSO,反应方程式为SO +Na SO NaSO,C正确;在
2 3 2 2 5 2 2 3 2 2 5
NaSO+H O 2NaHSO 中,没有元素化合价发生变化,为非氧化还原反应,D正确。
2 2 5 2 3
10.(2024·山东青岛二模)下列除杂试剂、分离方法选用正确且除杂过程不涉及氧化还原反应的是(
)
选项 物质(括号内为杂质) 除杂试剂 分离方法
A NO(NO ) HO 洗气
2 2
NaCl溶液
B NaOH溶液、BaCl 溶液、稀盐酸 过滤
2
(MgSO )
4
C 乙酸乙酯(乙酸) 饱和NaCO 溶液 分液
2 3
D 溴苯(Br) NaOH溶液 分液
2
答案:C
解析:A项,NO(NO )通过水时,NO 与水发生反应3NO +H O NO+2HNO,可以除去NO中的NO
2 2 2 2 3 2
杂质,但是反应是氧化还原反应;B项,MgSO 与NaOH反应生成的氢氧化镁会被稀盐酸溶解,镁又转化
4
为离子,无法除去;C项,饱和碳酸钠溶液可与乙酸反应从而除去乙酸,还可减小乙酸乙酯的溶解度,除
去乙酸后,乙酸乙酯与水相互不相溶,用分液法即可分离,所有反应不涉及氧化还原反应;D项,Br 与
2
NaOH反应生成可溶于水的NaBr和NaBrO,故可除去溴苯中溶解的溴,溴苯不溶于水,可用分液法与
水层分离,但Br 与NaOH反应属于氧化还原反应;选C。
2