文档内容
大题突破 01 工艺流程综合题中的几种常见命题热点
命题热点一 物质的制备和分离
命题热点二 生产中陌生方程式的书写
命题热点三 pH的调控和Ksp的计算
命题热点四 流程中的数据计算
(建议用时:60分钟)
【真题再现】
1.(2022·广东卷)稀土(RE)包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用
离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
已知:月桂酸 C H COOH 熔点为44C;月桂酸和 C H COO RE均难溶于水。该工艺条件下,稀土
11 23 11 23 3
离子保持3价不变; C H COO Mg的K 1.8108 ,Al(OH) 开始溶解时的pH为8.8;有关金属离子
11 23 2 sp 3
沉淀的相关pH见下表。
离子 Mg2 Fe3 Al3 RE3
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(1)“氧化调pH”中,化合价有变化的金属离子是_______。(2)“过滤1”前,用NaOH溶液调pH至_______的
范围内,该过程中Al3发生反应的离子方程式为_______。
(3)“过滤2”后,滤饼中检测不到Mg元素,滤液2中Mg2浓度为2.7gL1。为尽可能多地提取RE3,可提
高月桂酸钠的加入量,但应确保“过滤2”前的溶液中c
C
11
H
23
COO-
低于_______molL1(保留两位有效数
字)。
(4)①“加热搅拌”有利于加快RE3溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂Pt Y。
3①还原YCl 和PtCl 熔融盐制备Pt Y时,生成1molPt Y转移_______mol电子。
3 4 3 3
②Pt Y/C用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化O 的还原,发生的电极反应为_______。
3 2
2.(2022·湖南卷)钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为TiO ,含少量
2
V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
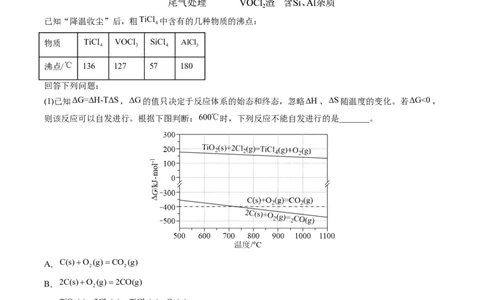
已知“降温收尘”后,粗TiCl 中含有的几种物质的沸点:
4
物质 TiCl VOCl SiCl AlCl
4 3 4 3
沸点/℃ 136 127 57 180
回答下列问题:
(1)已知ΔG=ΔH-TΔS,ΔG的值只决定于反应体系的始态和终态,忽略ΔH、ΔS随温度的变化。若ΔG<0,
则该反应可以自发进行。根据下图判断:600℃时,下列反应不能自发进行的是_______。
A.C(s)O (g)CO (g)
2 2
B.2C(s)O (g)2CO(g)
2
C.TiO (s)2Cl (g)TiCl (g)O (g)
2 2 4 2
D.TiO (s)C(s)2Cl (g)TiCl (g)CO (g)
2 2 4 2
(2)TiO 与C、Cl ,在600℃的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
2 2
物质 TiCl CO CO Cl
4 2 2
分压
4.59102 1.84102 3.70102 5.98109
MPa
①该温度下,TiO 与C、Cl 反应的总化学方程式为_______;
2 2②随着温度升高,尾气中CO的含量升高,原因是_______。
(3)“除钒”过程中的化学方程式为_______;“除硅、铝”过程中,分离TiCl
4
中含Si、Al杂质的方法是
_______。
(4)“除钒”和“除硅、铝”的顺序_______(填“能”或“不能”)交换,理由是_______。
(5)下列金属冶炼方法与本工艺流程中加入Mg冶炼Ti的方法相似的是_______。
A.高炉炼铁 B.电解熔融氯化钠制钠
C.铝热反应制锰 D.氧化汞分解制汞
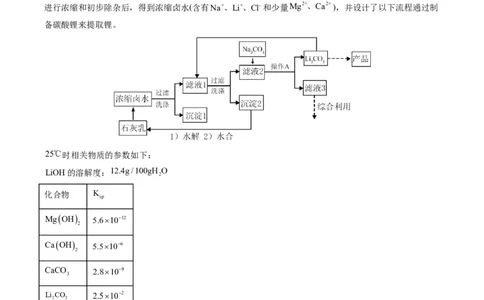
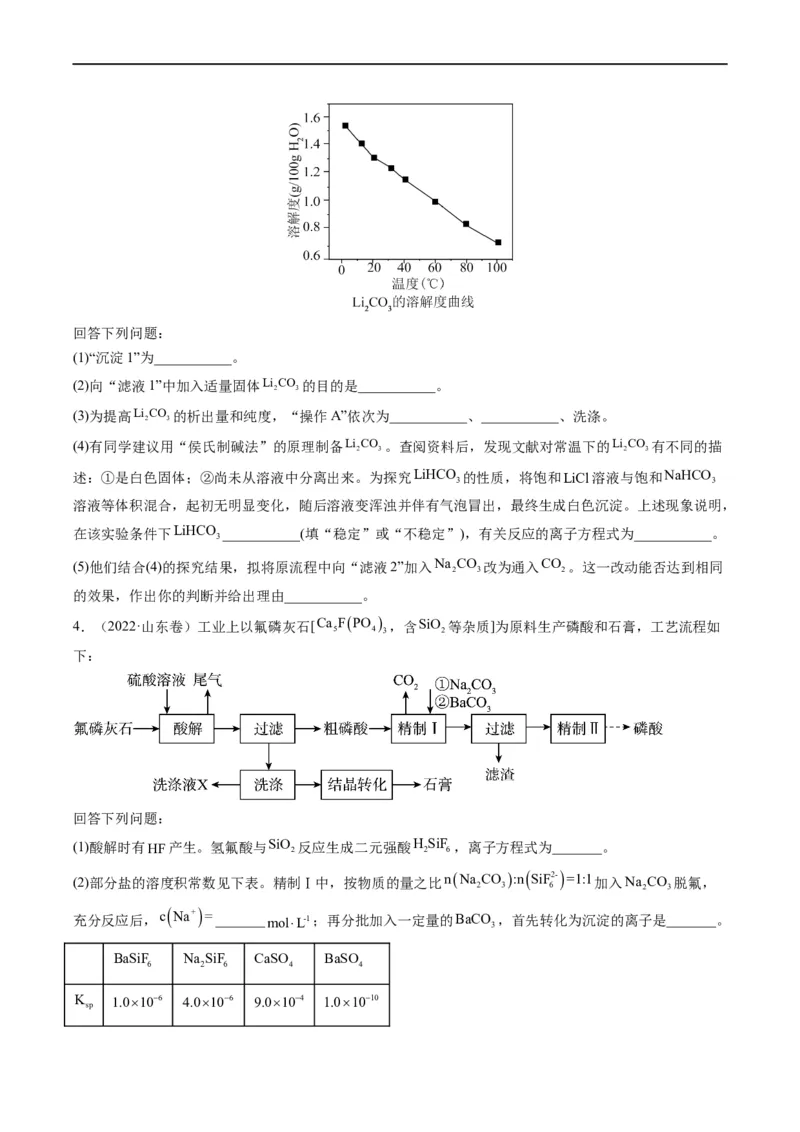
3.(2022·湖北卷)全球对锂资源的需求不断增长,“盐湖提锂”越来越受到重视。某兴趣小组取盐湖水
进行浓缩和初步除杂后,得到浓缩卤水(含有Na+、Li+、Cl-和少量Mg2+、Ca2+),并设计了以下流程通过制
备碳酸锂来提取锂。
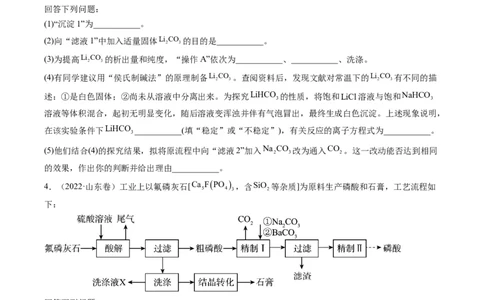
25℃时相关物质的参数如下:
LiOH的溶解度:12.4g/100gH O
2
化合物 K
sp
MgOH 5.61012
2
CaOH 5.5106
2
CaCO 2.8109
3
Li CO 2.5102
2 3回答下列问题:
(1)“沉淀1”为___________。
(2)向“滤液1”中加入适量固体Li CO 的目的是___________。
2 3
(3)为提高Li CO 的析出量和纯度,“操作A”依次为___________、___________、洗涤。
2 3
(4)有同学建议用“侯氏制碱法”的原理制备Li CO 。查阅资料后,发现文献对常温下的Li CO 有不同的描
2 3 2 3
述:①是白色固体;②尚未从溶液中分离出来。为探究LiHCO 的性质,将饱和LiCl溶液与饱和NaHCO
3 3
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。上述现象说明,
在该实验条件下LiHCO ___________(填“稳定”或“不稳定”),有关反应的离子方程式为___________。
3
(5)他们结合(4)的探究结果,拟将原流程中向“滤液2”加入Na CO 改为通入CO 。这一改动能否达到相同
2 3 2
的效果,作出你的判断并给出理由___________。
4.(2022·山东卷)工业上以氟磷灰石[Ca FPO ,含SiO 等杂质]为原料生产磷酸和石膏,工艺流程如
5 4 3 2
下:
回答下列问题:
(1)酸解时有HF产生。氢氟酸与SiO
2
反应生成二元强酸H
2
SiF
6
,离子方程式为_______。
(2)部分盐的溶度积常数见下表。精制Ⅰ中,按物质的量之比nNa CO :n SiF2- =1:1加入Na CO 脱氟,
2 3 6 2 3
充分反应后,c
Na+
=_______molL-1;再分批加入一定量的BaCO ,首先转化为沉淀的离子是_______。
3
BaSiF Na SiF CaSO BaSO
6 2 6 4 4
K 1.0106 4.0106 9.0104 1.01010
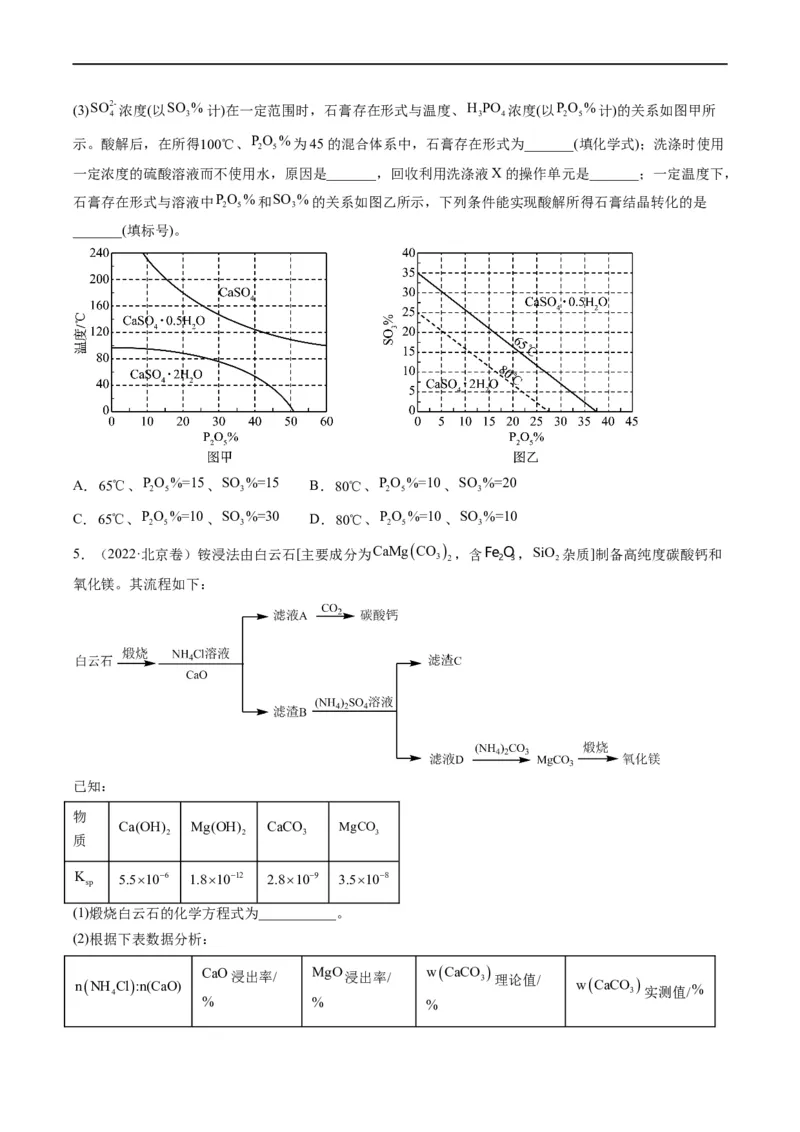
sp(3)SO2- 浓度(以SO %计)在一定范围时,石膏存在形式与温度、H PO 浓度(以PO %计)的关系如图甲所
4 3 3 4 2 5
示。酸解后,在所得100℃、PO %为45的混合体系中,石膏存在形式为_______(填化学式);洗涤时使用
2 5
一定浓度的硫酸溶液而不使用水,原因是_______,回收利用洗涤液X的操作单元是_______;一定温度下,
石膏存在形式与溶液中PO %和SO %的关系如图乙所示,下列条件能实现酸解所得石膏结晶转化的是
2 5 3
_______(填标号)。
A.65℃、PO %=15、SO %=15 B.80℃、PO %=10、SO %=20
2 5 3 2 5 3
C.65℃、PO %=10、SO %=30 D.80℃、PO %=10、SO %=10
2 5 3 2 5 3
5.(2022·北京卷)铵浸法由白云石[主要成分为CaMgCO
,含FeO,SiO 杂质]制备高纯度碳酸钙和
3 2 2 3 2
氧化镁。其流程如下:
已知:
物
Ca(OH) Mg(OH) CaCO MgCO
2 2 3 3
质
K 5.5106 1.81012 2.8109 3.5108
sp
(1)煅烧白云石的化学方程式为___________。
(2)根据下表数据分析:
nNH
4
Cl:n(CaO) CaO浸出率/ MgO 浸出率/ wCaCO 3 理论值/ wCaCO
3
实测值/%
% % %2.1:1 98.4 1.1 99.7 -
2.2:1 98.8 1.5 99.2 99.5
2.3:1 98.9 1.8 98.8 99.5
2.4:1 99.1 6.0 95.6 97.6
已知:i.对浸出率给出定义
ii.对wCaCO
给出定义
3
①“沉钙”反应的化学方程式为___________。
②CaO浸出率远高于MgO浸出率的原因为___________。
③不宜选用的“nNH Cl:n(CaO)”数值为___________。
4
④wCaCO
实测值大于理论值的原因为___________。
3
⑤蒸馏时,随馏出液体积增大,MgO浸出率可出68.7%增加至98.9%,结合化学反应原理解释MgO浸出
率提高的原因为___________。
(3)滤渣C为___________。
(4)可循环利用的物质为___________。
【优选特训】
1.高纯六水氯化锶晶体(SrCl •6H O)具有很高的经济价值,工业上用碳酸锶(SrCO )粉为原料(含少量钡和
2 2 3
铁的化合物等)制备高纯六水氯化锶晶体的过程如图:
已知:①K (SrSO )=3.3×10-7、K (BaSO)=1.1×10-10
sp 4 sp 4
②经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+、Fe2+、Fe3+杂质
③SrCl •6H O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水
2 2
请回答下列问题:
(1)已知Sr为第五周期IIA族元素,则不符合Sr>Ca的是_____。
①原子半径 ②最外层电子数 ③金属性 ④电负性 ⑤最高价氧化物对应的水化物的碱性
(2)写出碳酸锶与盐酸反应的离子方程式:_____。
(3)工业上用热风吹干六水氯化锶,适宜的温度是_____。
A.50~60℃ B.70~80℃ C.80~100℃ D.100℃以上(4)步骤④的操作是_____、_____、过滤。
(5)加入硫酸的目的是_____。
(6)滤渣的成分是_____。
(7)若滤液中Ba2+的浓度为1×10-5mol•L-1,依据题给信息计算滤液中Sr2+的物质的量浓度为_____mol•L-1。
2.(2022·湖北宜昌·高三期中)过氧化钡(BaO )是一种重要的漂白剂,在实验室利用重晶石(主要成分为
2
BaSO )制备BaO 的工艺流程如图所示:
4 2
回答下列问题:
(1)“步骤①”设计如图装置(夹持仪器已省略)制备BaS并检验所产生的气体X。
①实验前及实验结束时均要通入N ,其目的分别是_______、_______。
2
②实验过程中B中品红褪色,C中颜色变淡,D中无现象,G中有白色沉淀生成,气体X的成分为
_______(填化学式);装置C的作用是_______,其中发生主要反应的离子方程式为_______。
(2)“步骤②”中BaS固体与CO 、H O发生反应生成BaCO ,和H S的化学方程式为_______;由于“步骤
2 2 3 2
③”反应剧烈,易产生大量泡沫,为了避免此种情况的发生,应采用措施是_______。
(3)“步骤④"中BaCl 溶液与双氧水、氨水反应析出BaO 8H O沉淀,发生反应的离子方程式为_______,
2 2 2
反应过程中需要控制反应温度为0℃左右,其原因主要有:a.该反应是放热反应,降温有利于反应正向进行,
提高产率;b._______。
3.(2022·四川绵阳·一模)某废镍催化剂的主要成分是Ni-Al合金,还含有少量Cr、Fe及不溶于酸碱的有
机物。采用如下工艺流程回收其中的镍制备镍的氧化物 Ni O :
x y回答下列问题:
(1)“碱浸”所得“滤液1”的主要溶质为NaOH、_______,“灼烧”的目的是_______。
(2)“溶解”后的溶液中,所含金属离子有Cr3+、Fe2+、Na+、_______、_______。
(3)“分离除杂”中,发生氧化还原反应生成含铁滤渣的离子方程式为_______。
(4)“煅烧”NiCO 滤渣前需进行的两步操作是_______。
3
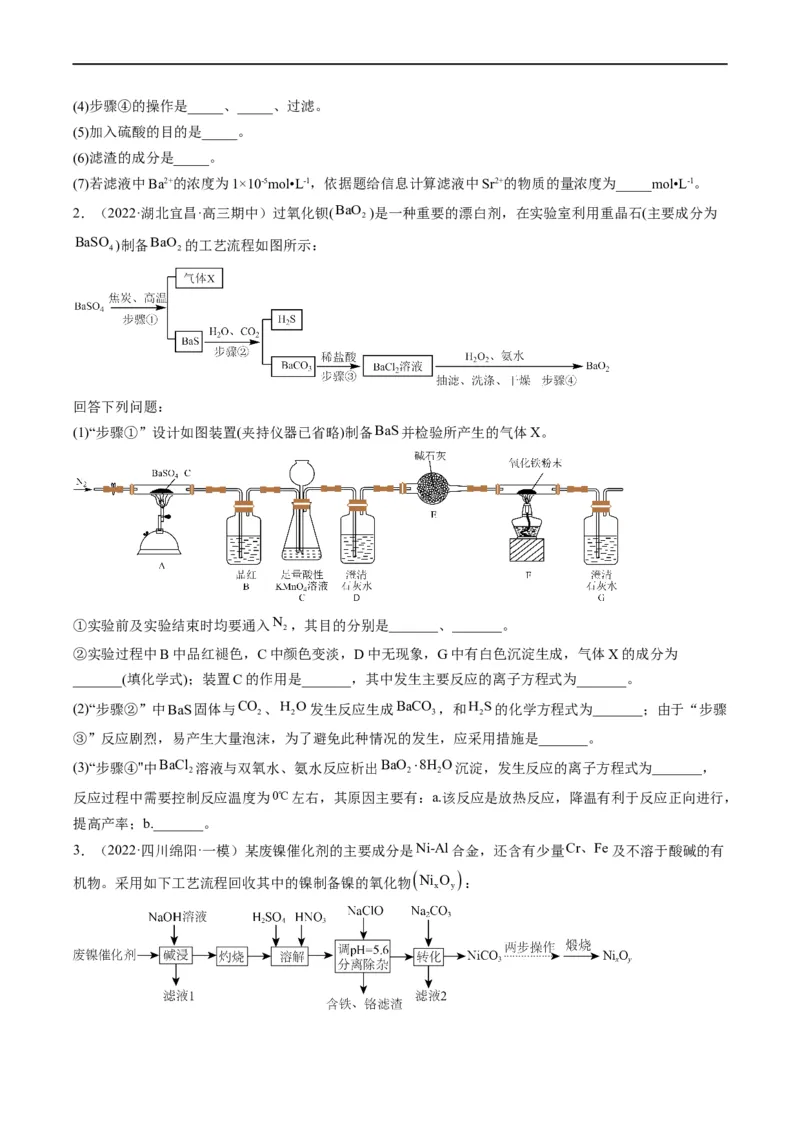
(5)在空气中煅烧NiCO ,其热重曲线如图所示。300~400℃NiCO 转化为Ni O ,反应的化学方程式为
3 3 2 3
_______;400~450℃生成产物的化学式为_______。
(6)利用 Ni O 制得NiCl 溶液,调节其pH至7.5~12,采用惰性电极进行电解,阳极上可沉淀出用作锌镍
x y 2
电池正极材料的NiOOH。电解时阳极的电极反应式为_______。
4.一种从铋冶炼浸渣(浸渣中的铅多数以硫酸铅的形态存在,少量以氧化铅、碳酸铅的形态存在)为原料生
产三盐基硫酸铅(3PbOPbSO H O)的工艺流程如图所示。
4 2
已知常温下,K PbCO 7.41014 ,K PbSO 1.6108,K NH HCO 1.25103 ,
sp 3 sp 4 h 4 3
K H CO 4107
a1 2 3
回答下列问题:
(1)常温下,NH H O的电离平衡常数K =_______。
3 2 b
(2)写出转化过程PbSO 发生反应的化学方程式_______,Pb的转化率随着NH HCO 用量的增加而增加,
4 4 3
醋酸可以促进硫酸铅溶解,但实验表明:Pb的转化率随醋酸用量的增加而减少,这是由于_______。
(3)测得滤液1中c SO2
4
0.1molL1 ,则该滤液中c CO
3
2 _______molL1(保留1位小数);滤液2中可
以循环利用的物质是_______;从滤液3可提取出一种含结晶水的钠盐副产品,若测定该晶体中结晶水的含
量,所需的仪器除三脚架、托盘天平、瓷坩埚、干燥器、酒精灯、玻璃棒,还需要的仪器有_______。
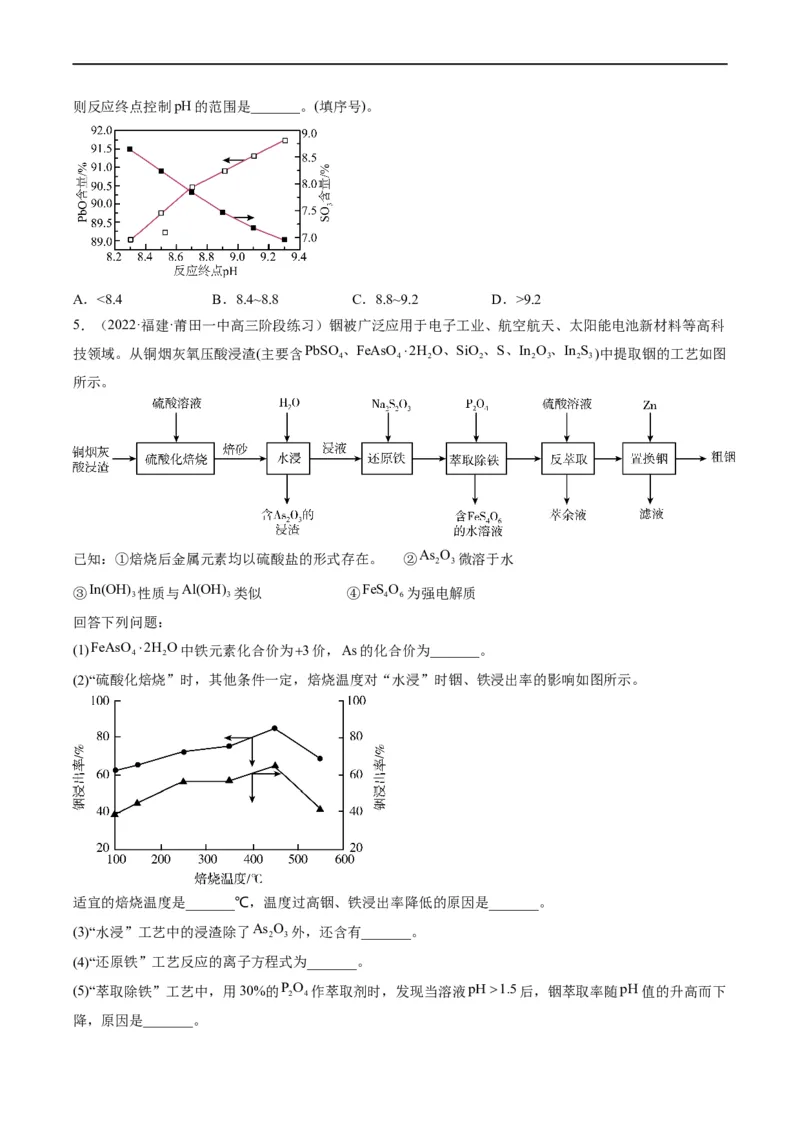
(4)合成三盐基硫酸铅时,影响产品纯度的因素很多,其中反应终点pH对产品中PbO和SO 含量的影响如
3
下图(将PbSO 看作是PbO和SO ,经测定三盐基硫酸铅中PbO理论含量90.10%,SO 理论含量8.08%),
4 3 3则反应终点控制pH的范围是_______。(填序号)。
A.<8.4 B.8.4~8.8 C.8.8~9.2 D.>9.2
5.(2022·福建·莆田一中高三阶段练习)铟被广泛应用于电子工业、航空航天、太阳能电池新材料等高科
技领域。从铜烟灰氧压酸浸渣(主要含PbSO、FeAsO 2H O、SiO 、S、In O、In S )中提取铟的工艺如图
4 4 2 2 2 3 2 3
所示。
已知:①焙烧后金属元素均以硫酸盐的形式存在。 ②As O 微溶于水
2 3
③In(OH) 性质与Al(OH) 类似 ④FeS O 为强电解质
3 3 4 6
回答下列问题:
(1)FeAsO 2H O中铁元素化合价为3价,As的化合价为_______。
4 2
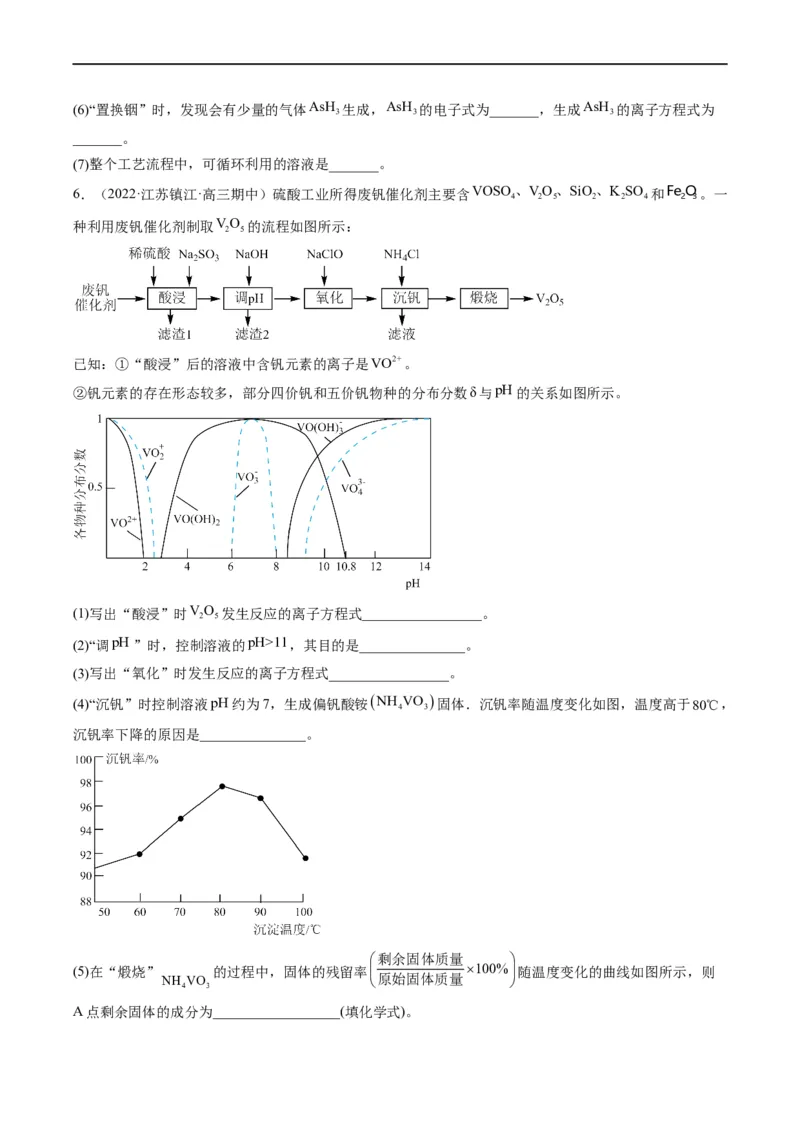
(2)“硫酸化焙烧”时,其他条件一定,焙烧温度对“水浸”时铟、铁浸出率的影响如图所示。
适宜的焙烧温度是_______℃,温度过高铟、铁浸出率降低的原因是_______。
(3)“水浸”工艺中的浸渣除了As O 外,还含有_______。
2 3
(4)“还原铁”工艺反应的离子方程式为_______。
(5)“萃取除铁”工艺中,用30%的PO 作萃取剂时,发现当溶液pH1.5后,铟萃取率随pH值的升高而下
2 4
降,原因是_______。(6)“置换铟”时,发现会有少量的气体AsH 生成,AsH 的电子式为_______,生成AsH 的离子方程式为
3 3 3
_______。
(7)整个工艺流程中,可循环利用的溶液是_______。
6.(2022·江苏镇江·高三期中)硫酸工业所得废钒催化剂主要含VOSO、VO、SiO、K SO 和FeO。一
4 2 5 2 2 4 2 3
种利用废钒催化剂制取VO 的流程如图所示:
2 5
已知:①“酸浸”后的溶液中含钒元素的离子是VO2+。
②钒元素的存在形态较多,部分四价钒和五价钒物种的分布分数δ与pH的关系如图所示。
(1)写出“酸浸”时VO 发生反应的离子方程式_________________。
2 5
(2)“调pH”时,控制溶液的pH>11,其目的是_______________。
(3)写出“氧化”时发生反应的离子方程式_________________。
(4)“沉钒”时控制溶液pH约为7,生成偏钒酸铵 NH
4
VO
3
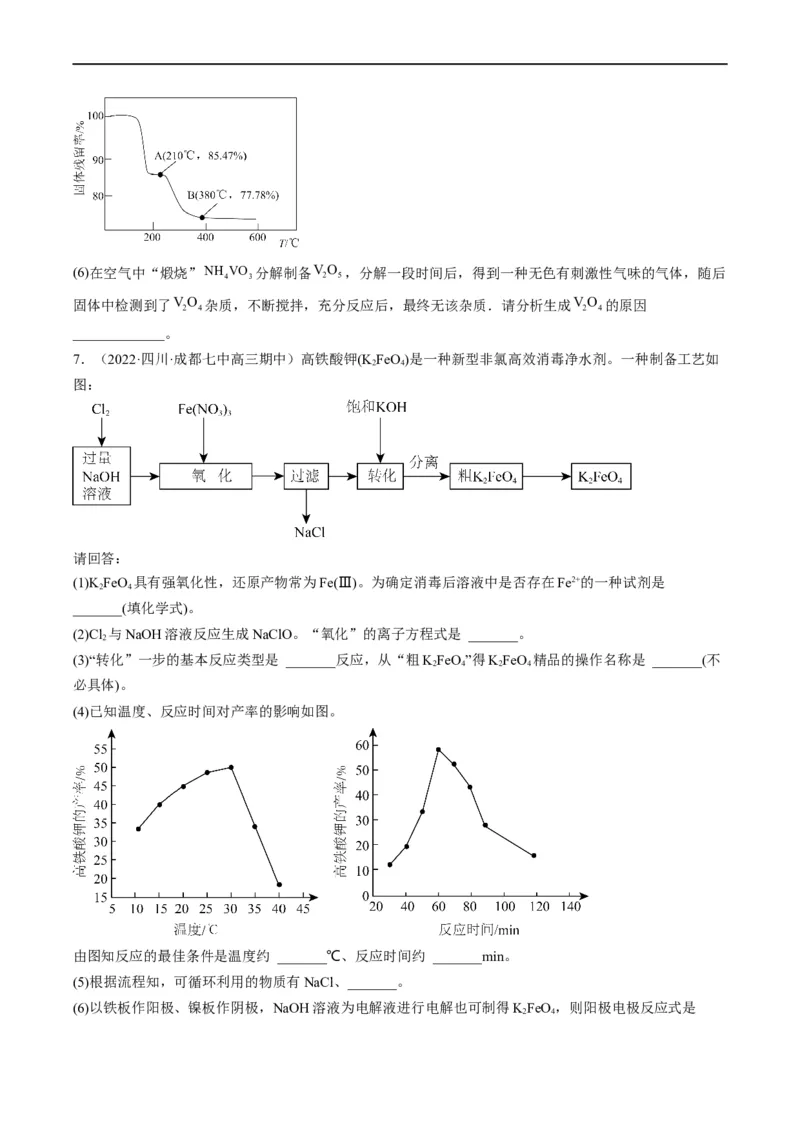
固体.沉钒率随温度变化如图,温度高于80℃,
沉钒率下降的原因是_______________。
剩余固体质量
(5)在“煅烧” 的过程中,固体的残留率 100% 随温度变化的曲线如图所示,则
NH VO 原始固体质量
4 3
A点剩余固体的成分为__________________(填化学式)。(6)在空气中“煅烧”NH VO 分解制备VO ,分解一段时间后,得到一种无色有刺激性气味的气体,随后
4 3 2 5
固体中检测到了VO 杂质,不断搅拌,充分反应后,最终无该杂质.请分析生成VO 的原因
2 4 2 4
_____________。
7.(2022·四川·成都七中高三期中)高铁酸钾(K FeO)是一种新型非氯高效消毒净水剂。一种制备工艺如
2 4
图:
请回答:
(1)K FeO 具有强氧化性,还原产物常为Fe(Ⅲ)。为确定消毒后溶液中是否存在Fe2+的一种试剂是
2 4
_______(填化学式)。
(2)Cl 与NaOH溶液反应生成NaClO。“氧化”的离子方程式是 _______。
2
(3)“转化”一步的基本反应类型是 _______反应,从“粗KFeO”得KFeO 精品的操作名称是 _______(不
2 4 2 4
必具体)。
(4)已知温度、反应时间对产率的影响如图。
由图知反应的最佳条件是温度约 _______℃、反应时间约 _______min。
(5)根据流程知,可循环利用的物质有NaCl、_______。
(6)以铁板作阳极、镍板作阴极,NaOH溶液为电解液进行电解也可制得KFeO,则阳极电极反应式是
2 4_______。
(7)某温度,若要从10m3含c(FeO 2 )=2.0×10﹣4mol•L﹣1的循环母液中沉淀FeO 2 (浓度降至10﹣5mol•L﹣1),
4 4
理论上需加入Ca(OH) 固体的物质的量不少于 _______mol。(已知CaFeO 的K =4.5×10﹣9,不考虑水解和
2 4 sp
溶液体积变化。)
8.铟是一种稀有贵金属,广泛应用于航空航天、太阳能电池等高科技领域。从铜烟灰酸浸渣(主要含
PbO、FeAsO ·2H O、InO)中提取铟和铅的工艺流程如下:
4 2 2 3
已知:①焙烧后金属元素均以硫酸盐的形式存在;
②In(OH) 性质与Al(OH) 类似。
3 3
回答下列问题:
(1)FeAsO ·2H O中铁元素化合价为_______。
4 2
(2)生成PbO粗品的化学反应方程式为_______。
(3)PbO在NaOH溶液中溶解度曲线如图所示,PbO粗品中的杂质难溶于NaOH溶液。结合溶解度曲线,简
述提纯PbO粗品的操作_______。
(4)“还原铁”反应的离子方程式为________
(5)“萃取除铁”中,发现当溶液pH>1.5后,钢萃取率随pH的升高而下降,原因是_______
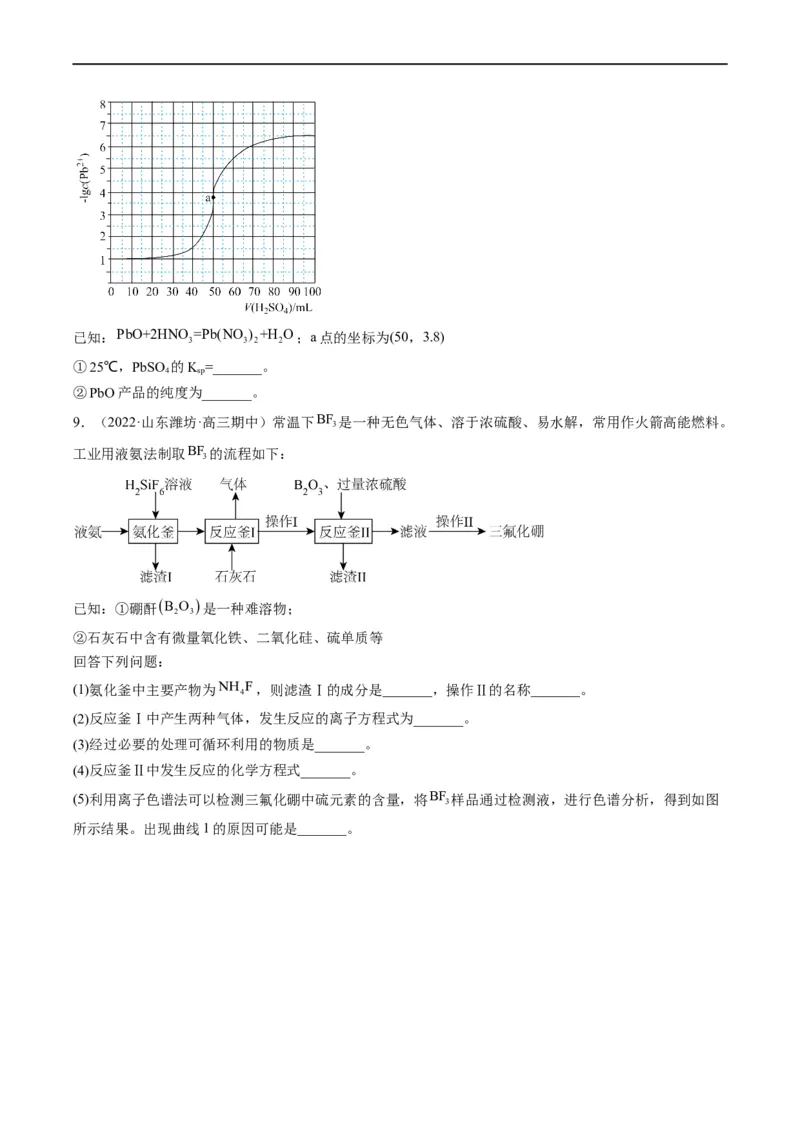
(6)为测定PbO产品的纯度,探究小组同学准确称取PbO1.161g,加入稀硝酸使其完全溶解,再加入蒸馏水
配制成50.00mL溶液:冷却至25℃,用0.100mol·L-1HSO 滴定该溶液,滴定曲线如图所示。
2 4已知:PbO+2HNO =Pb(NO ) +H O;a点的坐标为(50,3.8)
3 3 2 2
①25℃,PbSO 的K =_______。
4 sp
②PbO产品的纯度为_______。
9.(2022·山东潍坊·高三期中)常温下BF 是一种无色气体、溶于浓硫酸、易水解,常用作火箭高能燃料。
3
工业用液氨法制取BF 的流程如下:
3
已知:①硼酐 B O 是一种难溶物;
2 3
②石灰石中含有微量氧化铁、二氧化硅、硫单质等
回答下列问题:
(1)氨化釜中主要产物为NH F,则滤渣Ⅰ的成分是_______,操作Ⅱ的名称_______。
4
(2)反应釜Ⅰ中产生两种气体,发生反应的离子方程式为_______。
(3)经过必要的处理可循环利用的物质是_______。
(4)反应釜Ⅱ中发生反应的化学方程式_______。
(5)利用离子色谱法可以检测三氟化硼中硫元素的含量,将BF 样品通过检测液,进行色谱分析,得到如图
3
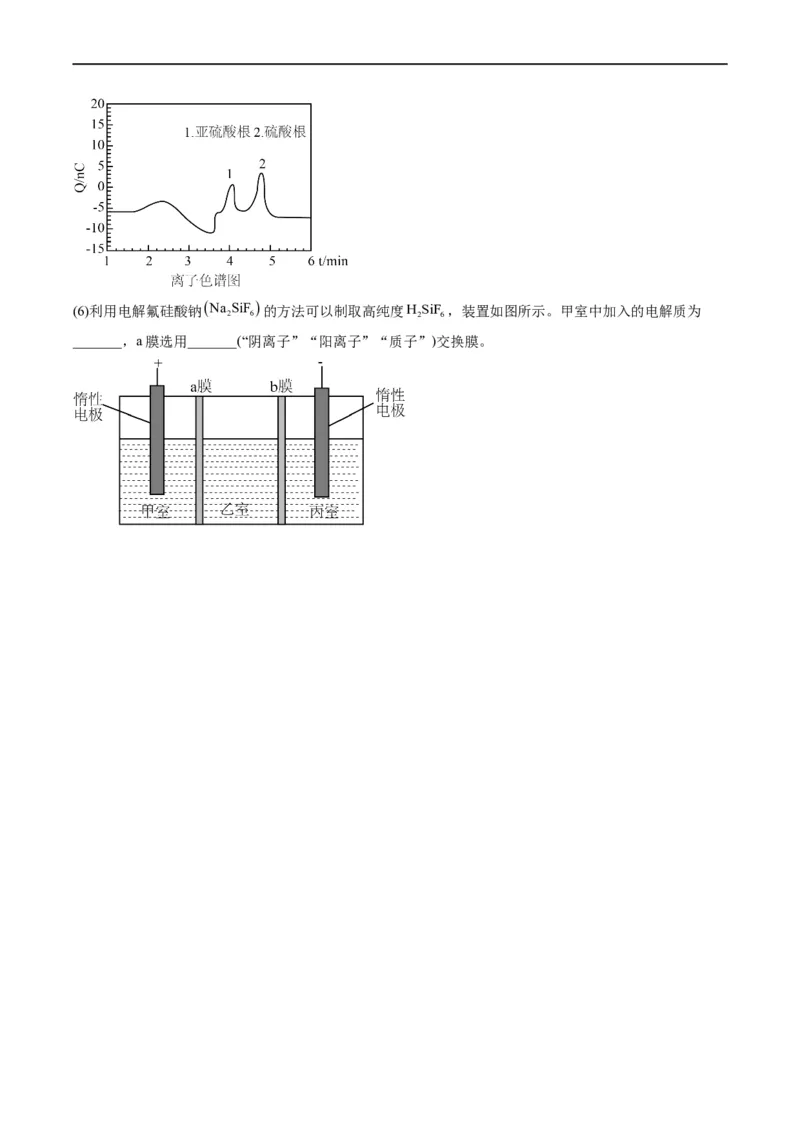
所示结果。出现曲线1的原因可能是_______。(6)利用电解氟硅酸钠 Na SiF 的方法可以制取高纯度H SiF ,装置如图所示。甲室中加入的电解质为
2 6 2 6
_______,a膜选用_______(“阴离子”“阳离子”“质子”)交换膜。