文档内容
枣庄三中 2022-2023 学年度高三年级 9 月质量检测考试
化学试题
本试卷分为第 I 卷(选择题)和第 II 卷(非选择题)两部分。满分 100 分,考试用时 90 分钟。答
卷前,考生务必将自己的姓名、准考证号、考试科目填涂在答题卡和答题纸规定的地方。
可能用到的相对原子质量: C 12 N 14 O 16 Na 23 S 32 Cl 35.5 K39 I 127 Ba 137
第 I 卷(选择题 共 40 分)
一、选择题:(本题共 10 小题,每小题 2 分,共 20 分。每小题只有一个选项符合题意。)
1.《医学入门》中记载我国传统中医提纯铜绿的方法:“水洗净,细研水飞,去石澄清,慢火熬干,”其中
未 涉 及 的操作 )
. . .
是 (
A.洗涤 B.粉碎 C.萃取 D.蒸发
2.化学实验操作是进行科学实验的基础。下列操作符合规范的是 ( )
A.碱式滴定管排气泡 B.溶液的转移 C.试剂存放 D.溶液滴加
3.以下说法正确的是 ( )
A.钠元素的第一电离能大于钾
B. 基态钾原子价层电子轨道表示式为
C. 钾能置换出 NaCl 溶液中的钠
D. 钠元素与钾元素的原子序数相差 18
4.下列关于 Na 的化合物之间转化反应的离子方程式书写正确的是 (
) A.碱转化为酸式盐:
B. 碱转化为两种盐:
C. 过氧化物转化为碱:
D. 盐转化为另一种盐:
5.劳动创造未来。下列劳动项目涉及的化学知识正确的是 ( )选项 劳动项目 化学知识
A 用小苏打做蛋糕膨松剂 NaCO 与酸反应产生气体
2 3
B 将新切土豆丝浸没在水里防止变色 土豆中的氧化性物质遇空气变色
C 煮豆浆点卤水制作豆腐 胶体聚沉
D 用铁质槽罐车运输浓硫酸 常温下,浓硫酸和铁不反应
6.某白色粉末样品,可能含有Na SO 、 Na SO 、 Na SO 和 Na CO 。取少量样品进行如下实验:
2 4 2 3 2 2 3 2 3
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加BaCl 溶液有沉淀生成。
2
该样品中确定存在的是 ( )
Na SO 、Na S O
A. 2 4 2 2 3 Na SO 、Na S O
B. 2 3 2 2 3
Na SO 、Na CO D. Na SO 、Na CO
C. 2 4 2 3 2 3 2 3
7.下列各组物质的分类正确的是 ( )
选项 混合物 电解质 酸性氧化物 化合物
A 氯水 乙醇 NO CaCl
2 5 2
B 氨水 冰醋酸 MnO NaOH
2 7
C 水玻璃 石膏 SO HD
2
D 水银 氟化氢 CO HCl
2
8.设 N 为阿伏加德罗常数的值,下列叙述正确的是 ( )
A
A.78gNaO 中含有的阴离子数为 2N
2 2 A
B. 2g 环状 S ( )分子中含有的 S-S 键数为 N
8 A
C. 在 25℃时,pH 为 12 的 Ba(OH) 溶液中含有 OH-数目为 0.01N
2 A
D. 常温下,5.6g 铁粉与足量浓硝酸反应,转移的电子数为 0.3N
A
9.依据下列实验,预测的实验现象正确的是 ( )
选项 实验内容 预测的实验现象
MgCl 溶液中滴加 NaOH 溶
A 2 产生白色沉淀后沉淀消失
液至过量
B FeCl 溶液中滴加 KSCN 溶液 溶液变血红色
2
下载最新免费模拟卷,到公众号:一枚试卷君AgI 悬浊液中滴加 NaCl 溶
C 黄色沉淀全部转化为白色沉淀
液至过量
酸性 KMnO 溶液中滴加乙醇
D 4 溶液紫红色褪去
至过量
10. 一种利用有机胺(TBA)联合生产碳酸氢钠和二氯乙烷的工艺流程如图所示。
下列说法错误的是 ( )
A.“制碱过程”后通过加热蒸发结晶得到 NaHCO
3
B.该工艺原子利用率 100%
C.“氯化过程”每生成 lmolCHCl,总反应中消耗 0.5molO
2 4 2 2
D.“胺再生过程”反应为 4CuCl+O+4TBA·HCl=4CuCl+4TBA+2HO
2 2 2
二、选择题:本题共 5 小题,每小题 4 分,共 20 分。每小题有一个或两个选项符合题意,全部选对得 4
分,选对但不全的得 2 分,有选错的得 0 分。
11. 由硫铁矿烧渣(主要含 FeO、AlO、SiO)制取绿矾(FeSO·7HO)的流程如下:
2 3 2 3 2 4 2
已知 SiO 是一种酸性氧化物。下列说法正确的是 ( )
2
A.“滤液Ⅰ”溶质中只含有 NaOH 和 NaAlO
2
B. “酸浸”时的离子反应方程式为
C. “还原”过程中铁粉只发生置换反应
D. D.将“滤液Ⅱ”蒸干后可获得
FeSO·7HO
4 2
12. 次磷酸(H PO )与足量的氢氧化钠溶液反应生成NaH PO 溶液,H PO ﹣可以用于镀铜,发生反应的离
3 2 2 2 2 2
子方程式为H PO ﹣+2Cu2++6OH﹣=PO 3﹣+2Cu↓+4H O。下列说法正确的是( )
2 2 4 2
A. H PO 中 P 元素的化合价为3 价 B. NaH PO 属于正盐
3 2 2 2
C.还原性: H PO Cu D.若反应生成 1mol Cu,转移 4mol e
2
13.亚硝酸钠俗称“工业盐”,其外观、口感与食盐相似,人若误服会中毒。现将适量某样品(成分为亚硝酸钠或氯化钠)溶于水配成溶液,分别取少量该溶液于试管中进行实验。下列方案设计、现象和结论都正
确的是 ( )
方案设计 现象和结论
先加入少量 KClO 溶液,再加 AgNO 溶液和足
A 3 3 若产生白色沉淀,则样品为亚硝酸钠
量稀硝酸,振荡
加到少量 KMnO 溶液中,再加硫酸酸化,振
B 4 若溶液褪色,则样品为亚硝酸钠
荡
先加到少量 FeCl 溶液中,再加入稀盐酸酸
C 2 若溶液变黄色,则样品为亚硝酸钠
化,振荡
先加入少量 NaSO 溶液,再加入 BaCl 溶液
D 2 3 2 若产生白色沉淀,则样品为亚硝酸钠
14.实验室制备 KMnO 过程为:①高温下在熔融强碱性介质中用 KClO 氧化 MnO 制备 KMnO;②水溶后冷却,
和稀硝酸,振荡4 3 2 2 4
调溶液pH 至弱碱性,KMnO 歧化生成 KMnO 和 MnO;③减压过滤,将滤液蒸发浓缩、冷却结晶,再减压过
2 4 4 2
滤得 KMnO。下列说法不正确的是
4
A.①中用瓷坩埚作反应器 B.①中用 KOH 作强碱性介质
C.②中 KMnO 只体现氧化性 D.MnO 转化为 KMnO 的理论转化率约为
2 4 2 4
66.7% 15.为探究 FeCl 的性质,进行了如下实验(FeCl 和 NaSO 溶液浓度均为
3 3 2 3
0.1mol L-1 )。
实验 操作与现象
① 在 5mL 水中滴加 2 滴 FeCl 溶液,呈棕黄色;煮沸,溶液变红褐
3
色。
在 5mLFeCl 溶液中滴加 2 滴 NaSO 溶液,变红褐
3 2 3
②
K Fe(CN)
色;再滴加 3 6 溶液,产生蓝色沉淀。
在 5mLNaSO 溶液中滴加 2 滴 FeCl 溶液,变红褐色;
2 3 3
K Fe(CN)
③ 将上述混合液分成两份,一份滴加 3 6 溶液,无蓝色沉淀
生;
另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是 ( )
A.实验①说明加热促进 Fe3+ 水解反应
B. 实验②说明Fe3+ 既发生了水解反应,又发生了还原反应
C. 实验③说明Fe3+ 发生了水解反应,但没有发生还原反应
D. 整个实验说明 SO2-对 Fe3+的水解反应无影响,但对还原反应有影响
3第 II 卷(非选择共 60 分)
16.(1)KIO 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为:
3
完善并配平该反应。
(2)铝与 在酸性或碱性条件下均可反应,为了降低饮用水中 的浓度,可以在碱性条件
下用铝粉
将 NO3- 还原为N2 ,完善并配平该反应:(产物中铝元素以偏铝酸根形式存在)
(3)已知:CCl 与水不相溶且密度比水大,Cl 的 CCl 溶液呈黄绿色,Br 的 CCl 溶液呈橙红色,且 Br 易
4 2 4 2 4 2
从水溶液中溶入 CCl 中。Cl 既能氧化Br- ,也能氧化Fe2+ 。
4 2
①取10mL 0.1mol/L FeBr 溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液
2
加入 KSCN 溶液,溶液变为红色。另取少量反应后的溶液加入 CCl,振荡后,下层为无色液体。以上实验
4
结论表明还原性: Fe2+ Br- (填“>”或“<”)。
②若在 400mL 0.1mol/L FeBr 溶液中通入标准状况下 672mL 的 Cl,取少量反应后的溶液加入 CCl,振荡
2 2 4
后下层液体呈 色,写出该反应的离子方程式 。
17. 二草酸合铜(Ⅱ)酸钾( K [Cu(C O ) ])可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)
2 2 4 2
酸钾可采用如下步骤:
Ⅰ.取已知浓度的CuSO 溶液,搅拌下滴加足量NaOH 溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,
4
过滤。
Ⅱ.向草酸( H C O )溶液中加入适量KCO 固体,制得KHC O 和KC O 混合溶液。
2 2 4 2 3 2 4 2 2 4
Ⅲ.将Ⅱ的混合溶液加热至 80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和
分析。
回答下列问题:
(1)由 CuSO 5H O 配制Ⅰ中的 CuSO 溶液,下列仪器中不需要的是 (填仪器名称)。
4 2 4(2)长期存放的 CuSO 5H O 中,会出现少量白色固体,原因是 。
4 2
(3)Ⅰ中的黑色沉淀是 (写化学式)。
(4)Ⅱ中原料配比为 n(H C O ):n(KCO )=1.5:1,写出反应的化学方程式 。
2 2 4 2 3
(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入 K CO 应采取 的方法。
2 3
(6)Ⅲ中应采用 进行加热。
(7)Ⅳ中“一系列操作”包括 。
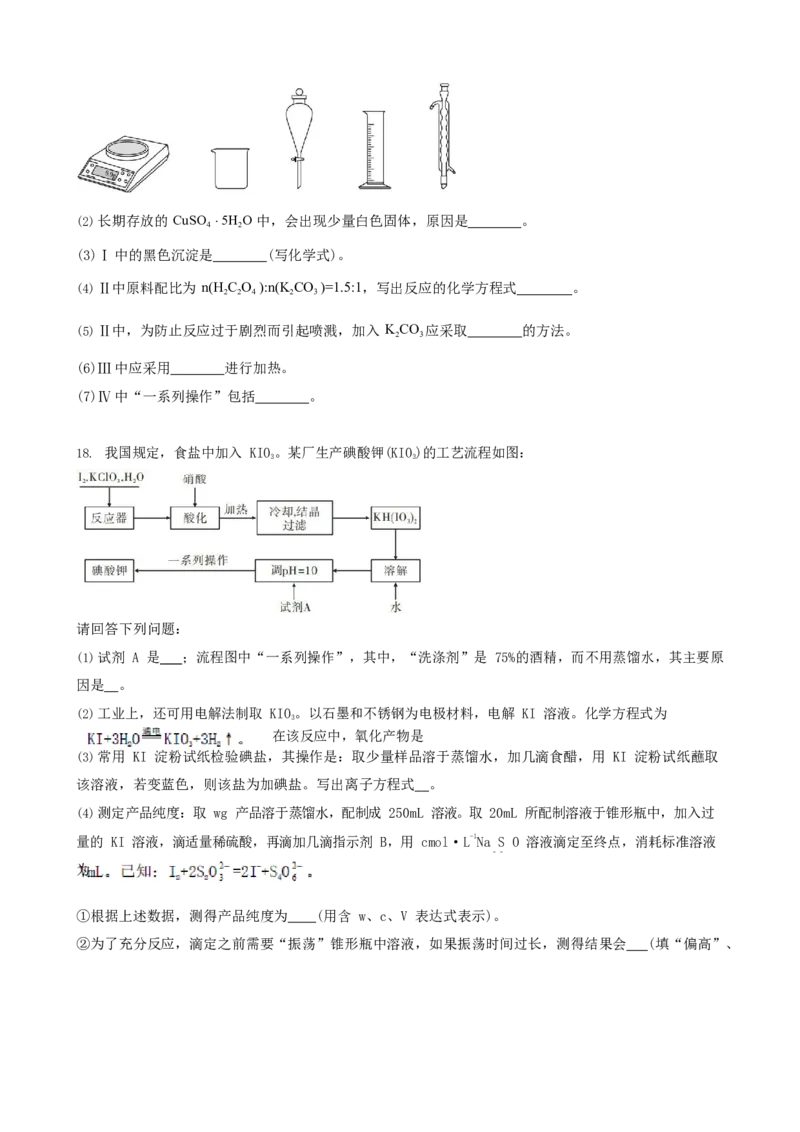
18. 我国规定,食盐中加入 KIO。某厂生产碘酸钾(KIO)的工艺流程如图:
3 3
请回答下列问题:
(1)试剂 A 是 ;流程图中“一系列操作”,其中,“洗涤剂”是 75%的酒精,而不用蒸馏水,其主要原
因是 。
(2)工业上,还可用电解法制取 KIO。以石墨和不锈钢为电极材料,电解 KI 溶液。化学方程式为
3
在该反应中,氧化产物是
(3)常用 KI 淀粉试纸检验碘盐,其操作是:取少量样品溶于蒸馏水,加几滴食醋,用 KI 淀粉试纸蘸取
该溶液,若变蓝色,则该盐为加碘盐。写出离子方程式 。
(4)测定产品纯度:取 wg 产品溶于蒸馏水,配制成 250mL 溶液。取 20mL 所配制溶液于锥形瓶中,加入过
量的 KI 溶液,滴适量稀硫酸,再滴加几滴指示剂 B,用 cmol·L-1Na S O 溶液滴定至终点,消耗标准溶液
2 2
为
①根据上述数据,测得产品纯度为 (用含 w、c、V 表达式表示)。
②为了充分反应,滴定之前需要“振荡”锥形瓶中溶液,如果振荡时间过长,测得结果会 (填“偏高”、“偏低”或“无影响”)。
19. 某实验小组以BaS 溶液为原料制备BaCl 2H O ,并用重量法测定产品中BaCl 2H O 的含量。设计了
2 2 2 2
如下实验方案:
可选用试剂: NaCl晶体、BaS 溶液、浓HSO 、稀HSO 、CuSO 溶液、蒸馏水
2 4 2 4 4
步骤 1. BaCl 2H O 的制备
2 2
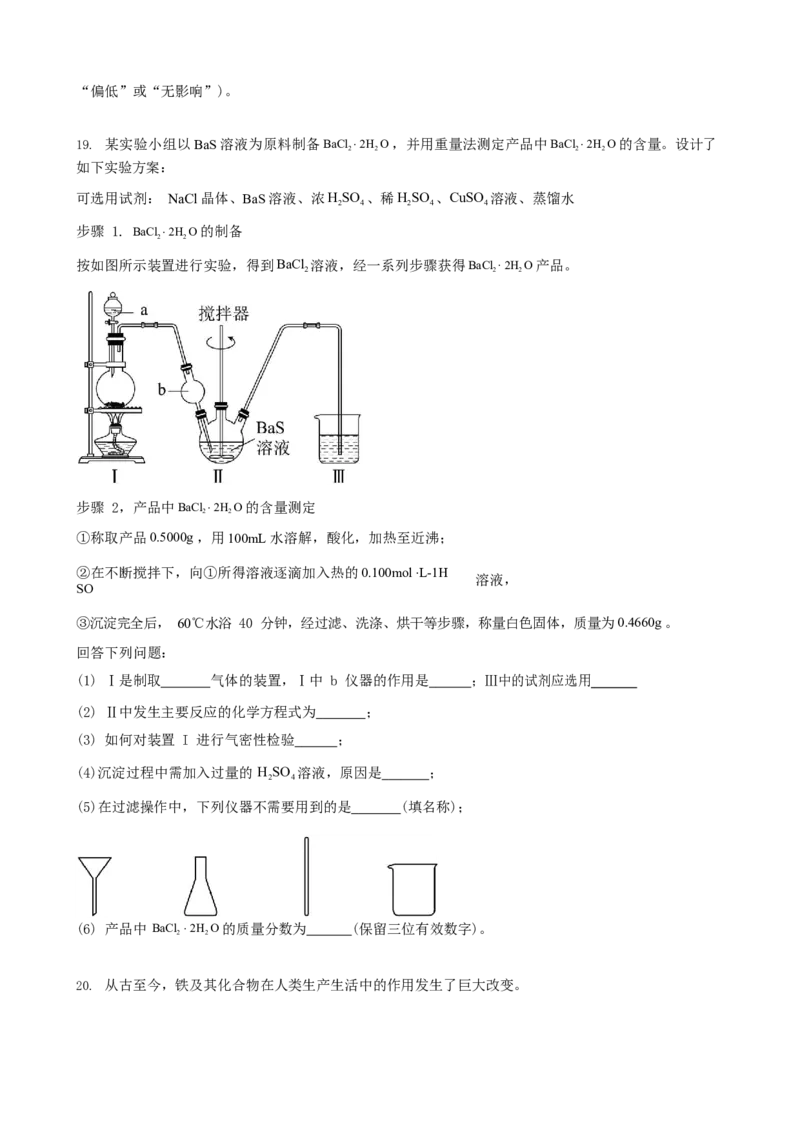
按如图所示装置进行实验,得到BaCl 溶液,经一系列步骤获得BaCl 2H O 产品。
2 2 2
步骤 2,产品中BaCl 2H O 的含量测定
2 2
①称取产品0.5000g ,用100mL 水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的0.100mol L-1H
溶液,
SO
2
③沉淀完全后, 60℃水浴 40 分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量为0.4660g 。
回答下列问题:
(1) Ⅰ是制取 气体的装置,Ⅰ中 b 仪器的作用是 ;Ⅲ中的试剂应选用
(2) Ⅱ中发生主要反应的化学方程式为 ;
(3) 如何对装置 I 进行气密性检验 ;
(4)沉淀过程中需加入过量的 H SO 溶液,原因是 ;
2 4
(5)在过滤操作中,下列仪器不需要用到的是 (填名称);
(6) 产品中 BaCl 2H O 的质量分数为 (保留三位有效数字)。
2 2
20. 从古至今,铁及其化合物在人类生产生活中的作用发生了巨大改变。(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是 (填字母序号)。
a.Fe b.FeO c.FeO d.FeO
3 4 2 3
若将该成分溶于足量的稀硫酸中,再滴加 KSCN 溶液,溶液变红,继续滴加双氧水至过量,溶液红色褪去,
同时有气泡产生。
猜想一:气泡可能是 SCN-的反应产物 N 、CO 、SO 或 N 、CO ;
2 2 2 2
猜想二:气泡还可能是 ,理由是 。(用化学方程式表示)
(2)硫酸渣的主要化学成分为:SiO 约 45%,FeO 约 40%,AlO 约 10%,MgO 约 5%。用该废渣制取药用辅料
2 2 3 2 3
——红氧化铁的工艺流程如下(部分操作和条件略):
回答下列问题:
①在步骤 i 中产生的有毒气体可能有 。
②步骤 iv 中,生成 FeCO 的离子方程式是 。
3
(3)古老而神奇的蓝色染料普鲁士蓝的合成方法如下:
复分解反应 ii 的离子方程式是 。