文档内容
考点 02 离子反应 离子方程式
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 电解质及其电离方程式.............................................................................................................2
考法02 离子反应与离子方程式的书写..................................................................................................5
考法03 “与量有关型”离子方程式的书写..........................................................................................8
...........................................................................................................................................12
1.高考真题考点分布
考点内容 考点分布
2023浙江6月9题,3分;2023浙江1月7题,3分;2023海南卷5题,2分;
2023全国卷9题,6分;2022全国甲卷9题,6分;2022湖南卷11题,4分;2022
离子方程式正误判
广东卷14题,4分;2022浙江1月13题,3分;2022浙江6月13题,3分;2021
断
全国乙卷9题,6分;2021浙江1月13题,3分;2021浙江6月13题,3分;
2021北京卷7题,3分;2021湖北卷4题,3分
电解质和非电解质 2024浙江1月卷1题,2分;2022浙江1月卷2题,2分;2021北京卷8题,3
分;
2021浙江6月卷2题,2分;2020浙江1月卷3题,2分
2.命题规律及备考策略
【命题规律】
从近几年全国高考试题来看,电解质的相关概念判断、电离方程式的书写、电解质溶液导电性、离子方程
式正误判断、陌生离子方程式书写仍是高考命题的热点。
【备考策略】
解答有关离子方程式正误判断试题的方法步骤【命题预测】
预计2025年高考会以新的情境载体考查有关离子方程式的书写及正误判断,在选择题中也会考查电解质的
判断及其电离知识,还会结合氧化还原反应、化学反应原理在工艺流程、实验题中考查,该类试题具有一
定的综合性。
考法01 电解质及其电离方程式
1.电解质和非电解质
项目 电解质 非电解质
范畴
条件
现象 电 电
实质 自身电离出离子 自身 电离出离子
2.强电解质和弱电解质的比较(水溶液中)
项目 强电解质 弱电解质
定义 在水溶液中能 电离的电解质 在水溶液中 电离的电解质
电离平衡
溶液中存在
微粒种类
电离过程
①强酸:HCl、HSO 、HNO、HClO、 ①弱酸:CHCOOH、HF、HS、HCO
2 4 3 4 3 2 2 3
HBr、HI等; 等;
举例 ②强碱:KOH、NaOH、Ba(OH) 等; ②弱碱:NH ·H O、Cu(OH) 等;
2 3 2 2
③绝大部分盐:BaSO、BaCl 等 ③少数盐:Fe(SCN) 等;
4 2 3
④金属氧化物:CaO、Al O 等; ④水(HO)
2 3 2
3.电解质和非电解质的判断方法【易错提醒】
(1)单质和混合物既不是电解质也不是非电解质。
(2)电解质不一定能导电,如固态NaCl、液态HCl等;能导电的物质不一定是电解质,如铁、铝等金属单
质。
(3)本身电离而导电的化合物才是电解质。如CO、SO 、NH 的水溶液能导电,但均是非电解质。
2 2 3
(4)电解质的强弱与电解质溶液导电能力的强弱、溶解性的大小没有直接关系。如碳酸钙,其溶解性小,
溶液导电性差,但其属于强电解质。
4.电离方程式的书写原则
(1)原子守恒:电解质电离前后,原子种类和个数不变。
(2)电离方程式要遵循电荷守恒规律,即在电解质溶液中,阳离子所带的正电荷总数等于阴离子所带的负电
荷总数,电解质溶液呈电中性。
(3)连接符号:强电解质用“===”,弱电解质用“ ”。
(4)多元弱酸分步书写,多元弱碱一步完成。
5.电解质溶液的导电性
(1)导电原理
电解质――→产生自由移动的离子―→导电
(2)影响因素
自由移动离子浓度 ,离子所带电荷 ,导电能力 。
(3)两个注意点
①溶液的导电性与电解质的强弱无关,强电解质的导电能力不一定强(如BaSO) ,弱电解质溶液的导电能
4
力不一定弱,如氨水、醋酸溶液。
②对于弱电解质溶液,温度升高时,弱电解质电离程度增大,离子浓度增大,导电性会增强。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)Cu、NaCl溶液均能导电,故二者都属于电解质。( )
(2)CO 、SO 、NH 的水溶液都能导电,故它们属于电解质。( )
2 2 3
(3)NaCl溶液在电流的作用下电离成钠离子和氯离子。( )
(4)强电解质溶液的导电性比弱电解质溶液的导电性强。( )
(5)强电解质都是离子化合物,弱电解质都是共价化合物。( )
(6)BaSO 、CaCO 水溶液的导电性很弱,故都是弱电解质。( )
4 3考向01 电解质相关概念与溶液导电性的判断
【例1】(2024·辽宁抚顺·一模)下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是(
)
选项 A B C D
强电解质 Fe NaCl CaCO HNO
3 3
弱电解质 CHCOOH NH HPO Fe(OH)
3 3 3 4 3
非电解质 蔗糖 BaSO 酒精 HO
4 2
【思维建模】
(1)判断电解质和非电解质的两个要点
①必须是化合物;
②看溶于水或受热熔化时能否自身电离出自由移动的离子而导电。
(2)判断强电解质和弱电解质的两个要点
①必须是电解质;
②看溶于水是否完全电离。
考向02 电离方程式的书写与判断正误判断
【例2】(2024·黑龙江哈尔滨·二模)下列物质在指定条件下电离方程式正确的是( )
A.Na CO 溶于水:NaCO===Na+CO
2 3 2 3
B.H SO 电离:HSO 2H++SO
2 3 2 3
C.NaHS溶于水HS-的电离:HS-+HO===H S+OH-
2 2
D.NaHSO 加热熔化:NaHSO===Na++HSO
4 4
【思维建模】
电离方程式书写的思维模型
【对点1】(2024·浙江宁波·模拟)下列物质属于非电解质但水溶液能导电的是
A. B. C. D.HF
【对点2】(2024·河北衡水·模拟)下列电离方程式正确的是( )
A.BaCl 溶于水:BaCl ===Ba2++Cl
2 2
B.Ba(OH) 溶于水:Ba(OH) ===Ba2++2OH-
2 2C.Al (SO ) 的电离:Al (SO )===Al3++SO
2 4 3 2 4 3
D.NaHCO 溶于水:NaHCO ===Na++H++CO
3 3
考法02 离子反应与离子方程式的书写
1.离子反应
(1)概念:电解质在溶液中的反应实质上是 的反应。
(2)本质:溶液中某些离子的浓度 。
2.离子反应类型
(1)复分解反应型
①生成 的物质,如Al(OH) 、BaSO 等;
3 4
②生成 的物质,如弱酸、弱碱、水等;
③生成 的物质,如CO、SO 、NH 等。
2 2 3
(2)氧化还原反应型
如FeCl 溶液与Cu反应的离子方程式为 。
3
(3)络合反应型
生成稳定的配合物或配离子。如向FeCl 溶液中滴入KSCN溶液,反应的离子方程式为 。
3
3.离子方程式
(1)概念:用实际参加反应的离子符号来表示反应的式子。
(2)意义:离子方程式不仅可以表示某一个具体的化学反应,还可以表示 的离子反应。
4.离子方程式书写的基本方法(以CaCO 溶于盐酸为例)
3
5.离子方程式意义:
不仅可以表示某一个具体的化学反应,还可以表示同一类型的离子反应。如氢氧化钠溶液和盐酸反应、氢
氧化钙溶液和硝酸反应的离子方程式,都可用 来表示。
6.离子方程式中物质的“拆分”
(1)一般规律
①能拆分写成离子形式的物质是易溶的 ,包括强酸、强碱、大多数可溶性盐。
②不能拆分的物质包括 、弱电解质、气体、单质、氧化物,写成化学式。
(2)微溶物的处理
①微溶物作为产物视为沉淀,不拆分。
②作反应物时,澄清溶液拆分为离子,浑浊液不拆分。
(3)产物NH ·H O的处理
3 2(4)酸式酸根离子的处理
强酸的酸式酸根离子如硫酸氢根离子在水溶液中完全电离能拆分,如HSO===H++SO;多元弱酸的酸式酸
根离子不完全电离不能拆分,如HCO、HSO等。
【方法技巧】溶液中离子共存的判断技巧
(1)审清题干要求的关键词语,如“一定大量共存”“可能大量共存”或“不能大量共存”等。
(2)规避颜色陷阱,如“无色溶液”“透明溶液”等。
(3)注意离子共存的条件,如酸性、碱性及特殊离子存在。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)向CuSO 溶液中通入HS气体:Cu2++S2-===CuS↓( )
4 2
(2)氯气溶于水:Cl+HO 2H++Cl-+ClO-( )
2 2
(3)向NaHCO 溶液中加入稀盐酸:CO+2H+===CO ↑+HO( )
3 2 2
(4)向硫酸铝溶液中加入过量氨水:Al3++3OH-===Al(OH) ↓( )
3
(5)MnO 和浓盐酸混合加热:MnO +4H++2Cl- Mn2++2HO+Cl↑( )
2 2 ===== 2 2
(6)酸性溶液中KIO 与KI反应生成I:IO+I-+6H+===I +3HO( )
3 2 2 2
(7)用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+HO+2H+===I +2HO( )
2 2 2 2
(8)FeO和稀HNO 的反应:FeO+2H+===Fe2++HO( )
3 2
(9)NaHCO 的水解:HCO+HO===H CO+OH-( )
3 2 2 3
(10)向NaClO溶液中通入少量SO :2ClO-+SO +HO===2HClO+SO( )
2 2 2
考向01 离子方程式正误判断
【例1】(2024·江苏扬州·一模)下列离子方程式错误的是( )
A.向NaHCO 溶液中滴加NaOH溶液:HCO+OH-===CO+HO
3 2
B.用FeCl 溶液制作印刷电路板:Fe3++Cu===Fe2++Cu2+
3
C.等物质的量的Cl 和SO 同时通入水中:Cl+SO +2HO===4H++SO+2Cl-
2 2 2 2 2
D.Ba(OH) 溶液与等体积、等物质的量浓度的NaHSO 溶液反应:Ba2++OH-+H++SO===BaSO ↓+HO
2 4 4 2
【易错警示】
离子反应应符合客观事实,而命题者往往设置不符合“反应原理”的陷阱,如Fe和非氧化性酸反应应生成
Fe2+,金属和氧化性酸反应不生成H,应注意隐含反应,“===”“ ”使用是否正确以及反应条件等。
2
【思维建模】
“五看”突破离子方程式正误判断
(1)看是否符合客观事实如Fe和非氧化性酸反应应生成Fe2+,金属和氧化性酸反应不生成H,忽略隐含反应,不符合配比关系,
2
“===”“ ”使用是否正确以及反应条件等。
(2)看拆分是否正确
氧化物、弱电解质、沉淀、多元弱酸的酸式酸根离子在离子方程式中均不能拆分。在复习时,应熟记常见
的弱电解质、溶解性表及常见多元弱酸的酸式酸根离子。
(3)看是否符合原子守恒和电荷守恒
如Cu与AgNO 溶液反应的离子方程式不能写成Cu+Ag+===Cu2++Ag,而应写成Cu+2Ag+===Cu2++
3
2Ag。
(4)看是否漏写参加反应的离子
如硫酸铜溶液和氢氧化钡溶液的反应,离子方程式不能写成SO+Ba2+===BaSO ↓,应写成Cu2++SO+Ba2
4
++2OH-===Cu(OH) ↓+BaSO↓。
2 4
(5)看是否符合题设条件
考向02 离子方程式书写及评价
【例2】(2024·安徽芜湖·二模)下列离子方程式书写及评价合理的是( )
选项 离子方程式 评价
NaHCO 中加入足量的澄清石灰水:Ca2++ 正确,Ca(OH) 过量,酸式盐与碱完全反应生
3 2
A
2HCO+2OH-===CaCO ↓+CO+2HO 成正盐和水
3 2
1 mol/L的AlCl 溶液与3.5 mol/L的NaOH溶液 正确,Al3+和OH-按物质的量1∶3反应转化为
3
B 等体积混合:2Al3++7OH-===Al(OH) ↓+ Al(OH) ,过量的OH-再将部分Al(OH) 的转
3 3 3
[Al(OH) ]- 化为[Al(OH) ]-
4 4
将Fe O 溶解在过量的稀HNO 中:Fe O+8H+
3 4 3 3 4
C 正确,Fe O 中Fe2+与Fe3+物质的量之比为1∶2
3 4
===Fe2++2Fe3++4HO
2
将少量FeCl 溶液加入到NaClO溶液中:2Fe2+
2
D 正确,Fe2+与ClO-发生氧化还原反应
+ClO-+5HO===2Fe(OH) ↓+Cl-+4H+
2 3
【易错警示】
在离子方程式正误判断中,做题时往往忽略相对量的影响,命题者往往设置“离子方程式正确,但不符合
相对量”的陷阱。突破“陷阱”的方法一是审准“相对量”的多少,二是看离子反应是否符合该量。
【思维建模】【对点1】(2024·广东·三模)下列物质性质实验对应的离子方程式书写正确的是
A.漂白粉溶液吸收 后产生白色沉淀:
B. 溶于氢碘酸:
C. 溶液与稀硫酸反应:
D.用 溶液处理锅炉水垢:
【对点2】(2024·湖南长沙·三模)下列有关离子方程式正确的是
A.工人用白醋除铁锈:
B.海水提溴时用 水溶液吸收溴蒸气:
C.向硫氰化铁溶液中加入铁粉使其颜色变浅:
D.向 中投入 固体:
考法03 “与量有关型”离子方程式的书写
一、少量与过量型
1.主要是指生成物与过量的反应物继续反应而导致其离子方程式与反应物的“用量”有关,书写时首先判
断出某种反应物过量,再依据反应原理确定生成物,如 CO 通入NaOH溶液时,CO 少量则得正盐:
2 2
CO(少)+2OH-===CO+HO,CO 过量则得酸式盐(即CO 与溶液中的CO进一步反应得HCO):CO +OH
2 2 2 2 2
-===HCO。
常见的此类反应主要有:
(1)可溶性多元弱酸(或其酸酐)与强碱溶液反应:
如少量SO 通入NaOH溶液:
2
足量SO 通入NaOH溶液:
2
(2)多元弱酸的正盐与强酸的反应:
如NaCO 溶液中滴加少量盐酸:
2 3NaCO 溶液中滴加足量盐酸:
2 3
(3)多元弱酸(或其对应的酸性氧化物)与更弱酸的盐溶液反应:
如少量CO 通入Na[Al(OH)]溶液:
2 4
足量CO 通入Na[Al(OH)]溶液:
2 4
(4)可溶性铝盐与强碱反应:
铝盐过量得Al(OH) :
3
强碱过量得[Al(OH) ]-:
4
(5)可溶性偏铝酸盐与强酸反应:
偏铝酸盐过量得Al(OH) :
3
强酸过量得Al3+:
2.酸式盐与碱反应依据先中和后沉淀的思路书写
如向Ca(HCO ) 溶液中加入过量NaOH溶液的离子方程式的书写方法为:
3 2
二、反应先后型
一种反应物的两种或两种以上的组成离子,都能跟另一种反应物的组成离子反应,但因反应次序不同而跟
用量有关。又可称为竞争型离子反应。
主要类型有:
(1)向含有OH-、CO、[Al(OH) ]-的溶液中,逐滴加入稀盐酸至过量,反应的离子方程式依次为
4
OH-+H+===H O,
2
[Al(OH) ]-+H+===Al(OH) ↓+HO,
4 3 2
CO+H+===HCO、HCO+H+===H O+CO↑,
2 2
Al(OH) +3H+===Al3++3HO。
3 2
(2)向含H+、Al3+、NH的溶液中逐滴加入NaOH溶液至过量,反应的离子方程式依次为:
H++OH-===H O,
2
Al3++3OH-===Al(OH) ↓,
3
NH+OH-===NH·H O,
3 2
Al(OH) +OH-===[Al(OH) ]-。
3 4
【易错提醒】
(1)多元弱酸盐与强酸反应时,应注意反应物的用量。如在 NaCO 溶液中滴加少量盐酸,离子方程式为
2 3
CO+H+===HCO;若盐酸过量,离子方程式为CO+2H+===CO ↑+HO。
2 2
(2)CO(或SO )与强碱溶液反应时,应注意CO(或SO )是否过量。一般地,若CO(或SO )少量,产物为
2 2 2 2 2 2碳酸盐(或亚硫酸盐),若CO(或SO )过量,产物为碳酸氢盐(或亚硫酸氢盐)。如将少量CO 气体通入澄
2 2 2
清石灰水中,离子方程式为CO +Ca2++2OH-===CaCO ↓+HO;若通入过量的CO ,离子方程式为CO
2 3 2 2 2
+OH-===HCO。
(3)酸式盐与碱反应时,应注意物质之间“量”的关系。如 NaHSO 溶液与Ba(OH) 溶液的反应,NaHCO
4 2 3
溶液与Ca(OH) 溶液的反应,Ca(HCO ) 溶液与NaOH溶液的反应等。
2 3 2
(4)同一氧化剂(或还原剂)可能与多种还原剂(或氧化剂)反应,应注意离子反应顺序。如将少量的Cl 通入
2
到FeBr 溶液中,离子方程式为2Fe2++Cl===2Fe3++2Cl-;若Cl 过量,则离子方程式为2Fe2++4Br-+
2 2 2
3Cl===2Fe3++2Br +6Cl-。解此类题应抓住三点:①确定氧化剂或还原剂强弱顺序。如还原性 I->Fe2+
2 2
>Br->Cl-,氧化性Ag+>Fe3+>Cu2+>H+>Fe2+>Zn2+等。②根据强弱规律,判断反应顺序。同一氧化
剂与多种还原剂反应,还原性强的还原剂优先发生反应;同一还原剂与多种氧化剂反应,氧化性强的氧化
剂优先发生反应
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)向FeBr 溶液中通入等量Cl:2Fe2++4Br-+3Cl===2Fe3++2Br +6Cl-( )
2 2 2 2
(2)向NaAlO 溶液中通入少量CO:2AlO+CO+3HO===2Al(OH) ↓+CO( )
2 2 2 2 3
(3)少量SO 和NaOH溶液反应:SO +OH-===HSO( )
2 2
(4)向NaCO 溶液中滴入少量盐酸:CO+2H+===H O+CO↑( )
2 3 2 2
(5)少量Ca(OH) 和NaHCO 溶液反应:Ca2++OH-+HCO===CaCO ↓+HO( )
2 3 3 2
考向01 与量有关的离子方程式
【例1】(2024·福建三明·一模)下列离子方程式书写正确的是( )
A.饱和NaCO 溶液中通入过量CO:CO+CO+HO===2HCO
2 3 2 2 2
B.NaClO溶液中通入少量SO :SO +HO+ClO-===SO+Cl-+2H+
2 2 2
C.FeI 溶液中通入少量Cl:Cl+2Fe2+===2Fe3++2Cl-
2 2 2
D.Ca(HCO ) 溶液中滴入少量Ca(OH) 溶液:
3 2 2
Ca2++OH-+HCO===CaCO ↓+HO
3 2
【易错提醒】
在离子方程式正误判断中,做题时往往忽略相对量的影响,命题者往往设置“离子方程式正确,但不符合
相对量”的陷阱。突破“陷阱”的方法,一是审准“相对量”的多少,二是看离子反应是否符合该量。
【思维建模】
与“量”有关的离子方程式的书写技巧
多组离子反应,且反应比例不协调的离子方程式的书写——“少定多变”法
(1)“少定”就是把相对量较少的物质定为“1 mol”,若少量物质有两种或两种以上离子参加反应,则参加反
应的离子的物质的量之比与组成比相符。
(2)“多变”是把过量反应物离子的化学计量数根据反应实际需求量来确定,不受化学式中的比例制约,是可变的。
考向02 考查反应先后型离子方程式
【例2】(2024·山东烟台·二模)下列化学反应,相应的离子方程式一定正确的是( )
A.向NH Fe(SO ) 溶液中加入少量NaOH溶液:NH ++OH-=NH ·H O
4 4 2 4 3 2
B.1L1mol·L-1FeBr 溶液与一定量氯气反应,转移电子数为6.02×1023时:2Fe2++2Br-+2Cl=2Fe3++Br +4Cl-
2 2 2
C.将2.24L(标准状况)CO 通入500mL 0.3 mol·L-1NaOH溶液中:2CO+3OH-=CO 2-+HCO-+H O
2 2 3 3 2
D.向Ca(ClO) 溶液通入少量SO :Ca2++2ClO-+SO +H O=CaSO↓+2HClO
2 2 2 2 3
【思维建模】判断离子反应顺序的方法
(1)氧化还原型离子反应——强者优先
同一氧化剂(或还原剂)可能与多种还原剂(或氧化剂)反应,其中还原性(或氧化性)最强的还原剂(或氧化
剂)最先反应,反应完全后由强到弱依次进行。
(2)复分解型离子反应——最稳定生成物优先
采用“假设验证法”:假设某种离子先反应,若生成产物与其他成分能共存,则该离子优先反应,否则该
离子不能优先反应。如向含有Al3+、NH+ 、H+溶液中逐滴加入NaOH溶液,OH-按H+→Al3+→NH+
4 4
→Al(OH) 顺序依次反应。
3
【对点1】(2024·河北·模拟)下列实验对应的离子方程式不正确的是( )
A.将碳酸氢钙溶液与过量的澄清石灰水混合:HCO+Ca2++OH-===CaCO ↓+HO
3 2
B.将少量NO 通入NaOH溶液:2NO +2OH-===NO+NO+HO
2 2 2
C.硅酸钠溶液中通入过量二氧化碳:SiO+CO+HO===H SiO↓+CO
2 2 2 3
D.向氨水中滴入少量硝酸银溶液:Ag++2NH ·H O===[Ag(NH )]++2HO
3 2 3 2 2
【对点2】(2024·江苏宿迁·三模)下列离子方程式的书写及评价均合理的是( )
选项 离子方程式 评价
将1 mol Cl 通入含1 mol FeI 溶液中:
2 2
A 正确;Cl 过量,可将Fe2+、I-均氧化
2
2Fe2++2I-+2Cl===2Fe3++4Cl-+I
2 2
1 mol·L-1的NaAlO 溶液和2.5 mol·L-1的HCl溶液等体 正确;AlO与Al(OH) 消耗的H+的物
2 3
B
积均匀混合:2AlO+5H+===Al3++Al(OH) ↓+HO 质的量之比为2∶3
3 2
过量SO 通入NaClO溶液中:
2
C 正确;说明酸性:HSO 强于HClO
2 3
SO +HO+ClO-===HClO+HSO
2 2
Mg(HCO ) 溶液与足量的NaOH溶液反应:
3 2
D 正确;酸式盐与碱反应生成正盐和水
Mg2++HCO+OH-===MgCO↓+HO
3 2
题型一 电解质的判断与电离方程式1.(2024·浙江·模拟)下列物质不属于电解质的是
A.HNO B.ClO C.NaI D.冰水混合物
2 2 3
2.(2024·广东惠州·三模)下列物质溶于水能导电但属于非电解质的是
A.HCl B.Cl C.CaCO D.NH
2 3 3
3.(2024·辽宁大连·一模)下列物质属于非电解质的是
A.氯化铝 B.重晶石 C.氯仿 D.福尔马林
4.(2024·江苏盐城·三模)下列电离方程式书写正确的是
A. B.
C. D.
题型二 离子方程式的正误判断
5.(2024·河北唐山·模拟)下列相关离子方程式表示错误的是
A.向稀硫酸溶液中加入 固体出现黄色沉淀:
B.向氢氧化铁胶体中加入HI溶液,首先出现红褐色沉淀,后沉淀消失,溶液变为黄色:
C.向酸性 溶液中通入 后溶液由紫色变为无色:
D.向HI溶液中加入 后溶液变为棕黄色:
6.(2024·天津河西·模拟)下列方程式与所给事实不相符的是
A.氢化钠(NaH)可在野外用作生氢剂:
B.工业上制备高铁酸钠:
C.工业上用绿矾( )除去业废水中含有的重铬酸根离子( ):
D.用石灰除去盐碱地中 以降低土壤碱性:
7.(2024·湖北·三模)下列有关反应的离子方程式书写正确的是
A.新制氯水置于阳光下:2H++ClO-=2HCl+O ↑
2
B.泡沫灭火器反应原理:3HO+2Al3++3 =2Al(OH) ↓+3CO ↑
2 3 2
C.向NaAlF 溶液中滴加氨水:Al3++3NH•H O=Al(OH) ↓+3
3 6 3 2 3
D.向KCrO 溶液中滴加稀硫酸:2 +2H+ +H O
2 4 2
8.(2024·山东淄博·三模)下列离子方程式与所给事实不相符的是
A. 通入石灰乳中:
B.FeS去除废水中的 :C. 溶液滴入 溶液中:
D.铅酸蓄电池充电时的阳极反应:
题型三 过量的离子反应
9.(2024·重庆荣昌·模拟)下列过程中的化学反应,相应的离子方程式正确的是
A.用淀粉 溶液和醋酸检验加碘盐中的 :
B. 溶液中通入少量 :
C.氯化亚铁溶液中加入酸性的 溶液:
D. 固体与氢碘酸反应:
10.(2024·湖南长沙·三模)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反
应方程式书写错误的是
A.用过量饱和 溶液吸收废气中的
B.用惰性电极电解氯化镁溶液:
C.将少量溴水滴入过量 溶液中:
D.将 溶液滴入稀硫酸酸化的 溶液中:
11.(2024·黑龙江哈尔滨·模拟)下列离子方程式书写正确的是
A.少量二氧化硫气体通入次氯酸钠溶液:
B.少量氯气通入碳酸钠溶液:
C.少量氨气通入硫酸铝钾溶液:
D.少量二氧化碳气体通入次氯酸钙溶液:
12.(2024·河北沧州·三模)下列离子方程式书写正确的是
A.过量的 溶液吸收尾气 :
B.向Mg(HCO ) 溶液中滴加少量NaOH溶液:
3 2
C.用石灰乳吸收尾气 :
D.向硫酸铝铵溶液中滴加氢氧化钡至沉淀的物质的量最大:
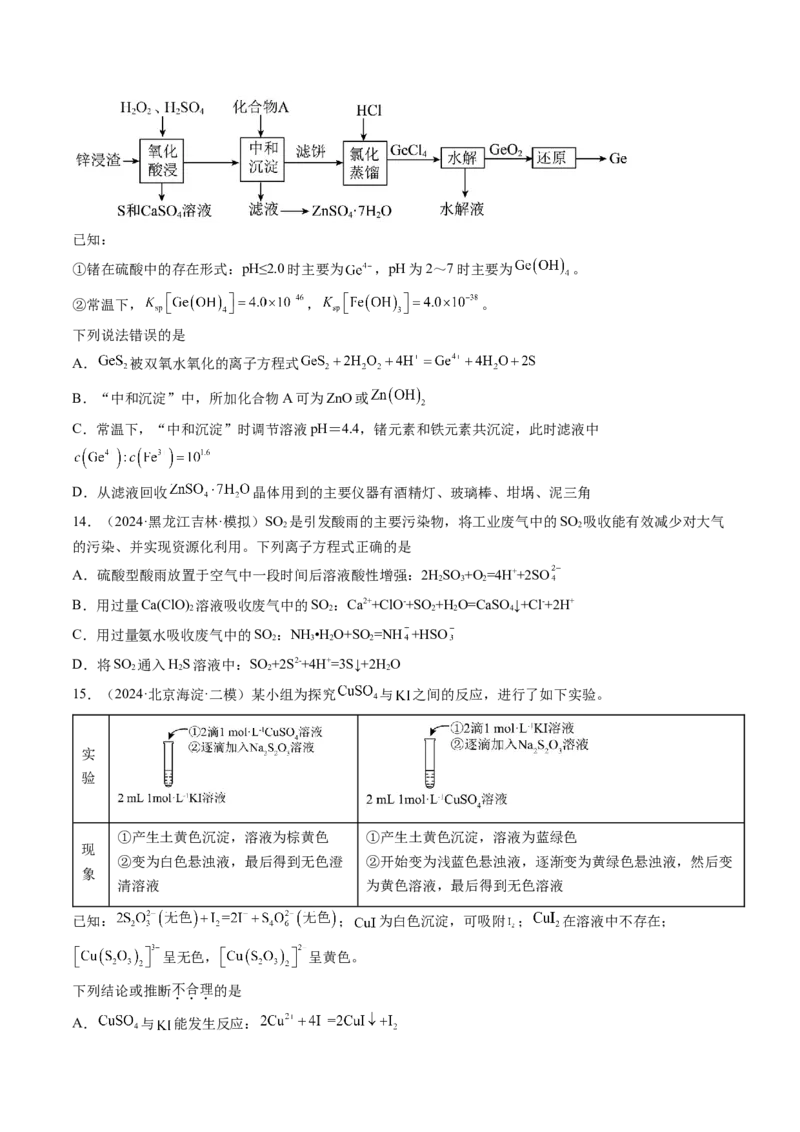
13.(2024·山东日照·三模)从锌浸渣(主要含 、 ,少量ZnS和 )中提取Ge的流程如
下:已知:
①锗在硫酸中的存在形式:pH≤2.0时主要为 ,pH为2~7时主要为 。
②常温下, , 。
下列说法错误的是
A. 被双氧水氧化的离子方程式
B.“中和沉淀”中,所加化合物A可为ZnO或
C.常温下,“中和沉淀”时调节溶液pH=4.4,锗元素和铁元素共沉淀,此时滤液中
D.从滤液回收 晶体用到的主要仪器有酒精灯、玻璃棒、坩埚、泥三角
14.(2024·黑龙江吉林·模拟)SO 是引发酸雨的主要污染物,将工业废气中的SO 吸收能有效减少对大气
2 2
的污染、并实现资源化利用。下列离子方程式正确的是
A.硫酸型酸雨放置于空气中一段时间后溶液酸性增强:2HSO +O =4H++2SO
2 3 2
B.用过量Ca(ClO) 溶液吸收废气中的SO :Ca2++ClO-+SO+H O=CaSO↓+Cl-+2H+
2 2 2 2 4
C.用过量氨水吸收废气中的SO :NH •H O+SO =NH +HSO
2 3 2 2
D.将SO 通入HS溶液中:SO +2S2-+4H+=3S↓+2H O
2 2 2 2
15.(2024·北京海淀·二模)某小组为探究 与 之间的反应,进行了如下实验。
实
验
①产生土黄色沉淀,溶液为棕黄色 ①产生土黄色沉淀,溶液为蓝绿色
现
②变为白色悬浊液,最后得到无色澄 ②开始变为浅蓝色悬浊液,逐渐变为黄绿色悬浊液,然后变
象
清溶液 为黄色溶液,最后得到无色溶液
已知: ; 为白色沉淀,可吸附 ; 在溶液中不存在;
呈无色, 呈黄色。
下列结论或推断不合理的是
A. 与 能发生反应:B. 与 反应的速率快于 与 反应的速率
C.黄绿色悬浊液变为黄色溶液时,有 、 生成
D. 与 生成配合物反应的限度小于二者发生氧化还原反应的限度
16.在化学研究中,往往可以通过观察现象认识物质变化的情况。请分析以下一组有现象变化的化学反应。
实验 实验及操作
现象
试管 滴管
饱和NaSiO 溶液(含酚酞) 先滴加1.0 mL Ⅰ.红色溶液中出现胶状沉淀。
2 3
0.5 mol·L-1 Ⅱ.加碱时________;加酸时产生白色沉淀,又
0.1 mol·L-1AlCl 溶液
3
NaOH溶液;再 逐渐溶解至消失。
0.1 mol·L-1Fe(NO ) 溶液 滴加1.0 mol·L-1 Ⅲ.加碱时________;加酸后得黄色溶液
3 2
新制饱和氯水 HSO 溶液 Ⅳ.加碱时溶液变为无色;加酸后_______。
2 4
(1)用离子方程式解释现象Ⅰ中出现胶状沉淀的原因:__________________________________。
(2)Ⅱ中加碱时出现的现象是_________________________________________________,
现象说明溶液中发生反应的离子方程式是___________________________________。
(3)Ⅲ中加碱时出现的现象是_________________________________________________。
(4)Ⅳ中加酸时出现的现象是________________________________________________,
用离子方程式解释产生此现象的原因________________________________________。
(5)滴加试剂顺序的变化会影响溶液中的现象和发生的反应。请继续分析以下实验。
实验 实验及操作
现象
试管 滴管
0.1 mol·L-1 先滴加1.0 mol·L-1 HSO 溶液; Ⅴ.加酸时溶液无明显现象;加碱后
2 4
Fe(NO ) 溶 再滴加1.0 mL 0.5 mol·L-1 溶液依然没有明显变化
3 2
液 NaOH溶液
①探究加酸时Fe(NO ) 溶液中是否发生了反应:
3 2
向1.0 mL 0.1 mol·L-1 Fe(NO ) 溶液中____________________,如果溶液变红色,说明溶液中含Fe3+,证明
3 2
加酸时溶液中发生了反应。(请将上述操作补充完整)
②推测溶液中产生Fe3+的可能原因有两种:
a._________________________________________________________________;
b._________________________________________________________________。
1.(2024·浙江选考1月第1题)下列物质不属于电解质的是
A. B. C. D.2.(2023·湖南卷第5题)下列有关电极方程式或离子方程式错误的是
A. 碱性锌锰电池的正极反应:MnO +H O+e-=MnO(OH)+OH-
2 2
B. 铅酸蓄电池充电时的阳极反应:Pb2++2H O-2e-=PbO+4H+
2 2
C. K[Fe(CN) ]溶液滴入FeCl 溶液中:K++Fe2++[Fe(CN)]3-=KFe[Fe(CN) ]↓
3 6 2 6 6
D. TiCl 加入水中:TiCl +(x+2)H O=TiO·xHO↓+4H++4Cl-
4 4 2 2 2
3.(2023·浙江卷6月第9题)下列反应的离子方程式正确的是
A. 碘化亚铁溶液与等物质的量的氯气:
B. 向次氯酸钙溶液通入足量二氧化碳:
C. 铜与稀硝酸:
D. 向硫化钠溶液通入足量二氧化硫:
4.(2023·北京卷第6题)下列离子方程式与所给事实不相符的是
A. Cl 制备84消毒液(主要成分是 ):
2
B. 食醋去除水垢中的 :
C. 利用覆铜板制作印刷电路板:
D. Na S去除废水中的 :
2
5. (2023·重庆卷第2题)下列离子方程式中,错误的是
A. 通入水中:
B. 通入石灰乳中:
C. 放入 溶液中:
D. 放入 溶液中:
6.(2023·浙江选考1月第7题)下列反应的离子方程式不正确的是( )
A. Cl 通入氢氧化钠溶液:
2
B. 氧化铝溶于氢氧化钠溶液:
C. 过量CO 通入饱和碳酸钠溶液:
2
D. HSO 溶液中滴入氯化钙溶液:
2 3
7.(2022·浙江卷)下列物质属于非电解质的是
A.CH B.KI C.NaOH D.CHCOOH
4 3
8.(2022·广东卷)下列关于Na的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:B.碱转化为两种盐:
C.过氧化物转化为碱:
D.盐转化为另一种盐:
9.(2022·湖南卷)下列离子方程式正确的是
A. 通入冷的 溶液:
B.用醋酸和淀粉 溶液检验加碘盐中的 :
C. 溶液中加入 产生沉淀:
D. 溶液与少量的 溶液混合:
10.(2022·全国甲卷)能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水湿合:Al3++4NH+2H O=AlO-+4NH+
3 2 2 4
C.硅酸钠溶液中通入二氧化碳:SiO2-+CO +H O=HSiO -+HCO-
3 2 2 3 3
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO2-=BaSO ↓+2H O
2 4 4 4 4 2
11.(2022·浙江卷)下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2
B.将少量NO 通入NaOH溶液:2NO +2OH-= + +H O
2 2 2
C.将少量SO 通入NaClO溶液:SO +H O+2ClO-= +2HClO
2 2 2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH·H O= +2H O
3 2 2