文档内容
考点 28 盐类的水解
(核心考点精讲精练)
一、3年真题考点分布
考点内容 考题统计
2022浙江1月选考1题,2分;2022浙江6月选考23题,2分;
盐类水解的概念
2021广东卷8题,2分;2021北京卷12题,3分;
盐类水解的应用 2022海南卷13题,4分;
离子浓度大小比较 2022重庆卷11题,3分;202天津卷10题,3分;
2022福建卷10题,4分;2022浙江1月选考23题,2分;2021
离子曲线 浙江1月选考23题,2分;2021浙江6月选考23题,2分;2021
湖南卷9题,3分;
二、命题规律及备考策略
【命题规律】
从近三年高考试题来看,高考中主要以盐类水解为载体考查溶液的酸碱性、溶液的pH计算及粒子浓
度的大小比较等,通过图像分析、反应条件控制等考查难溶电解质的溶解平衡,题型为选择题和非选择题。
试题以日常生活情境、生产环保情境和实验探究情景为主,集中在图象和图示的分析。
【备考策略】
(1)通过实验归纳盐溶液的酸碱性与其类型之间的关系,进一步探究盐溶液呈现不同酸碱性的原因,总
结盐类水解的规律、盐类水解的影响因素、盐溶液酸碱性的判断、溶液中离子浓度的比较等;
(2)熟练掌握盐类水解离子方程式的书写,运用平衡模型解释化学现象,揭示现象本质和规律。
(3)熟练掌握各种图象以及图象的分析方法,注意图象纵、横坐标的含义;学会特别复杂图象、一个图
象含有多条曲线情况的分析。
【命题预测】
预测2024年应重点关注水解平衡常数的计算、影响水解平衡的因素、电解质溶液中电荷守恒关系的应
用;侧重于理解与辨析能力、分析与推测能力,从题干及图象中提取有效信息,结合平衡移动原理和各种
守恒思想,具体问题具体分析,提高试题的灵活性与创新性。
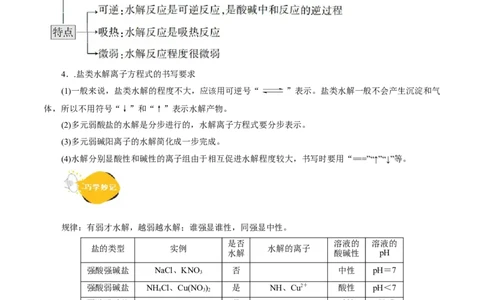
考法 1 盐类水解及规律4..盐类水解离子方程式的书写要求
(1)一般来说,盐类水解的程度不大,应该用可逆号“ ”表示。盐类水解一般不会产生沉淀和气
体,所以不用符号“↓”和“↑”表示水解产物。
(2)多元弱酸盐的水解是分步进行的,水解离子方程式要分步表示。
(3)多元弱碱阳离子的水解简化成一步完成。
(4)水解分别显酸性和碱性的离子组由于相互促进水解程度较大,书写时要用“===”“↑”“↓”等。
规律:有弱才水解,越弱越水解;谁强显谁性,同强显中性。
是否 溶液的 溶液的
盐的类型 实例 水解的离子
水解 酸碱性 pH
强酸强碱盐 NaCl、KNO 否 中性 pH=7
3
强酸弱碱盐 NH Cl、Cu(NO ) 是 NH、Cu2+ 酸性 pH<7
4 3 2
弱酸强碱盐 CHCOONa、NaCO 是 CHCOO-、CO 碱性 pH>7
3 2 3 3
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)盐类水解的实质是促进水电离,水电离平衡右移( )
(2)酸式盐溶液可能呈酸性,也可能呈碱性( )
(3)某盐溶液呈酸性,该盐一定发生了水解反应( )
(4)离子能够发生水解的盐溶液一定呈酸性或碱性( )(5)溶液呈中性的盐一定是强酸、强碱生成的盐( )
(6)常温下,pH=10的CHCOONa溶液与pH=4的NH Cl溶液,水的电离程度相同( )
3 4
(7)常温下,pH=11的CHCOONa溶液与pH=3的CHCOOH溶液,水的电离程度相同( )
3 3
(8)NaHCO 、NaHSO 都能促进水的电离( )
3 4
(9)向NaAlO 溶液中滴加NaHCO 溶液,有沉淀和气体生成( )
2 3
(10)Na CO 的水解:CO+2HO===H CO+2OH-( )
2 3 2 2 3
(11)FeCl 溶液与NaHCO 溶液混合:Fe3++3HCO===Fe(OH) ↓+3CO↑( )
3 3 3 2
(12)同浓度的NaCO 溶液和CHCOONa溶液相比前者pH大;同浓度的NaCO 和NaHCO 溶液相比后
2 3 3 2 3 3
者pH小( )
答案:(1)√ (2)√ (3)× (4)× (5)× (6)√ (7)× (8)× (9)× (10)× (11)√ (12)√
例1 下列物质的水溶液因水解而呈碱性的是( )
A.NaCO B.AlCl C.Ca(OH) D.NaNO
2 3 3 2 3
【答案】A
【解析】A项,碳酸钠溶液中存在碳酸根的水解CO2-+H O HCO -+OH-,溶液显碱性,A符合题
3 2 3
意;B项,AlCl 溶液中存在Al3+的水解而显酸性,B不符合题意;C项,Ca(OH) 可以在水溶液中电离出
3 2
OH-而显碱性,与水解无关,C不符合题意;D项,NaNO 为强酸强碱盐,溶液显中性,D不符合题意;故
3
选A。
例2 下列方程式属于水解反应方程式的是( )
A.HCO HCO -+H+ B.HCO -+H O HO++CO 2-
2 3 3 3 2 3 3
C.HCO -+OH-=H O+CO2- D.CO2-+ H O HCO -+ OH-
3 2 3 3 2 3
【答案】D
【解析】A项,碳酸是一种二元弱酸,选项所给为碳酸的第一步电离方程式,A不符合题意;B项,
碳酸氢根水解生成碳酸和氢氧根,选项所给为碳酸氢根的电离方程式,B不符合题意;C项,碳酸氢根水
解生成碳酸和氢氧根,选项所给为碳酸氢根和氢氧根的反应,C不符合题意;D项,碳酸根水解生成碳酸
氢根和氢氧根,方程式为CO2-+ H O HCO -+ OH-,D符合题意;故选D。
3 2 3
⇌
对点1 下列物质的水溶液因水解而呈碱性的是( )
A.NH NO B.NaCO C.NaCl D.Al (SO )
4 3 2 3 2 4 3
【答案】B
【解析】A项,NH NO 溶液中铵根离子水解使溶液显酸性,故A不符合题意;B项,NaCO 溶液中
4 3 2 3
碳酸根离子水解使溶液显碱性,故B符合题意;C项,NaCl不水解,显中性,故C不符合题意;D项,Al (SO ) 溶液中铝离子水解使溶液显酸性,故D不符合题意;故选B。
2 4 3
对点2 下列操作会促进HO的电离,且使溶液pH>7的是( )
2
A.将纯水加热到90 ℃ B.向水中加少量NaOH溶液
C.向水中加少量NaCO 溶液 D.向水中加少量FeCl 溶液
2 3 3
【答案】C
【解析】将纯水加热到90 ℃,水的电离程度增大,c(H+)=c(OH-)>10-7 mol·L-1,pH<7,A错;向
水中加少量NaOH溶液,水中c(OH-)增大,pH>7,但水的电离平衡向逆方向移动,即水的电离受到抑制,
B错;向水中加少量NaCO 溶液,CO与H+结合,水中c(H+)减小,水的电离平衡向正方向移动,c(OH-)
2 3
增大,c(OH-)>c(H+),pH>7,C对;向水中加少量FeCl 溶液,Fe3+与OH-结合为弱电解质Fe(OH) ,水
3 3
中c(OH-)减小,水的电离平衡向正方向移动,c(H+)增大,c(H+)>c(OH-),pH<7,D错。
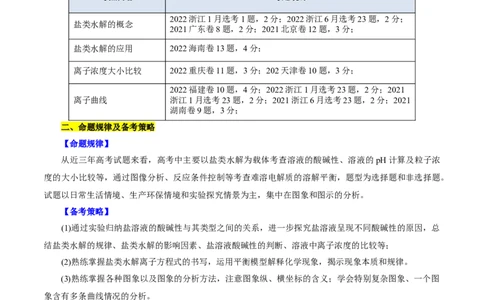
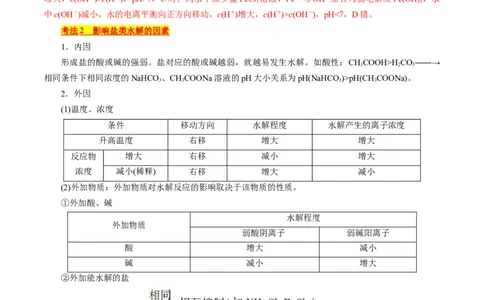
考法 2 影响盐类水解的因素
1.内因
形成盐的酸或碱的强弱。盐对应的酸或碱越弱,就越易发生水解。如酸性:CHCOOH>H CO――→
3 2 3
相同条件下相同浓度的NaHCO 、CHCOONa溶液的pH大小关系为pH(NaHCO)>pH(CHCOONa)。
3 3 3 3
2.外因
(1)温度、浓度
条件 移动方向 水解程度 水解产生的离子浓度
升高温度 右移 增大 增大
反应物 增大 右移 减小 增大
浓度 减小(稀释) 右移 增大 减小
(2)外加物质:外加物质对水解反应的影响取决于该物质的性质。
①外加酸、碱
水解程度
外加物质
弱酸阴离子 弱碱阳离子
酸 增大 减小
碱 减小 增大
②外加能水解的盐
利用平衡移动原理解释问题的思维模板
(1)解答此类题的思维过程①找出存在的平衡体系(即可逆反应或可逆过程)
②找出影响平衡的条件
③判断平衡移动的方向
④分析平衡移动的结果及移动结果与所解答问题的联系
(2)答题模板
……存在……平衡,……(条件)……(变化),使平衡向……(方向)移动,……(结论)。
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)外界条件对盐水解程度的大小起决定作用( )
(2)影响盐类水解的因素有温度、浓度、压强等( )
(3)能水解的盐的浓度越低,水解程度越大,溶液的酸碱性越强( )
(4)盐溶液显酸碱性,一定是由水解引起的( )
(5)水解平衡右移,盐的离子的水解程度一定增大( )
(6)NaHCO 和NaHSO 都能促进水的电离( )
3 4
(7)水解反应NH+HO NH ·H O+H+达到平衡后,升高温度平衡逆向移动( )
2 3 2
(8)Na CO 溶液加水稀释,促进水的电离,溶液的碱性增强( )
2 3
(9)稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强( )
(10)在滴有酚酞的NaCO 溶液中慢慢滴入BaCl 溶液,溶液的红色逐渐退去( )
2 3 2
(11)pH相等的①NaHCO 、②NaCO、③NaOH溶液的物质的量浓度大小:①>②>③( )
3 2 3
(12)在NH Cl溶液中加入稀HNO,能抑制NH水解( )
4 3
(13)在CHCOONa溶液中加入冰醋酸,能抑制CHCOO-水解( )
3 3
答案:(1)× (2)× (3)× (4)× (5)× (6)× (7)√ (8)× (9)× (10)√ (11)√ (12)√
例1 下列关于FeCl 水解的说法错误的是( )
3
A.在FeCl 稀溶液中,水解达到平衡时,无论加FeCl 饱和溶液还是加水稀释,平衡均向右移动
3 3
B.浓度为5 mol·L-1和0.5 mol·L-1的两种FeCl 溶液,其他条件相同时,前者Fe3+的水解程度小于后者
3
C.其他条件相同时,同浓度的FeCl 溶液在50 ℃和20 ℃时发生水解,50 ℃时Fe3+的水解程度比20
3
℃时的小
D.为抑制Fe3+的水解,更好地保存FeCl 溶液,应加少量盐酸
3
【答案】C
【解析】增大FeCl 的浓度,水解平衡向右移动,但Fe3+水解程度减小,加水稀释,水解平衡向右移动,
3Fe3+水解程度增大,A、B两项正确;盐类水解是吸热过程,温度升高,水解程度增大,C项错误;Fe3+水
解后溶液呈酸性,增大H+的浓度可抑制Fe3+的水解,D项正确。
例2 室温下,将0.20mol NaCO 固体溶于水配成100mL溶液,向溶液中加入下列物质,有关结论
2 3
正确的是( )
加入的物质 结论
A 100mL2mol·L-1HSO 反应结束后, (Na+)=c(SO2-),
2 4 4
B 溶液中 增大
C 200mLH O 由水电离出的c(H+)·c(OH-)不变
2
D 0.4mol NaHSO 固体 反应完全后,溶液pH减小,c(Na+)不变
4
【答案】B
【解析】n(Na CO)=0.2mol,碳酸钠是强碱弱酸盐,碳酸根离子水解导致溶液呈碱性,水解方程式为
2 3
CO2-+H O HCO -+OH- 。 A 项 , n(H SO )=2mol/L×0.1L=0.2mol , HSO 和 NaCO 反 应 方 程 式 为
3 2 3 2 4 2 4 2 3
Na
2
CO
3
+H 2⇌SO
4
=Na
2
SO
4
+CO
2
↑+H
2
O,根据方程式知,二者恰好反应生成强酸强碱溶液Na
2
SO
4
,溶液呈中性,
则 c(H+)=c(OH-) , 根 据 电 荷 守 恒 得 (Na+)=2c(SO2-) , 故 A 错 误 ; B 项 , CaO+H O=Ca(OH) 、
4 2 2
Ca(OH) +Na CO=CaCO ↓+2NaOH,随着CO2-的消耗,CO2-+H O HCO -+OH-向左移动,c(HCO -)减小,
2 2 3 3 3 3 2 3 3
⇌
反应生成OH-,则c(OH-)增大,导致溶液中 增大,故B正确;C项,加水稀释,促进碳酸钠水解,
则由水电离出的n(H+)、n(OH-)都增大,但氢离子、氢氧根离子物质的量增大倍数小于溶液体积增大倍数,
c(H+)、c(OH-)减小,二者浓度之积减小,故 C 错误;D 项,NaHSO 和 NaCO 反应方程式为:
4 2 3
2NaHSO+Na CO=Na SO +H O+CO↑,根据方程式知,二者恰好反应生成NaSO 、HO、CO ,溶液中的
4 2 3 2 4 2 2 2 4 2 2
溶质是硫酸钠,溶液呈中性,溶液由碱性变为中性,溶液的 pH减小,因为硫酸氢钠中含有钠离子,所以
c(Na+)增大,故D错误;故选B。
对点1 NaCO 溶液中存在水解平衡:CO2-+H O HCO -+OH-。下列说法错误的是( )
2 3 3 2 3
A.加水稀释,溶液中所有离子的浓度都减小 B.通入CO,溶液pH减小
2
C.加入NaOH固体, 减小 D.升高温度,平衡常数增大
【答案】A【解析】A项,碳酸钠溶液显碱性,其中加水稀释时,溶液中OH-离子浓度减小,由于溶液中存在水
的离子积常数,所以溶液中c(H+)增大,A错误;B项,通入CO ,其与水反应生成碳酸,碳酸与碳酸根离
2
子反应产生HCO -,溶液中HCO -的水解程度小于CO2-的水解程度。向碱性的溶液中加入酸,溶液的碱性
3 3 3
一定会减弱,故溶液pH减小,B正确;C项,加入NaOH固体会抑制碳酸钠水解,所以 减小,
C正确;D项,温度升高,促进盐的水解,因此水解平衡常数增大,D正确;故选A。
对点2 用棕黄色FeCl 溶液探究影响盐类水解的因素,根据实验现象和原理,下列对水解程度判断正
3
确的是( )
选项 实验 现象 水解程度
A 加入FeCl 固体 溶液变成红褐色 变大
3
B 加热FeCl 溶液 溶液变成红褐色 不变
3
C 通入HCl气体 溶液颜色变浅 减小
D 加入NaCl溶液 溶液颜色变浅 不变
【答案】C
【解析】棕黄色FeCl 溶液中Fe3+水解,水解离子方程式Fe3++3H O Fe(OH) +3H+。A项,加
3 2 3
FeCl 固体,水解平衡向右移动,溶液变成红褐色,水解程度减小,A错误;B项,加热,水解平衡右移,
3
溶液变成红褐色,水解程度增大,B错误;C项,加HCl,c(H+)增大,水解平衡左移,溶液颜色变浅,水
解程度减小,C正确;D项,加入NaCl溶液,相当于加水稀释,水解平衡向右移动,水解程度增大,D错
误;故选C。
考法 3 盐类水解的应用
1.判断离子能否大量共存
若阴、阳离子发生相互促进的水解反应,水解程度较大而不能大量共存,有的甚至水解完全。常见的
相互促进的水解反应进行完全的有:Fe3+、Al3+与[Al(OH) ]-、CO、HCO。
4
2.判断盐溶液蒸干时所得的产物
(1)盐溶液水解生成难挥发性酸和酸根阴离子易水解的强碱盐,蒸干后一般得原物质,如 CuSO (aq)蒸
4
干得CuSO ;NaCO(aq)蒸干得NaCO(s)。
4 2 3 2 3
(2)盐溶液水解生成挥发性酸时,蒸干灼烧后一般得对应的氧化物,如 AlCl (aq)蒸干得Al(OH) ,灼烧
3 3
得Al O。
2 3
(3)考虑盐受热时是否分解,如Ca(HCO )、NaHCO 、KMnO 、NH Cl固体受热易分解,因此蒸干灼烧
3 2 3 4 4
后分别为Ca(HCO )→CaCO (CaO);NaHCO →NaCO;KMnO →
3 2 3 3 2 3 4