文档内容
重难点 03 离子反应
一、电解质溶液导电情况分析
1.电解质溶液的导电原理
电解质电离出的阴、阳离子在外加电场的作用下,发生定向移动实现导电过程,一般情况下,自由移动离
子的浓度越大,所带的电荷数越多,电解质溶液的导电能力越强。
2.同一温度下,强电解质溶液(a)、弱电解质溶液(b)、金属导体(c)的导电能力相同,若升高温度,它们的导
电能力大小顺序为b>a>c。
二、书写离子方程式时的易错点
1.两种电解质溶液混合,至少电离出两种阴离子和两种阳离子,这四种(或更多种)离子之间都能两两结合成
难电离(或难溶)的物质或后续离子之间的氧化还原反应,这样的离子反应称为多重反应。在写这类反应的
离子方程式时易丢失其中的一组反应。
如:(1)Ba(OH) 溶液与HSO 溶液混合
2 2 4
Ba 2 + + 2OH - + 2H + + SO == =BaSO ↓ + 2H O。
4 2
(2)Ba(OH) 溶液与(NH )SO 溶液混合
2 4 2 4
Ba 2 + + 2OH - + 2NH + SO == =BaSO ↓ + 2NH ·H O。
4 3 2
(3)CuSO 溶液与Ba(OH) 溶液混合
4 2
Cu 2 + + SO + Ba 2 + + 2OH - == =Cu(OH) ↓ + BaSO ↓。
2 4
2.“拆分”陷阱
离子方程式的正误判断中,常常设置物质是否能“拆分”陷阱,氧化物、弱电解质、沉淀、多元弱酸的酸
式酸根(HSO除外)在离子方程式中均不能拆分。在复习时,应熟记常见的弱电解质、溶解度表及常见多元
弱酸的酸式酸根。
3.“守恒”陷阱
离子方程式除符合质量守恒外,还应符合电荷守恒,做题时往往只注意质量守恒,而忽略电荷守恒,这也
是命题者经常设置的“陷阱”。
4.“原理”陷阱
离子反应应符合客观事实,而试题往往设置不符合“反应原理”的陷阱,如 Fe和非氧化性酸反应应生成
Fe2+,金属和氧化性酸反应不生成H,应注意隐含反应,“===”“ ”使用是否正确以及反应条件等。
2
5.“量比”陷阱
在离子方程式正误判断中,做题时往往忽略相对量的影响,试题往往设置“离子方程式正确,但不符合相
对量”的陷阱。突破“陷阱”的方法一是审准“相对量”的多少,二是看离子反应是否符合该量。
如:(1)CO 通入NaOH溶液中:
2
碱过量:CO + 2OH - == =CO + H O;
2 2
碱不足:CO + OH - == =HCO 。
2
1
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司(2)Na CO 溶液与稀盐酸反应:
2 3
稀盐酸不足: CO + H + == =HCO ;
稀盐酸过量: CO + 2H + == =CO ↑ + H O。
2 2
(3)铝盐溶液与强碱溶液反应:
铝盐过量: Al 3 + + 3OH - == =Al(OH) ↓;
3
强碱过量: Al 3 + + 4OH - == =AlO + 2H O。
2
(4)NaAlO 溶液与强酸溶液反应:
2
NaAlO 过量: AlO + H + + H O == =Al(OH) ↓;
2 2 3
强酸过量: AlO + 4H + == =Al 3 + + 2H O。
2
(5)CO 通入NaAlO 溶液中:
2 2
NaAlO 过量: 2AlO + CO + 3H O == =2Al(OH) ↓ + CO ;
2 2 2 3
NaAlO 不足: AlO + CO + 2H O == =Al(OH) ↓ + HCO 。
2 2 2 3
(6)Fe与稀HNO 溶液反应:
3
Fe过量: 3Fe + 2NO + 8H + == =3Fe 2 + + 2NO↑ + 4H O;
2
稀HNO 过量: Fe + NO + 4H + == =Fe 3 + + NO↑ + 2H O。
3 2
(7)NH HSO 溶液与NaOH溶液的反应:
4 4
NaOH不足: H + + OH - == =H O;
2
NaOH过量: NH + H + + 2OH - == =NH ·H O + H O。
3 2 2
(8)向FeBr 溶液中通Cl:
2 2
Cl 少量:Cl + 2F e 2 + == =2F e 3 + + 2C l - ;
2 2
Cl 过量: 2Fe 2 + + 4Br - + 3Cl == =2Fe 3 + + 2Br + 6C l - 。
2 2 2
(9)Ba(OH) 溶液与NaHSO 溶液反应:
2 4
①n[Ba(OH) ]∶n(NaHSO)=1∶1
2 4
Ba 2 + + OH - + H + + SO == =BaSO ↓ + H O,此时溶液呈碱性;
4 2
②n[Ba(OH) ]∶n(NaHSO)=1∶2
2 4
Ba 2 + + 2OH - + 2H + + SO == =BaSO ↓ + 2H O,此时溶液呈中性,若向该溶液中再加入Ba(OH) 溶液,反应为
4 2 2
SO + Ba 2 + == =BaSO ↓。
4
三、判断离子能否大量共存的“四个要点”
判断多种离子能否大量共存于同一溶液中,归纳起来就是:一色、二性、三特殊、四反应。
(1)一色——溶液颜色
几种常见离子的颜色:
离子 Cu2+ Fe3+ Fe2+ MnO
溶液颜色 蓝色 棕黄色 浅绿色 紫红色
(2)二性——溶液的酸碱性
①在酸性溶液中,OH-及弱酸根阴离子(如CO、SO、S2-、CHCOO-等)不能大量存在。
3
②在碱性溶液中,H+及弱碱阳离子(如NH、Al3+、Fe3+等)不能大量存在。
2
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司(3)三特殊——三种特殊情况:
①AlO与HCO不能大量共存:AlO+HCO+HO===Al(OH) ↓+CO。
2 3
②“NO+H+”组合具有强氧化性,能与S2-、Fe2+、I-、SO等还原性的离子发生氧化还原反应而不能大
量共存。
③NH与CHCOO-、CO,Mg2+与HCO等组合中,虽然两种离子都能水解且水解相互促进,但总的水解
3
程度仍很小,它们在溶液中仍能大量共存。
(4)四反应——四种反应类型
四反应是指离子间通常能发生的四种类型的反应,能相互反应的离子显然不能大量共存。
①复分解反应:如Ba2+与SO,NH与OH-,H+与CHCOO-等。
3
②氧化还原反应:如Fe3+与I-、S2-,NO(H+)与Fe2+等。
③相互促进的水解反应:如Al3+与CO、HCO或AlO等。
④络合反应:如Fe3+与SCN-等。
四、常见离子的检验和推断
1.常见阳离子的检验与推断依据
根据离子性质不同而在实验中所表现出的现象不同,可以把检验离子的方法归纳为三种类型:①生成沉淀;
②生成气体;③显现特殊颜色。
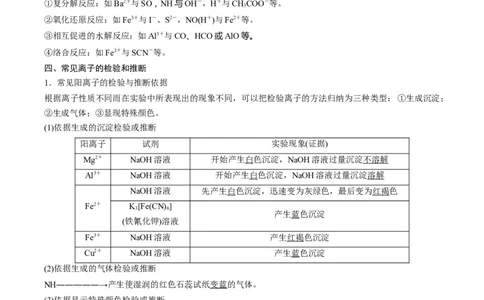
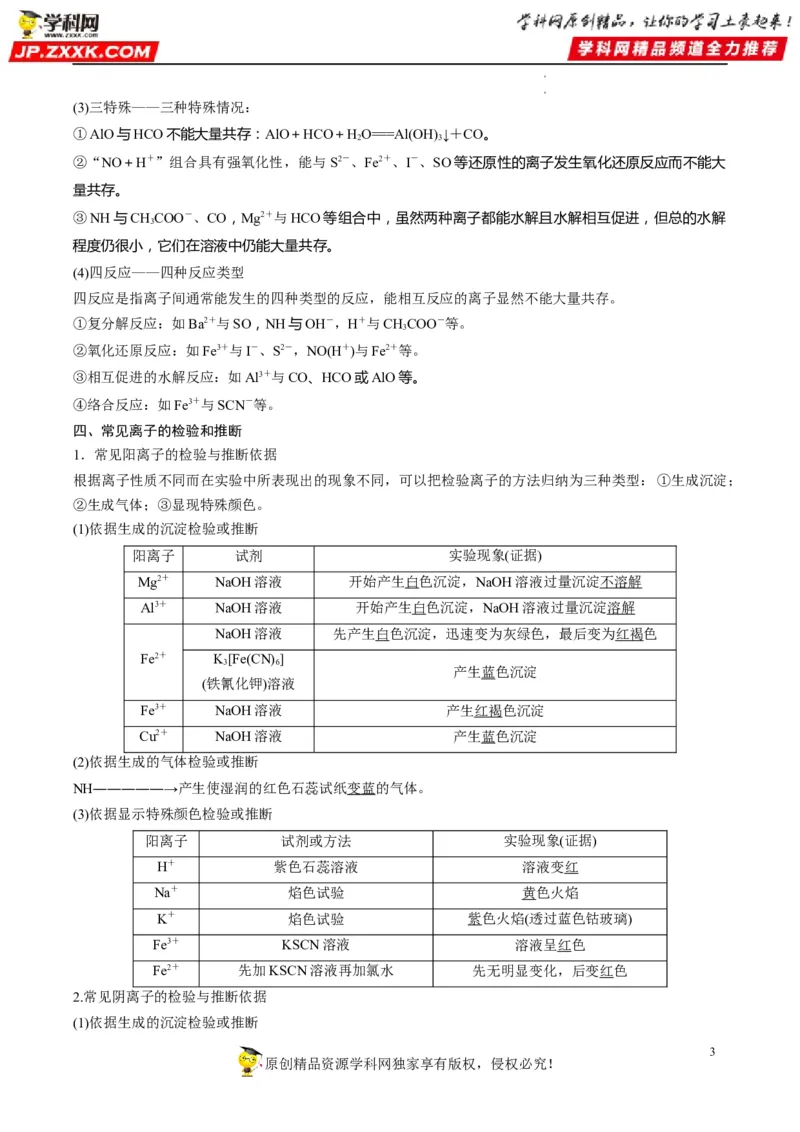
(1)依据生成的沉淀检验或推断
阳离子 试剂 实验现象(证据)
Mg2+ NaOH溶液 开始产生白色沉淀,NaOH溶液过量沉淀不溶解
Al3+ NaOH溶液 开始产生白色沉淀,NaOH溶液过量沉淀溶解
NaOH溶液 先产生白色沉淀,迅速变为灰绿色,最后变为红褐色
Fe2+ K[Fe(CN) ]
3 6
产生蓝色沉淀
(铁氰化钾)溶液
Fe3+ NaOH溶液 产生红褐色沉淀
Cu2+ NaOH溶液 产生蓝色沉淀
(2)依据生成的气体检验或推断
NH―――――→产生使湿润的红色石蕊试纸变蓝的气体。
(3)依据显示特殊颜色检验或推断
阳离子 试剂或方法 实验现象(证据)
H+ 紫色石蕊溶液 溶液变红
Na+ 焰色试验 黄色火焰
K+ 焰色试验 紫色火焰(透过蓝色钴玻璃)
Fe3+ KSCN溶液 溶液呈红色
Fe2+ 先加KSCN溶液再加氯水 先无明显变化,后变红色
2.常见阴离子的检验与推断依据
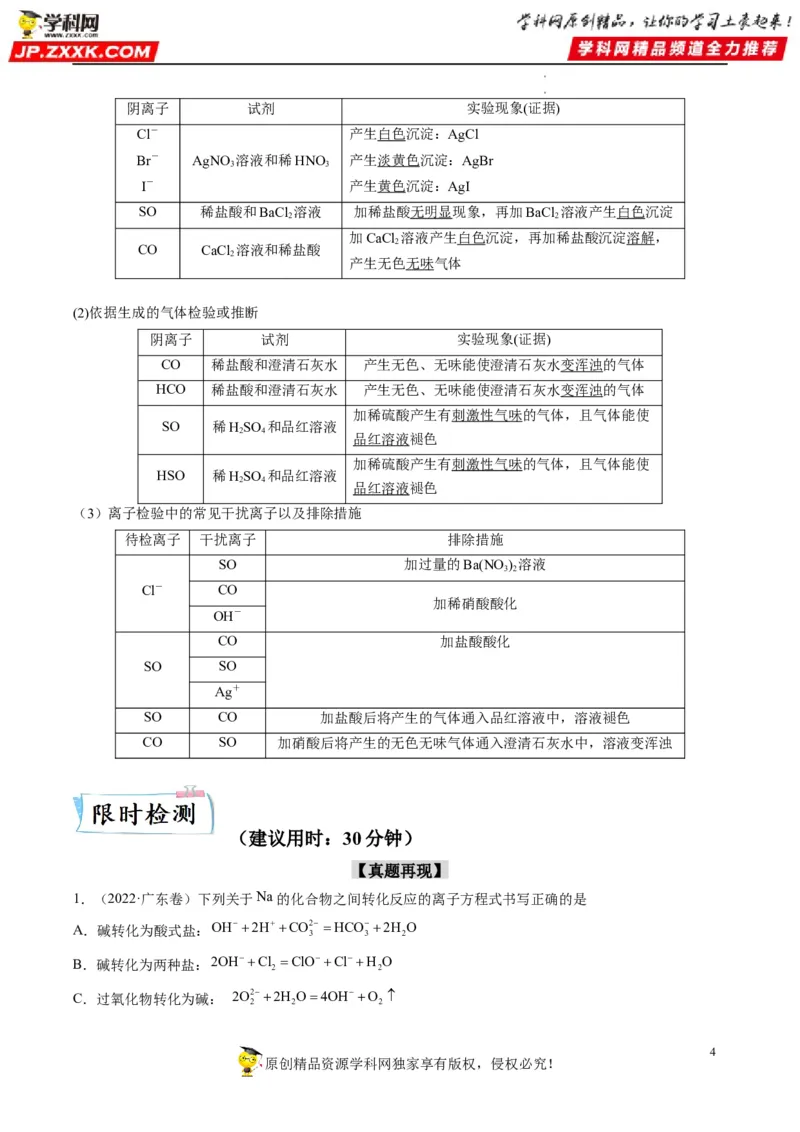
(1)依据生成的沉淀检验或推断
3
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司阴离子 试剂 实验现象(证据)
Cl- 产生白色沉淀:AgCl
Br- AgNO 溶液和稀HNO 产生淡黄色沉淀:AgBr
3 3
I- 产生黄色沉淀:AgI
SO 稀盐酸和BaCl 溶液 加稀盐酸无明显现象,再加BaCl 溶液产生白色沉淀
2 2
加CaCl 溶液产生白色沉淀,再加稀盐酸沉淀溶解,
2
CO CaCl 溶液和稀盐酸
2
产生无色无味气体
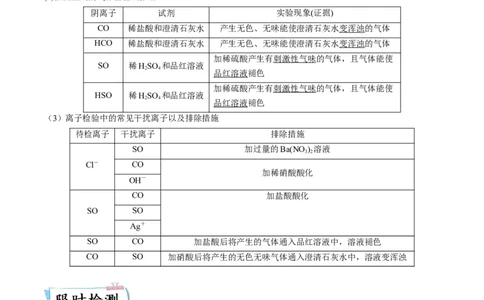
(2)依据生成的气体检验或推断
阴离子 试剂 实验现象(证据)
CO 稀盐酸和澄清石灰水 产生无色、无味能使澄清石灰水变浑浊的气体
HCO 稀盐酸和澄清石灰水 产生无色、无味能使澄清石灰水变浑浊的气体
加稀硫酸产生有刺激性气味的气体,且气体能使
SO 稀HSO 和品红溶液
2 4
品红溶液褪色
加稀硫酸产生有刺激性气味的气体,且气体能使
HSO 稀HSO 和品红溶液
2 4
品红溶液褪色
(3)离子检验中的常见干扰离子以及排除措施
待检离子 干扰离子 排除措施
SO 加过量的Ba(NO ) 溶液
3 2
Cl- CO
加稀硝酸酸化
OH-
CO 加盐酸酸化
SO SO
Ag+
SO CO 加盐酸后将产生的气体通入品红溶液中,溶液褪色
CO SO 加硝酸后将产生的无色无味气体通入澄清石灰水中,溶液变浑浊
(建议用时:30分钟)
【真题再现】
1.(2022·广东卷)下列关于Na的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:OH2HCO2 HCO2H O
3 3 2
B.碱转化为两种盐:2OHCl ClOClH O
2 2
C.过氧化物转化为碱: 2O22H O4OHO
2 2 2
4
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司D.盐转化为另一种盐: Na SiO 2H H SiO 2Na
2 3 2 3
2.(2022·湖南卷)下列离子方程式正确的是
A.Cl 通入冷的NaOH溶液:Cl +2OH-=Cl-+ClO-+H O
2 2 2
B.用醋酸和淀粉-KI溶液检验加碘盐中的IO
3
-:IO
3
-+5I-+6H+=3I
2
+3H
2
O
C.FeSO 溶液中加入H O 产生沉淀:2Fe2++H O +4H O=2Fe(OH) +4H+
4 2 2 2 2 2 3
D.NaHCO 溶液与少量的Ba(OH) 溶液混合:HCO-+Ba2++OH-=BaCO +H O
3 2 3 3 2
3.(2022·全国甲卷)能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH+2H O=AlO+4NH
3 2 2 4
C.硅酸钠溶液中通入二氧化碳:SiO 2 +CO +H O=HSiO+HCO
3 2 2 3 3
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO 2
2 4 4 4
=BaSO ↓+2H O
4 2
4.(2022·广东卷)实验室进行粗盐提纯时,需除去Ca2+、Mg2+和SO2 ,所用试剂包括BaCl 以及
4 2
A.Na CO、NaOH、HCl B.Na CO、HCl、KOH
2 3 2 3
C.K CO、HNO、NaOH D.Na CO、NaOH、HNO
2 3 3 2 3 3
5.(2022·全国乙卷)某白色粉末样品,可能含有Na SO 、Na SO 、Na S O 和Na CO 。取少量样品进
2 4 2 3 2 2 3 2 3
行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加BaCl 溶液有沉淀生成。
2
该样品中确定存在的是
A.Na SO、Na S O B.Na SO、Na S O
2 4 2 2 3 2 3 2 2 3
C.Na SO、Na CO D.Na SO、Na CO
2 4 2 3 2 3 2 3
6.(2021·广东)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应方程式书
写正确的是
A.Na O 放入水中:Na O H O2NaOHO
2 2 2 2 2 2
B.H O(g)通过灼热铁粉: 3H O2FeFe O 3H
2 2 2 3 2
C.铜丝插入热的浓硫酸中:CuH SO CuSO H
2 4 4 2
D.SO 通入酸性 KMnO 溶液中:5SO 2H O2MnO 5SO2 4H 2Mn2
2 4 2 2 4 4
7.(2021·湖南)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
5
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司粒子组 判断和分析
不能大量共存,因发生反应:
A Na、Al3、Cl、NH H O
3 2 Al3 4NH H O=AlO 4NH 2H O
3 2 2 4 2
不能大量共存,因发生反应:
B H、K、S
2
O
3
2 、SO2
4
2H S O2=SSO H O
2 3 2 2
C Na、Fe3、SO2 、H O 能大量共存,粒子间不反应
4 2 2
D H、Na、Cl、MnO 能大量共存,粒子间不反应
4
【优选特训】
1.滴有酚酞的Ba(OH) 溶液显红色,在上述溶液中分别滴加X溶液后有下列现象。下列说法不正确的是(
2
)
序号 装置 X溶液 现象
Ⅰ 盐酸 溶液红色褪去,无沉淀,灯泡亮度没有明显变化
溶液红色不变,有白色沉淀生成,灯泡亮度没有
Ⅱ NaSO 溶液
2 4
明显变化
Ⅲ HSO 溶液 溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗
2 4
A.实验Ⅰ中溶液红色褪去,说明发生了反应:H++OH-===H O
2
B.实验Ⅱ中溶液红色不变,且灯泡亮度没有明显变化,说明溶液中依然存在大量的Na+与OH-
C.实验Ⅲ中溶液红色褪去,有白色沉淀生成,灯泡逐渐变暗,说明发生了反应:Ba2++2OH-+2H++
SO===BaSO ↓+2HO
4 2
D.将实验Ⅱ中NaSO 溶液换成CuSO 溶液,现象与原实验Ⅱ中的现象相同
2 4 4
2.(2022·广东梅州·一模)宏观—微观—符号是化学的三重表征,下列说法对应的离子方程式正确的是
A.氯化铁溶液腐蚀铜箔:Fe3++Cu=Fe2++Cu2+
B.侯氏制碱法中NaHCO 晶体的制备:NH +CO +H O=HCO+NH
3 3 2 2 3 4
C.软锰矿与浓盐酸加热制取Cl:MnO +4Cl-+4H+=MnCl +2H O+Cl ↑
2 2 2 2 2
D.含氢氧化铝的胃舒平治疗胃酸过多:Al(OH) +3H+=Al3++3H O
3 2
3.(2022·北京西城·一模)下列方程式不能准确解释相应实验现象的是
Δ
A.MnO 和浓盐酸共热产生黄绿色气体:MnO +4H++2Cl- Mn2++Cl +2H O
2 2 2 2
B.Na加入滴有酚酞的水中,溶液变红:2Na+2H O=2Na2OH H
2 2
Δ
C.加热Fe和S的混合物生成黑色固体:2Fe+3S Fe S
2 3
6
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司D.加热蓝色的CuCl 溶液,溶液变绿: [Cu(H O) ]2+(aq,蓝色) +4Cl-(aq) [CuCl ]2-(aq,黄色)+4H O(l)
2 2 4 4 2
4.下列反应的离子方程式正确的是( )
A.氢氧化钠溶液中通入少量二氧化硫:SO +OH-=== HSO
2
B.碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO+Ba2++OH-=== BaCO↓+HO
3 2
C.盐酸滴入氨水中:H++OH-=== H O
2
D.碳酸钙溶解于稀硝酸中:CO+2H+ ===CO ↑+HO
2 2
5.下列离子方程式书写正确的是
A.向CuSO 溶液中通入H S气体:Cu2++S2-=CuS
4 2
B.将FeO固体放入稀硝酸中:FeO+2H+=Fe2++H O
2
C.NaHSO 溶液与BaOH 溶液反应至溶液是中性;2H++SO2-+Ba2++2OH-=BaSO +2H O
4 2 4 4 2
D.向FeCl 溶液中加入铜粉:Fe3++Cu=Fe2++Cu2+
3
6.(2022·北京通州·一模)下列用于解释事实的方程式书写不正确的是
A.新切开的钠的光亮表面在空气中很快变暗:4NaO =2Na O
2 2
B.将 通入苯酚钠溶液中出现浑浊:2 +CO +H O→2 +Na CO
CO 2 2 2 3
2
C.向AlCl 溶液中滴加氨水产生白色沉淀:Al3 3NH H OAl(OH) 3NH
3 3 2 3 4
D.向AgCl悬浊液中滴加KI溶液产生黄色沉淀:AgCl(s)I(aq)AgI(s)Cl(aq)
7.(2022·湖北武汉·模拟预测)对于下列实验,能正确描述其反应的离子方程式是
A.向氢氧化钡溶液中滴加硫酸氢钠溶液:H OH=H O
2
B.向覆铜板上滴加FeCl 溶液:2Fe3 Cu=2Fe2 Cu2
3
C.向纯碱溶液中滴加少量盐酸:CO22H=CO H O
3 2 2
D.向次氯酸钙溶液中通入少量SO 气体:2ClOSO H O=2HClOSO2
2 2 2 3
8.常温下,下列各组离子能大量共存的是( )
A.Mg2+、Na+、MnO、SO
B.Fe2+、NH、NO、H+
C.OH-、Na+、SO、Cu2+
D.Al3+、K+、CO、Cl-
9.(2022·重庆·一模)常温下,下列各组离子在指定环境中一定能大量共存的是
A.澄清透明的中性溶液:Fe3、Ba2、Cl、NO
3
B.能使pH试纸变深红的溶液:K、Na、I、CrO2
4
C.pH13的NaOH溶液:Na、Cl、SO2、AlO
4 2
7
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司D.c
OH-
< K
w
的溶液:Ca2、K、NO
2
、CHCOO
10.(2022·湖南长沙·一模)25℃时,下列各组离子或分子在指定溶液中一定能大量共存的是
A.由水电离的c H 11014molL1 的溶液中:NO
3
、I、Na、Al3
B.甲基橙呈红色的溶液:NH、Ba2、AlO、Cl
4 2
C.0.1molL1FeCl
3
溶液:K、H、SO2
4
、MnO
4
Kw
11013molL1
D.
c
H 的溶液中:
NH
、
Ca2
、
Cl
、
NO
4 3
11.(2022·湖南·岳阳市教育科学技术研究院二模)下列各组澄清溶液中离子能大量共存,且加入X试剂
后发生反应的离子方程式书写正确的是
选项 离子组 X试剂 离子方程式
A Na+、Fe3+、SO 2 4 、Cl- 过量H 2 S 2Fe3++H 2 S=2Fe2++S↓+2H+
B Fe2+、K+、NO3 、Br- 少量HI 4H++3Fe2++NO3 =3Fe3++NO↑+2HO
2
C NH4 、Fe3+、AlO2 、Na+ 少量铜粉 2Fe3++Cu=2Fe2++Cu2+
D AlO2 、Na+、K+、HCO3 过量HCl 5H++HCO3 +AlO -=Al3++CO ↑+3H O
2 2 2
12.(2022·湖南衡阳·二模)下列各组澄清溶液中的离子能大量共存,且加入试剂后发生反应的离子方程
式书写正确的是
选
离子 试剂 离子方程式
项
A NH4 、Mg2+、Fe3+、SO 2 4 少量铜粉 Fe3++Cu=Fe2++Cu2+
B Fe2+、H+、Cl-、NO3 KNO 3 溶液 3Fe2++ NO3 +4H+=3Fe3++NO↑+2H 2 O
C K+、Na+、ClO-、SO 2 4 少量SO 2 SO 2 +H 2 O+ClO-=SO 2 4 +HClO+Cl-
D K+、Na+、SO3 2 、AlO2 少量NH 4 Cl NH4 +AlO2 +2H 2 O=Al(OH) 3 ↓+NH 3 ·H 2 O
13.(2022·北京西城·一模)向100mL 0.01mol/L BaOH 溶液中滴加0.1mol/L NaHCO 溶液,测得溶液
2 3
电导率的变化如图。下列说法不正确的是
8
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司A.BaOH 和NaHCO 都是强电解质
2 3
B.A→B电导率下降的主要原因是发生了反应:Ba22OH2HCO=BaCO 2H OCO2
3 3 2 3
C.B→C,溶液中的c
OH
减小
D.A、B、C三点水的电离程度:A<B<C
14.对某无色溶液分别进行下列操作,所得现象和结论均正确的是( )
A.加入氨水,产生白色沉淀,证明原溶液中存在Al3+
B.加入AgNO 溶液,产生白色沉淀,证明原溶液中存在Cl-
3
C.加入盐酸酸化的BaCl 溶液,生成白色沉淀,证明原溶液中存在SO
2
D.加入NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,证明原溶液中存在NH
15.(2022·湖南岳阳·一模)下列离子组中加(或通)入相应试剂后,判断和分析均正确的是
选项 离子组 加(或通)入试剂 判断和分析
足量NaHCO 溶液 AlO- HCO-
A Na+、K+、
AlO-
2、Cl-
3 不能大量共存,因 2和 3之间会发生完全双
水解生成CO 气体和Al(OH) 沉淀
2 3
Na+、Mg2+、 SO2 4 - 、 不能大量共存,会发生下列反应
B 足量NaOH溶液
HCO- Mg2++HCO
3
-+OH-=MgCO
3
+H
2
O
3
NH+
4、Ca2+、Cl-、
C 足量CO 能大量共存,粒子间不反应
2
NO-
3
不能大量共存,会发生下列氧化还原反应
D Na+、K+、ClO-、Cl- 少量SO
2 ClO-+H O+SO =Cl-+SO2-+2H+
2 2 4
16.某无色溶液中可能含有①Na+、②Ba2+、③Cl-、④Br-、⑤SO、⑥SO、⑦Fe2+中的几种离子,依
次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
步骤 操作 现象
Ⅰ 用pH试纸检验 溶液的pH大于7
Ⅱ 向溶液中滴加氯水,再加入CCl ,振荡,静置 CCl 层呈橙红色
4 4
9
原创精品资源学科网独家享有版权,侵权必究!
学学科科网网((北北京京))股股份份有有限公司Ⅲ 取Ⅱ的上层溶液,加入Ba(NO ) 溶液和稀硝酸 有白色沉淀产生
3 2
将 Ⅲ 过滤,向滤液中加入AgNO 溶液和稀硝
3
Ⅳ 有白色沉淀产生
酸
下列结论正确的是( )
A.肯定含有的离子是①④⑤
B.肯定没有的离子是②⑤⑦
C.可能含有的离子是①②⑥
D.不能确定的离子是①③⑥
17.一瓶无色澄清的溶液,其中可能含有H+、NH、Na+、Al3+、Fe3+、I-、NO、CO、SO、AlO。取该溶
液进行以下实验:
①用pH试纸检验,溶液呈强酸性 ②取溶液适量,加入少量CCl 和数滴新制氯水,振荡,CCl 层呈紫红
4 4
色 ③该溶液的焰色试验没有黄色;根据以上实验结果,下列推断正确的是( )
A.向该溶液中加入BaCl 不一定能观察到白色沉淀
2
B.可以确定没有Na+、Fe3+、CO、AlO,不能确定是否有NO
C.该溶液可能是NH NO 与HI的混合
4 3
D.一定没有Al3+、CO和NO
18.根据图示信息书写方程式。
(1)NaN 是一种易溶于水(NaN ===Na++N)的白色固体,可用于有机合成和汽车安全气囊的产气等。钠法
3 3
(液氨法)制备NaN 的工艺流程如下:
3
①反应Ⅰ的化学方程式为________________________________________________________。
②销毁NaN 可用NaClO溶液,该销毁反应的离子方程式为_____________________________________(N
3
被氧化为N)。
2
(2)利用钴渣[含Co(OH) 、Fe(OH) 等]制备钴氧化物的工艺流程如下:
3 3
Co(OH) 溶解还原反应的离子方程式为____________________________________________________。
3
1
原创精品资源学科网独家享有版权,侵权必究! 0
学学科科网网((北北京京))股股份份有有限公司1
原创精品资源学科网独家享有版权,侵权必究! 1
学学科科网网((北北京京))股股份份有有限公司