AI颠覆RNA结构预测!从原理到工具,一篇看懂生命科学新革命!

生命科学新革命
结构决定功能这句话,在RNA身上体现得淋漓尽致。可传统实验测结构慢、贵、难,直到AI入局,一切都变了。
01
引言
为什么RNA结构预测,需要靠AI?
传统RNA结构解析,全靠X射线晶体衍射、冷冻电镜,耗时耗力,根本快不起来。
而RNA有多重要?
它是蛋白质翻译模板、调控基因表达、参与免疫应答,生命活动处处离不开。
精准预测RNA空间结构,能帮我们:
– 深刻理解RNA功能
– 加速RNA药物研发
– 推进基因调控与合成生物学研究
从结构上看,RNA分三级:
1. 一级结构:核苷酸排列顺序,A/U/C/G碱基序列
2. 二级结构:单链回折,形成茎区、发夹环、凸环、内环
3. 三级结构:在二级基础上,靠氢键、碱基堆积力、范德华力折叠成3D构象
残酷现实是:
人类基因组中转录RNA的区域是蛋白编码区的30倍,但实验解析的RNA 3D结构,不到蛋白质的1%。
数据极度稀缺,AI成了破局出路。
02
AI预测原理

01
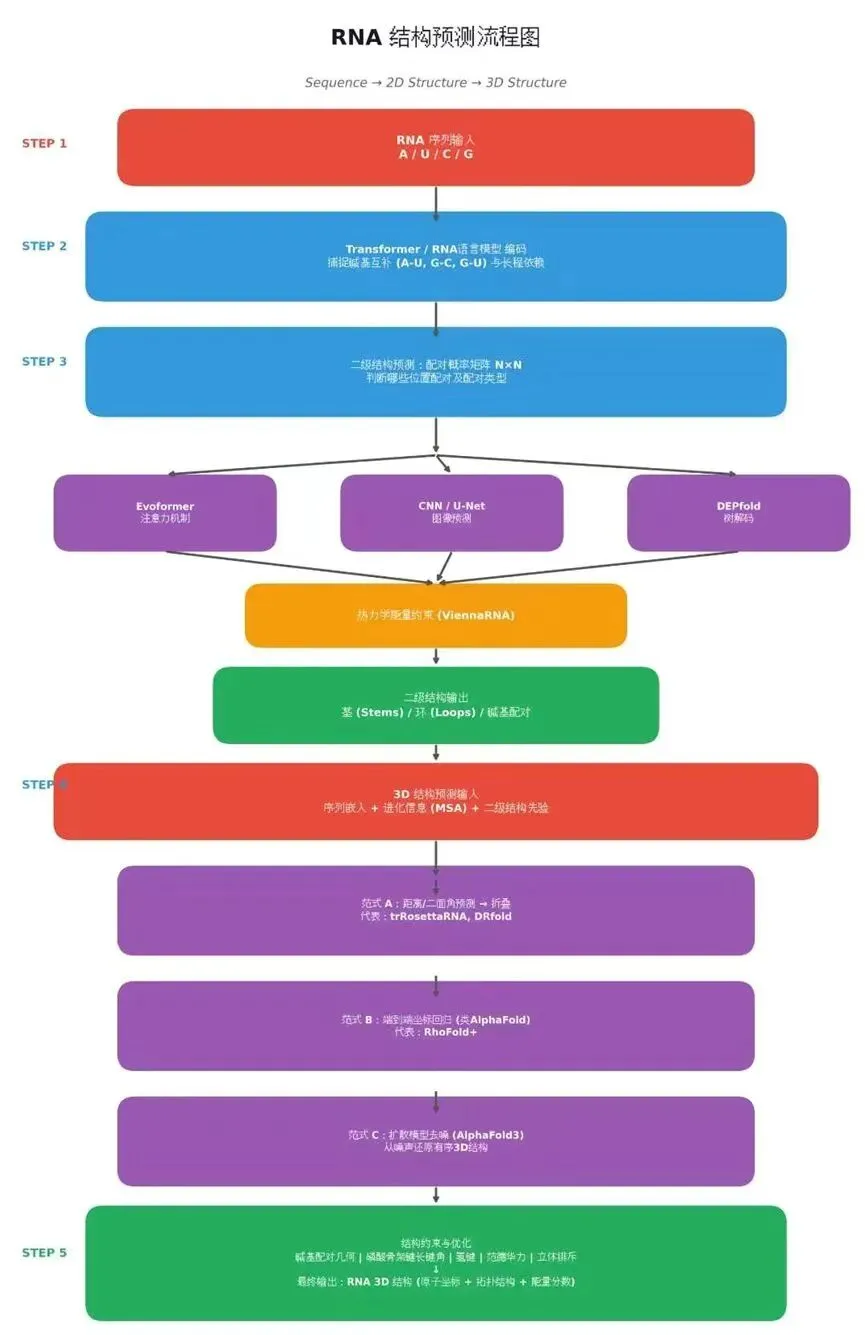
整体构架流程
序列输入 → 特征编码 → 结构预测 → 物理优化
02
二级结构预测
– 把RNA序列转为高维嵌入,捕捉长程依赖
– 输出N×N配对概率矩阵
– 用CNN、Transformer、残差网络等架构
– 结合热力学约束,输出茎区、环区、假结
03
3D结构预测
– 输入序列嵌入、共变信息、二级结构先验
– 三类范式:距离/二面角预测、端到端坐标回归、
扩散模型生成
– 加入键长键角、氢键等物理约束,得到稳定构象
04
关键技术突破
– RNA大语言模型:自监督预训练,解决数据少问题
– Evoformer/IPA:统一序列、成对、几何特征
– 扩散模型:更灵活精准的3D生成
– 生物合理解码:避免冲突、无效结构
05
明星模型:ARES(纯几何驱动)
斯坦福团队打造,小样本学习天花板:
– 只输原子坐标+元素类型
– 不用任何生物学先验(碱基对、双螺旋全不用)
– 等变网络层:旋转平移不变,保证物理规律
– 分层学习:原子→片段→分子,多尺度建模
– 仅18个结构就能训练,突破数据瓶颈
特点:纯几何、等变对称、多尺度、数据高效、通用性极强。
03
主流预测工具

01
核心对比
当前RNA结构预测已从传统热力学算法全面进入AI深度学习时代,尤其在二级结构、长序列、假结预测上实现精度与速度双重突破。结合最新研究,对主流AI工具、核心性能、适用场景做一站式对比。
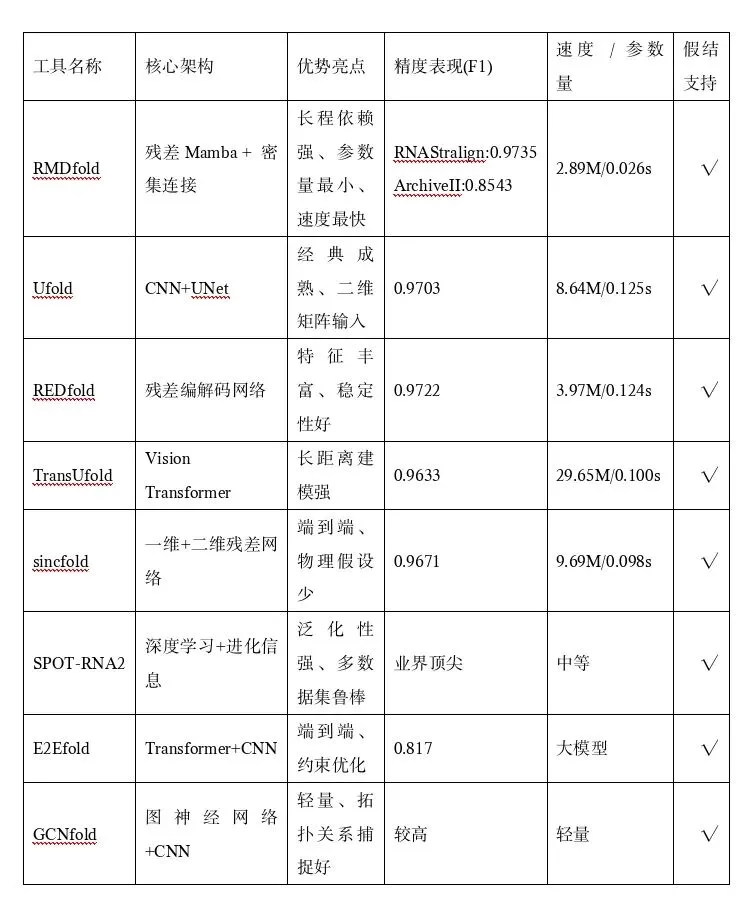

02
传统模型与AI模型的对比
-传统热力学模型(基础工具)
代表:ViennaRNA、RNAstructure、Mfold
特点:基于最小自由能、速度快、可解释强
局限:长序列/假结精度低(约50%–70%)
场景:教学演示、短序列快速验证、基础实验
-深度学习AI模型(主流)
CNN路线:Ufold、REDfold、sincfold——局部特征强、稳定可靠
Transformer路线:TransUfold、E2Efold、Wfold——长程依赖好、算力要求
Mamba新路线:RMDfold——线性复杂度、长序列更快更准


1.科研高精度预测(首选)
推荐:RMDfold > REDfold > Ufold
适用:ncRNA、tRNA、rRNA、长链非编码RNA
理由:RMDfold在标准数据集F1/MCC全面领先,200–500nt仍保持0.70以上准确率,假结预测最优。
2.长序列RNA预测(关键)
推荐:RMDfold > TransUfold > E2Efold
适用:病毒基因组、长链 RNA、核糖体 RNA
要点:Mamba/Transformer 架构更擅长长程配对,避免 CNN 感受野不足。
3.假结结构预测(难点)
推荐:RMDfold > SPOT-RNA2 > Ufold
适用:含假结的调控 RNA、核酶、病毒 RNA
数据:RMDfold 假结 F1=0.7414,MCC=0.7433,显著优于同类。
4.轻量化/快速批量预测
推荐:RMDfold > REDfold
适用:批量测序数据、高通量筛选、个人电脑运行
优势:RMDfold参数量最小(2.89M)、单条推理仅0.026s。
5.跨家族/新RNA泛化预测
推荐:SPOT-RNA2 > MXfold2 > sincfold
适用:新发现RNA家族、低同源序列
要点:融合进化信息与多任务训练,跨集稳定性更强。
6.教学与入门使用
推荐:Ufold、ViennaRNA网页版
理由:教程多、可视化友好、结果稳定,适合课堂演示与新手练习。

模型特点总结:
AI已成为RNA结构预测的标配方案,2025年以RMDfold为代表的Mamba架构模型,在精度、速度、参数量、长序列、假结五大维度全面领先,成为科研首选工具。
实际使用中,建议采用“AI主预测+传统工具验证”的组合策略,兼顾效率与可靠性。
挑战与展望
当前,以RMDfold、Ufold、SPOT-RNA2等为代表的AI模型已在精度、速度、长序列处理和假结预测等方面显著优于传统热力学方法。不同架构(CNN、Transformer、Mamba、扩散模型)各有优势,适用于科研高精度预测、批量快速推理、教学演示等多样场景。
然而,RNA结构预测仍面临数据稀缺、长序列建模困难、物理一致性不足等挑战。未来,融合多模态数据、引入物理约束、发展可解释AI与RNA反向设计,将是推动该领域走向成熟与广泛应用的关键方向。
总体而言,人工智能已从辅助工具转变为RNA结构预测的核心驱动力,其发展将为RNA生物学研究、合成生物学及RNA靶向药物开发提供坚实的技术支撑。
图片:万子怡
文字:王新新 杨欣梓玉 裴雨婷 卢含璞
编辑:王新新、万子怡
润色:deepseek
审核:安然
 夜雨聆风
夜雨聆风




