文档内容
第3章 晶体结构与性质
3.2 分子晶体
一.选择题(共11小题)
1.下列关于分子晶体的说法正确的是
A.晶体中分子间作用力越大,分子越稳定
B.在分子晶体中一定存在共价键
C.冰和Br 都是分子晶体
2
D.稀有气体不能形成分子晶体
2.下列说法正确的是( )
A.离子化合物中可能含有共价键
B.分子晶体中的分子内不含有共价键
C.分子晶体中一定有非极性共价键
D.分子晶体中分子一定紧密堆积
3.下列说法中正确的是( )
A.冰融化时,分子中H—O键发生断裂
B.共价晶体中,共价键越强,熔点越高
C.分子晶体中,共价键键能越大,该分子晶体的熔、沸点一定越高
D.分子晶体中,分子间作用力越大,该物质越稳定
4.关于氢键,下列说法正确的是
A.氢键比分子间作用力强,所以它属于化学键
B.冰中存在氢键,水中不存在氢键
C.分子间形成的氢键使物质的熔点和沸点升高
D.氢键可以增大物质的化学性质
。
5.关于氢键,下列说法正确的是( )
A.分子间形成的氢键使物质的熔点和沸点升高
B.冰中存在氢键,水中不存在氢键
C.每一个水分子内含有两个氢键
D.HO是一种非常稳定的化合物,这是由于氢键所致
2
6.中科院国家纳米科学中心科研员在国际上首次“拍”到氢键的“照片”,实现了氢键的实空间成像,为
“氢键的本质”这一化学界争论了80多年的问题提供了直观证据。下列有关氢键说法中不正确的是A.由于氢键的存在,HF的稳定性强于HS
2
B.由于氢键的存在,乙醇比甲醚(CH-O-CH )更易溶于水
3 3
C.由于氢键的存在,沸点:HF> HI >HBr> HCl
D.由于氢键的存在,冰能浮在水面上
7.下列关于氢键的说法中正确的是
A.由于氢键的存在,氨气易溶于水
B.氢键是自然界中最重要、存在最广泛的化学键之一
C.由于氢键的存在,沸点:
D.由于氢键的存在,酸性:
8.在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是
A.范德华力、范德华力、范德华力
B.范德华力、范德华力、共价键
C.范德华力、共价键、共价键
D.共价键、共价键、共价键
9.下列关于范德华力的叙述中,正确的是( )
A.范德华力的实质也是一种电性作用,所以范德华力是一种特殊化学键
B.任何分子间在任意情况下都会产生范德华力
C.范德华力与化学键的区别是作用力的强弱问题
D.范德华力非常微弱,故破坏范德华力不需要消耗能量
10.下列关于范德华力对物质性质的影响的描述正确的是( )
A.范德华力是决定物质熔点和沸点高低的唯一因素
B.范德华力是影响物质部分物理性质的一种因素
C.范德华力能够影响物质的化学性质和物理性质
D.范德华力与物质的性质没有必然的联系
11.在“HI(s)→HI(g)→H 和I”的变化过程中,被破坏的作用力依次是( )
2 2
A.范德华力、范德华力 B.共价键、离子键
C.范德华力、共价键 D.共价键、共价键
三、填空题(共2题)
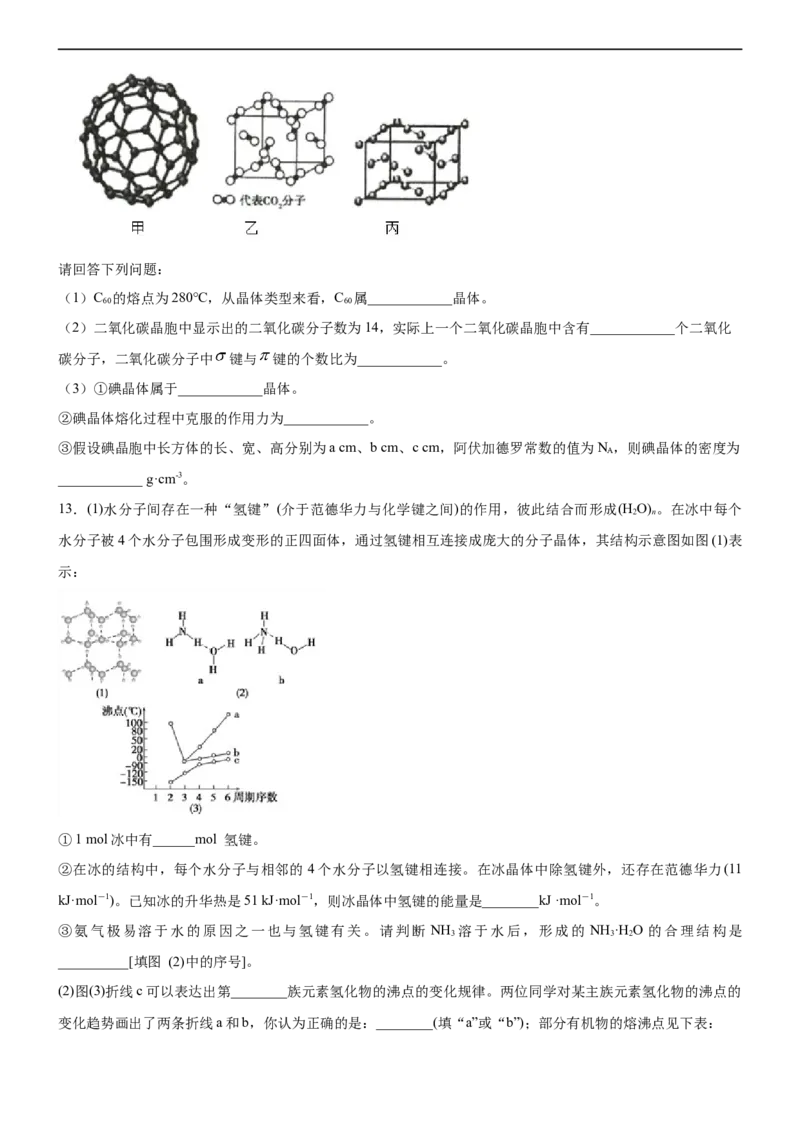
12.如图所示,甲、乙、丙分别表示C、二氧化碳、碘晶体的晶胞结构模型。请回答下列问题:
(1)C 的熔点为280℃,从晶体类型来看,C 属____________晶体。
60 60
(2)二氧化碳晶胞中显示出的二氧化碳分子数为14,实际上一个二氧化碳晶胞中含有____________个二氧化
碳分子,二氧化碳分子中 键与 键的个数比为____________。
(3)①碘晶体属于____________晶体。
②碘晶体熔化过程中克服的作用力为____________。
③假设碘晶胞中长方体的长、宽、高分别为a cm、b cm、c cm,阿伏加德罗常数的值为N ,则碘晶体的密度为
A
____________ g·cm-3。
13.(1)水分子间存在一种“氢键”(介于范德华力与化学键之间)的作用,彼此结合而形成(H O) 。在冰中每个
2 n
水分子被4个水分子包围形成变形的正四面体,通过氢键相互连接成庞大的分子晶体,其结构示意图如图(1)表
示:
①1 mol冰中有______mol 氢键。
②在冰的结构中,每个水分子与相邻的 4个水分子以氢键相连接。在冰晶体中除氢键外,还存在范德华力(11
kJ·mol-1)。已知冰的升华热是51 kJ·mol-1,则冰晶体中氢键的能量是________kJ ·mol-1。
③氨气极易溶于水的原因之一也与氢键有关。请判断 NH 溶于水后,形成的 NH ·H O 的合理结构是
3 3 2
__________[填图 (2)中的序号]。
(2)图(3)折线c可以表达出第________族元素氢化物的沸点的变化规律。两位同学对某主族元素氢化物的沸点的
变化趋势画出了两条折线a和b,你认为正确的是:________(填“a”或“b”);部分有机物的熔沸点见下表:CH
3
烃 CH CHCH 硝基苯酚
4 3 3
(CH)CH
2 2 3
沸点/℃ -164 -88.6 -0.5 熔点/℃ 45 96 114
由这些数据你能得出的结论是:______________________,______________(至少写2条)。