文档内容
北京市朝阳区高三年级第二学期质量检测一
化学
2023.3
(考试时间90分钟 满分100分)
本试卷共10页。考生务必将答案答在答题卡上,在试卷上作答无效。考试结束后,将本试卷和
答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5 Fe 56
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
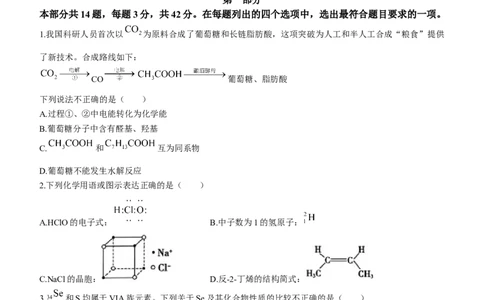
1.我国科研人员首次以 为原料合成了葡萄糖和长链脂肪酸,这项突破为人工和半人工合成“粮食”提供
了新技术。合成路线如下:
CO 葡萄糖、脂肪酸
下列说法不正确的是( )
A.过程①、②中电能转化为化学能
B.葡萄糖分子中含有醛基、羟基
C. 和 互为同系物
D.葡萄糖不能发生水解反应
2.下列化学用语或图示表达正确的是( )
A.HClO的电子式: B.中子数为1的氢原子:
C.NaCl的晶胞: D.反-2-丁烯的结构简式:
3. 和S均属于VIA族元素。下列关于Se及其化合物性质的比较不正确的是( )
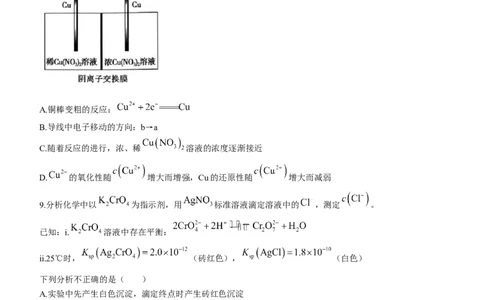
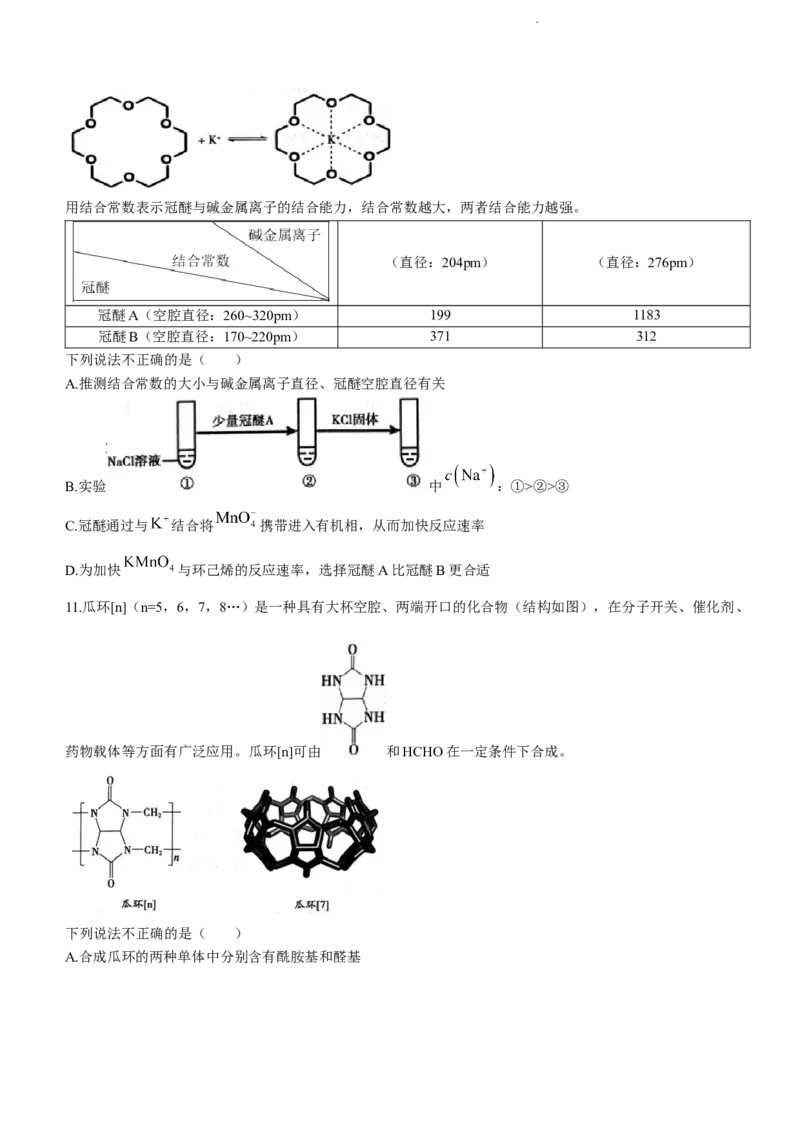
A.第一电离能: B.原子半径:Se②>③
C.冠醚通过与 结合将 携带进入有机相,从而加快反应速率
D.为加快 与环己烯的反应速率,选择冠醚A比冠醚B更合适
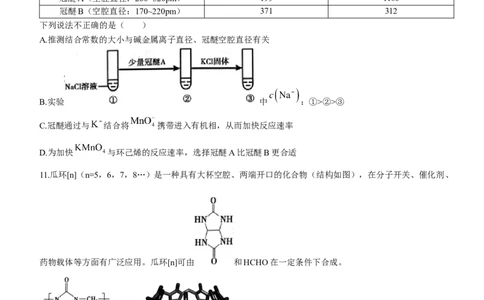
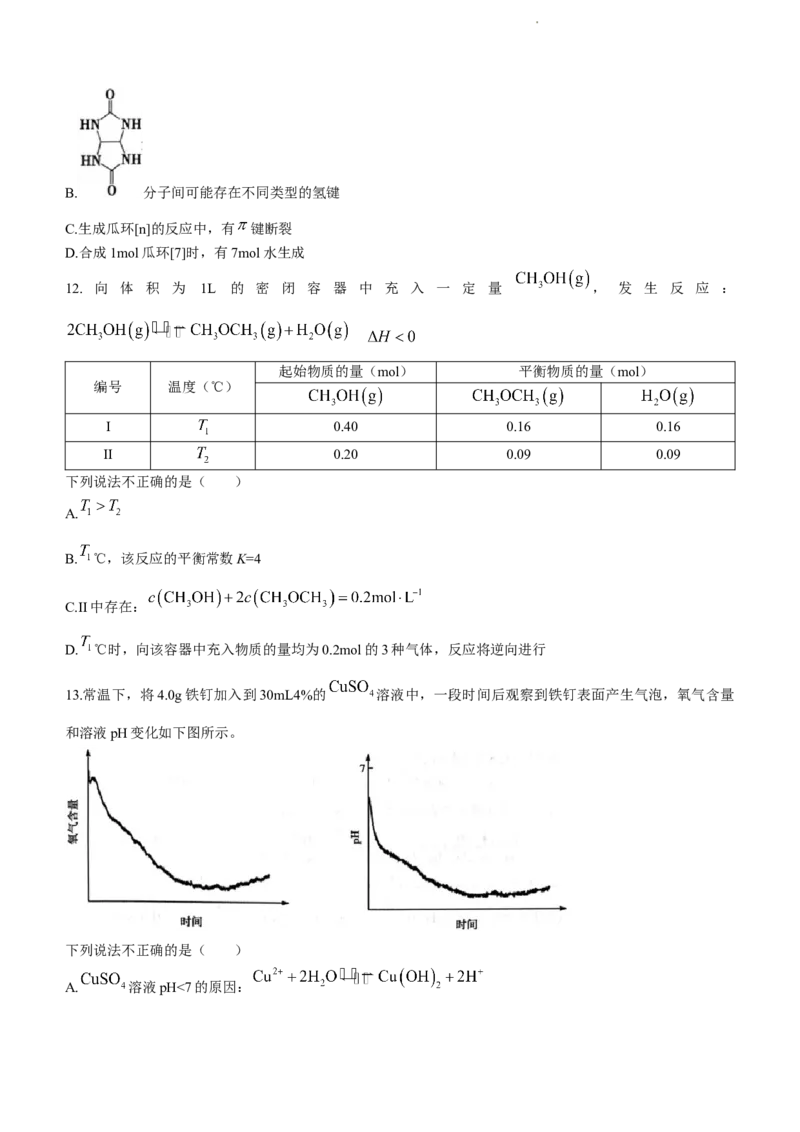
11.瓜环[n](n=5,6,7,8…)是一种具有大杯空腔、两端开口的化合物(结构如图),在分子开关、催化剂、
药物载体等方面有广泛应用。瓜环[n]可由 和HCHO在一定条件下合成。
下列说法不正确的是( )
A.合成瓜环的两种单体中分别含有酰胺基和醛基
学科网(北京)股份有限公司B. 分子间可能存在不同类型的氢键
C.生成瓜环[n]的反应中,有 键断裂
D.合成1mol瓜环[7]时,有7mol水生成
12. 向 体 积 为 1L 的 密 闭 容 器 中 充 入 一 定 量 , 发 生 反 应 :
起始物质的量(mol) 平衡物质的量(mol)
编号 温度(℃)
I 0.40 0.16 0.16
II 0.20 0.09 0.09
下列说法不正确的是( )
A.
B. ℃,该反应的平衡常数K=4
C.II中存在:
D. ℃时,向该容器中充入物质的量均为0.2mol的3种气体,反应将逆向进行
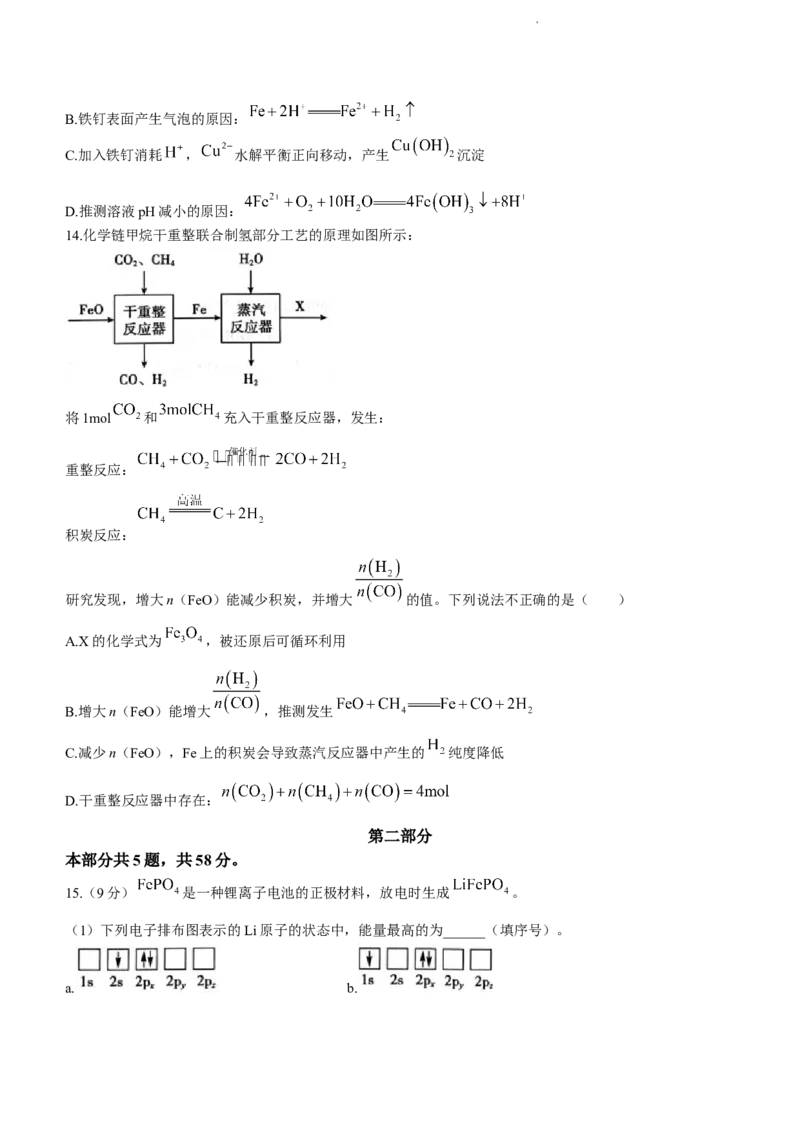
13.常温下,将4.0g铁钉加入到30mL4%的 溶液中,一段时间后观察到铁钉表面产生气泡,氧气含量
和溶液pH变化如下图所示。
下列说法不正确的是( )
A. 溶液pH<7的原因:
学科网(北京)股份有限公司B.铁钉表面产生气泡的原因:
C.加入铁钉消耗 , 水解平衡正向移动,产生 沉淀
D.推测溶液pH减小的原因:
14.化学链甲烷干重整联合制氢部分工艺的原理如图所示:
将1mol 和 充入干重整反应器,发生:
重整反应:
积炭反应:
研究发现,增大n(FeO)能减少积炭,并增大 的值。下列说法不正确的是( )
A.X的化学式为 ,被还原后可循环利用
B.增大n(FeO)能增大 ,推测发生
C.减少n(FeO),Fe上的积炭会导致蒸汽反应器中产生的 纯度降低
D.干重整反应器中存在:
第二部分
本部分共5题,共58分。
15.(9分) 是一种锂离子电池的正极材料,放电时生成 。
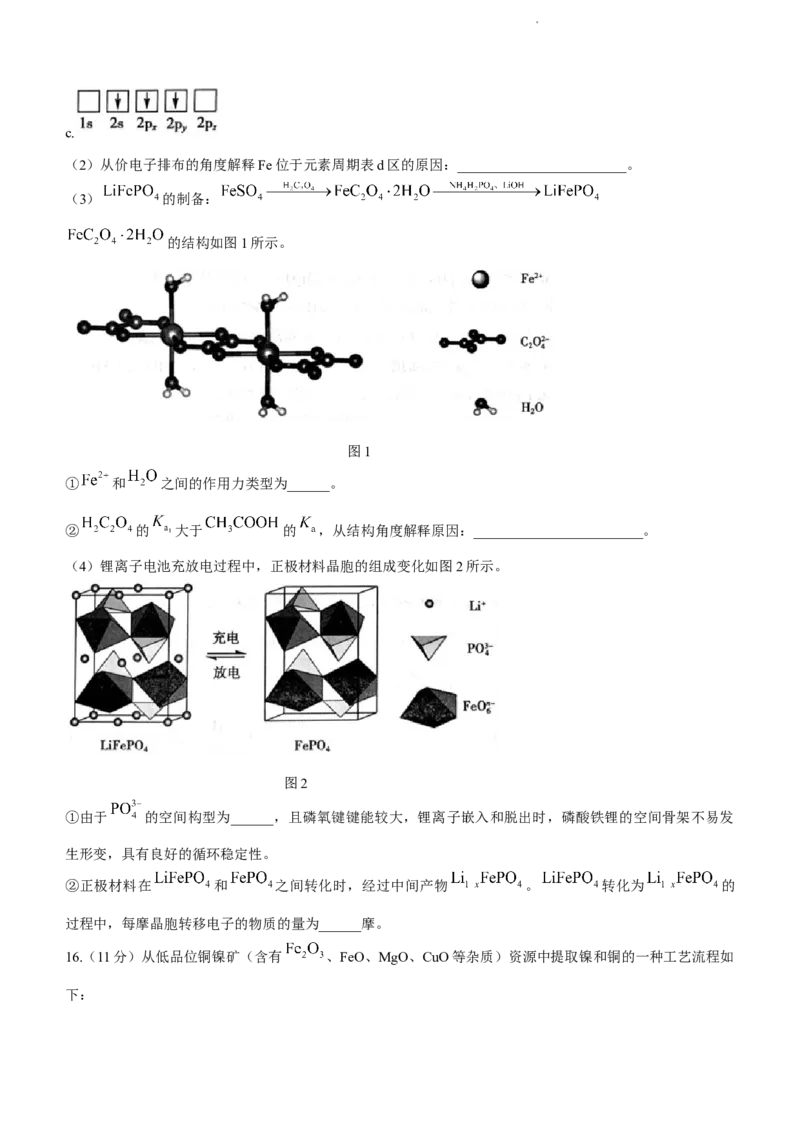
(1)下列电子排布图表示的Li原子的状态中,能量最高的为______(填序号)。
a. b.
学科网(北京)股份有限公司c.
(2)从价电子排布的角度解释Fe位于元素周期表d区的原因:________________________。
(3) 的制备:
的结构如图1所示。
图1
① 和 之间的作用力类型为______。
② 的 大于 的 ,从结构角度解释原因:________________________。
(4)锂离子电池充放电过程中,正极材料晶胞的组成变化如图2所示。
图2
①由于 的空间构型为______,且磷氧键键能较大,锂离子嵌入和脱出时,磷酸铁锂的空间骨架不易发
生形变,具有良好的循环稳定性。
②正极材料在 和 之间转化时,经过中间产物 。 转化为 的
过程中,每摩晶胞转移电子的物质的量为______摩。
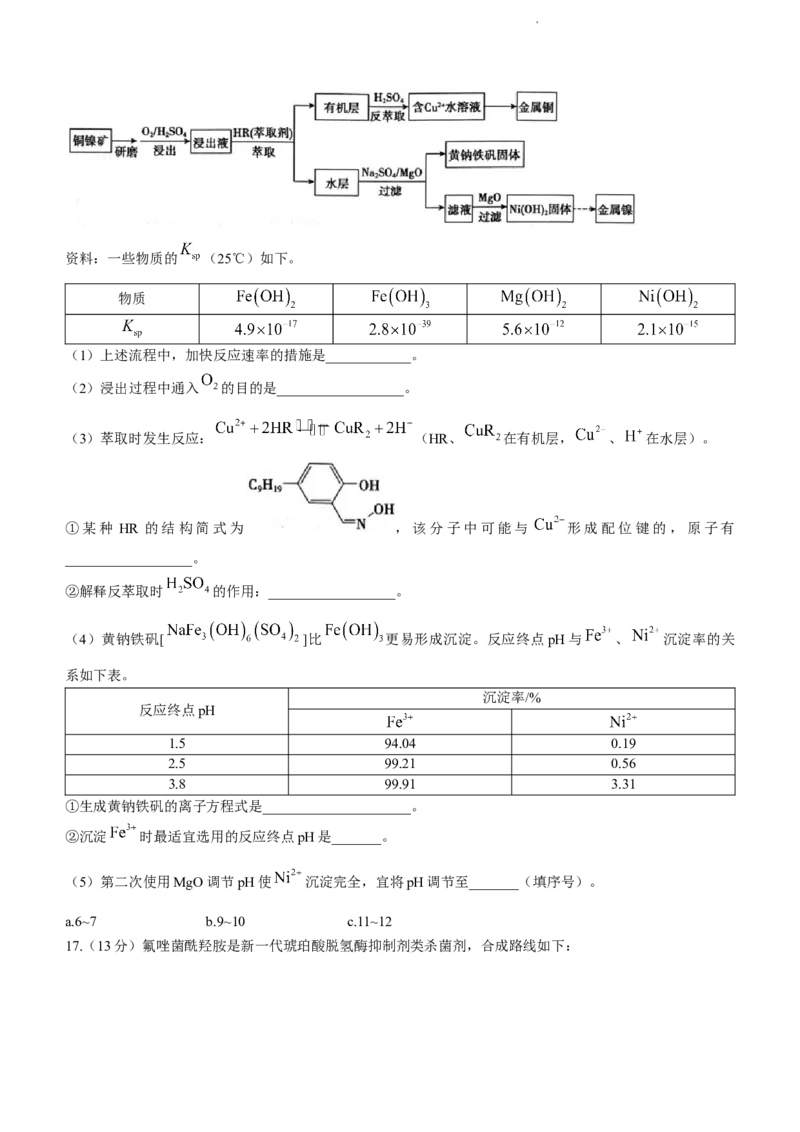
16.(11分)从低品位铜镍矿(含有 、FeO、MgO、CuO等杂质)资源中提取镍和铜的一种工艺流程如
下:
学科网(北京)股份有限公司资料:一些物质的 (25℃)如下。
物质
(1)上述流程中,加快反应速率的措施是____________。
(2)浸出过程中通入 的目的是__________________。
(3)萃取时发生反应: (HR、 在有机层, 、 在水层)。
①某种 HR 的结构简式为 ,该分子中可能与 形成配位键的,原子有
__________________。
②解释反萃取时 的作用:__________________。
(4)黄钠铁矾[ ]比 更易形成沉淀。反应终点pH与 、 沉淀率的关
系如下表。
沉淀率/%
反应终点pH
1.5 94.04 0.19
2.5 99.21 0.56
3.8 99.91 3.31
①生成黄钠铁矾的离子方程式是_____________________。
②沉淀 时最适宜选用的反应终点pH是_______。
(5)第二次使用MgO调节pH使 沉淀完全,宜将pH调节至_______(填序号)。
a.6~7 b.9~10 c.11~12
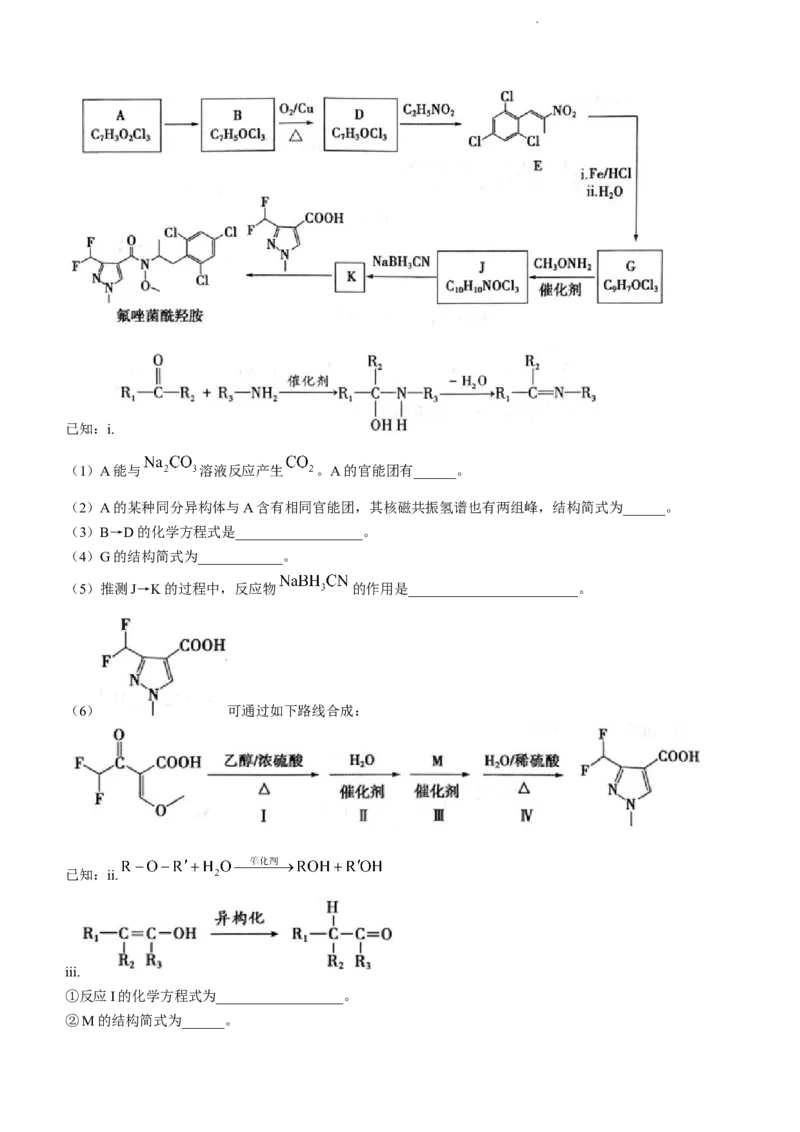
17.(13分)氟唑菌酰羟胺是新一代琥珀酸脱氢酶抑制剂类杀菌剂,合成路线如下:
学科网(北京)股份有限公司已知:i.
(1)A能与 溶液反应产生 。A的官能团有______。
(2)A的某种同分异构体与A含有相同官能团,其核磁共振氢谱也有两组峰,结构简式为______。
(3)B→D的化学方程式是__________________。
(4)G的结构简式为____________。
(5)推测J→K的过程中,反应物 的作用是________________________。
(6) 可通过如下路线合成:
已知:ii.
iii.
①反应I的化学方程式为__________________。
②M的结构简式为______。
学科网(北京)股份有限公司③设计步骤I和IV的目的是________________________。
18.(11分)工业烟气中常含有 (NO、 )。用NaClO溶液将 氧化为 ,实现烟气中
的脱除。
(1) 在大气中会形成酸雨。形成酸雨的过程中,NO表现______性。
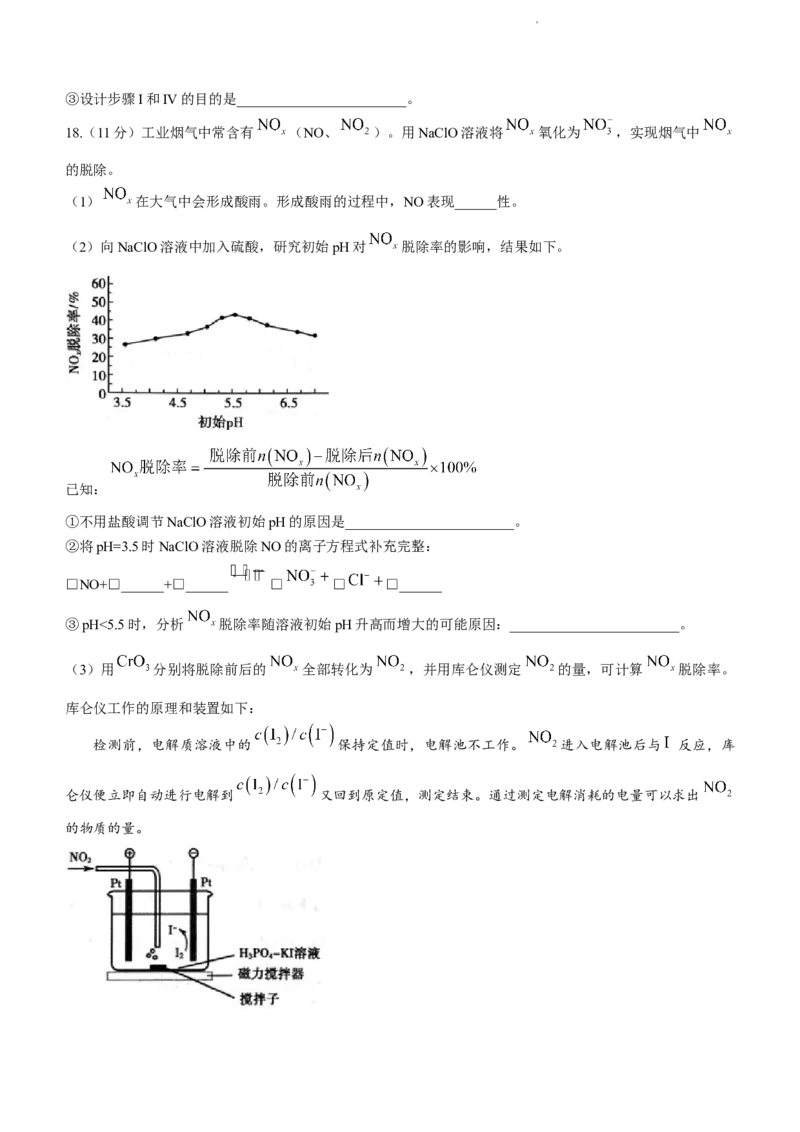
(2)向NaClO溶液中加入硫酸,研究初始pH对 脱除率的影响,结果如下。
已知:
①不用盐酸调节NaClO溶液初始pH的原因是________________________。
②将pH=3.5时NaClO溶液脱除NO的离子方程式补充完整:
□NO+□______+□______ □ □ □______
③pH<5.5时,分析 脱除率随溶液初始pH升高而增大的可能原因:________________________。
(3)用 分别将脱除前后的 全部转化为 ,并用库仑仪测定 的量,可计算 脱除率。
库仑仪工作的原理和装置如下:
检测前,电解质溶液中的 保持定值时,电解池不工作。 进入电解池后与 反应,库
仑仪便立即自动进行电解到 又回到原定值,测定结束。通过测定电解消耗的电量可以求出
的物质的量。
学科网(北京)股份有限公司① 在电解池中被 还原为NO的离子方程式为__________________。
②将脱除前、后等体积的烟气分别用上述装置进行测定,电解时转移电子的物质的量分别为amol、bmol。
脱除率是______。
③测量结束后,电解池中还检测到少量 和 ,这将导致 测定结果______(填“偏高”或“偏
低”),需进行校正。
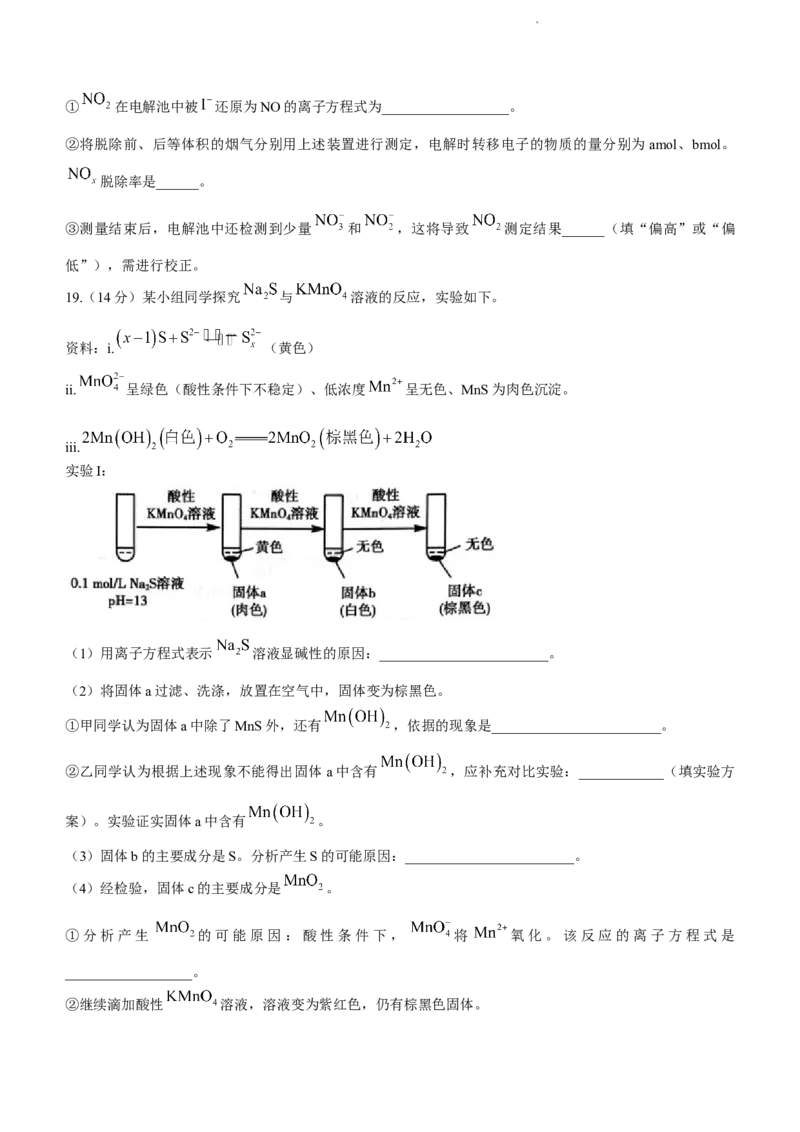
19.(14分)某小组同学探究 与 溶液的反应,实验如下。
资料:i. (黄色)
ii. 呈绿色(酸性条件下不稳定)、低浓度 呈无色、MnS为肉色沉淀。
iii.
实验I:
(1)用离子方程式表示 溶液显碱性的原因:________________________。
(2)将固体a过滤、洗涤,放置在空气中,固体变为棕黑色。
①甲同学认为固体a中除了MnS外,还有 ,依据的现象是________________________。
②乙同学认为根据上述现象不能得出固体a中含有 ,应补充对比实验:____________(填实验方
案)。实验证实固体a中含有 。
(3)固体b的主要成分是S。分析产生S的可能原因:________________________。
(4)经检验,固体c的主要成分是 。
①分析产生 的可能原因:酸性条件下, 将 氧化。该反应的离子方程式是
__________________。
②继续滴加酸性 溶液,溶液变为紫红色,仍有棕黑色固体。
学科网(北京)股份有限公司实验II:改用未经酸化的 溶液重复实验I,产生棕黑色固体时溶液呈绿色。
(5)分析实验I未见绿色的原因:取少量实验II的绿色溶液,滴加硫酸,溶液变为紫红色,产生棕黑色固体
该反应的离子方程式是__________________。
实验III:向未经酸化的 溶液中滴加少量 ,产生棕黑色沉淀并检测到 。
(6)检验 的实验方案:____________(填操作和现象)。
注:该实验条件下, 与 不反应。
(7)综合上述实验, 与 溶液反应的产物与____________等因素有关(答出两点即可)。
北京市朝阳区高三年级第二学期质量检测一
化学参考答案
2023.3
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C B A C A C A B D B D D C D
15.(9分)
(1)a
(2)基态Fe原子的价电子排布为 ,最后填入电子的能级为3d
(3)①配位键
② 中的甲基为推电子基团,使羧基中的氧氢键极性减弱; 中的羧基为吸电子基团,使
另一羧基中的氧氢键极性增强。
(4)①正四面体
②4x
16.(11分)
(1)研磨
(2)将 氧化为 ,便于转化为沉淀除去
(3)①O、N
②加入 ,使 逆向进行, 进入水层
(4)①
学科网(北京)股份有限公司或
②2.5
(5)b
17.(13分)
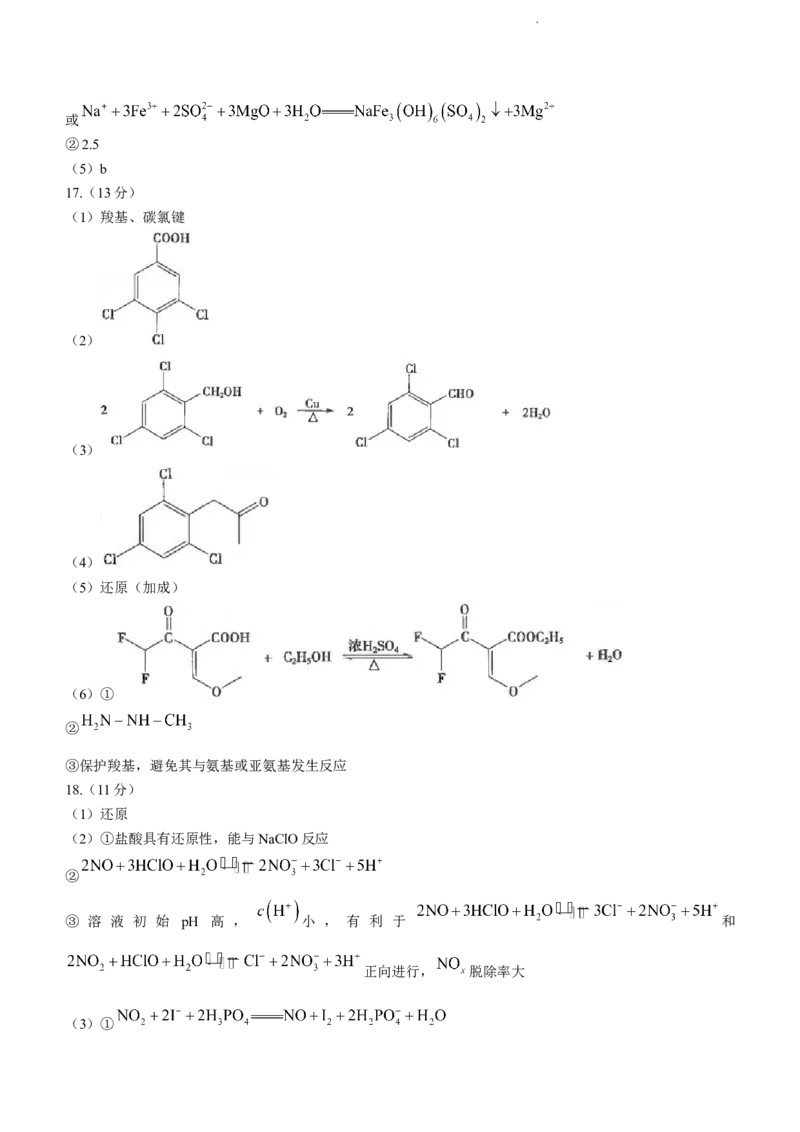
(1)羧基、碳氯键
(2)
(3)
(4)
(5)还原(加成)
(6)①
②
③保护羧基,避免其与氨基或亚氨基发生反应
18.(11分)
(1)还原
(2)①盐酸具有还原性,能与NaClO反应
②
③ 溶 液 初 始 pH 高 , 小 , 有 利 于 和
正向进行, 脱除率大
(3)①
学科网(北京)股份有限公司②
③偏低
19.(14分)
(1)
(2)①固体a放置在空气中变为棕黑色
②将MnS放置在空气中,观察相同时间内是否变为棕黑色
(3) 、 、MnS被酸性 溶液氧化生成S; 在酸性条件下转化生成S
(4)①
(5)
(6)取少量反应后的上层溶液,加入 (或 )溶液,产生白色沉淀,过滤,向沉淀中加过
量盐酸,沉淀不溶解
(7)反应物用量、添加顺序、溶液pH
学科网(北京)股份有限公司学科网(北京)股份有限公司