文档内容
第 51 讲 水溶液中四大平衡常数的综合应用
复习目标 1.掌握四大平衡常数[K(K )、K 、K 、K ]的简单计算。2.利用题目信息或图像,
a b h w sp
结合离子平衡,解决实际问题。
1.四大平衡常数的比较
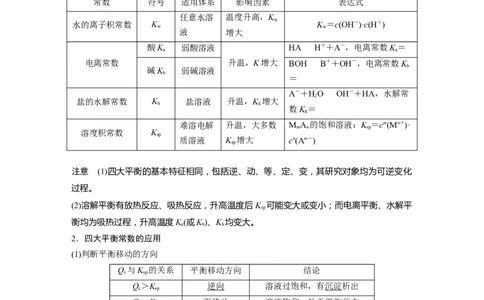
常数 符号 适用体系 影响因素 表达式
任意水溶 温度升高,K
w
水的离子积常数 K K =c(OH-)·c(H+)
w w
液 增大
酸K 弱酸溶液 HAH++A-,电离常数K=
a a
电离常数 升温,K增大 BOHB++OH-,电离常数K
b
碱K 弱碱溶液
b
=
A-+HOOH-+HA,水解常
2
盐的水解常数 K 盐溶液 升温,K 增大
h h
数K =
h
难溶电解 升温,大多数 M A 的饱和溶液:K =cm(Mn+)·
m n sp
溶度积常数 K
sp
质溶液 K 增大 cn(Am-)
sp
注意 (1)四大平衡的基本特征相同,包括逆、动、等、定、变,其研究对象均为可逆变化
过程。
(2)溶解平衡有放热反应、吸热反应,升高温度后 K 可能变大或变小;而电离平衡、水解平
sp
衡均为吸热过程,升高温度K(或K )、K 均变大。
a b h
2.四大平衡常数的应用
(1)判断平衡移动的方向
Q 与K 的关系 平衡移动方向 结论
c sp
Q>K 逆向 溶液过饱和,有沉淀析出
c sp
Q=K 不移动 溶液饱和,处于平衡状态
c sp
Q<K 正向 溶液未饱和,无沉淀析出
c sp
(2)常数间的关系
①强碱弱酸盐:K =;②强酸弱碱盐:K =。
h h
(3)判断离子浓度比值的大小变化。如将NH ·H O溶液加水稀释,c(OH-)减小,由于电离平
3 2
衡常数为,此值不变,故的值增大。(4)利用四大平衡常数进行有关计算。
类型一 四大平衡常数在平衡移动中的应用
1.室温下,通过下列实验探究NaHSO 溶液的性质。下列有关说法正确的是( )
3
实验 实验操作和现象
1 用pH计测定0.5 mol·L-1 NaHSO 溶液的pH,测得pH约为6.4
3
2 向0.05 mol·L-1 NaHSO 溶液中滴加过量0.1 mol·L-1 Ca(OH) 溶液,产生白色沉淀
3 2
向10 mL 0.05 mol·L-1 NaHSO 溶液中滴加10 mL 0.05 mol·L-1盐酸,反应结束,测
3
3
得pH约为3.2
向10 mL 0.05 mol·L-1 NaHSO 溶液中滴加10 mL 0.05 mol·L-1 NaOH溶液,反应
3
4
结束,测得pH约为9.3
A.实验1中:NaHSO 溶液中满足HSO的水解程度大于其电离程度
3
B.实验2反应静置后的上层清液中:c(Ca2+)·c(SO)<K (CaSO)
sp 3
C.实验3滴加过程中:c(Na+)+c(H+)=c(HSO)+2c(SO)+c(OH-)
D.实验4滴加过程中:c(HSO)+2c(SO)+c(OH-)逐渐减小
答案 D
解析 实验1中0.05mol·L-1 NaHSO 溶液的pH约为6.4,溶液呈酸性,故NaHSO 溶液中
3 3
HSO的水解程度小于其电离程度,A项错误;实验2上层清液中已经达到CaSO 溶解平衡,
3
故c(Ca2+)·c(SO)=K (CaSO),B项错误;实验3滴加过程中,根据电荷守恒可知,c(Na+)
sp 3
+c(H+)=c(HSO)+2c(SO)+c(OH-)+c(Cl-),C项错误;根据电荷守恒:c(Na+)+c(H+)=
c(HSO)+2c(SO)+c(OH-),c(Na+)+c(H+)逐渐减小,D项正确。
2.(2022·徐州模拟)室温下,通过下列实验探究0.010 0 mol·L-1 Na C O 溶液的性质。
2 2 4
实验1:实验测得0.010 0 mol·L-1 Na C O 溶液pH为8.6
2 2 4
实验2:向溶液中滴加等体积0.010 0 mol·L-1 HCl溶液,pH由8.6降为4.8
实验3:向溶液中加入等体积0.020 0 mol·L-1 CaCl 溶液,出现白色沉淀
2
实验4:向稀硫酸酸化的KMnO 溶液中滴加NaC O 溶液至溶液褪色
4 2 2 4
下列说法正确的是( )
A.0.010 0 mol·L-1 Na C O 溶液中满足:<2
2 2 4
B.实验2滴加盐酸过程中存在某一点满足:c(Na+)=c(HC O)+2c(C O)+c(Cl-)
2 2
C.实验3所得上层清液中c(C O)=2.5×10-7 mol·L-1[已知室温时K (CaC O)=2.5×
2 sp 2 4
10-9]
D.实验4发生反应的离子方程式为C O+4MnO+12H+===2CO↑+4Mn2++6HO
2 2 2
答案 B解析 0.010 0 mol·L-1 Na C O 溶液中满足物料守恒:c(Na+)=2[c(C O)+c(HC O)+
2 2 4 2 2
c(H C O)],则>2,A项错误;实验2中存在电荷守恒:c(Na+)+c(H+)=c(HC O)+2c(C O)
2 2 4 2 2
+c(Cl-)+c(OH-),在滴加盐酸过程中存在某一点满足c(H+)=
c(OH-),则c(Na+)=c(HC O)+2c(C O)+c(Cl-),B项正确;c(Ca2+)==0.005 mol·L-1,实
2 2
验3所得上层清液中c(C O)== mol·L-1=5×10-7 mol·L-1,C项错误;实验4发生反应的
2
离子方程式为5C O+2MnO+16H+===10CO↑+2Mn2++8HO,D项错误。
2 2 2
3.(2022·泰安模拟)已知25 ℃时,K (BaSO)=1.0×10-10,K (BaCO)=2.5×10-9,下列说
sp 4 sp 3
法不正确的是( )
A.向同浓度的NaSO 和NaCO 的混合溶液中滴加BaCl 溶液,BaSO 先析出
2 4 2 3 2 4
B.向BaCO 的悬浊液中加入少量的新制氯水,c(Ba2+)增大
3
C.BaSO 和BaCO 共存的悬浊液中,=
4 3
D.向BaSO 的悬浊液中加入NaCO 的浓溶液,BaSO 不可能转化为BaCO
4 2 3 4 3
答案 D
解析 由于K (BaSO)<K (BaCO),向同浓度的NaSO 和NaCO 的混合溶液中滴加BaCl
sp 4 sp 3 2 4 2 3 2
溶液,BaSO 先达到沉淀溶解平衡,故先析出BaSO ,A正确;向BaCO 溶液中加少量氯水,
4 4 3
CO+2H+===HO+CO↑,平衡BaCO (s)Ba2+(aq)+CO(aq)向右移动,c(Ba2+)增大,B
2 2 3
正确;BaSO 和BaCO 共存时,===,C正确;由于K (BaSO)和K (BaCO)相差不大,
4 3 sp 4 sp 3
所以向BaSO 的悬浊液中加入浓NaCO 溶液,BaSO 可以转化为BaCO ,D错误。
4 2 3 4 3
类型二 四大平衡常数在图像题中的应用
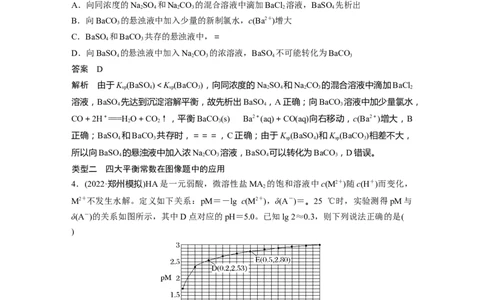
4.(2022·郑州模拟)HA是一元弱酸,微溶性盐MA 的饱和溶液中c(M2+)随c(H+)而变化,
2
M2+不发生水解。定义如下关系:pM=-lg c(M2+),δ(A-)=。25 ℃时,实验测得pM与
δ(A-)的关系如图所示,其中D点对应的pH=5.0。已知lg 2≈0.3,则下列说法正确的是(
)
A.D点存在2c(M2+)=3c(HA)
B.E点的pH≈5.6
C.25 ℃时,K (MA )的数量级为10-10
sp 2
D.25 ℃时,HA的电离常数K 为2.5×10-5
a
答案 B
解析 MA 的饱和溶液中加入H+时,H++A-HA,使MA 溶解平衡正向移动,在D点
2 2时,=0.2,所以c(HA)=4c(A-),pH=5.0,故c(H+)=10-5 mol·L-1,K==2.5×10-6,D
a
错误;D点时根据物料守恒2c(M2+)=c(A-)+c(HA),又c(A-)=c(HA),所以2c(M2+)=
c(HA),A错误;E点时,=0.5,因此c(HA)=c(A-),K==2.5×10-6,pH=-lg c(H+)=
a
-lg(2.5×10-6)≈5.6,B正确;当δ(A-)=1时,pM=3,即c(M2+)=10-3 mol·L-1,=1,
说明c(HA)=0,即溶液中的A-均为MA 电离的,根据MA (s)M2+(aq)+2A-(aq),c(A-)
2 2
=2c(M2+)=2×10-3 mol·L-1,K (MA )=c(M2+)·c2(A-)=4×10-9,数量级为10-9,C错误。
sp 2
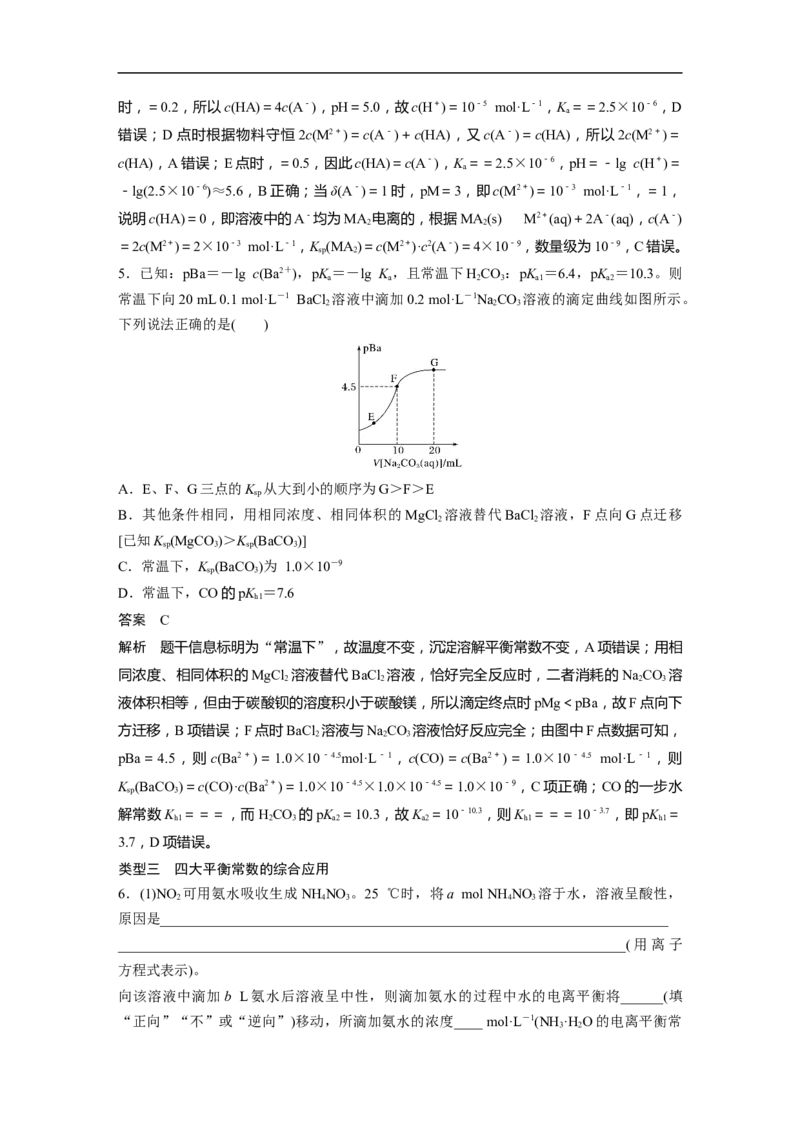
5.已知:pBa=-lg c(Ba2+),pK=-lg K,且常温下HCO :pK =6.4,pK =10.3。则
a a 2 3 a1 a2
常温下向20 mL 0.1 mol·L-1 BaCl 溶液中滴加0.2 mol·L-1NaCO 溶液的滴定曲线如图所示。
2 2 3
下列说法正确的是( )
A.E、F、G三点的K 从大到小的顺序为G>F>E
sp
B.其他条件相同,用相同浓度、相同体积的MgCl 溶液替代BaCl 溶液,F点向G点迁移
2 2
[已知K (MgCO )>K (BaCO)]
sp 3 sp 3
C.常温下,K (BaCO)为 1.0×10-9
sp 3
D.常温下,CO的pK =7.6
h1
答案 C
解析 题干信息标明为“常温下”,故温度不变,沉淀溶解平衡常数不变,A项错误;用相
同浓度、相同体积的MgCl 溶液替代BaCl 溶液,恰好完全反应时,二者消耗的NaCO 溶
2 2 2 3
液体积相等,但由于碳酸钡的溶度积小于碳酸镁,所以滴定终点时pMg<pBa,故F点向下
方迁移,B项错误;F点时BaCl 溶液与NaCO 溶液恰好反应完全;由图中F点数据可知,
2 2 3
pBa=4.5,则 c(Ba2+)=1.0×10-4.5mol·L-1,c(CO)=c(Ba2+)=1.0×10-4.5 mol·L-1,则
K (BaCO)=c(CO)·c(Ba2+)=1.0×10-4.5×1.0×10-4.5=1.0×10-9,C项正确;CO的一步水
sp 3
解常数K ===,而HCO 的pK =10.3,故K =10-10.3,则K ===10-3.7,即pK =
h1 2 3 a2 a2 h1 h1
3.7,D项错误。
类型三 四大平衡常数的综合应用
6.(1)NO 可用氨水吸收生成NH NO 。25 ℃时,将a mol NH NO 溶于水,溶液呈酸性,
2 4 3 4 3
原因是________________________________________________________________________
________________________________________________________________________(用离子
方程式表示)。
向该溶液中滴加b L氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将______(填
“正向”“不”或“逆向”)移动,所滴加氨水的浓度____ mol·L-1(NH ·H O的电离平衡常
3 2数取K =2×10-5)。
b
(2)向氨水中加入0.05 mol·L-1稀硫酸至溶液正好呈中性,则c(NH)________(填“>”“<”
或“=”)2c(SO),此时混合溶液中c(NH)=176c(NH ·H O),则NH ·H O的电离常数K 为
3 2 3 2 b
________________。
(3)向10 mL 0.10 mol·L-1的氨水中加入10 mL 0.02 mol·L-1的CaCl 溶液,通过计算说明是否
2
会生成沉淀[已知Ca(OH) 的K =5.5×10-6,氨水中c(OH-)≈ ]。
2 sp
答案 (1)NH+HONH ·H O+H+ 逆向 (2)= 1.76×10-5
2 3 2
(3)由(2)可知,NH ·H O的电离常数K =1.76×10-5,因氨水中c(OH-)≈,故混合后c2(OH
3 2 b
-)≈×0.10×1.76×10-5 mol2·L-2=8.8×10-7 mol2·L-2,混合后c(Ca2+)=
0.01 mol·L-1,则Q=c(Ca2+)·c2(OH-)=0.01×8.8×10-7=8.8×10-91.0×105
3 3 2
答案 D
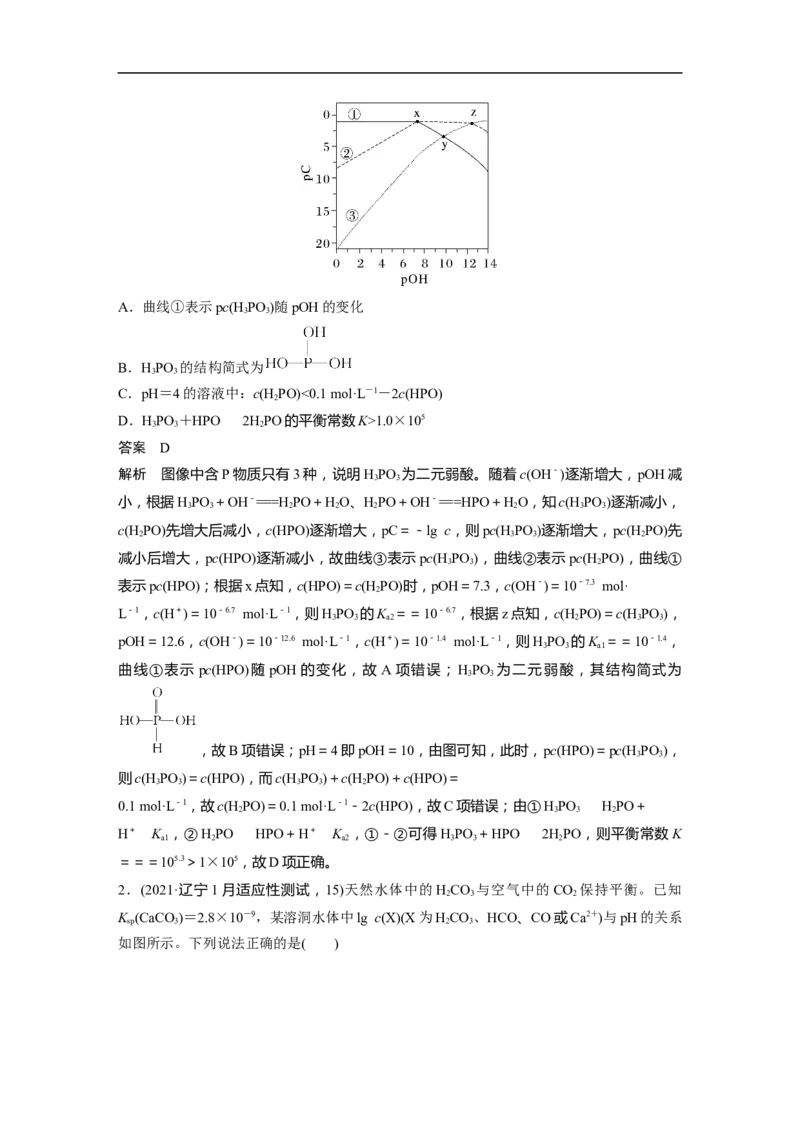
解析 图像中含P物质只有3种,说明HPO 为二元弱酸。随着c(OH-)逐渐增大,pOH减
3 3
小,根据HPO +OH-===HPO+HO、HPO+OH-===HPO+HO,知c(H PO )逐渐减小,
3 3 2 2 2 2 3 3
c(H PO)先增大后减小,c(HPO)逐渐增大,pC=-lg c,则pc(H PO )逐渐增大,pc(H PO)先
2 3 3 2
减小后增大,pc(HPO)逐渐减小,故曲线③表示pc(H PO ),曲线②表示pc(H PO),曲线①
3 3 2
表示pc(HPO);根据x点知,c(HPO)=c(H PO)时,pOH=7.3,c(OH-)=10-7.3 mol·
2
L-1,c(H+)=10-6.7 mol·L-1,则HPO 的K ==10-6.7,根据z点知,c(H PO)=c(H PO ),
3 3 a2 2 3 3
pOH=12.6,c(OH-)=10-12.6 mol·L-1,c(H+)=10-1.4 mol·L-1,则HPO 的K ==10-1.4,
3 3 a1
曲线①表示 pc(HPO)随 pOH 的变化,故 A 项错误;HPO 为二元弱酸,其结构简式为
3 3
,故B项错误;pH=4即pOH=10,由图可知,此时,pc(HPO)=pc(H PO ),
3 3
则c(H PO )=c(HPO),而c(H PO )+c(H PO)+c(HPO)=
3 3 3 3 2
0.1 mol·L-1,故c(H PO)=0.1 mol·L-1-2c(HPO),故C项错误;由①HPO HPO+
2 3 3 2
H+ K ,②HPOHPO+H+ K ,①-②可得HPO +HPO2HPO,则平衡常数K
a1 2 a2 3 3 2
===105.3>1×105,故D项正确。
2.(2021·辽宁1月适应性测试,15)天然水体中的HCO 与空气中的CO 保持平衡。已知
2 3 2
K (CaCO)=2.8×10-9,某溶洞水体中lg c(X)(X为HCO、HCO、CO或Ca2+)与pH的关系
sp 3 2 3
如图所示。下列说法正确的是( )A.曲线①代表CO
B.HCO 的一级电离常数为10-8.3
2 3
C.c(Ca2+)随pH升高而增大
D.pH=10.3时,c(Ca2+)=2.8×10-7.9 mol·L-1
答案 D
解析 根据图像可知,曲线①代表HCO,A错误;曲线①代表HCO,由点(6.3,-5)可知,
HCO 的一级电离常数K ==1.0×10-6.3,B错误;曲线③代表Ca2+,根据图像可知,c(Ca2
2 3 a1
+)随pH升高而减小,C错误;已知K (CaCO)=2.8×10-9,根据图像,pH=10.3时,
sp 3
c(HCO)=c(CO)=10-1.1 mol·L-1,则c(Ca2+)== mol·L-1=2.8×10-7.9 mol·L-1,D正确。
课时精练
1.(2022·杭州质检)已知:常温下,K(HA)=3.0×10-4,K (H B)=4.3×10-2,K (H B)=
a a1 2 a2 2
5.6×
10-6。下列说法正确的是( )
A.NaOH与等浓度等体积的HA、HB溶液完全反应,消耗NaOH的物质的量前者更大
2
B.pH=a的NaA溶液中,水电离出的c(OH-)为10-a mol·L-1
C.向NaA溶液中滴加少量HB溶液的离子方程式为A-+HB===HB-+HA
2 2
D.向NaB溶液中滴加等浓度等体积的盐酸,充分反应后溶液呈碱性
2
答案 C
解析 与等浓度等体积的HA、HB溶液即n(HA)=n(H B),由关系式HA~NaOH、HB~
2 2 2
2NaOH可知,完全反应消耗NaOH的物质的量后者更大,A项错误;由信息知,HA是弱酸,
NaA溶液因水解呈碱性,促进水的电离,则pH=a的NaA溶液中,c(H+)为10-a mol·L-1,
水电离出的c(OH-)为10a-14 mol·L-1,B项错误;向NaB溶液中滴加等浓度等体积的盐酸,
2
充分反应后得到NaCl和NaHB的混合溶液,NaHB水解常数K ====,则K (H B)>
h a2 2
K ,溶液呈酸性,D项错误。
h
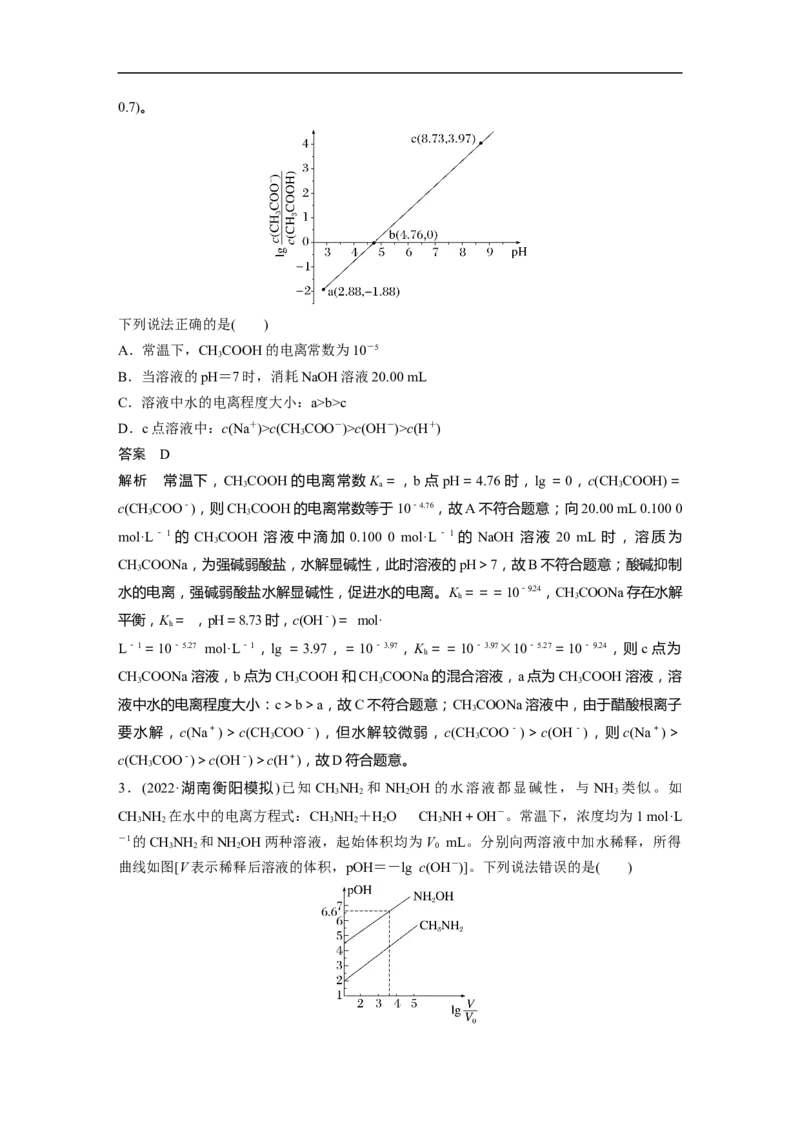
2.(2021·湖南1月适应性考试,14改编)常温下,向20.00 mL 0.100 0 mol·L-1的CHCOOH
3
溶液中滴加0.100 0 mol·L-1的NaOH溶液,溶液中,lg 随pH的变化关系如图所示(取lg 5=0.7)。
下列说法正确的是( )
A.常温下,CHCOOH的电离常数为10-5
3
B.当溶液的pH=7时,消耗NaOH溶液20.00 mL
C.溶液中水的电离程度大小:a>b>c
D.c点溶液中:c(Na+)>c(CHCOO-)>c(OH-)>c(H+)
3
答案 D
解析 常温下,CHCOOH的电离常数K =,b点pH=4.76时,lg =0,c(CHCOOH)=
3 a 3
c(CHCOO-),则CHCOOH的电离常数等于10-4.76,故A不符合题意;向20.00 mL 0.100 0
3 3
mol·L-1 的 CHCOOH 溶液中滴加 0.100 0 mol·L-1 的 NaOH 溶液 20 mL 时,溶质为
3
CHCOONa,为强碱弱酸盐,水解显碱性,此时溶液的pH>7,故B不符合题意;酸碱抑制
3
水的电离,强碱弱酸盐水解显碱性,促进水的电离。K ===10-9.24,CHCOONa存在水解
h 3
平衡,K = ,pH=8.73时,c(OH-)= mol·
h
L-1=10-5.27 mol·L-1,lg =3.97,=10-3.97,K ==10-3.97×10-5.27=10-9.24,则 c点为
h
CHCOONa溶液,b点为CHCOOH和CHCOONa的混合溶液,a点为CHCOOH溶液,溶
3 3 3 3
液中水的电离程度大小:c>b>a,故C不符合题意;CHCOONa溶液中,由于醋酸根离子
3
要水解,c(Na+)>c(CHCOO-),但水解较微弱,c(CHCOO-)>c(OH-),则 c(Na+)>
3 3
c(CHCOO-)>c(OH-)>c(H+),故D符合题意。
3
3.(2022·湖南衡阳模拟)已知 CHNH 和 NH OH 的水溶液都显碱性,与 NH 类似。如
3 2 2 3
CHNH 在水中的电离方程式:CHNH +HOCHNH+OH-。常温下,浓度均为1 mol·L
3 2 3 2 2 3
-1的CHNH 和NH OH两种溶液,起始体积均为V mL。分别向两溶液中加水稀释,所得
3 2 2 0
曲线如图[V表示稀释后溶液的体积,pOH=-lg c(OH-)]。下列说法错误的是( )A.常温下,CHNH的水解常数约为9.9×10-11
3
B.常温下,用盐酸滴定NH OH时,可选用甲基橙作指示剂
2
C.CHNH Cl溶液中存在关系:2c(H+)-2c(OH-)=c(CHNH )+c(Cl-)-c(CHNH)
3 3 3 2 3
D.等物质的量浓度的CHNH Cl和NH OHCl混合溶液中离子浓度的大小关系为c(NH OH
3 3 3 3
+)>c(CHNH)
3
答案 D
解析 起点时,pOH=2,c(OH-)=1×10-2 mol·L-1,所以K ==≈1.01×10-4,则CHNH
b 3
的水解常数K ==≈9.9×10-11,A项正确;NH OH与盐酸反应生成强酸弱碱盐,滴定终点
h 2
时溶液显酸性,可用甲基橙作指示剂,B项正确;CHNH Cl溶液中,根据物料守恒:c(Cl
3 3
-)=c(CHNH )+c(CHNH),根据电荷守恒:c(H+)+c(CHNH)=c(Cl-)+c(OH-),所以
3 2 3 3
c(CHNH)=c(Cl-)-c(CHNH ),
3 3 2
2c(H+)-2c(OH-)=2c(Cl-)-2c(CHNH)=2c(Cl-)-c(CHNH)-[c(Cl-)-c(CHNH )],得到
3 3 3 2
2c(H+)-2c(OH-)=c(CHNH )+c(Cl-)-c(CHNH),C项正确;由图可知,浓度均为
3 2 3
1 mol·L-1的 CHNH 和 NH OH 两种溶液,NH OH 的 pOH 大于 CHNH 的 pOH,说明
3 2 2 2 3 2
NH OH 的碱性较弱,则其对应的盐越易水解,所以等物质的量浓度的 CHNH Cl 和
2 3 3
NH OHCl混合溶液中离子浓度的大小关系为c(NH OH+)<c(CHNH),D项错误。
3 3 3
4.制备锌印刷电路板是用稀硝酸腐蚀锌板,产生的废液称为“烂板液”。“烂板液”中除
含有硝酸锌外,还含有自来水带入的 Cl-和 Fe3+。在实验室里用“烂板液”制取
ZnSO·7H O的过程如下:
4 2
(1)若稀硝酸腐蚀锌板时还原产物为NH NO ,氧化剂与还原剂的物质的量之比为________。
4 3
(2)若步骤①的pH>12,则Zn(OH) 溶解生成偏锌酸钠,写出Zn(OH) 被溶解的离子方程式
2 2
________________________________________________________________________
________________________________________________________________________。
(3)滤液D中除了含有OH-外,还含有的阴离子为__________(填离子符号)。
(4)若滤液E的pH=4,c(Zn2+)=2 mol·L-1,c(Fe3+)=2.6×10-9 mol·L-1,能求得的溶度积
是______(填字母)。
A.K [Zn(OH) ]
sp 2
B.K [Zn(OH) ]和K [Fe(OH) ]
sp 2 sp 3
C.K [Fe(OH) ]
sp 3
(5)已知:①Fe(OH) (s)Fe3+(aq)+3OH-(aq)
3ΔH=a kJ·mol-1
②HO(l)H+(aq)+OH-(aq)
2
ΔH=b kJ·mol-1
请写出Fe3+发生水解反应的热化学方程式:_________________________________
________________________________________________________________________。
(6)若Fe(OH) 的溶度积常数为K ,HO的离子积常数为K ,Fe3+发生水解反应的平衡常数
3 sp 2 w
K=______________(用含K 、K 的代数式表示)。
sp w
答案 (1)1∶4 (2)Zn(OH) +2OH-===ZnO+2HO (3)Cl-、NO (4)C (5)Fe3+(aq)+
2 2
3HO(l)Fe(OH) (s)+3H+(aq) ΔH=(3b-a) kJ·mol-1 (6)
2 3
解析 “烂板液”中除含硝酸锌外,还含有自来水带入的Cl-和Fe3+,加入氢氧化钠调节溶
液的pH=8,使铁离子、锌离子转化为Fe(OH) 、Zn(OH) 沉淀,过滤分离,滤液C中含有
3 2
NaNO 、NaCl等,沉淀上会附着NaNO 、NaCl等,用水洗涤除去,沉淀B用硫酸溶解、控
3 3
制一定pH,Fe(OH) 不溶解,过滤分离得到ZnSO 溶液,再经过蒸发浓缩、冷却结晶、过滤、
3 4
洗涤、干燥得ZnSO·7H O,以此解答该题。
4 2
(1)稀硝酸腐蚀锌板时还原产物为NH NO ,反应中N元素化合价由+5降低到-3,Zn元素
4 3
化合价由0升高到+2,则氧化剂与还原剂的物质的量之比是1∶4。(4)若滤液E的pH=4,
c(Zn2+)=2 mol·L-1,c(Fe3+)=2.6×10-9 mol·L-1,可知铁离子完全沉淀,因此可计算氢氧
化铁的溶度积。(5)根据盖斯定律,将②×3-①可得Fe3+发生水解反应的热化学方程式:
Fe3+(aq)+3HO(l)Fe(OH) (s)+3H+(aq) ΔH=(3b-a) kJ·mol-1。
2 3
(6)K===。
5.工业合成氨的反应为N(g)+3H(g)2NH (g)
2 2 3
ΔH=-92.4 kJ·mol-1
(1)一定温度下,向2 L密闭容器中充入2 mol N (g)和8 mol H (g),反应过程中氨气物质的量
2 2
与时间的关系如下表所示:
时间/min 0 5 10 15 20 25 30 35
NH /mol 0 0.5 0.9 0.12 0.15 0.15 0.15 0.15
3
①0~20 min内氢气的平均反应速率为____________________。
②升高温度,该平衡常数K将______(填“增大”“减小”或“不变”)。
(2)常温下,一水合氨电离常数K =1.8×10-5,向蒸馏水中通入一定量氨气配制浓度为0.5
b
mol·
L-1的氨水,氨水的pH约为___________________________________________。
(已知lg 2≈0.3,lg 3≈0.5)
(3)常温下,Ni(OH) 的溶度积为5.5×10-16。在0.01 mol·L-1的含Ni2+的溶液中滴加氨水到
2
pH=8时,溶液中c(Ni2+)=_______________________________________________。(4)常温下,0.1 mol·L-1氯化铵溶液 pH 约为 5,在该条件下,氯化铵水解常数 K 约为
h
__________________________________。
答案 (1)①5.625×10-3 mol·L-1·min-1 ②减小 (2)11.5 (3)5.5×10-4mol·L-1 (4)1.0×
10-9
解析 (1)①v(H )=v(NH )=×=5.625×10-3 mol·L-1·min-1。②合成氨反应的正反应是放热
2 3
反应,升高温度,平衡向逆反应方向移动,平衡常数减小。(2)设0.5 mol·L-1氨水电离出的
c(OH-)为 x mol·L-1,由 NH ·H ONH+OH-可知:K ===1.8×10-5,解得:
3 2 b
x≈3.0×10-3,则c(H+)== mol·L-1=×
10-11 mol·L-1,pH=-lg(×10-11)=11+lg 3≈11.5。(3)pH=8时,c(OH-)=1.0×10-6 mol·
L-1,由Ni(OH) (s)Ni2+(aq)+2OH-(aq)可知:c(Ni2+)= mol·L-1=5.5×
2
10-4 mol·L-1。(4)氯化铵溶液中存在水解平衡:NH+HONH ·H O+H+,0.1 mol·L-1氯
2 3 2
化铵溶液pH约为5,则c(H+)≈1.0×10-5mol·L-1,则氯化铵水解常数K =≈=1.0×10-9。
h
6.已知K、K、K 、K 分别表示化学平衡常数、弱酸的电离平衡常数、水的离子积常数、
a w sp
难溶电解质的溶度积常数。
(1)已知25 ℃时CHCOONH 溶液呈中性,则该温度下CHCOONH 溶液中水电离的H+浓
3 4 3 4
度为________,溶液中离子浓度大小关系为____________________。
(2)NH Cl溶液呈______(填“酸”“碱”或“中”)性,其原因是_________________
4
________________________________________________________________________(用离子
方程式表示)。
NaHCO 溶液呈______(填“酸”“碱”或“中”)性,其原因是_________________________
3
________________________________________________________________________(用离子
方程式表示)。
(3)常温下,Fe(OH) 和Mg(OH) 的K 分别为8.0×10-38、1.0×10-11,向浓度均为0.1 mol·L
3 2 sp
-1的FeCl 、MgCl 的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不沉淀,应该调节溶
3 2
液pH的范围是____________(已知lg 2≈0.3,离子浓度低于10-5mol·L-1时认为沉淀完全)。
答案 (1)1.0×10-7 mol·L-1 c(NH)=c(CHCOO-)>c(OH-)=c(H+) (2)酸 NH+
3
HONH ·H O+H+ 碱 HCO+HOHCO+OH- (3)3.3≤pH<9
2 3 2 2 2 3
解析 (1)CH COOH和NH ·H O的电离常数相等,则该温度下CHCOONH 溶液中铵根离子
3 3 2 3 4
和醋酸根离子水解程度相同,导致醋酸铵溶液呈中性,水电离出氢离子的浓度为 1.0×10-7
mol·L-1;水的电离程度很小,溶液中离子浓度大小顺序是 c(NH)=c(CHCOO-)>c(OH-)=
3
c(H+)。(3) mol·L-1≤c(OH-)< mol·L-1, mol·
L-1≤c(OH-)< mol·L-1,2×10-11 mol·L-1≤c(OH-)<1×10-5 mol·L-1, mol·
L-1<c(H+)≤ mol·L-1,则3.3≤pH<9。
7.(2022·贵阳检测)平衡常数是分析平衡问题的重要依据。回答下列问题:
(1)高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大,但在冰醋酸中却有一定的差异,以下是某温度下这四种酸在冰醋酸中的电离常数:
酸 HClO HSO HCl HNO
4 2 4 3
K 3.0×10-8 6.3×10-9 1.6×10-9 4.2×10-10
a
从表格中的数据判断以下说法不正确的是______(填字母)。
a.在冰醋酸中这四种酸都没有完全电离
b.在冰醋酸中高氯酸是这四种酸中酸性最强的酸
c.在冰醋酸中硫酸的电离方程式为HSO ===2H++SO
2 4
d.水对于这四种酸的强弱没有区分能力,但冰醋酸可以区分这四种酸的强弱
(2)已知:25 ℃时,HA的K=1.0×10-6,则1 mol·L-1的HA溶液的pH=______。
a
(3)在温度为t时,某研究人员测定NH ·H O的电离常数K 为2×10-5,NH的水解常数K 为
3 2 b h
1.5×10-8,则该温度下水的离子积常数 K 为________,请判断t____(填“>”“<”或
w
“=”)25 ℃。
(4)化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)CuS(s)+
Mn2+(aq)。
该反应的平衡常数K为__________(保留两位有效数字,CuS和MnS的K 分别为6.0×10-
sp
36、2.0×10-10)。
(5)25 ℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合所得溶液中c(NH)=
c(Cl-),则溶液显______(填“酸”“碱”或“中”)性;用含a的代数式表示NH ·H O的电
3 2
离常数K =____________。
b
答案 (1)c (2)3 (3)3×10-13 > (4)3.3×1025 (5)中
解析 (1)根据电离平衡常数知,在冰醋酸中这几种酸都不完全电离,a正确;在冰醋酸中,
高氯酸的电离平衡常数最大,所以高氯酸的酸性最强,b正确;在冰醋酸中硫酸存在电离平
衡,所以其电离方程式为HSO H++HSO,c错误;这四种酸在水中都完全电离,在冰
2 4
醋酸中电离程度不同,所以水对于这四种酸的强弱没有区分能力,但冰醋酸可以区分这四种
酸的强弱,d正确。(2)由c2(H+)≈K·c(HA)=1.0×10-6×1,所以c(H+)=10-3 mol·L-1,pH
a
=3。(3)K =K ·K =2×10-5×1.5×10-8=3×10-13;t温度时水的离子积常数大于25 ℃时
w b h
水的离子积常数,水的电离吸热,温度越高离子积常数越大,因此温度应高于 25 ℃。(4)平
衡常数K====≈3.3×1025。(5)根据电荷守恒有c(NH)+c(H+)=c(Cl-)+c(OH-),由于
c(NH)=c(Cl-),故c(H+)=c(OH-),溶液呈中性,故溶液中c(OH-)=10-7 mol·L-1,溶液中
c(NH)=c(Cl-)=×0.01 mol·L-1=0.005 mol·L-1,故混合后溶液中c(NH ·H O)=×a mol·L-1
3 2
-0.005 mol·L-1=(0.5a-0.005) mol·L-1,NH ·H O的电离常数K ==。
3 2 b