文档内容
热点强化 13 元素推断与元素性质
元素推断与元素性质主要以元素周期表为工具考查“位—构—性”三者的关系,命题既可对
原子结构、元素周期表、元素周期律进行单独考查,也可结合元素及其化合物的性质进行综
合考查。原子结构知识主要考查核素、同位素、核外电子排布(电子排布式、轨道表示式和
未成对电子数)、原子轨道的能量和形状等;元素周期律主要考查金属性、非金属性、气态
氢化物稳定性和最高价含氧酸的酸性、原(离)子半径、电离能、电负性的比较等。元素周期
表一般给出片段,结合原子结构和元素周期律进行考查。在复习过程中,应针对以下几点进
行:
(1)原子结构——构造原理(1~36号元素核外电子排布)、原子内粒子数量之间的关系;
(2)元素性质——原子半径、主要化合价、金属性、非金属性、第一电离能、电负性的周期
性变化规律;
(3)“位—构—性”——用好元素周期表这一工具,实现分析与推理能力、宏观辨识与微观
探析的学科核心素养的提升。
题组一 文字叙述型
1.(2022·江苏模拟)前四周期主族元素X、Y、Z、W的原子序数依次增大。X与Z同主族,
且基态X原子中p能级和s能级上的电子数相同。Y、Z同周期,Y位于第ⅢA族,W最外
层有2个电子。下列说法正确的是( )
A.原子半径:r(X)Z>W
B.简单离子半径:r(W)>r(R)
C.第一电离能:I(W)>I(Z)>I(Y)
1 1 1
D.X、Z、W形成的化合物一定不含离子键
答案 B
解析 X、Y、Z、W、R为原子序数依次增大的短周期主族元素,X、Z原子中分别有1个、
7个运动状态完全不同的电子,则X、Z原子序数分别为1、7,则X是H元素、Z是N元素;
Y原子中各能级电子数相等,则其电子排布为1s22s22p2,Y为C元素;W的基态原子的最外
层电子数是内层电子数的3倍,W只能含有2个电子层,最外层含有6个电子,W为O元
素;R在同周期中原子半径最大,则R是Na元素。元素非金属性越强,其气态氢化物越稳
定,非金属性:CO>C,C错误;X、Z、W形成的化合物NH NO 含离子键,D错误。
4 3
3.已知元素X、Y、Z、W为原子序数依次增大的短周期主族元素,其中 X与W同主族,
且W的最外层电子数是其内层电子总数的一半,X和Y的原子序数之和等于W的原子序数,
用He粒子轰击Z核会产生W核和中子(即n),可表示为He+Z→W+n。下列说法正确的是
( )
A.Z与W互为同位素
B.第一电离能:X<W
C.Y和W形成的化合物不止一种
D.W的最高价氧化物对应的水化物是强酸
答案 C
解析 由题给信息分析可知,X为N、Y为O、Z为Al、W为P。Z、W的质子数不同,不
互为同位素,故A错误;同主族元素从上到下第一电离能逐渐减小,则第一电离能:X>
W,故B错误;Y和W形成的化合物有三氧化二磷、五氧化二磷等,故 C正确;W的最高
价氧化物对应的水化物为磷酸,不属于强酸,故D错误。
题组二 结构推断型
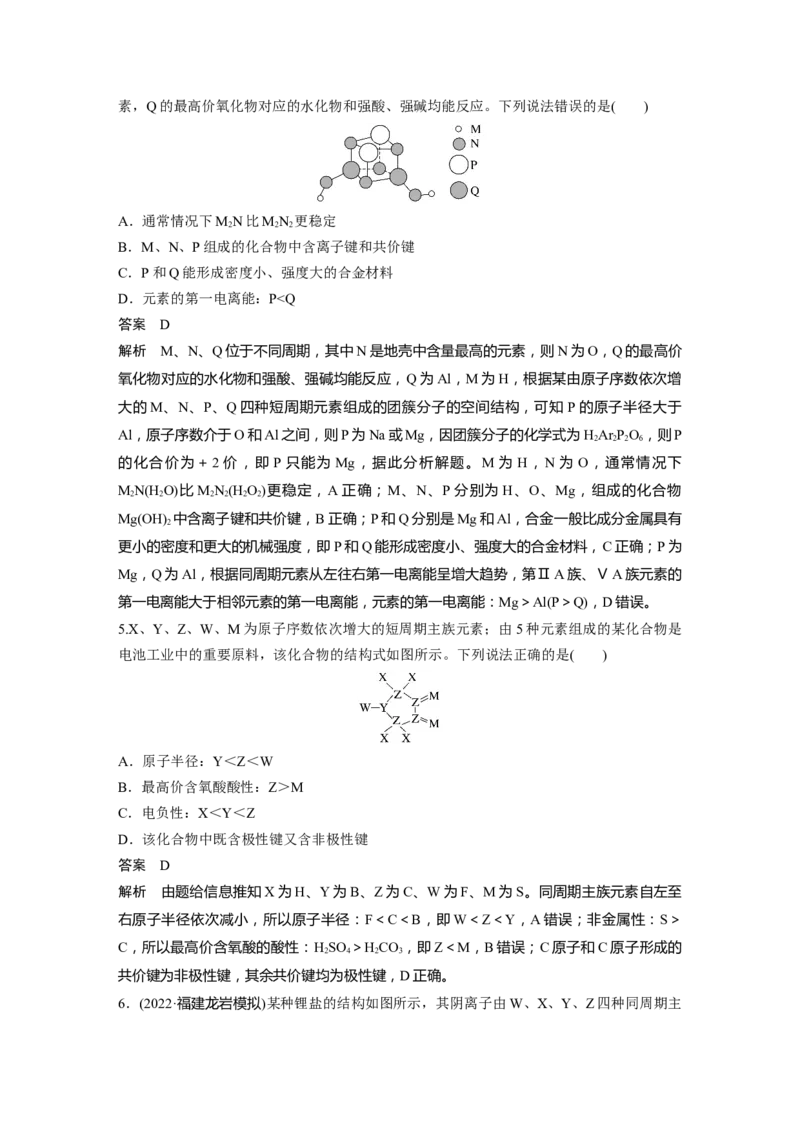
4.(2022·福建省惠安第一中学模拟)某团簇分子由原子序数依次增大的M、N、P、Q四种短
周期元素组成,其空间结构如图,M、N、Q位于不同周期,其中N是地壳中含量最高的元素,Q的最高价氧化物对应的水化物和强酸、强碱均能反应。下列说法错误的是( )
A.通常情况下MN比MN 更稳定
2 2 2
B.M、N、P组成的化合物中含离子键和共价键
C.P和Q能形成密度小、强度大的合金材料
D.元素的第一电离能:P
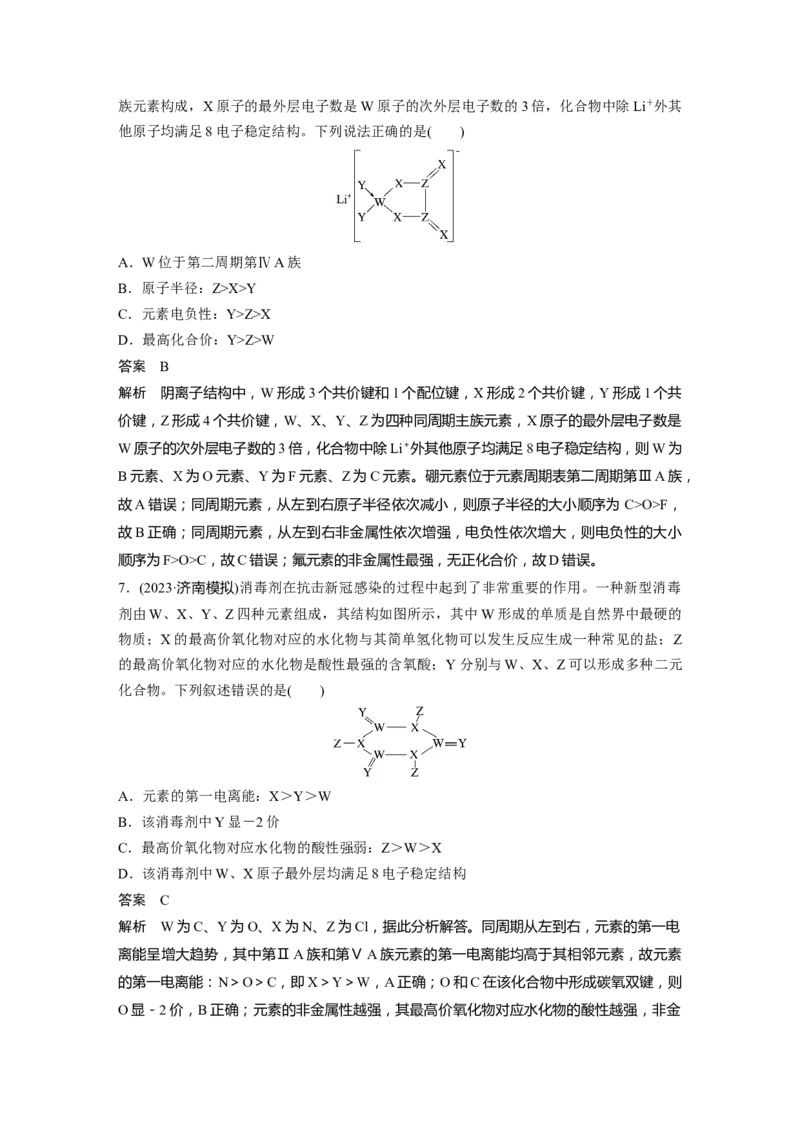
X>Y C.元素电负性:Y>Z>X D.最高化合价:Y>Z>W 答案 B 解析 阴离子结构中,W形成3个共价键和1个配位键,X形成2个共价键,Y形成1个共 价键,Z形成4个共价键,W、X、Y、Z为四种同周期主族元素,X原子的最外层电子数是 W原子的次外层电子数的3倍,化合物中除Li+外其他原子均满足8电子稳定结构,则W为 B元素、X为O元素、Y为F元素、Z为C元素。硼元素位于元素周期表第二周期第ⅢA族, 故A错误;同周期元素,从左到右原子半径依次减小,则原子半径的大小顺序为 C>O>F, 故B正确;同周期元素,从左到右非金属性依次增强,电负性依次增大,则电负性的大小 顺序为F>O>C,故C错误;氟元素的非金属性最强,无正化合价,故D错误。 7.(2023·济南模拟)消毒剂在抗击新冠感染的过程中起到了非常重要的作用。一种新型消毒 剂由W、X、Y、Z四种元素组成,其结构如图所示,其中W形成的单质是自然界中最硬的 物质;X的最高价氧化物对应的水化物与其简单氢化物可以发生反应生成一种常见的盐;Z 的最高价氧化物对应的水化物是酸性最强的含氧酸;Y分别与W、X、Z可以形成多种二元 化合物。下列叙述错误的是( ) A.元素的第一电离能:X>Y>W B.该消毒剂中Y显-2价 C.最高价氧化物对应水化物的酸性强弱:Z>W>X D.该消毒剂中W、X原子最外层均满足8电子稳定结构 答案 C 解析 W为C、Y为O、X为N、Z为Cl,据此分析解答。同周期从左到右,元素的第一电 离能呈增大趋势,其中第ⅡA族和第ⅤA族元素的第一电离能均高于其相邻元素,故元素 的第一电离能:N>O>C,即X>Y>W,A正确;O和C在该化合物中形成碳氧双键,则 O显-2价,B正确;元素的非金属性越强,其最高价氧化物对应水化物的酸性越强,非金属性:Cl>N>C,则酸性:HClO >HNO >HCO ,即Z>X>W,C错误;由结构图可知, 4 3 2 3 C周围有1个双键和2个单键,N周围有3个单键,且N含有孤电子对,故C、N最外层均 满足8电子稳定结构,D正确。 分子(离子)结构与元素推断的关键 ——成键情况与化合价信息 (1)化学键信息:如能形成4个共价键的元素为C、Si等,能形成2个共价键的元素为O、S 等,能形成1个共价键的元素为H或卤族元素。 (2)根据形成的简单阴、阳离子可确定原子的最外层电子数,如X2+和Y2-,即X、Y原子最 外层电子数分别为2和6。 (3)化合价信息:化合物中各元素化合价代数和为0,结合某些常见元素的化合价或化学键等, 可确定未知元素的化合价,间接确定最外层电子数目。