文档内容
章末综合检测(五)
(时间:45分钟 分值:100分)
一、选择题(本题包括12小题,每小题5分,共60分)
1.(2019·江西南康中学、于都中学联考)下列化学用语表示正确的是( )
A.原子序数为35、中子数为45的溴原子:Br
B.Mg2+的结构示意图:
C.CCl 的比例模型:
4
D.CHF 的电
2 2
解析:选B。溴为第四周期ⅦA族元素,原子序数为35,中子数为45,则质量数为80,故
为Br, A错误。Mg原子的核外电子排布各层电子数为2、8、2,失去最外层两个电子形成镁离
子,故Mg2+的结构示意图为 , B正确。CCl 的比例模型中Cl原子的半径比C原子的
4
大,但是题图中的Cl原子的半径比C原子的小,C错误。F原子周围应该为4对电子对,8个电
子,而题图中的F只有2个电子, D错误。
2.(2019·石家庄第二中学高三联考)2017年1月26日,美国《科学》杂志刊发论文称发现
了一种新材料——金属氢,证实了一百多年前提出的存在金属氢的假说。下列事实不能说明
氢可能具有金属性的是( )
A.可以把H写入金属活动性顺序表
B.H与Na、K等碱金属元素同属于第ⅠA族
C.H存在H-
D.H与非金属反应,产物中H通常显正价
解析:选C。A.可以把H写入金属活动性顺序表,说明氢可能具有金属性,故A正确;B.H
与Na、K等碱金属元素同属于第ⅠA族,说明氢有与钠相似的化学性质,可能具有金属性,故
B正确;C.金属只能失电子,只有正价,现H存在H-,不能说明氢具有金属性,故C错误;D.H
与非金属反应,产物中H通常显正价,说明H有失电子倾向,可能具有金属性,故D正确。
3.(2019·汉中模拟)北京大学和中国科学院的化学工作者已成功研制出碱金属与C 形成
60
的球碳盐KC ,实验测知该物质属于离子化合物,具有良好的超导性。下列有关分析正确的
3 60
是( )
A.KC 中只有离子键
3 60
B.KC 中不含共价键
3 60
C.该晶体在熔融状态下能导电
D.C 与12C互为同素异形体
60
解析:选C。离子化合物在熔融状态下能导电,C项正确。KC 内部还存在非极性键,A项
3 60
和B项均错误;12C为核素,同素异形体的研究对象是单质,D项错误。
4.根据原子结构及元素周期律的知识,下列推断正确的是( )A.同主族元素的含氧酸的酸性随核电荷数的增加而减弱
B.核外电子排布相同的微粒化学性质也相同
C.Cl-、S2-、Ca2+、K+半径逐渐减小
D.Cl与Cl得电子能力相同
解析:选D。同主族元素的最高价含氧酸的酸性随核电荷数的增加而减弱,A错误;核外
电子排布相同的微粒,化学性质不一定相同,如K+与Cl-,B错误;当核外电子排布相同时,核
电荷数越大,微粒半径越小,半径大小顺序应为S2->Cl->K+>Ca2+,C错误;同种元素的原子
得电子能力相同,D正确。
5.(2019·商丘高三模拟)在短周期元素中,X元素与Y、Z、W三元素相邻。X、Y的原子序
数之和等于Z的原子序数,这四种元素原子的最外层电子数之和为20。下列判断一定正确的
是( )
A.单质熔点:Z>W
B.离子半径:X<Y
C.X和Z可存在于同一离子化合物中
D.氧化物对应水化物的酸性X>Z
解析:选C。由短周期同主族相邻元素核电荷数相差8,可推知Y为氧元素,结合题中条
件又可知X、Z、W依次为氮、磷、碳。金刚石的熔点高于磷单质,A项错误;X、Y在同周期,且
Y的核电荷数较大,离子半径:Y<X,B项错误;X和Z可存在于离子化合物(NH )PO 中,C
4 3 4
项正确;最高价氧化物对应水化物的酸性X>Z,D项错误。
6.有a、b、c、d四种短周期主族元素,它们在周期表中的位置如图所示,已知四种元素中
只有b为金属元素,则下列有关说法中正确的是( )
a
b c d
A.离子半径:b>c>d>a
B.bn+与dm-在水溶液中可形成化合物b d
m n
C.简单气态氢化物的稳定性:aS2->N3->Al3+,A项错误;Al3
+、S2-相互促进水解,故在水溶液中不能形成Al S,B项错误;非金属性N>P,则简单气态氢
2 3
化物的稳定性NH >PH,C项错误;Al(OH) 与HSO 可发生反应,D项正确。
3 3 3 2 4
7.(2019·开封模拟)甲、乙、丙、丁4种物质分别含2种或3种元素,它们的分子中均含18
个电子,甲是气态氢化物,在水中分步电离出两种阴离子,下列推断错误的是( )
A.若某钠盐溶液含甲电离出的阴离子,则该溶液既可能与酸反应又可能与碱反应
B.若乙与氧气的摩尔质量相同,则乙只能由2种元素组成
C.若丙中含有第二周期ⅣA族的元素,则丙可能是甲烷的同系物
D.若丁中各元素质量比跟甲中各元素质量比相同,则丁中一定含有-1价的元素
解析:选B。甲是含18个电子的气态氢化物,且为二元弱酸,不难得出甲为HS,若其钠盐
2
溶液为NaS溶液,溶液呈碱性,不能与碱反应,若为NaHS溶液,其既能与盐酸等反应生成
2
HS,也能与NaOH反应生成NaS,故A正确;氧气的摩尔质量为32 g·mol-1,若乙的摩尔质量
2 2
也为32 g·mol-1,且含有18个电子,CHOH符合,由3种元素组成,故B错误;丙中含有第二
3
周期ⅣA族的元素,即丙中含C,C H 符合,C H 是CH 的同系物,故C正确;HS中各元素的
2 6 2 6 4 2
质量比为1∶16,HO 中各元素的质量比也为1∶16,则丁为HO,HO 中氧元素的价态为-
2 2 2 2 2 2
1价,故D正确。
8.(2019·威海模拟)下列根据元素周期表和元素周期律得出的推断中正确的是( )A.金属元素原子最外层电子数越少,该金属失电子能力越强
B.若存在简单阴离子R2-,则R一定位于ⅥA族
C.A2+、B+、C3-三种离子具有相同的电子层结构,则原子序数c>a>b
a b c
D.铅位于周期表中金属和非金属的交界处,可做半导体材料
解析:选B。A选项,由Na与Ca可知错误;C选项,原子序数a>b>c,错误;D选项,铅属
于金属,不位于金属和非金属的交界处,不可做半导体材料,错误。
9.(2019·唐山高三第二次模拟)短周期元素X、Y、Z、W的原子序
数依次增大,X和W为同主族元素,Z的简单离子半径在第三周期元
素中最小,由这四种元素的一种或几种元素组成的物质存在如图转化关系。其中P是元素X
的氢化物,其稀溶液可用于伤口消毒,Q为一种二元化合物,常温下0.01 mol·L-1 M(化合物)
溶液的pH=12。下列说法错误的是( )
A.X和Y、W均至少能形成两种化合物
B.离子半径:W>Y>Z>X
C.Q和M中都存在离子键
D.气态氢化物的稳定性:X>W
解析:选B。Z的简单离子半径在第三周期元素中最小,则Z为Al;P是元素X的氢化物,
其稀溶液可用于伤口消毒,则P为HO,X为O;由常温下0.01 mol·L-1 M溶液的pH=12可
2 2
知,M为一元强碱,且组成元素都为短周期元素,则M为NaOH,Na的原子序数介于O与Al
之间,故Y为Na;Q为一种二元化合物,X与W同主族,再结合转化关系可知,Q为NaS,W
2
为S。A项,O和Na、S分别可形成化合物NaO、NaO,SO 、SO ,A正确;B项,离子半径为S2
2 2 2 2 3
->O2->Na+>Al3+,即为W>X>Y>Z,B错误;C项,Q为NaS,M为NaOH,它们都是离子化合
2
物,都存在离子键,C正确;D项,HO的稳定性强于HS,D正确。
2 2
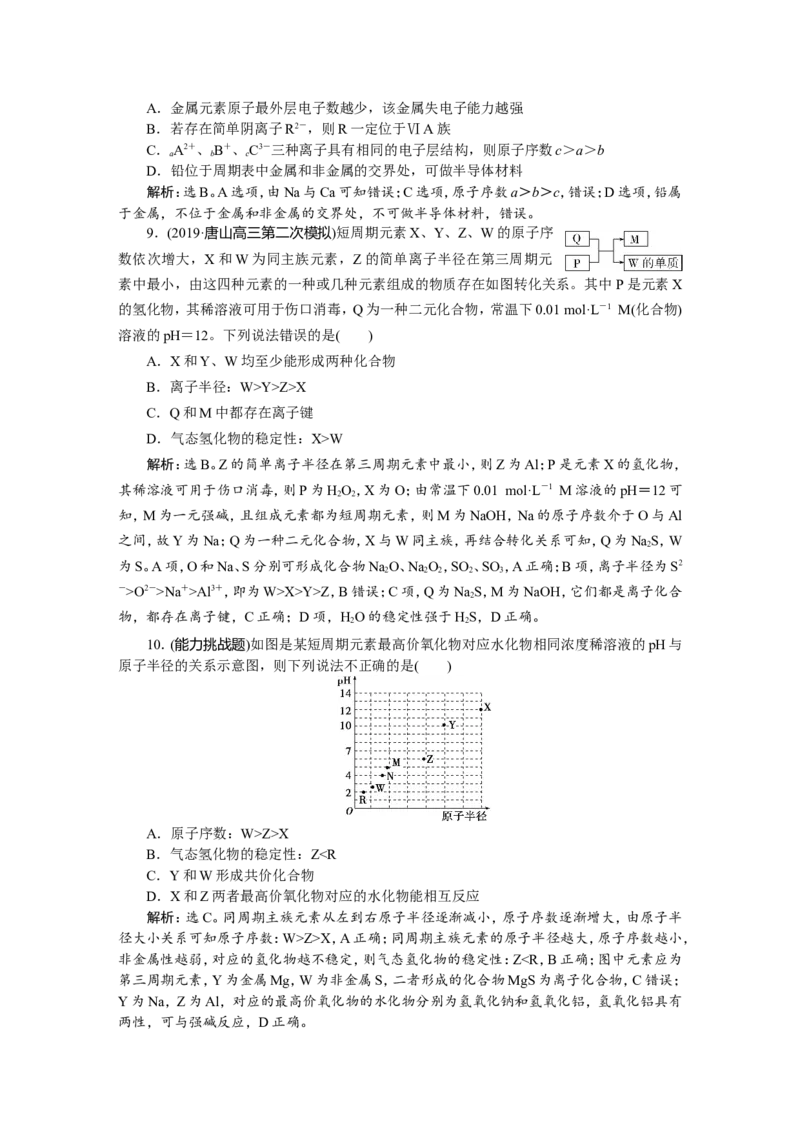
10.(能力挑战题)如图是某短周期元素最高价氧化物对应水化物相同浓度稀溶液的pH与
原子半径的关系示意图,则下列说法不正确的是( )
A.原子序数:W>Z>X
B.气态氢化物的稳定性:ZZ>X,A正确;同周期主族元素的原子半径越大,原子序数越小,
非金属性越弱,对应的氢化物越不稳定,则气态氢化物的稳定性:Zr(M2-)
B.气态氢化物的稳定性:M>X
C.X、Y形成的化合物中只有离子键
D.X、Y、N所形成化合物的水溶液可能显中性或碱性
解析:选D。X、Y、M、N是元素周期表中短周期主族元素,且原子序数依次增大,已知X
的最外层电子数是次外层电子数的3倍,则X是O元素;X、M同主族,且M的原子序数大于
X,则M是S元素;N是原子序数大于M的短周期主族元素,则N是Cl元素;Y的原子在短周
期主族元素中原子半径最大,则Y是Na元素。电子层结构相同的离子,离子半径随原子序数
增大而减小,所以离子半径:r(Cl-)C>B
B.A与B两种元素共同形成的10电子粒子有3种
C.D元素在周期表中的位置是第二周期ⅡA族
D.丁物质均由非金属元素构成,只含共价键
解析:选B。A、B、C、D、E是原子序数依次增大的五种短周期元素。A元素可以与B、C、E
元素分别形成甲、乙、丙三种物质且甲、乙均为10电子化合物,丙为18电子化合物,则A为H
元素,10电子化合物可能为CH、NH 、HO、HF;已知甲+E―→丙+B ,甲+丙―→丁,则E
4 3 2 2 2
的单质为双原子分子,故E为Cl元素,则B为氮元素,B、C相邻,则C为氧元素,故甲为
NH 、乙为HO、丙为HCl、丁为NH Cl;D元素的最外层电子数与核外电子层数相等,原子序
3 2 4
数大于氧元素,则D元素处于第三周期,最外层电子数为3,故D为Al元素。N3-、O2-、Al3+电
子层结构相同,核电荷数越大离子半径越小,故离子半径:N3->O2->Al3+,A错误;H与N两
种元素共同形成的10电子粒子有NH、NH 、NH3种,B正确;Al元素在周期表中的位置为第
3
三周期ⅢA族,C错误;丁为NH Cl,含有离子键、共价键,故D错误。
4
二、非选择题(本题包括3小题,共40分)
13.(12分)现有部分短周期主族元素的性质或原子结构如下表所示:
元素编号 元素性质或原子结构
X 周期序数=主族序数=原子序数
Y 原子最外层电子数为a,次外层电子数为b
Z 原子L层电子数为a+b,M层电子数为a-b
M 单质在自然界中的硬度最大
N 位于第三周期,最外层电子数是电子层数的2倍
(1)写出X、Y、Z、N四种元素的名称:
X________,Y________,Z________,N________。
(2)由X、Y、Z、M、N五种元素两两组成的分子中,许多分子含有的电子数相等,写出符合
下列要求的分子式:①含10e-且呈正四面体结构的分子________;②含14e-的双原子分子________;
③含16e-且能使溴水褪色的分子________;
④含18e-且常温下呈液态的分子________。
解析:(1)根据周期序数=主族序数=原子序数,推知X为氢元素;根据Z元素原子L层
电子数为a+b,M层电子数为a-b,Y元素最外层电子数为a,次外层电子数为b,得出b=2,
a=6,则Y、Z分别为氧元素、硅元素;金刚石在自然界中的硬度最大,故M为碳元素;N位于
第三周期,最外层电子数是电子层数的2倍,则N为硫元素。(2)①CH 为10e-的正四面体分子;
4
②CO为14e-的双原子分子;③乙烯含16e-,能和溴水发生加成反应,使溴水褪色;④HO 含
2 2
18e-,常温下呈液态。
答案:(1)氢 氧 硅 硫
(2)①CH ②CO ③C H ④HO
4 2 4 2 2
14.(14分)A、B、D、E、F、G为短周期元素,且原子序数依次递增。A、F同主族,E、G同主
族。A与其他非金属元素化合时易形成共价键,F与其他非金属元素化合时易形成离子键,且
F+与E2-核外电子排布相同。由以上元素组成的物质BE和D 具有相同的电子数。
2
请回答下列问题:
(1)F位于第________周期________族。
(2)G的离子结构示意图为_____________________________________________。
(3)用电子式表示D 的形成过程:_______________________________________。
2
(4)由A、E、F三种元素形成的化合物的化学式为________,属于________化合物。
(5)B的最高价是________。由A、B组成的化合物中,含A的质量分数最高的物质的化学
式是________;与D 相对分子质量相等的物质的化学式是________,有________对共用电子
2
对。
解析:A、F同主族,且A与其他非金属元素化合时易形成共价键,但F与其他非金属元素
化合时易形成离子键,则为第ⅠA族元素,且A为H;F+与E2-核外电子排布相同,则F为
Na,E为O;E、G同主族,且为短周期元素,则G为S;BE和D 具有相同的电子数,则B为C,
2
D为N。
(1)Na位于第三周期ⅠA族。
(2)硫原子得到2个电子形成离子,最外层有8个电子。
(3)用电子式表示物质的形成过程时,箭头前为原子的电子式,箭头后为单质或化合物的
电子式。
(4)NaOH属于离子化合物。
(5)C的最高化合价为+4;CH 是碳氢化合物中含氢质量分数最高的物质;N 的相对分子
4 2
质量为28,与其相对分子质量相等的碳氢化合物为C H,其有6对共用电子对。
2 4
(4)NaOH 离子
(5)+4 CH C H 6
4 2 4
15.(14分)(2019·晋中模拟)X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大。X是
原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的
元素,R与X同主族,Y、R、Q最外层电子数之和为8,M的单质为黄绿色有害气体。请回答下列问题:
(1)R在元素周期表中的位置为________。
(2)Z、Q、M简单离子半径由大到小的顺序为________(写离子符号)。
(3)X 、 Y 、 Z 三 种 元 素 形 成 盐 类 化 合 物 的 水 溶 液 呈 酸 性 的 原 因 :
________________________________________________________________________
( 用 离 子 方 程 式 表 示 ) , 溶 液 中 所 含 离 子 浓 度 由 大 到 小 的 顺 序 为
________________________________________________________________________。
(4)YX M的电子式为____________;QY 与水可剧烈反应,产生沉淀与气体,反应的化学
4 3 2
方程式为______________________________________________________________
________________________________________________________________________。
(5)X、Z两元素形成的原子个数比为1∶1的化合物中含有的化学键类型为________。
(6)M 的 单 质 与 R 的 最 高 价 氧 化 物 对 应 的 水 化 物 反 应 的 离 子 方 程 式 为
________________________________________________________________________。
解析:X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大。X是原子半径最小的元
素,则X为H;Y的气态氢化物能使湿润的红色石蕊试纸变蓝,则Y为N;Z为地壳中含量最
多的元素,则Z为O;R与X同主族,则R为Na;Y、R、Q最外层电子数之和为8,则Q为Mg;
M的单质为黄绿色有害气体,则M为Cl。
(1)钠元素在周期表中的位置为第三周期ⅠA族。
(2)Cl-有三个电子层,半径最大,O2-与Mg2+有两个电子层,电子层结构相同,核电荷数
越大,半径越小,所以简单离子半径由大到小的顺序为Cl->O2->Mg2+。
(3)H、N、O三种元素形成的盐类化合物为 NH NO ,其水溶液呈酸性,原因是NH+
4 3
HONH ·HO+H+;溶液中所含离子浓度由大到小的顺序为c(NO)>c(NH)>c(H+)>c(OH
2 3 2
-)。
(4)H、N、Cl形成的化合物为NH Cl,其电子式为 ;MgN
4 3 2
易水解生成Mg(OH) 和NH ,反应的化学方程式为MgN+6HO===3Mg(OH) +2NH ↑。
2 3 3 2 2 2 3
(5)过氧化氢中含有共价键。
(6)Cl 与NaOH反应的离子方程式为Cl+2OH-===ClO-+Cl-+HO。
2 2 2
答案:(1)第三周期ⅠA族
(2)Cl->O2->Mg2+
(3)NH+HONH ·H O+H+
2 3 2
c(NO)>c(NH)>c(H+)>c(OH-)
(4)
MgN+6HO===3Mg(OH) +2NH ↑
3 2 2 2 3
(5)共价键
(6)Cl +2OH-===ClO-+Cl-+HO
2 2