文档内容
专题 11 镁及其重要化合物
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 镁及其化合物的结构、性质及应用
考点二 镁及其化合物制备的工艺流程
考点三 镁及其化合物的有关计算
考点一 镁及其化合物的结构、性质及应用
1.下列关于镁的叙述正确的是( )
A.镁在氮气中不能燃烧 B.镁与水不能反应释放出氢气
C.镁在氯气中燃烧会产生白烟 D.镁可在二氧化碳气体中燃烧,只生成白色固体
2.(2023秋·陕西西安·高三西安市铁一中学校考期末)金属钛可用下列方法提炼:
。下列叙述正确的是
A.该反应属于复分解反应 B.该反应中镁元素被氧化
C.该反应中 是还原剂 D.该反应中 发生了氧化反应
3.(2023春·河北保定·高三河北安国中学校联考)科学家已经发现火星的沉积层内存在数量众多的硫酸镁
水合盐( ),从而证实了这个红色星球早期存在水。下列说法错误的是
A.硫酸镁是离子化合物 B.无水硫酸镁可作干燥剂
C.硫酸镁既是镁盐也是硫酸盐 D.水合盐中存在极性键和氢键等化学键
4.(2023·湖北·华中师大一附中校联考模拟预测) 是一种新型储氢合金,该合金在一定条件下完
全吸氢的化学方程式为 ,得到的混合物 在
4.0molL-1HCl溶液中能完全释放出氢气。下列说法正确的是
A.该合金的熔点介于金属镁和金属铝的熔点之间
⋅
B. 中,两种元素的化合价均为零价
C.在氮气保护下,将一定比例的Mg、Al单质熔炼可获得该合金
D.一定条件下,17mol 和12molAl与盐酸完全反应,释放氢气的总量为52mol
5.(2023·全国·高三)镁是一种活泼的金属单质,下列关于金属镁的说法中正确的是( )
A.镁能与NaOH溶液反应生成Mg(OH) 沉淀
2
B.大量镁条燃烧引起的火灾不能用干冰灭火器灭火
C.镁在任何条件下都不能与水反应
D.镁能在N 中燃烧,且生成MgN
2
6.(2023春·河北石家庄·高三校联考期中)室温下,用质量和表面积相同的镁条(已用砂纸打磨),分别探
1
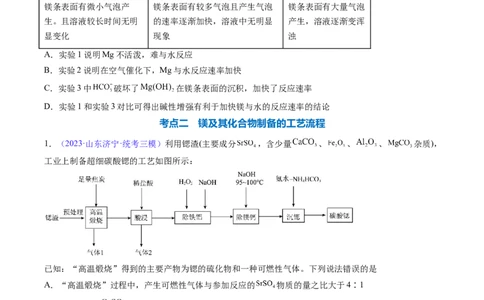
原创精品资源学科网独家享有版权,侵权必究!究不同条件下镁与水反应的实验(装置图如下),实验2的镁条放在尖嘴玻璃导管内并浸于蒸馏水中,实验3
产生的浑浊物主要为碱式碳酸镁 [ ]。下列说法正确的是
实验1 实验2 实验3
镁条表面有微小气泡产 镁条表面有较多气泡且产生气泡 镁条表面有大量气泡
生。且溶液较长时间无明 的速率逐渐加快,溶液中无明显 产生,溶液逐渐变浑
显变化 现象 浊
A.实验1说明Mg不活泼,难与水反应
B.实验2说明在空气催化下,Mg与水反应速率加快
C.实验3中 破坏了 在镁条表面的沉积,加快了反应速率
D.实验1和实验3对比可得出碱性增强有利于加快镁与水的反应速率的结论
考点二 镁及其化合物制备的工艺流程
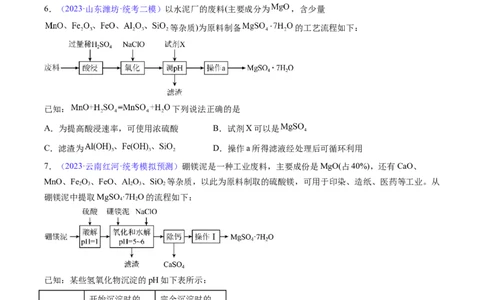
1.(2023·山东济宁·统考三模)利用锶渣(主要成分 ,含少量 、 、 、 杂质),
工业上制备超细碳酸锶的工艺如图所示:
已知:“高温煅烧”得到的主要产物为锶的硫化物和一种可燃性气体。下列说法错误的是
A.“高温煅烧”过程中,产生可燃性气体与参加反应的 物质的量之比大于4∶1
B.气体2通入 溶液产生黑色沉淀
C.“除镁钙”时控制温度95℃~100℃是为了降低氢氧化钙的溶解度,保证除钙效果
D.“沉锶”的离子反应方程式为
2.(2023秋·河北邢台·高三统考期末)工业通过菱镁矿 (含杂质 )制取镁的工艺流程
如图:下列说法正确的是
A.“酸浸池”中一定不发生氧化还原反应
B.“氧化池”中通入 的目的是杀菌消毒
C.甲可能是 或 等,加入甲的目的是调节溶液
D.将 溶液加热蒸干可得到无水 晶体
3.(2023·辽宁·校联考二模)以镁铝复合氧化物(MgO-Al O)为载体的负载型镍铜双金属催化剂(Ni-
2 3
Cu/MgO-Al O)是一种新型高效加氢或脱氢催化剂,其制备流程如图(常温下,K [Cu(OH) ]=2.21×10-20,
2 3 sp 2
K [Al(OH) ]=1.30×10-33,),以下说法错误的是
sp 3
A.常温下,若“悬浊液”中 =1.7×109,则溶液的pH=10
B.“晶化”过程中,需保持恒温60℃,可采用的加热方式为水浴加热
C.“还原”过程中所发生反应的化学方程式为NiO+H Ni+H O,CuO+H Cu+H O
2 2 2 2
D.洗涤过程中,检验滤饼是否洗净的方法是取上层清液于试管中,先滴加稀盐酸,再滴加氯化钡溶液,
若无白色沉淀生成,则已洗净
4.(2023·江苏南通·海门中学校考模拟预测)用镁还原 可制取高熔点的金属钛,工艺流程如图。下
列说法不正确的是
A.工业上电解熔融 可制备金属Mg
B.“高温还原”时,发生反应的化学方程式为
C.用金属镁还原 过程中需通入 或Ar作保护气
D.“真空蒸馏”的目的是使Mg、 气化,实现与Ti的分离
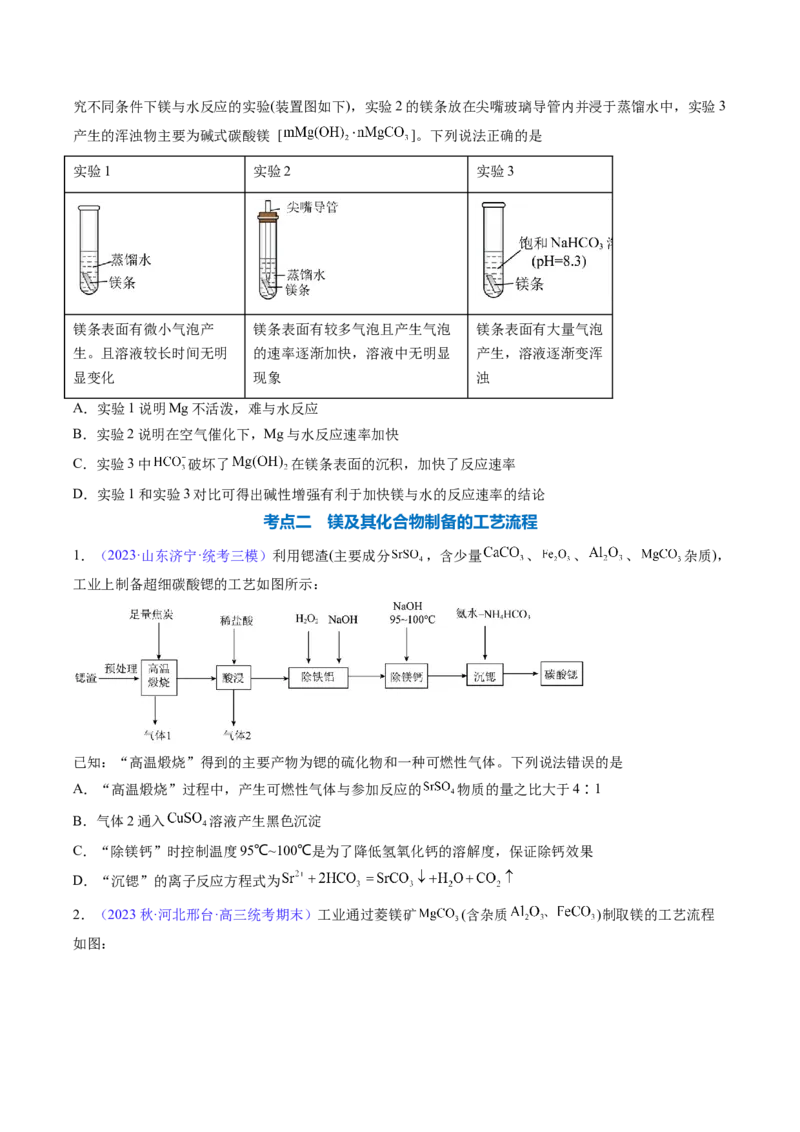
5.(2023·全国·模拟预测)MgO在医药上用作抗酸剂和轻泻剂,在化学工业中用作催化剂和制造镁盐的原料。某学习小组拟用氯化镁废液(主要成分是 ,含 、 等杂质)制取MgO,部分流程如图所
示。下列说法错误的是
A.试剂1可为 溶液 B.滤渣的主要成分为
C.操作③为蒸发结晶 D.将碱式碳酸镁在坩埚中灼烧可制得MgO
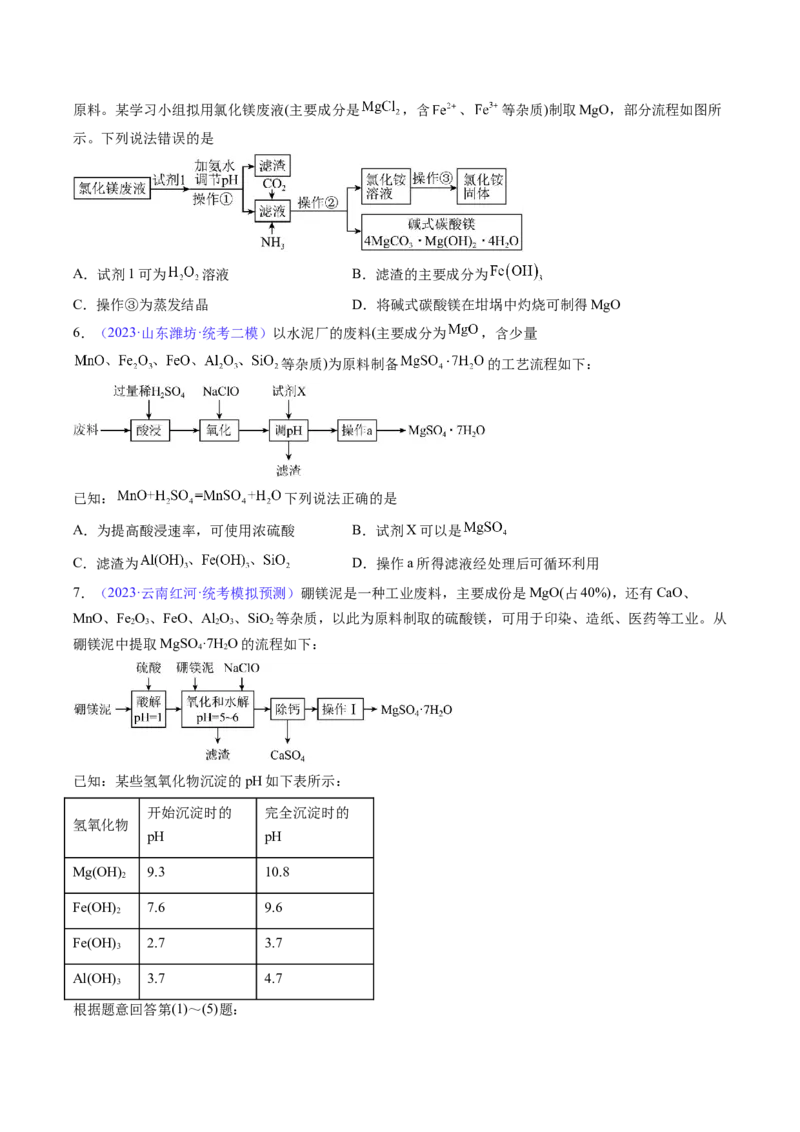
6.(2023·山东潍坊·统考二模)以水泥厂的废料(主要成分为 ,含少量
等杂质)为原料制备 的工艺流程如下:
已知: 下列说法正确的是
A.为提高酸浸速率,可使用浓硫酸 B.试剂X可以是
C.滤渣为 D.操作a所得滤液经处理后可循环利用
7.(2023·云南红河·统考模拟预测)硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、
MnO、Fe O、FeO、Al O、SiO 等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从
2 3 2 3 2
硼镁泥中提取MgSO ·7H O的流程如下:
4 2
已知:某些氢氧化物沉淀的pH如下表所示:
开始沉淀时的 完全沉淀时的
氢氧化物
pH pH
Mg(OH) 9.3 10.8
2
Fe(OH) 7.6 9.6
2
Fe(OH) 2.7 3.7
3
Al(OH) 3.7 4.7
3
根据题意回答第(1)~(5)题:(1)在酸解过程中,欲加快酸解时的化学反应速率,请提出两种可行的措施: 、 。
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H O=MnO ↓+2H++Cl-,还有一种离子也会被NaClO氧化,并
2 2
发生水解,该反应的离子方程式为 。
(3)滤渣的主要成份除含有Fe(OH) ,Al(OH) 、MnO 外,还有 。
3 3 2
(4)已知MgSO 、CaSO 的溶解度如下表:
4 4
温度(℃) 40 50 60 70
MgSO 30.9 33.4 35.6 36.9
4
CaSO 0.210 0.207 0.201 0.193
4
“除钙”是将MgSO 和CaSO 混合溶液中的CaSO 除去,根据上表数据,简要说明操作步骤是
4 4 4
, 。
(5)实验中提供的硼镁泥共100g,得到的MgSO ·7H O为172.2g,计算MgSO ·7H O的产率为 。
4 2 4 2
考点三 镁及其化合物的有关计算
1.(2023·全国·高三)铜和镁的合金4.6 g完全溶于浓硝酸,若反应中硝酸被还原只产生4 480 mL NO 气
2
体和336 mL的NO 气体(气体的体积已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,
2 4
生成沉淀的质量为 ( )
A.9.02 g B.8.51 g C.8.26 g D.7.04 g
2.(2023·全国·高三)镁与不同浓度的硝酸溶液反应可得到 、 、 、 、 等还原产物
(每种情况只考虑生成一种还原产物),下列说法错误的是
A.24g镁与足量某浓度的硝酸溶液充分反应生成 时消耗
B.消耗等量的镁生成的还原产物物质的量最多的是
C.生成氢气时所用硝酸浓度应小于生成其它产物时所用硝酸浓度
D.生成等物质的量的 和 消耗镁的物质的量之比为3:4
3.(2023·全国·高三)镁带在空气中燃烧生成的固体产物主要是氧化镁和氮化镁。将燃烧后的固体产物溶
解在60mL浓度为2.0mol/L的盐酸溶液中,(氮化镁和盐酸反应的化学方程式为:
MgN+8HCl=3MgCl +2NHCl)以20mL0.5mol/L的氢氧化钠溶液中和多余的盐酸,然后在此溶液中加入过
3 2 2 4
量的碱,把氨全部蒸发出来,用稀盐酸吸收,稀盐酸增重0.17g。镁带的质量为
A.0.6g B.1.2g C.2.4g D.3.6g
4.(2023·辽宁沈阳·东北育才学校校考模拟预测)2.28 g铜镁合金完全溶解于75 mL密度为1.40 g/mL、质
量分数为63%的浓硝酸中,得到 和 的混合气体1680 mL(标准状况),向反应后的溶液中加入l.0
mol/L NaOH溶液,当金属离子全部沉淀时,得到3.81 g沉淀,下列说法正确的是
A.该合金中,镁的物质的量为0.03 mol
B. 和 混合气体的平均相对分子质量约为55.2
C.得到3.81 g沉淀时,加入NaOH溶液的体积为900 mLD.该浓硝酸中 的物质的量浓度为12.0 mol/L
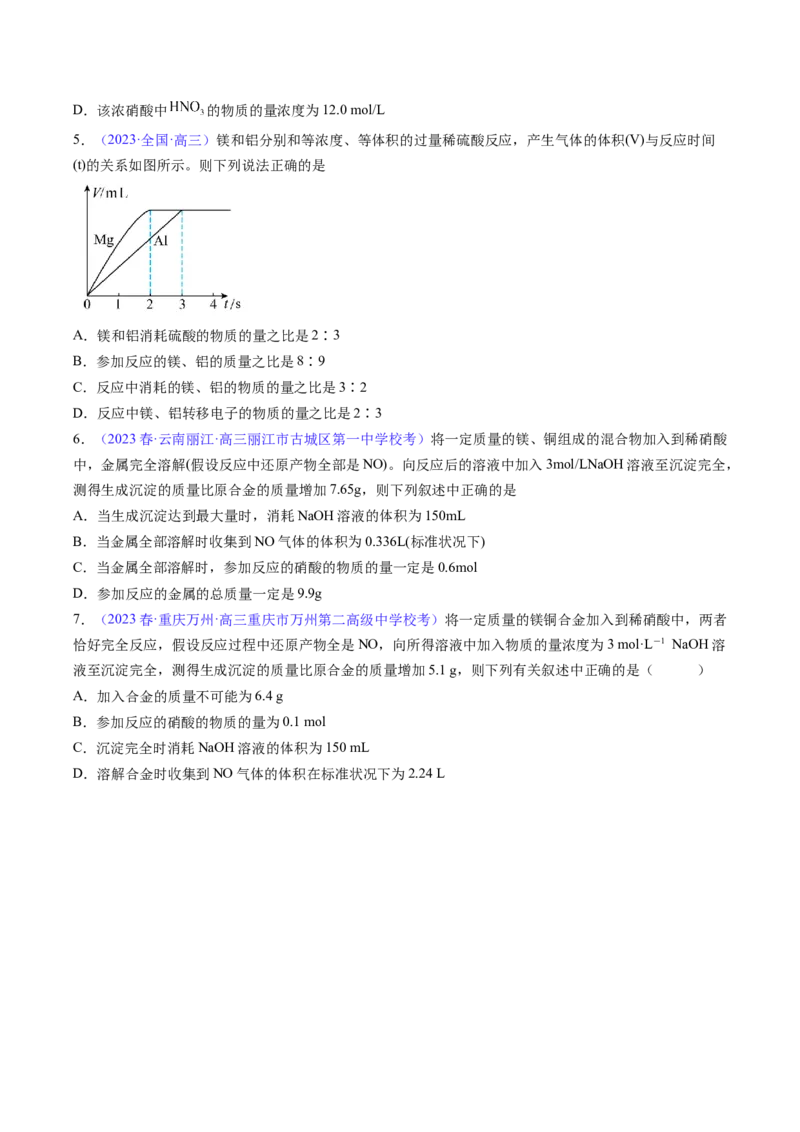
5.(2023·全国·高三)镁和铝分别和等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与反应时间
(t)的关系如图所示。则下列说法正确的是
A.镁和铝消耗硫酸的物质的量之比是2∶3
B.参加反应的镁、铝的质量之比是8∶9
C.反应中消耗的镁、铝的物质的量之比是3∶2
D.反应中镁、铝转移电子的物质的量之比是2∶3
6.(2023春·云南丽江·高三丽江市古城区第一中学校考)将一定质量的镁、铜组成的混合物加入到稀硝酸
中,金属完全溶解(假设反应中还原产物全部是NO)。向反应后的溶液中加入3mol/LNaOH溶液至沉淀完全,
测得生成沉淀的质量比原合金的质量增加7.65g,则下列叙述中正确的是
A.当生成沉淀达到最大量时,消耗NaOH溶液的体积为150mL
B.当金属全部溶解时收集到NO气体的体积为0.336L(标准状况下)
C.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.6mol
D.参加反应的金属的总质量一定是9.9g
7.(2023春·重庆万州·高三重庆市万州第二高级中学校考)将一定质量的镁铜合金加入到稀硝酸中,两者
恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3 mol·L-1 NaOH溶
液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g,则下列有关叙述中正确的是( )
A.加入合金的质量不可能为6.4 g
B.参加反应的硝酸的物质的量为0.1 mol
C.沉淀完全时消耗NaOH溶液的体积为150 mL
D.溶解合金时收集到NO气体的体积在标准状况下为2.24 L