文档内容
化工生产中物质的分离与提纯
1.常考分离、提纯的操作
(1)从滤液中提取一般晶体(溶解度随温度升高而增大)的方法:蒸发浓缩(至少有晶膜出现)、冷却结晶、
过滤、洗涤(冰水洗、热水洗、乙醇洗等)、干燥。
(2)从滤液中提取溶解度受温度影响较小或随温度升高而减小的晶体的方法:蒸发浓缩、趁热过滤(如果
温度下降,杂质也会以晶体的形式析出来)、洗涤、干燥。
(3)减压蒸发的原因:减压蒸发降低了蒸发温度,可以防止某物质分解(如H O 、浓硝酸、NH HCO )或
2 2 4 3
失去结晶水(如题目要求制备结晶水合物产品)。
(4)洗涤
洗涤试剂 适用范围 目的
除去固体表面吸附着的××杂质,可适当降低
冷水 产物不溶于水
固体因为溶解而造成的损失
蒸
馏
有特殊的物质其溶解度随 除去固体表面吸附着的××杂质,可适当降低
水
热水
着温度升高而下降 固体因为温度变化溶解而造成的损失
有机溶剂
固体易溶于水、难溶于有 减少固体溶解;利用有机溶剂的挥发性除去
(酒精、丙
机溶剂 固体表面的水分,产品易干燥
酮等)
饱和溶液 对纯度要求不高的产品 减少固体溶解
除去固体表面吸附着的可溶于酸、碱的杂
酸、碱溶液 产物不溶于酸、碱
质;减少固体溶解
洗涤沉淀的方法:向过滤器中加入洗涤试剂至浸没沉淀,待洗涤试剂自然流下后,重
复以上操作2~3次
检验沉淀是否洗涤干净的方法:取少量最后一次的洗涤液于试管中,向其中滴入某试
剂,若未出现特征反应现象,则沉淀洗涤干净
(5)萃取与反萃取①萃取:利用物质在两种互不相溶的溶剂中的溶解度不同,将物质从一种溶剂转移到另一种溶剂的过
程。如用CCl 萃取溴水中的Br 。
4 2
②反萃取:用反萃取剂使被萃取物从负载有机相返回水相的过程,为萃取的逆过程。
(6)其他
①蒸发时的气体氛围抑制水解:如从溶液中析出AlCl 、MgCl 等溶质时,应在HCl的气流中加热,以
3 2
防其水解。
②减压蒸馏的原因:减小压强,使液体沸点降低,防止受热分解、氧化等。
2.根据溶解度曲线判断结晶的方法
(1)溶解度受温度影响较小的(如NaCl)采取蒸发结晶的方法。
(2)溶解度受温度影响较大的采取蒸发浓缩、冷却结晶的方法。
(3)带有结晶水的盐,一般采取蒸发浓缩、冷却结晶的方法。
应用示例
1.萃取法分离
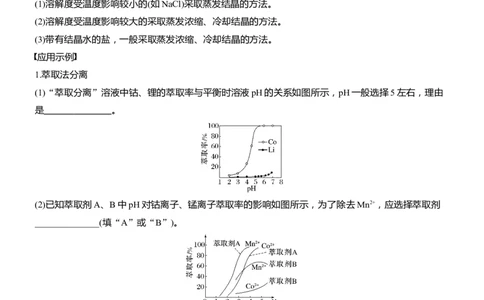
(1)“萃取分离”溶液中钴、锂的萃取率与平衡时溶液pH的关系如图所示,pH一般选择5左右,理由
是 。
(2)已知萃取剂A、B中pH对钴离子、锰离子萃取率的影响如图所示,为了除去Mn2+,应选择萃取剂
______________(填“A”或“B”)。
答案 (1)pH在5左右时,钴、锂的分离效率高
(2)B
2.反萃取法分离
(1)钒及其化合物在工业上有许多用途。从废钒(主要成分V O 、V O 、Fe O 、FeO、SiO )中提取五氧
2 3 2 5 2 3 2
化二钒的一种工艺流程如图:已知:①VOSO 能溶于水,VO2+与Fe不能反应;
4
②有机溶剂H R对VO2+及Fe3+萃取率高,但不能萃取Fe2+。
2
“溶剂萃取与反萃取”可表示为VO2++H R VOR+2H+。为了提高VO2+的产率,反萃取剂可选
2
用 (填字母)。
a.NaCl b.NaOH c.H SO
2 4
答案 c
(2)钼(Mo)是重要的过渡金属元素,具有广泛用途。由钼精矿(主要成分是MoS )湿法回收钼酸铵
2
[(NH ) MoO ]部分工艺流程如图:
4 2 4
“滤液2”先加入有机溶剂“萃取”,再加氨水“反萃取”,进行“萃取”和“反萃取”操作的目的是
。
答案 富集钼酸根离子(或将钼酸根离子和其他杂质分离)
3.结晶与过滤
从溶液中得到晶体的过程:蒸发浓缩→冷却结晶→过滤→洗涤、干燥。
需要加热得到的晶体(或物质):蒸发结晶、趁热过滤。
需要冷却得到的晶体(或物质):蒸发浓缩、冷却结晶。
(1)制备MnSO ·H O晶体。已知溶解度曲线如图1所示,MnSO ·H O晶体在曲线拐点右侧。
4 2 4 2操作方法:滴加稀硫酸酸化,温度 (填“高于”“低于”或“等于”)40 ℃, 结晶、
过滤,酒精洗涤,低温干燥。
答案 高于 蒸发 趁热
(2)制备FeSO ·7H O晶体。已知溶解度曲线如图2所示,FeSO ·7H O晶体在曲线拐点左侧。
4 2 4 2
操作方法:加热 ,得到 ℃饱和溶液,冷却至 ℃结晶,过滤,少量冰水洗涤,
低温干燥。
答案 浓缩 60 0
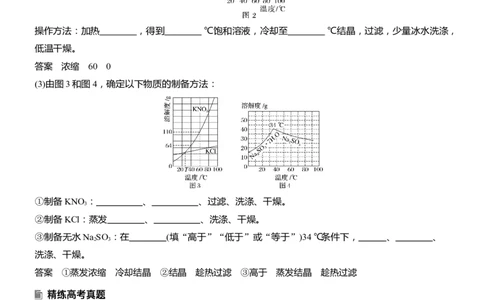
(3)由图3和图4,确定以下物质的制备方法:
①制备KNO : 、 、过滤、洗涤、干燥。
3
②制备KCl:蒸发 、 、洗涤、干燥。
③制备无水Na SO :在 (填“高于”“低于”或“等于”)34 ℃条件下, 、 、
2 3
洗涤、干燥。
答案 ①蒸发浓缩 冷却结晶 ②结晶 趁热过滤 ③高于 蒸发结晶 趁热过滤
1.[2024·湖北,16(2)(3)(4)]铍用于宇航器件的构筑。一种从其铝硅酸盐[Be Al (SiO ) ]中提取铍的路径
3 2 3 6
为已知:Be2++4HA BeA (HA) +2H+
2 2
回答下列问题:
(2)为了从“热熔冷却”步骤得到玻璃态,冷却过程的特点是 。
(3)“萃取分液”的目的是分离Be2+和Al3+,向过量烧碱溶液中逐滴加入少量“水相1”的溶液,观察到
的现象是 。
(4)写出反萃取生成Na [Be(OH) ]的化学方程式 。 “滤液2”可以进入 步骤再
2 4
利用。
答案 (2)快速冷却 (3)先产生白色沉淀,后白色沉淀快速溶解
(4)BeA (HA) +6NaOH===Na [Be(OH) ]+4NaA+2H O 反萃取
2 2 2 4 2
解析 在本流程生产过程中,先将铝硅酸盐加热熔融后快速冷却得到其玻璃态,加入稀硫酸酸浸得到的滤
渣成分为H SiO ;“滤液1”中含有Be2+和Al3+,加入含HA的煤油后HA与Be2+反应生成BeA (HA) 进入
2 3 2 2
有机相中,Al3+进入水相1中;在有机相中加入过量氢氧化钠后BeA (HA) 转化为Na [Be(OH) ]进入水相2
2 2 2 4
中,分离出含NaA的煤油;对水相2加热,Na [Be(OH) ]转化为Be(OH) ,通过过滤分离出来,最后通过
2 4 2
一系列操作得到金属铍。(2)熔融态物质冷却凝固时,若缓慢冷却则会形成晶体,若快速冷却则会形成非晶
态,即玻璃态。(3)“滤液1”中有Be2+和Al3+,加入含HA的煤油后HA将Be2+萃取到有机相中,则水相1
中含有Al3+;若向过量烧碱的溶液中逐滴加入少量水相1的溶液,可观察到的现象为:先产生白色沉淀,
后白色沉淀快速溶解。(4)反萃取过程中BeA (HA) 与烧碱反应生成Na [Be(OH) ],化学方程式为
2 2 2 4
BeA (HA) +6NaOH===Na [Be(OH) ]+4NaA+2H O;滤液2的主要成分为NaOH,可进入反萃取步骤再利用。
2 2 2 4 2
2.[2017·全国卷Ⅲ,27(4)]重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为
FeO·Cr O ,还含有硅、铝等杂质。制备流程如图所示:
2 3
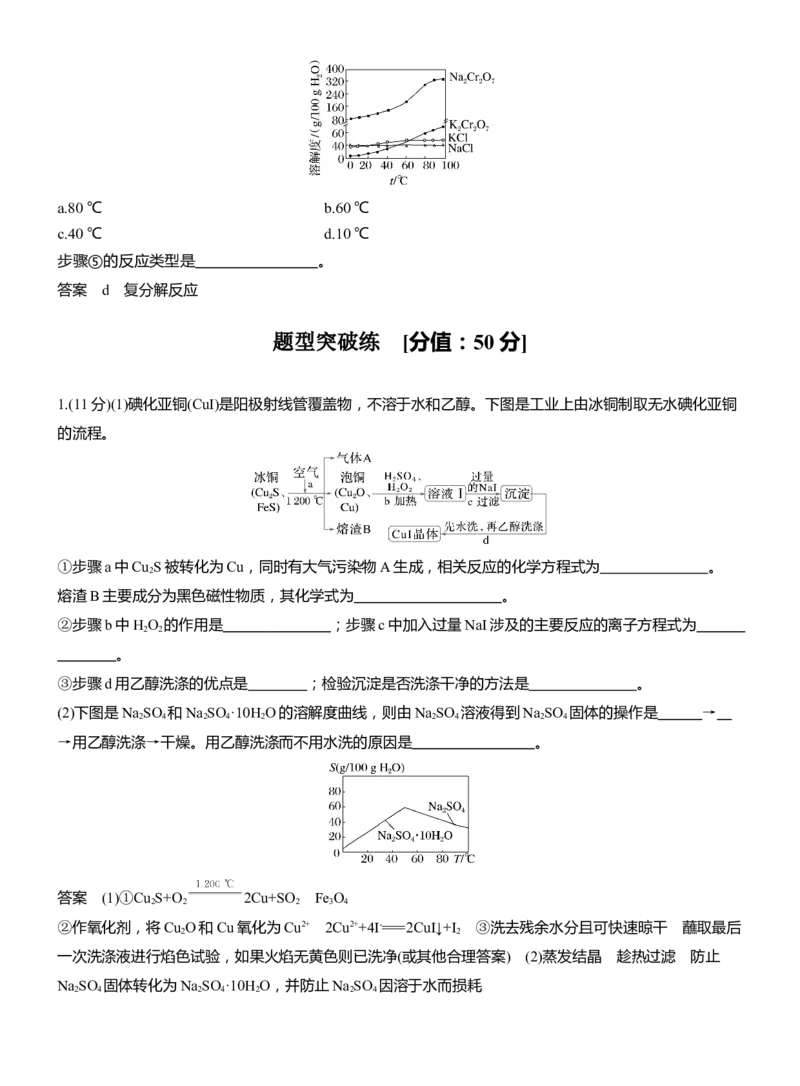
有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K Cr O
2 2 7
固体。冷却到 (填字母)得到的K Cr O 固体产品最多。
2 2 7a.80 ℃ b.60 ℃
c.40 ℃ d.10 ℃
步骤⑤的反应类型是 。
答案 d 复分解反应
题型突破练 [分值:50 分]
1.(11分)(1)碘化亚铜(CuI)是阳极射线管覆盖物,不溶于水和乙醇。下图是工业上由冰铜制取无水碘化亚铜
的流程。
①步骤a中Cu S被转化为Cu,同时有大气污染物A生成,相关反应的化学方程式为 。
2
熔渣B主要成分为黑色磁性物质,其化学式为 。
②步骤b中H O 的作用是 ;步骤c中加入过量NaI涉及的主要反应的离子方程式为
2 2
。
③步骤d用乙醇洗涤的优点是 ;检验沉淀是否洗涤干净的方法是 。
(2)下图是Na SO 和Na SO ·10H O的溶解度曲线,则由Na SO 溶液得到Na SO 固体的操作是 →
2 4 2 4 2 2 4 2 4
→用乙醇洗涤→干燥。用乙醇洗涤而不用水洗的原因是 。
答案 (1)①Cu S+O 2Cu+SO Fe O
2 2 2 3 4
②作氧化剂,将Cu O和Cu氧化为Cu2+ 2Cu2++4I-===2CuI↓+I ③洗去残余水分且可快速晾干 蘸取最后
2 2
一次洗涤液进行焰色试验,如果火焰无黄色则已洗净(或其他合理答案) (2)蒸发结晶 趁热过滤 防止
Na SO 固体转化为Na SO ·10H O,并防止Na SO 因溶于水而损耗
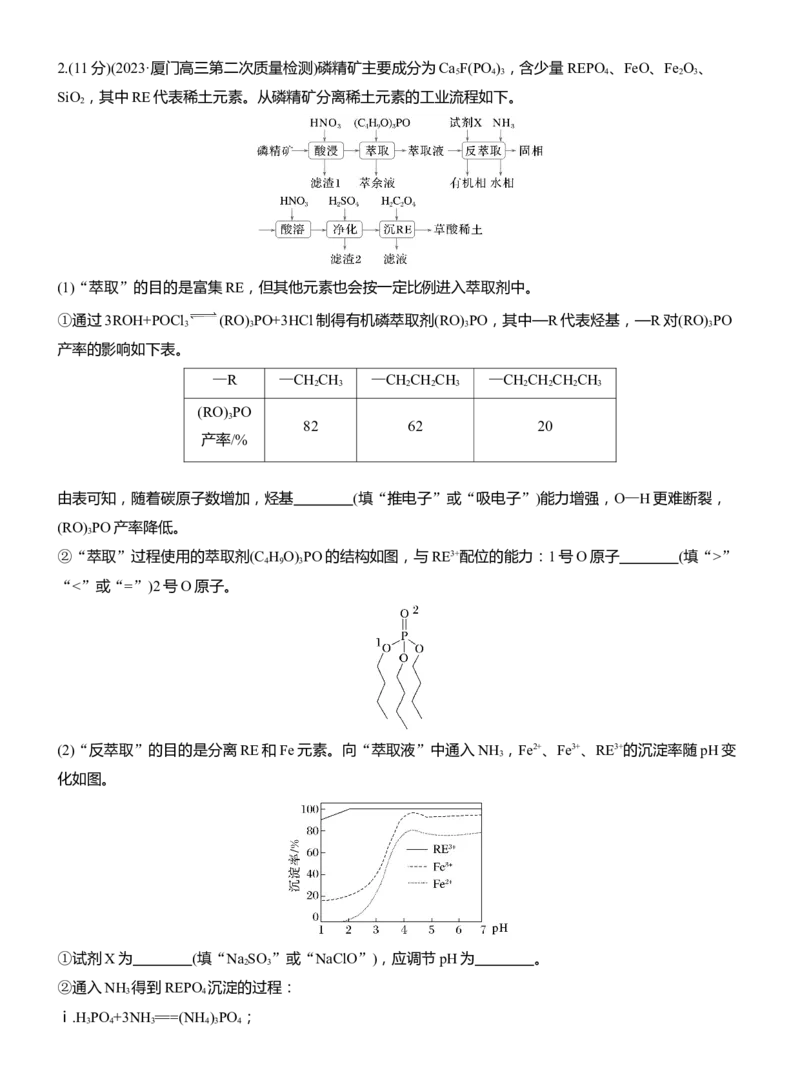
2 4 2 4 2 2 42.(11分)(2023·厦门高三第二次质量检测)磷精矿主要成分为Ca F(PO ) ,含少量REPO 、FeO、Fe O 、
5 4 3 4 2 3
SiO ,其中RE代表稀土元素。从磷精矿分离稀土元素的工业流程如下。
2
(1)“萃取”的目的是富集RE,但其他元素也会按一定比例进入萃取剂中。
①通过3ROH+POCl (RO) PO+3HCl制得有机磷萃取剂(RO) PO,其中—R代表烃基,—R对(RO) PO
3 3 3 3
产率的影响如下表。
—R —CH CH —CH CH CH —CH CH CH CH
2 3 2 2 3 2 2 2 3
(RO) PO
3
82 62 20
产率/%
由表可知,随着碳原子数增加,烃基 (填“推电子”或“吸电子”)能力增强,O—H更难断裂,
(RO) PO产率降低。
3
②“萃取”过程使用的萃取剂(C H O) PO的结构如图,与RE3+配位的能力:1号O原子 (填“>”
4 9 3
“<”或“=”)2号O原子。
(2)“反萃取”的目的是分离RE和Fe元素。向“萃取液”中通入NH ,Fe2+、Fe3+、RE3+的沉淀率随pH变
3
化如图。
①试剂X为 (填“Na SO ”或“NaClO”),应调节pH为 。
2 3
②通入NH 得到REPO 沉淀的过程:
3 4
ⅰ.H PO +3NH ===(NH ) PO ;
3 4 3 4 3 4ⅱ. (写出该过程的化学方程式)。
③若萃取剂改用三丁基氧化膦[(C H ) PO]会导致“反萃取”RE产率降低,其原因为 。
4 9 3
(3)若略去“净化”过程,则制得的草酸稀土会混有 (填化学式)杂质。
(4)在整个工艺中,可从副产物中提取 (填名称),用于生产氮肥。
答案 (1)①推电子 ②<
(2)①Na SO 2 ②(NH ) PO +RE(NO ) ===REPO ↓+3NH NO ③—C H 有较强的推电子作用,导致稀土
2 3 4 3 4 3 3 4 4 3 4 9
与萃取剂形成的配位键牢固,难以断裂实现反萃取 (3)CaC O (4)硝酸铵、硝酸
2 4
解析 磷精矿加入硝酸酸浸,二氧化硅不反应得到滤渣1,稀土元素、铁、钙元素进入滤液,加入萃取剂
萃取出稀土元素,然后加入亚硫酸钠将三价铁转化为二价铁,通入氨气,调节pH分离出含有稀土的固相,
再加入硝酸溶解,加入硫酸除去钙元素得到滤渣2硫酸钙,滤液加入草酸分离出草酸稀土。(1)②由随着碳
原子数增加,烃基推电子能力增强可知,烃基导致1号位氧更难与RE3+配位,故与RE3+配位的能力:1号
O原子<2号O原子。(2)①由图可知,亚铁离子与RE的分离效果更好,则试剂X为将铁离子转化为亚铁
离子的物质,故应选择Na SO ;结合图像可知,应调节pH为2,此时RE几乎完全沉淀,而亚铁离子几乎
2 3
没有沉淀,分离效果好。②总反应为通入NH 得到REPO 沉淀,反应ⅰ.H PO +3NH ===(NH ) PO ,则反
3 4 3 4 3 4 3 4
应ⅱ为(NH ) PO 和稀土的硝酸盐转化为REPO 沉淀的反应:(NH ) PO +RE(NO ) ===REPO ↓+3NH NO 。
4 3 4 4 4 3 4 3 3 4 4 3
(4)在整个工艺中,通入氨气生成的硝酸铵,以及酸溶加入的硝酸均含有氮元素,故可从副产物中提取硝酸
铵、硝酸用于生产氮肥。
3.(6分)废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为CuIn Ga Se 。某探究小组回收处
0.5 0.5 2
理流程如图:
(1)高温焙烧得到的烧渣主要成分是氧化物(如:Cu O、In O 、Ga O ),“酸浸氧化”得蓝色溶液,则该过
2 2 3 2 3
程发生的主要氧化还原反应的离子方程式为 。
(2)“滤渣”与SOCl 混合前需要洗涤、干燥,检验滤渣是否洗净的操作: 。
2
(3)SOCl 的作用: 。
2
答案 (1)Cu O+H O +4H+===2Cu2++3H O (2)取最后一次洗涤液于试管中,加入盐酸酸化,无明显现象,
2 2 2 2
再加氯化钡溶液,若无白色沉淀生成,则证明洗涤干净;若有白色沉淀生成,则证明没有洗涤干净 (3)将
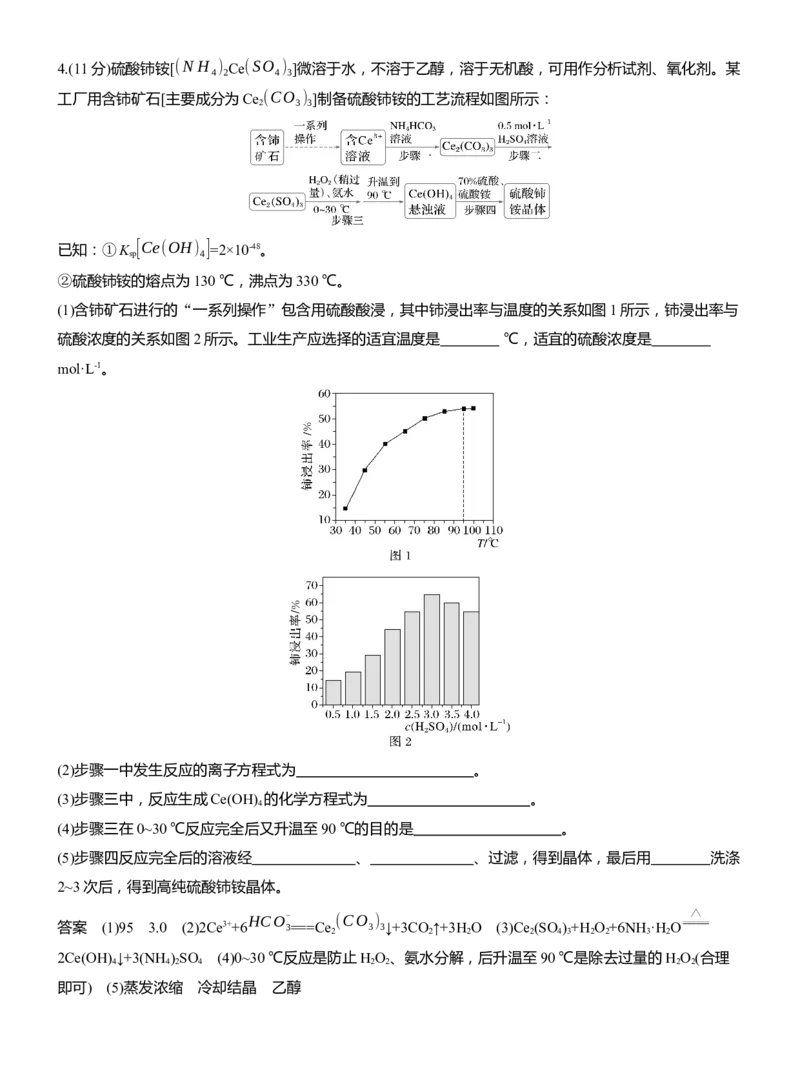
氢氧化物转化为氯化物;作溶剂4.(11分)硫酸铈铵[(N H ) Ce(SO ) ]微溶于水,不溶于乙醇,溶于无机酸,可用作分析试剂、氧化剂。某
4 2 4 3
工厂用含铈矿石[主要成分为Ce (CO ) ]制备硫酸铈铵的工艺流程如图所示:
2 3 3
已知:①K [Ce(OH) ]=2×10-48。
sp 4
②硫酸铈铵的熔点为130 ℃,沸点为330 ℃。
(1)含铈矿石进行的“一系列操作”包含用硫酸酸浸,其中铈浸出率与温度的关系如图1所示,铈浸出率与
硫酸浓度的关系如图2所示。工业生产应选择的适宜温度是 ℃,适宜的硫酸浓度是
mol·L-1。
(2)步骤一中发生反应的离子方程式为 。
(3)步骤三中,反应生成Ce(OH) 的化学方程式为 。
4
(4)步骤三在0~30 ℃反应完全后又升温至90 ℃的目的是 。
(5)步骤四反应完全后的溶液经 、 、过滤,得到晶体,最后用 洗涤
2~3次后,得到高纯硫酸铈铵晶体。
HCO- (CO )
答案 (1)95 3.0 (2)2Ce3++6 3===Ce
2
3 3↓+3CO
2
↑+3H
2
O (3)Ce
2
(SO
4
)
3
+H
2
O
2
+6NH
3
·H
2
O
2Ce(OH) ↓+3(NH ) SO (4)0~30 ℃反应是防止H O 、氨水分解,后升温至90 ℃是除去过量的H O (合理
4 4 2 4 2 2 2 2
即可) (5)蒸发浓缩 冷却结晶 乙醇解析 含铈矿石经过一系列操作,Ce3+进入溶液中,加入NH HCO 溶液得到Ce (CO ) ,加入0.5 mol·L-1
4 3 2 3 3
H SO 溶液得到Ce (SO ) 溶液,加入过氧化氢将Ce3+氧化为Ce4+,加入氨水控温在0~30 ℃,然后升温至
2 4 2 4 3
90 ℃得到Ce(OH) 悬浊液,加入硫酸、硫酸铵得到硫酸铈铵晶体。
4
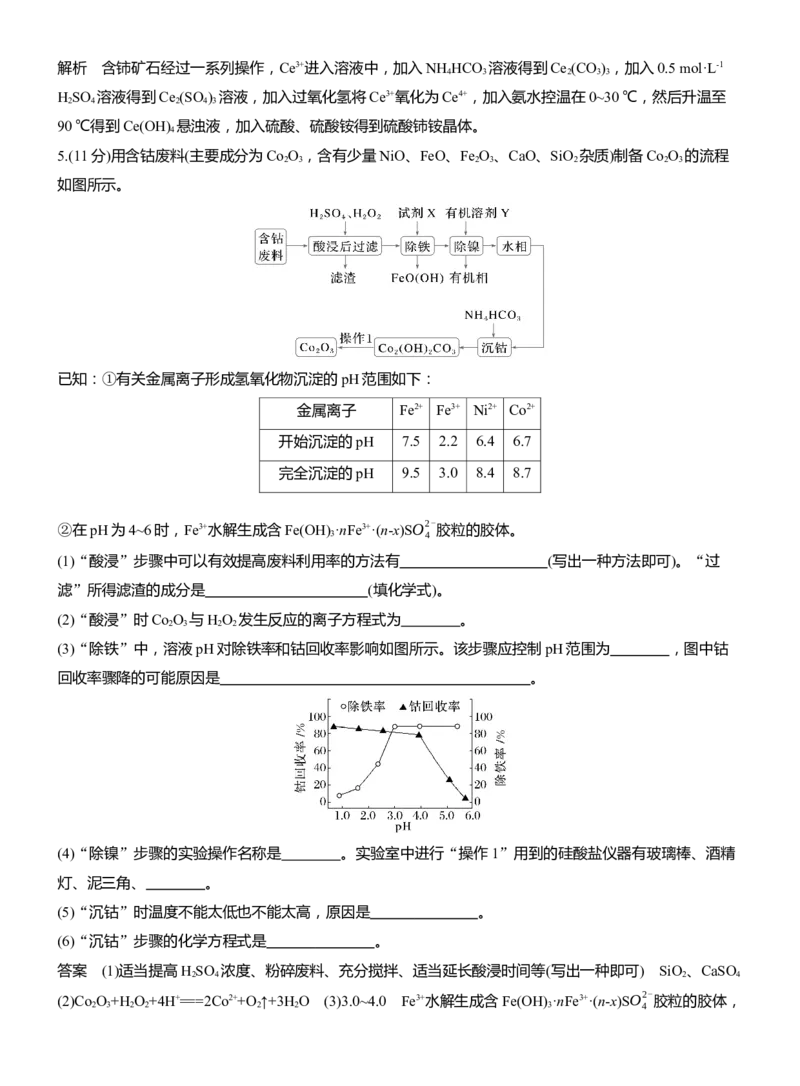
5.(11分)用含钴废料(主要成分为Co O ,含有少量NiO、FeO、Fe O 、CaO、SiO 杂质)制备Co O 的流程
2 3 2 3 2 2 3
如图所示。
已知:①有关金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 Fe2+ Fe3+ Ni2+ Co2+
开始沉淀的pH 7.5 2.2 6.4 6.7
完全沉淀的pH 9.5 3.0 8.4 8.7
②在pH为4~6时,Fe3+水解生成含Fe(OH)
·nFe3+·(n-x)SO2-
胶粒的胶体。
3 4
(1)“酸浸”步骤中可以有效提高废料利用率的方法有 (写出一种方法即可)。“过
滤”所得滤渣的成分是 (填化学式)。
(2)“酸浸”时Co O 与H O 发生反应的离子方程式为 。
2 3 2 2
(3)“除铁”中,溶液pH对除铁率和钴回收率影响如图所示。该步骤应控制pH范围为 ,图中钴
回收率骤降的可能原因是 。
(4)“除镍”步骤的实验操作名称是 。实验室中进行“操作1”用到的硅酸盐仪器有玻璃棒、酒精
灯、泥三角、 。
(5)“沉钴”时温度不能太低也不能太高,原因是 。
(6)“沉钴”步骤的化学方程式是 。
答案 (1)适当提高H SO 浓度、粉碎废料、充分搅拌、适当延长酸浸时间等(写出一种即可) SiO 、CaSO
2 4 2 4
(2)Co O +H O +4H+===2Co2++O ↑+3H O (3)3.0~4.0 Fe3+水解生成含Fe(OH)
·nFe3+·(n-x)SO2-
胶粒的胶体,
2 3 2 2 2 2 3 4吸附大量的Co2+,导致钴回收率下降 (4)萃取(或萃取分液) 坩埚 (5)温度过低,反应速率慢;温度过高,
NH HCO 不稳定受热易分解 (6)2CoSO +4NH HCO ===Co (OH) CO ↓+3CO ↑+H O+2(NH ) SO
4 3 4 4 3 2 2 3 2 2 4 2 4
解析 含钴废料主要成分为Co O ,含有少量NiO、FeO、Fe O 、CaO、SiO 杂质,用硫酸溶解,过氧化氢
2 3 2 3 2
把Co3+还原为Co2+,把Fe2+氧化为Fe3+得到含有Co2+、Fe3+、Ni2+的溶液,CaSO 微溶、SiO 难溶,过滤出
4 2
沉淀;调节溶液的pH在3.0~4.0,除去Fe3+;滤液中加入萃取剂,萃取除去Ni2+,取水相加入NH HCO 生
4 3
成Co (OH) CO ,在空气中灼烧Co (OH) CO 生成Co O 。
2 2 3 2 2 3 2 3