文档内容
第 44 讲 化学反应速率及影响因素
[复习目标] 1.了解化学反应速率的概念及表示方法,能提取信息计算化学反应速率。2.掌
握影响化学反应速率的因素,并能用有关理论解释。
考点一 化学反应速率及表示方法
1.化学反应速率
(1)
(2)各物质的化学反应速率之比=__________之比。
如mA(g)+nB(g)pC(g)+qD(g),v ∶v ∶v ∶v =____________。
A B C D
(3)注意事项
①化学反应速率一般指平均速率而不是某一时刻的瞬时速率,且无论用反应物还是用生成物
表示均取正值。
②同一化学反应,相同条件下用不同物质表示的反应速率,其数值可能不同,但表示的意义
相同。
③固体或纯液体的浓度视为常数,不能用固体或纯液体的浓度变化计算化学反应速率。
2.应用“三段式”计算化学反应速率
列起始量、转化量、某时刻量,再根据定义式或比例关系计算。
对于反应mA(g)+nB(g)pC(g),起始时A的浓度为a mol·L-1,B的浓度为b mol·L-1,C
的浓度为c mol·L-1,反应进行至t s时,A消耗了x mol·L-1,则化学反应速率的计算如下:
1
mA(g)+nB(g)pC(g)起始浓度/mol·L-1 a b c
(转化浓度/mol·L-1 x _______ ________
t s时浓度/mol·L-1 a-x _______ ________
1
则v(A)=________________,v(B)=________________,v(C)=________________。
[应用举例]
1.一定条件下,在体积为10 L的固定容器中发生反应:N(g)+3H(g)2NH (g),反应过
2 2 3
程如图。
(1)表示NH 的物质的量变化的曲线是_____________________________________________。
3
(2)计算0~8 min,H 的平均反应速率(写出计算过程,下同)。
2
______________________________________________________________________________
(3)计算10~12 min,N 的平均反应速率。
2
______________________________________________________________________________
2.已知反应:4CO+2NO =====N+4CO 在不同条件下的化学反应速率如下。
2 2 2
①v(CO)=1.5 mol·L-1·min-1
②v(NO )=0.7 mol·L-1·min-1
2
③v(N )=0.4 mol·L-1·min-1
2
④v(CO)=1.1 mol·L-1·min-1
2
⑤v(NO )=0.01 mol·L-1·s-1
2
请 比 较 上 述 5 种 情 况 反 应 的 快 慢 :
________________________________________________(由大到小的顺序)。
1.对于任何化学反应来说,反应速率越大,反应现象越明显( )
2.由v=计算平均反应速率,用反应物表示为正值,用生成物表示为负值( )
3.化学反应速率为0.8 mol·L-1·s-1是指1 s时某物质的浓度为0.8 mol·L-1( )
4.同一化学反应,相同条件下用不同物质表示的反应速率,数值越大,表示化学反应速率
越快( )
一、用其他物理量表示的化学反应速率的计算
1.温度为T 时,2 g某合金4 min内吸收氢气240 mL,吸氢速率v=______mL·g-1·min-1。
12.(2023·陕西榆林统考一模)在某一恒容密闭容器中加入CO 、H ,其分压分别为15 kPa、
2 2
30 kPa,加入催化剂并加热使其发生反应:CO(g)+4H(g)CH(g)+2HO(g)。研究表明
2 2 4 2
CH 的反应速率v(CH)=1.2×10-6×p(CO)·p4(H ) kPa·s-1,某时刻测得HO(g)的分压为10
4 4 2 2 2
kPa,则该时刻v(H )=________________。
2
二、速率方程与化学反应速率
3.[2020·全国卷Ⅱ,28(2)①]高温下,甲烷生成乙烷的反应如下:2CH――→C H +H 。反应
4 2 6 2
在初期阶段的速率方程为r=k× ,其中k为反应速率常数。设反应开始时的反应速率
为r,甲烷的转化率为α时的反应速率为r,则r=________ r。
1 2 2 1
4.[2018·全国卷Ⅰ,28(2)②]F.Daniels 等曾利用测压法在刚性反应器中研究了 25 ℃时
NO(g)分解反应:
2 5
其中NO 二聚为NO 的反应可以迅速达到平衡。体系的总压强p随时间t 的变化如下表所
2 2 4
示[t=∞时,NO(g)完全分解]:
2 5
t/min 0 40 80 160 260 1 300 1 700 ∞
p/kPa 35.8 40.3 42.5 45.9 49.2 61.2 62.3 63.1
研究表明,NO(g)分解的反应速率v=2×10-3× kPa·min-1。t=62 min时,测得体系
2 5
中 =2.9 kPa,则此时 =________kPa,v=________kPa·min-1。
考点二 影响化学反应速率的因素
1.内因
反应物________是主要因素。如相同条件下 Mg、Al 与稀盐酸反应的速率大小关系为
Mg____Al。
2.外因[应用举例]
下列措施可以增大化学反应速率的是____________(填序号)。
①Al在氧气中燃烧生成Al O ,将Al片改成Al粉;②Fe与稀硫酸反应制取H 时,改用
2 3 2
98%浓硫酸;③HSO 与BaCl 溶液反应时,增大压强;④2SO +O2SO ΔH<0,升
2 4 2 2 2 3
高温度;⑤Na与水反应时,增大水的用量;⑥2HO===2HO+O↑反应中,加入少量
2 2 2 2
MnO ;⑦H 与Cl 混合后光照
2 2 2
3.有效碰撞理论解释外因对化学反应速率的影响
(1)有效碰撞
能够发生____________的碰撞为有效碰撞。化学反应发生的先决条件是反应物分子间必须发
生碰撞。有效碰撞必须具备两个条件:一是发生碰撞的分子具有____________,二是碰撞时
要有____________。
(2)活化分子
有足够的________,能够发生______________的分子叫活化分子。
活化分子百分数=×100%。
(3)活化分子、有效碰撞与反应速率的关系
条件→活化分子→有效碰撞→反应速率变化
单位体积内 有效碰 化学反
条件改变
分子总数 活化分子数 活化分子百分数 撞次数 应速率
增大反应物浓度
增大压强
升高温度
加催化剂
1.催化剂参与化学反应,改变了活化能,但反应前后物理和化学性质均保持不变( )
2.升温时吸热反应速率增大,放热反应速率减小( )3.一定量的锌与过量的稀硫酸反应制取氢气,滴入少量硫酸铜与醋酸钠均能够提高反应速
率( )
4.增大反应物的浓度,能够增大活化分子的百分数,所以反应速率增大( )
5.100 mL 2 mol·L-1盐酸与锌片反应,加入适量的氯化钠溶液,反应速率不变( )
一、压强对化学反应速率的影响
1.一定温度下,反应N(g)+O(g)2NO(g)在密闭容器中进行,回答下列措施对化学反应
2 2
速率的影响(填“增大”“减小”或“不变”)。
(1)缩小体积使压强增大:__________________________________________________,原因
是______________________________________________________________________________。
(2)恒容充入N:__________。
2
(3)恒容充入He:__________,原因是_____________________________________________
______________________________________________________________________________。
(4)恒压充入He:__________。
惰性气体对反应速率的影响
恒温恒容条件下 通入惰性气体,总压增大,反应物浓度不变,反应速率不变
恒温恒压条件下 通入惰性气体,总体积增大,反应物浓度减小,反应速率减小
二、固体表面积对化学反应速率的影响
2.图1为从废钼催化剂(主要成分为MoO 、MoS ,含少量NiS、NiO、Fe O 等)中回收利用
3 2 2 3
金属的部分流程。
“焙烧”时将纯碱和废钼催化剂磨成粉末后采取如图2所示的“多层逆流焙烧”,其目的是
______________________________________________________________________________
______________________________________________________________________________。
3.[2019·北京,27(1)①]甲烷水蒸气催化重整制氢的主要反应为:CH+2HO(g)=====CO+
4 2 2
4H ,用CaO可以去除CO ,H 体积分数和CaO消耗率随时间变化关系如图所示。从t 时开
2 2 2 1
始,H 体积分数显著降低,单位时间 CaO消耗率________(填“升高”“降低”或“不
2
变”)。此时 CaO 消耗率约为 35%,但已失效,结合化学方程式解释原因:___________________
______________________________________________________________________________。
三、对照实验及其设计
4.某小组拟用酸性KMnO 溶液与HC O 溶液的反应(此反应为放热反应)来探究“条件对化
4 2 2 4
学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试
剂和仪器:0.20 mol·L-1 HC O 溶液、0.010 mol·L-1 KMnO 溶液(酸性)、蒸馏水、试管、
2 2 4 4
量筒、秒表、恒温水浴槽。
V(0.010 mol·L-1
实验 V(0.20 mol·L-1 V(蒸馏
酸性KMnO 溶液)/ m(MnSO )/g T/℃ 乙
4 4
编号 HC O 溶液)/mL 水)/mL
2 2 4
mL
① 2.0 0 4.0 0 50
② 2.0 0 4.0 0 25
③ 1.5 a 4.0 0 25
④ 2.0 0 4.0 0.1 25
回答下列问题:
(1)KMnO 溶液用________________(填名称)酸化;写出上述反应的离子方程式:
4
_____________________________________________________________________________。
(2)实验①②是探究________对化学反应速率的影响;实验②④是探究________对化学反应
速率的影响。
(3)若实验②③是探究浓度对化学反应速率的影响,则 a为________;表格中的“乙”填写
t/s , 其 测 量 的 是
____________________________________________________________________。
关于“变量控制法”题目的解题策略1.(2022·浙江6月选考,20)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
2NH (g)N(g)+3H(g),测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,
3 2 2
如下表所示,下列说法不正确的是( )
时间/min
编
cNH /10-3 mol·L-1 0 20 40 60 80
3
号
表面积/cm2
① a 2.40 2.00 1.60 1.20 0.80
② a 1.20 0.80 0.40 x
③ 2a 2.40 1.60 0.80 0.40 0.40
A.实验①,0~20 min,v(N )=1.00×10-5 mol·L-1·min-1
2
B.实验②,60 min时处于平衡状态,x≠0.40
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
2.(2021·辽宁,12)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓
度及时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是( )
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大C.条件①,反应速率为0.012 mol·L-1·min-1
D.条件②,降冰片烯起始浓度为3.0 mol·L-1时,半衰期为62.5 min
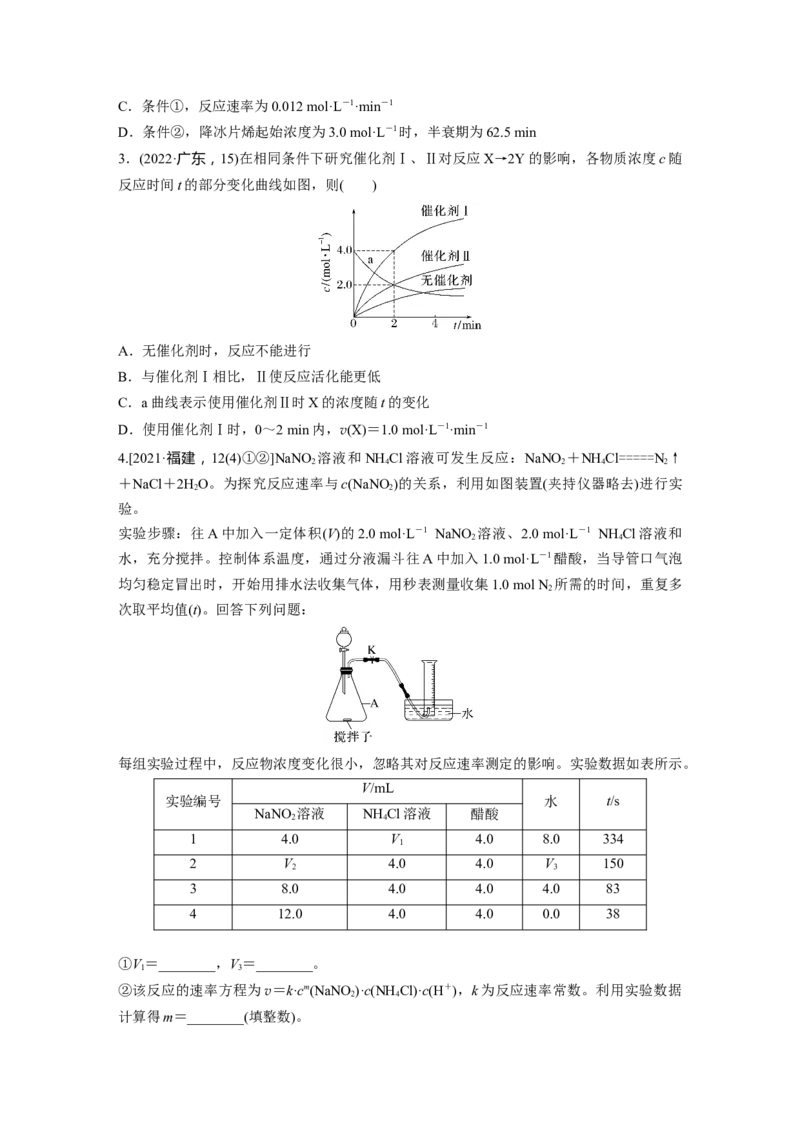
3.(2022·广东,15)在相同条件下研究催化剂Ⅰ、Ⅱ对反应X→2Y的影响,各物质浓度c随
反应时间t的部分变化曲线如图,则( )
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时,0~2 min内,v(X)=1.0 mol·L-1·min-1
4.[2021·福建,12(4)①②]NaNO 溶液和NH Cl溶液可发生反应:NaNO +NH Cl=====N↑
2 4 2 4 2
+NaCl+2HO。为探究反应速率与c(NaNO )的关系,利用如图装置(夹持仪器略去)进行实
2 2
验。
实验步骤:往A中加入一定体积(V)的2.0 mol·L-1 NaNO 溶液、2.0 mol·L-1 NH Cl溶液和
2 4
水,充分搅拌。控制体系温度,通过分液漏斗往A中加入1.0 mol·L-1醋酸,当导管口气泡
均匀稳定冒出时,开始用排水法收集气体,用秒表测量收集1.0 mol N 所需的时间,重复多
2
次取平均值(t)。回答下列问题:
每组实验过程中,反应物浓度变化很小,忽略其对反应速率测定的影响。实验数据如表所示。
V/mL
实验编号 水 t/s
NaNO 溶液 NH Cl溶液 醋酸
2 4
1 4.0 V 4.0 8.0 334
1
2 V 4.0 4.0 V 150
2 3
3 8.0 4.0 4.0 4.0 83
4 12.0 4.0 4.0 0.0 38
①V=________,V=________。
1 3
②该反应的速率方程为v=k·cm(NaNO )·c(NH Cl)·c(H+),k为反应速率常数。利用实验数据
2 4
计算得m=________(填整数)。