文档内容
易错点 8 金属材料
易错题【01】两性氢氧化物
(1)“两性”是指既具有酸性氧化物性质(能与碱反应生成盐和水),又具有具有碱性氧
化物的性质(能与酸反应生成盐和水)。
(2)分离提纯含铝物质:利用Al、Al O、Al(OH) 可溶于强碱的特性,可除去许多物质中
2 3 3
的含铝杂质(括号内为杂质):Mg(Al):加足量NaOH溶液;Fe O(AlO):加足量NaOH
2 3 2 3
溶液;Mg(OH) [Al(OH) ]:加足量NaOH溶液。Mg2+(Al3+):加过量NaOH溶液,过滤,
2 3
再加酸充分溶解。
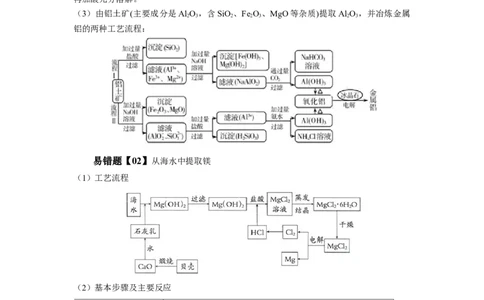
(3)由铝土矿(主要成分是Al O ,含SiO 、Fe O 、MgO等杂质)提取Al O ,并冶炼金属
2 3 2 2 3 2 3
铝的两种工艺流程:
易错题【02】从海水中提取镁
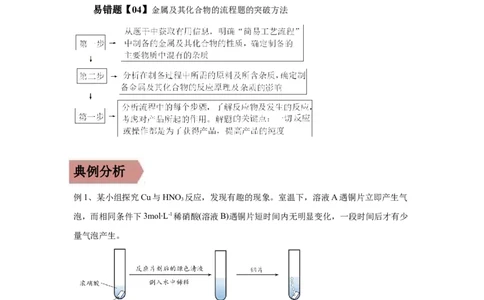
(1)工艺流程
(2)基本步骤及主要反应
易错题【03】常见金属的冶炼方法工业上通常利用CO还原氧化铁的方法来炼铁,采用电解熔融氧化铝的方法冶炼铝,采用
电解熔融氯化镁的方法冶炼镁。
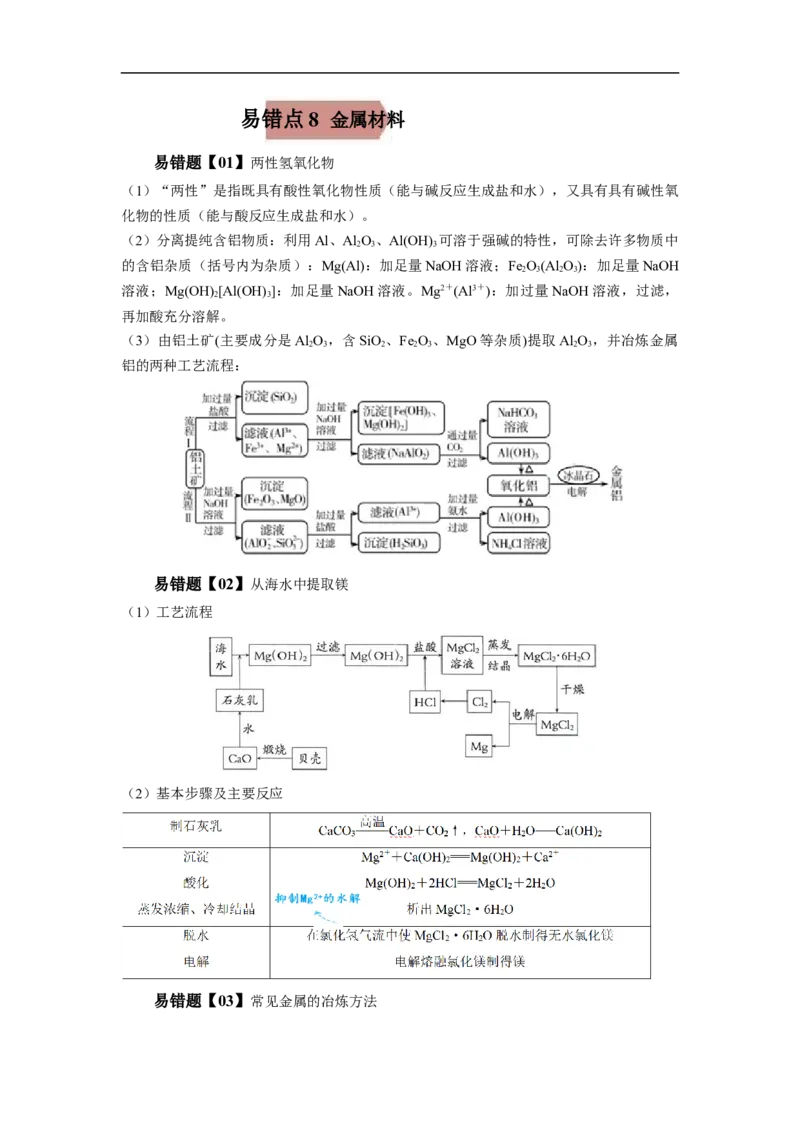
易错题【04】金属及其化合物的流程题的突破方法
典例分析
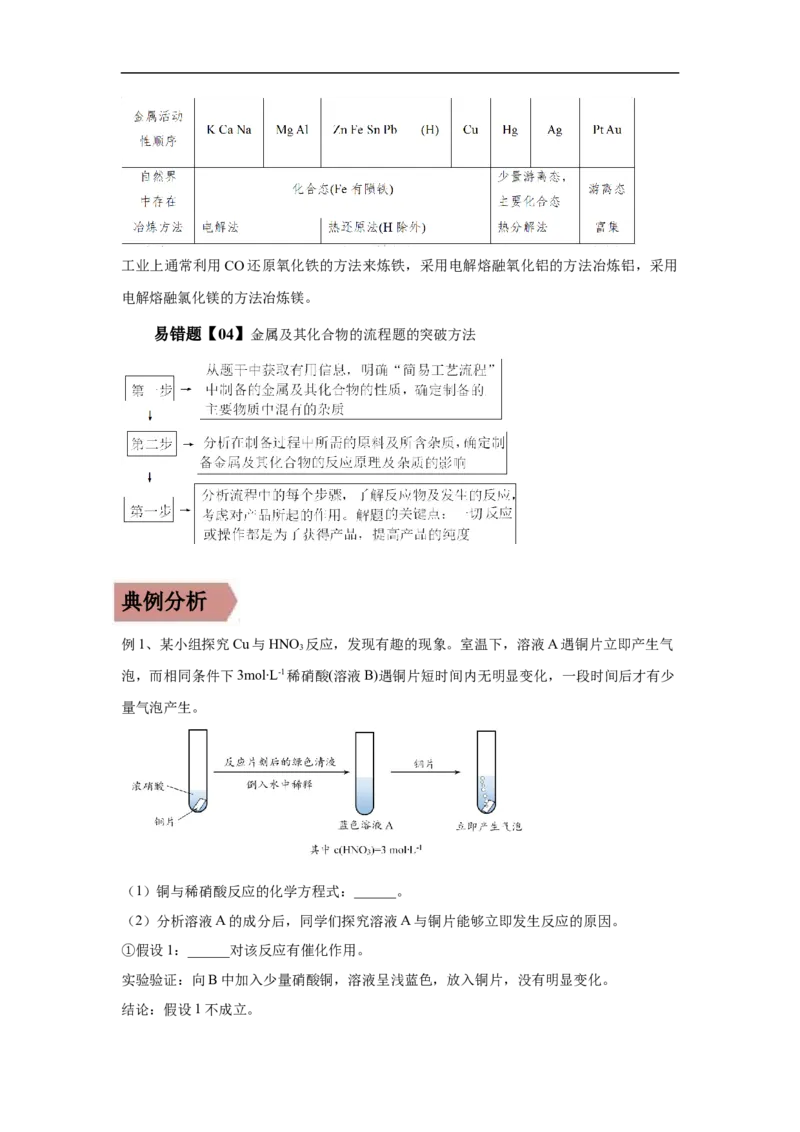
例1、某小组探究Cu与HNO 反应,发现有趣的现象。室温下,溶液A遇铜片立即产生气
3
泡,而相同条件下3mol∙L-1稀硝酸(溶液B)遇铜片短时间内无明显变化,一段时间后才有少
量气泡产生。
(1)铜与稀硝酸反应的化学方程式:______。
(2)分析溶液A的成分后,同学们探究溶液A与铜片能够立即发生反应的原因。
①假设1:______对该反应有催化作用。
实验验证:向B中加入少量硝酸铜,溶液呈浅蓝色,放入铜片,没有明显变化。
结论:假设1不成立。②假设2:NO 对该反应有催化作用。
2
方案1:向放有铜片的B中通入少量NO ,铜片表面立即产生气泡,反应持续进行。有同
2
学认为应补充对比实验:向放有铜片的B中加入数滴5mol∙L-1硝酸,无明显变化。补充该
实验的目的是______。
方案2:向A中鼓入N 数分钟得溶液C。相同条件下,铜片与A、B、C溶液的反应速率:
2
v(A)>v(C)>v(B)。该实验能够证明假设2成立的理由是______。
③经检验,A溶液中还含有少量HNO。实验证明HNO 也对该反应有催化作用,操作和现
2 2
象是:向含有铜片的B溶液中______。
结论:NO 和HNO 对铜与硝酸的反应都有催化作用。
2 2
(3)请推测Cu与稀硝酸反应中NO 和HNO 参与的可能催化过程:
2 2
①Cu+2NO+2H+=Cu2++2HNO
2 2
②______。
③______。
【答案】(1)3Cu+8HNO (稀)=3Cu(NO)+2NO↑+4HO
3 3 2 2
(2)①Cu2+
②排除通NO 带来的硝酸浓度增大的影响;鼓入N 可以带走溶液中的NO ,因此三份溶液
2 2 2
中NO 的浓度A>C>B,反应速率随NO 浓度降低而减慢,说明NO 对该反应有催化作用
2 2 2
③加入少量的NaNO ,B中铜片上立即生成气泡,反应持续进行
2
(3)②NO +HNO +H+=2NO+H O
2 2 2
③2HNO=NO+NO +H O(或Cu+2HNO +2H+=Cu2++2NO+2HO等)
2 2 2 2 2
【解析】(1)铜与稀硝酸反应生成硝酸铜、一氧化氮和水,反应的化学方程式为
3Cu+8HNO (稀)=3Cu(NO)+2NO↑+4HO,故答案为:
3 3 2 2
3Cu+8HNO (稀)=3Cu(NO)+2NO↑+4HO;
3 3 2 2
(2)①由实验设计和实验结论可知,假设1为铜离子对铜与硝酸的反应有催化作用,故答
案为:Cu2+;
②由假设2可知,方案1设计的目的是通过向含有铜片的B溶液中通入二氧化氮,反应速
率明显加快,而含有铜片的B溶液中滴入稀硝酸,反应无明显变化证明二氧化氮与水反应
生成生成硝酸,硝酸浓度增大对铜与硝酸的反应速率加快无影响;方案2设计的目的是通
过向含有铜片的A溶液中通入氮气排出溶液中的二氧化氮,降低溶液中二氧化氮的浓度得
到溶液中二氧化氮浓度大的A、二氧化氮浓度小的C和没有二氧化氮的B三组对比实验,由反应速率v(A)>v(C)>v(B)证明二氧化氮的浓度越大,对铜与硝酸的反应催化效果越好,
从而说明二氧化氮对铜与硝酸的反应有催化作用,故答案为:排除通NO 带来的硝酸浓度
2
增大的影响;鼓入N 可以带走溶液中的NO ,因此三份溶液中NO 的浓度A>C>B,反应
2 2 2
速率随NO 浓度降低而减慢,说明NO 对该反应有催化作用;
2 2
③由实验目的可知,向含有铜片的B溶液中加入亚硝酸钠后,亚硝酸钠与溶液中的硝酸反
应生成亚硝酸,亚硝酸浓度增大,若铜片上立即生成气泡,反应持续进行证明亚硝酸对铜
与硝酸的反应有催化作用,故答案为:加入少量的NaNO ,B中铜片上立即生成气泡,反
2
应持续进行;
(3)由铜与稀硝酸反应的方程式和反应①可知,若二氧化氮和亚硝酸参与反应,反应②和
③中硝酸和亚硝酸应是反应的反应物,一氧化氮和二氧化氮是反应的生成物,则反应②可
能为硝酸与亚硝酸反应生成二氧化氮和水,反应③可能为亚硝酸分解生成一氧化氮、二氧
化氮和水或铜与硝酸、亚硝酸反应生成硝酸铜、一氧化氮和水,反应的离子方程式为NO
+HNO +H+=2NO+H O、2HNO=NO+NO +H O(或Cu+2HNO +2H+=Cu2++2NO+2HO等),
2 2 2 2 2 2 2 2
故答案为:NO +HNO +H+=2NO+H O;2HNO=NO+NO +H O(或Cu+2HNO +2H+=Cu2+
2 2 2 2 2 2 2
+2NO+2HO等)。
2
例2、我国C919大飞机制造过程中用到的某些新型材料是以氯化亚铜作催化剂制备的。
氯化亚铜是白色粉末,不溶于水、乙醇、硫酸,在空气中迅速被氧化成绿色。某实验小组
设计如下装置,用二氧化硫、硫酸铜和氯化钠制备氯化亚铜。
(1)装置A是制备二氧化硫的装置,A中反应方程式是________________,反应不选用稀
硫酸的原因是________________。
(2)装置B的作用是________________。
(3)装置C中主要发生了两个反应,通入二氧化硫前,CuSO 与NaCl在溶液中反应生成
4Na[CuCl ]和NaSO 混合溶液,反应的离子方程式为________________;将SO 通入上述
2 4 2 4 2
溶液中,Na[CuCl ]转化为CuCl沉淀和茶褐色的NaH[CuCl ]溶液,反应中的还原产物为
2 4 3
_____________。
(4)在无氧的条件下,向三颈烧瓶中加水稀释,NaH[CuCl ]会完全水解转化为CuCl沉淀,
3
完全沉淀的实验现象为____________ ,请用化学平衡移动原理解释转化
的原因_____________。
(5)完全反应后,倾出清液,抽滤出沉淀,沉淀依次用水、无水乙醇洗涤多次,干燥得白
色粉末固体,用无水乙醇洗涤的目的是_____________。
(6)以碳棒为电极电解CuCl 溶液也可得到CuCl。写出电解CuCl 溶液后的阴极上发生的
2 2
反应为 ,生成1molCuCl,阳极上生成物的物质的量为_____。
【答案】(1)NaSO +H SO (浓)==Na SO +SO↑+H O 二氧化硫易溶于水,稀硫酸不
2 3 2 4 2 4 2 2
利于二氧化硫的逸出(2)做安全瓶,防倒吸(3)Cu2++4Cl—=[CuCl ]2— CuCl 和
4
NaH[CuCl ](4)溶液由茶褐色变为无色 稀释时生成物浓度减小大于反应物,平衡正向移
3
动(5)加快去除CuCl表面水,分防止CuCl氧化(6)Cu2++Cl-+e-=CuCl↓ 0.5mol
【解析】(1)亚硫酸钠与浓硫酸反应生成二氧化硫气体,反应的化学方程式为:
NaSO +H SO (浓)═NaSO +SO↑+H O;因为二氧化硫易溶于水,如果用稀硫酸制备二
2 3 2 4 2 4 2 2
氧化硫,不利于二氧化硫的逸出;(2)装置B为空载仪器,可以防止二氧化硫易溶于水
而产生倒吸;(3)由题意可知,通入二氧化硫前,CuSO 与NaCl在溶液中反应生成络合
4
物Na[CuCl ]和NaSO 混合溶液,反应的离子方程式为:Cu2++4Cl—=[CuCl ]2—;Na[CuCl ]
2 4 2 4 4 2 4
中铜元素为+2价,CuCl和NaH[CuCl ]中铜元素化合价均为+1价,将SO 通入上述溶液中,
3 2
Na[CuCl ]转化为CuCl沉淀和茶褐色的NaH[CuCl ]溶液,说明Na[CuCl ]被二氧化硫还原
2 4 3 2 4
为 CuCl 和 NaH[CuCl ] ; ( 4 ) NaH[CuCl ] 加 水 水 解 的 方 程 式 为 :
3 3
NaH[CuCl ]+H O=NaCl+HCl+CuCl↓,为防止CuCl被氧化,应该在无氧环境中进行反应,
3 2
完全反应后茶褐色的NaH[CuCl ]溶液转化为无色的NaCl和HCl混合液;由方程式可知,
3
稀释时生成物浓度减小大于反应物,平衡正向移动;(5)因乙醇沸点低,易挥发,用乙醇
洗涤,可快速除去固体表面的水分,防止CuCl氧化;(6)电解池中阴极发生还原反应,
元素化合价降低,CuCl 中Cu是+2价,CuCl中Cu是+1价,所以阴极上发生的反应是Cu2
2
++Cl-+e-=CuCl↓,阳极上Cl-放电被氧化生成氯气,电极反应式为2Cl-—2e-=Cl↑,由
2
得失电子数目守恒可知,生成1mol CuCl,阳极上生成Cl 的物质的量为0.5mol。
2
例3、利用铝锂钴废料(主要成分为Co O ,还含有少量铝箔、LiCoO 等杂质) 制备CoO的
3 4 2工艺流程如下图所示:
已知:I.
II、Al(OH) 在pH为5. 2沉淀完全。
3
III、LiF的Ksp为1. 8×10-3
请回答下列问题:
(1)“碱溶”时为提高浸出率可采取的措施是 (写一种即可),并写出主要
的离子反应方程式 ;
(2)“酸溶”时最佳的浸出剂应选择 ,并说明理由 。
(3)“酸溶”后,滤液②中加入 NaCO 溶液调节 pH 为 4~6目的是 。
2 3
(4)“净化”时加NaF目的是沉淀Li+,当滤液③中c(F-)= 4. 0×10-3mol·L-1 时计算净化后
残余 c(Li+)= mol·L-1
(5)写出滤渣②酸溶后与草酸铵反应的离子反应方程式 。
【答案】(1)搅拌(答案合理即可) 2Al+2OH-+2H O=2AlO-+3H ↑
2 2 2
(2)HSO +Na SO 两种浸出剂对钴的浸出率差别不大,但是HCl与Co O 会发生反应
2 4 2 2 3 3 4
产生Cl,直接排放会污染空气,不符合绿色化学思想。
2
(3)除去滤液②中残留的 Al3+
(4)0. 45
(5)Co2++C O2-+2H O=CoC O·2H O↓
2 4 2 2 4 2
【解析】(1)“碱溶”时主要是铝箔与氢氧化钠溶液反应,其离子反应方程式为:
2Al+2OH-+2H O=2AlO-+3H ↑
2 2 2
(2)从钴浸出率数据来看,选择浸出剂HCl显然效果最好,但是其与Co O 会发生反应
3 4
Co O+2Cl-+8H+=3Co2++Cl↑+4H O,其氧化产物Cl 直接排放会污染空气,不符合绿色化学
3 4 2 2 2思想。因此结合浸出率和绿色化学综合考量,选择“HSO +Na SO”作为浸出剂。
2 4 2 2 3
(3)结合浸出液化学成分及信息Al(OH) 在 pH为5. 2沉淀完全同时抓住调节 pH为4~
3
6可知目的是为了除去滤液②中残留的 Al3+。
(4)c(Li+)= Ksp(LiF) / c(F-)= 1. 8×10-3 /4. 0×10-3mol·L-1 = 0. 45mol·L-1
(5)滤渣②酸溶后钴元素以Co2+形式存在,所以离子反应方程式为:Co2++C O2-
2 4
+2H O=CoC O·2H O↓
2 2 4 2
1.武当山金殿是铜铸鎏金大殿。传统鎏金工艺是将金溶于汞中制成“金汞漆”,涂在器物
表面,然后加火除汞,使金附着在器物表面。下列说法错误的是
A.鎏金工艺利用了汞的挥发性 B.鎏金工艺中金发生了化学反应
C.鎏金工艺的原理可用于金的富集 D.用电化学方法也可实现铜上覆金
2.北京冬奥会备受世界瞩目。下列说法错误的是
A.冰壶主材料花岗岩属于无机非金属材料
B.火炬“飞扬”使用的碳纤维属于有机高分子材料
C.冬奥会“同心”金属奖牌属于合金材料
D.短道速滑服使用的超高分子量聚乙烯属于有机高分子材料
3.《本草图经》有“白矾多入药用”。白矾[KAl(SO)·12H O]又称明矾、钾明矾等,是一
4 2 2
种重要的化学试剂。下列说法正确的是
A.白矾可用于自来水杀菌消毒
B.白矾溶液中n(K+):n(Al3+)=1:1
C.白矾溶液可清洗铜镜表面铜锈
D.灼烧白矾时可直接观察焰色呈紫色
4.下列说法错误的是
A.纯铁比生铁易生锈 B.臭氧可用于自来水消毒
C.酚醛树脂可用作绝缘、隔热材料 D.高纯硅可用于制芯片
5.中华文明源远流长,在世界文明中独树一帜,汉字居功至伟。随着时代发展,汉字被不
断赋予新的文化内涵,其载体也发生相应变化。下列汉字载体主要由合金材料制成的是汉字
载体
选项 A.兽骨 B.青铜器 C.纸张 D.液晶显示屏
6.近年我国在科学技术领域取得了举世瞩目的成就。对下列成就所涉及的化学知识的判断
错误的是
A.北斗三号卫星搭载了精密计时的铷原子钟,铷(Rb)是金属元素
B.奋斗者号潜水器载人舱外壳使用了钛合金,钛合金属于无机非金属材料
C.长征五号B遥二火箭把天和核心舱送入太空,火箭动力源于氧化还原反应
D.天问一号探测器着陆火星过程中使用了芳纶制作的降落伞,芳纶是高分子材料
7.化学与生活密切相关,下列不涉及化学变化的是
A.加入明矾后泥水变澄清 B.北京冬奥会用水快速制冰
C.炖排骨汤时加点醋味道更鲜 D.切开的茄子放置后切面变色
8.北京时间2022年4月16日9时56分,神舟十三号载人飞船返回舱在东风着陆场成功着
陆,神舟十三号载人飞行任务取得圆满成功。下列说法错误的是
A.飞船逃逸系统复合材料中的酚醛树脂由加聚反应获得
B.飞船返回舱表面的耐高温陶瓷材料,属于新型无机非金属材料
C.空间站舷你使用的耐辐射石英玻璃的主要成分为SiO
2
D.运载火箭加注的液氢燃料是高能清洁燃料
9.下列说法不正确的是
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
C.氧化铝熔点高,常用于制造耐高温材料
D.用石灰石-石膏法对燃煤烟气进行脱硫,同时可得到石膏
10.劳动开创未来。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 面包师用小苏打作发泡剂烘焙面包 可与酸反应
B 环保工程师用熟石灰处理酸性废水 熟石灰具有碱性C 工人将模具干燥后再注入熔融钢水 铁与 高温下会反应
D 技术人员开发高端耐腐蚀镀铝钢板 铝能形成致密氧化膜
11.能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH+2H O=AlO +4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO +CO +H O=HSiO +HCO
2 2
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H+
2 4 4
+SO =BaSO ↓+2H O
4 2
12.“矾”是一类金属硫酸盐的结晶水合物,在生活和生产中有着重要应用,下列有关
“矾”的说法正确的是
A.蓝矾(CuSO ·5H O)是一种纯净物,可用于检验酒精中是否含有水
4 2
B.明矾[KAl(SO)·12H O]常用于净水,其水溶液显中性
4 2 2
C.铁铵矾[NH Fe(SO )·12H O]是一种媒染剂,其中Fe的化合价为+3价
4 4 2 2
D.皓矾(ZnSO·7H O)常用作医学收敛剂,铁单质与其溶液反应能置换出Zn
4 2
13.一种工业制备无水氯化镁的工艺流程如下:
下列说法错误的是
A.物质X常选用生石灰
B.工业上常用电解熔融 制备金属镁
C.“氯化”过程中发生的反应为
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水
14.铝电解厂烟气净化的一种简单流程如下:下列说法错误的是
A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有 和
D.滤液可回收进入吸收塔循环利用
15.硼酸(H BO)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼
3 3
镁矿(含MgB O·H O、SiO 及少量Fe O、Al O)为原料生产硼酸及轻质氧化镁的工艺流程
2 2 5 2 2 2 3 2 3
如图:
已知:HBO 的解离反应:HBO+H O H++[B(OH) ]-,K =5.81×10-10。下列说法不正确
3 3 3 3 2 4 a
的是
A.在95℃“溶浸”硼镁矿粉,产生的气体为NH
3
B.可选用KCSN溶液检验“过滤1”后的滤液中是否含有Fe3+离子
C.在“过滤2”前,将溶液pH调节至3.5,主要目的是除去Fe3+和Al3+
D.HBO 与足量NaOH溶液反应的化学方程式:NaOH+H BO=Na[B(OH) ]
3 3 3 3 4
16.钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为 ,含少量
V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:已知“降温收尘”后,粗 中含有的几种物质的沸点:
物质
沸点/ 136 127 57 180
回答下列问题:
(1)已知 , 的值只决定于反应体系的始态和终态,忽略 、 随温度的
变化。若 ,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进
行的是_______。
A. B.
C. D.
(2) 与C、 ,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
物质
分压
①该温度下, 与C、 反应的总化学方程式为_______;②随着温度升高,尾气中 的含量升高,原因是_______。
(3)“除钒”过程中的化学方程式为_______;“除硅、铝”过程中,分离 中含 、
杂质的方法是_______。
(4)“除钒”和“除硅、铝”的顺序_______(填“能”或“不能”)交换,理由是_______。
(5)下列金属冶炼方法与本工艺流程中加入 冶炼 的方法相似的是_______。
A.高炉炼铁
B.电解熔融氯化钠制钠
C.铝热反应制锰
D.氧化汞分解制汞
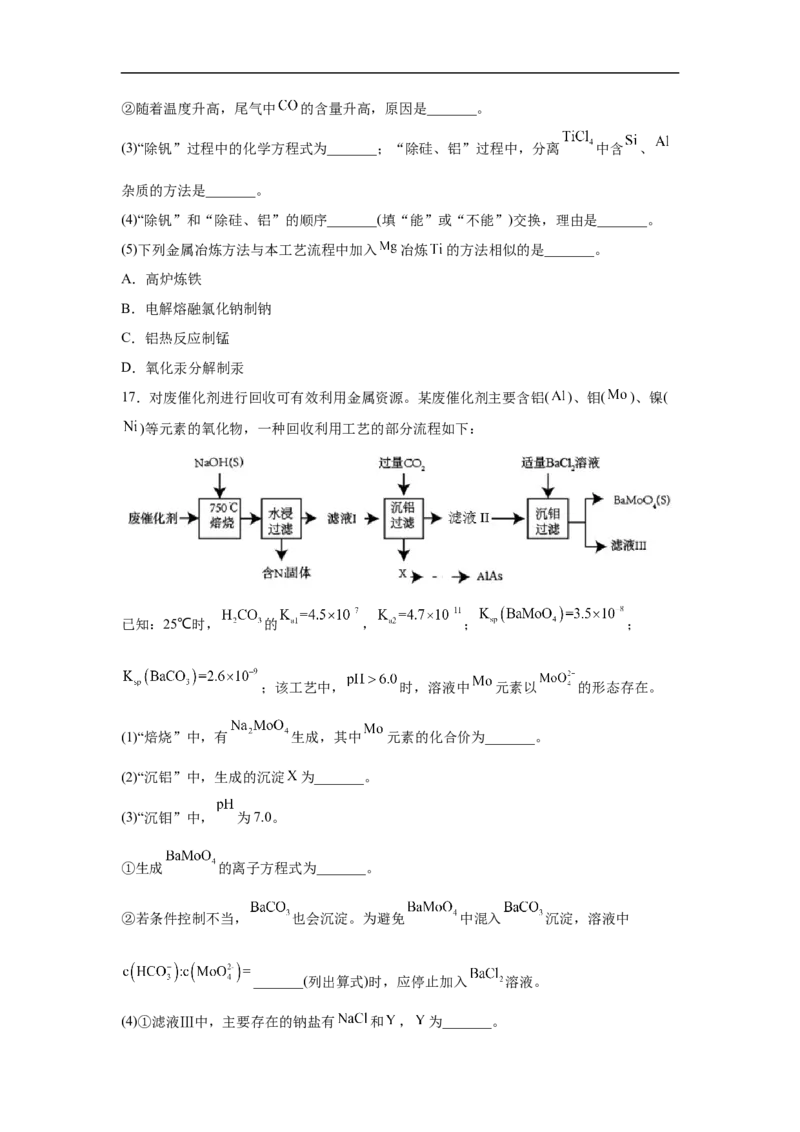
17.对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼( )、镍(
)等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25℃时, 的 , ; ;
;该工艺中, 时,溶液中 元素以 的形态存在。
(1)“焙烧”中,有 生成,其中 元素的化合价为_______。
(2)“沉铝”中,生成的沉淀 为_______。
(3)“沉钼”中, 为7.0。
①生成 的离子方程式为_______。
②若条件控制不当, 也会沉淀。为避免 中混入 沉淀,溶液中
_______(列出算式)时,应停止加入 溶液。
(4)①滤液Ⅲ中,主要存在的钠盐有 和 , 为_______。②往滤液Ⅲ中添加适量 固体后,通入足量_______(填化学式)气体,再通入足量 ,
可析出 。
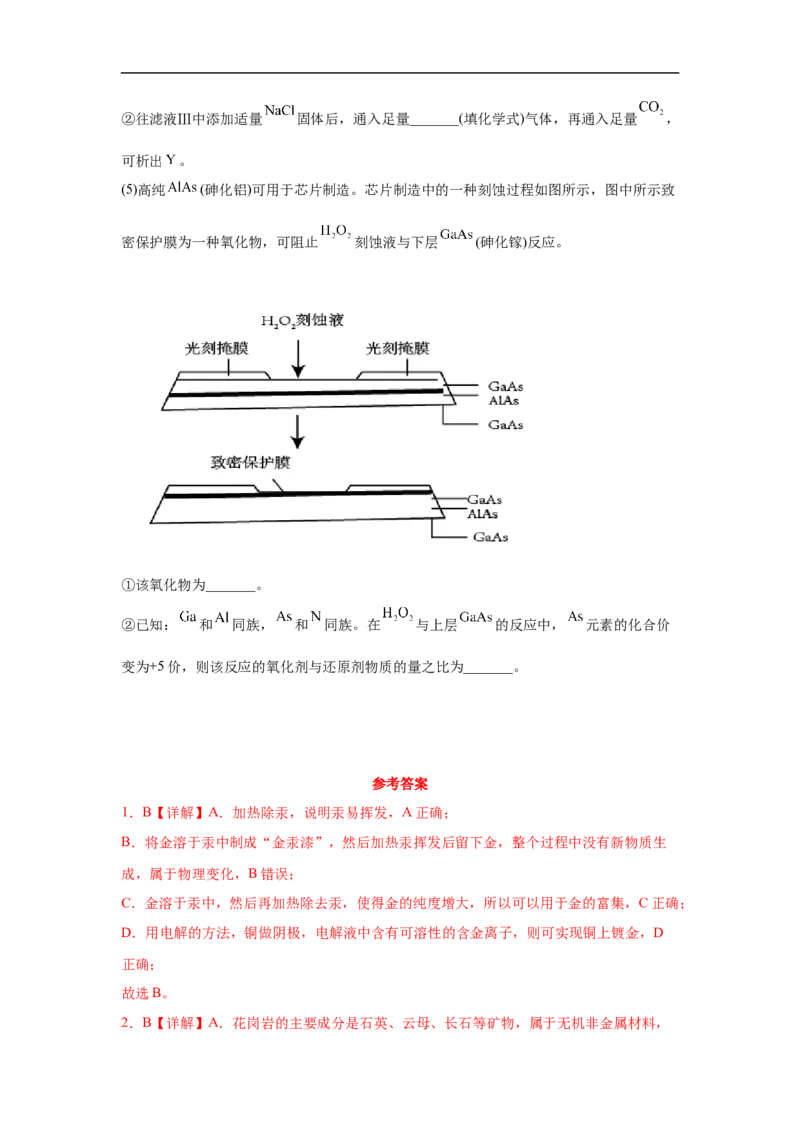
(5)高纯 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致
密保护膜为一种氧化物,可阻止 刻蚀液与下层 (砷化镓)反应。
①该氧化物为_______。
②已知: 和 同族, 和 同族。在 与上层 的反应中, 元素的化合价
变为+5价,则该反应的氧化剂与还原剂物质的量之比为_______。
参考答案
1.B【详解】A.加热除汞,说明汞易挥发,A正确;
B.将金溶于汞中制成“金汞漆”,然后加热汞挥发后留下金,整个过程中没有新物质生
成,属于物理变化,B错误;
C.金溶于汞中,然后再加热除去汞,使得金的纯度增大,所以可以用于金的富集,C正确;
D.用电解的方法,铜做阴极,电解液中含有可溶性的含金离子,则可实现铜上镀金,D
正确;
故选B。
2.B【详解】A.花岗岩的主要成分是石英、云母、长石等矿物,属于无机非金属材料,A正确;
B.碳纤维指的是含碳量在90%以上的高强度高模量纤维,属于无机非金属材料,B错误;
C.金属奖牌属于合金材料,C正确;
D.聚乙烯属于有机高分子材料,D正确;
故答案选B。
3.C【详解】A.白矾不具有强氧化性,不能杀菌消毒,故A错误;
B.Al3+是弱碱根离子,发生水解,因此白矾溶液中n(K+)∶n(Al3+)>1∶1,故B错误;
C.Al3+是弱碱根离子,发生水解,其水解方程式为Al3++3H O Al(OH) +3H+,溶液显
2 3
酸性,铜锈主要成分是Cu (OH) CO,能与酸反应,因此白矾溶液可清洗铜镜表面铜锈,
2 2 3
故C正确;
D.需要通过蓝色钴玻璃观察,故D错误;
答案为C。
4.A【详解】A.由于生铁发生电化学腐蚀,而纯铁只能发生化学腐蚀,故生铁比纯铁易
生锈,A错误;
B.臭氧具有强氧化性,能使蛋白质发生变性,可用于自来水消毒,B正确;
C.酚醛树脂具有空间立体网状结构,具有热固体,绝缘性,故可用作绝缘、隔热材料,C
正确;
D.高纯硅是良好的半导体材料,可用于制芯片,D正确;
故答案为:A。
5.B【详解】A.兽骨,甲骨文的契刻载体之一,主要是牛的肩胛骨,一小部分是羊、猪、
鹿的肩胛骨,还有极少部分的牛肋骨,其主要成分是碳酸钙和其它钙盐,故A不符合题意;
B.青铜器是红铜与其他化学元素锡、铅等的合金,属于合金材料,故B项符合题意;
C.纸张的主要成分是纤维素,故C不符合题意;
D.液晶显示器是一种采用液晶为材料的显示器,液晶是一类介于固态和液态间的有机化
合物,故D不符合题意;
综上所述,答案为B项。
6.B【详解】A.铷位于周期表第六周期第ⅠA族,属于碱金属,属于铷(Rb)是金属元素,
故A正确;
B.钛合金为合金,属于金属材料,故B错误;
C.火箭动力源于火箭燃料的燃烧,属于氧化还原反应,故C正确;D.芳纶属于合成纤维,是高分子材料,故D正确;
故选B。
7.B【详解】A.明矾净水的原理为: , 胶体具有吸
附性,可以使泥水变澄清,涉及化学变化,A错误;
B.水和冰的分子式都是HO,水快速制冰为物理变化,B正确;
2
C.炖排骨汤时放点醋,可使骨头中的钙、磷、铁等矿物质溶解出来,营养值更价高。此
外,醋还可以防止食物中的维生素被破坏,涉及化学变化,C错误;
D.茄子中存在一类叫“酚氧化酶”的物质,它见到氧气之后,发生化学反应产生一些有
色的物质。反应时间越长,颜色越深,D错误;
故选B。
8.A【详解】A.酚醛树脂由苯酚和甲醛通过缩聚反应获得,故A不正确;
B.耐高温陶瓷材料主要含有硅元素,属于新型无机非金属材料,故B正确;
C.石英玻璃的主要成分为SiO,故C正确;
2
D.液氢燃料燃烧产物是水,故属于清洁燃料,故D正确;
故选答案A。
9.A【详解】A.晶体硅的导电性介于导体和绝缘体之间,是良好的半导体材料,可用于
制造晶体管、集成电路等,而二氧化硅常用于制造光导纤维,A错误;
B.钠的焰色反应为黄色,可用作透雾能力强的高压钠灯,B正确;
C.耐高温材料应具有高熔点的性质,氧化铝熔点高,可用作耐高温材料,C正确;
D.石灰石的主要成分为碳酸钙,石灰石-石膏法脱硫过程中发生反应:CaCO
3
CaO+CO ↑,SO +CaCO =CaSO +CO ,2CaSO+O =2CaSO ,得到了石膏,D正确;
2 2 3 3 2 3 2 4
答案选A。
10.A【详解】A.小苏打是碳酸氢钠,不是碳酸钠,主要用来做膨松剂,故A符合题意;
B.熟石灰是氢氧化钙,具有碱性,可以用于处理酸性废水,故B不符合题意;
C.熔融的铁与水蒸气在高温下反应会生成四氧化三铁和氢气,因此必须将模具干燥,故C
不符合题意;
D.钢板上镀铝,保护钢板,金属铝表面形成致密氧化膜而保护金属铝不被腐蚀,,故D
不符合题意。
综上所述,答案为A。
11.D【详解】A.硝酸具有强氧化性,可以将S2-氧化为S单质,自身根据其浓度大小还原为NO或NO ,反应的离子方程式为4H++2NO +S2-=S↓+2NO↑+2H O(浓)或8H++2NO
2 2 2
+3S2-=3S↓+2NO↑+4H O(稀),A错误;
2
B.明矾在水中可以电离出Al3+,可以与氨水电离出的OH-发生反应生成Al(OH) ,但由于
3
氨水的碱性较弱,生成的Al(OH) 不能继续与弱碱发生反应,故反应的离子方程式为Al3+
3
+3NH·H O=Al(OH) ↓+3NH ,B错误;
3 2 3
C.硅酸的酸性小于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳则
根据其通入的量的多少反应为碳酸根或碳酸氢根,反应的离子方程式为SiO
+H O+CO=H SiO↓+CO (CO 少量)或SiO +2H O+2CO=H SiO↓+2HCO (CO 过量),C
2 2 2 3 2 2 2 2 3 2
错误;
D.将等物质的量浓度的Ba(OH) 与NH HSO 溶液以体积比1:2混合,Ba(OH) 电离出的
2 4 4 2
OH-与NH HSO 电离出的H+反应生成水,Ba(OH) 电离出的Ba2+与NH HSO 电离出的SO
4 4 2 4 4
反应生成BaSO 沉淀,反应的离子方程为为Ba2++2OH-+2H++SO =BaSO ↓+2H O,D正确;
4 4 2
故答案选D。
12.C【详解】A.无水硫酸铜遇水变蓝,可用于检验酒精中是否含有水,而蓝矾
(CuSO ·5H O)不能,故A错误;
4 2
B.明矾[KAl(SO4) ·12H O]在水中电离出的铝离子很容易水解生成氢氧化铝胶体,水溶液
2 2
显酸性,故B错误;
C.铁铵矾[NH Fe(SO4) ·12H O]中,铵根显+1价,硫酸根显-2价,故铁元素显 +3价,故
4 2 2
C正确;
D.铁单质金属活动性顺序排在Zn之后,不能皓矾溶液反应能置换出Zn,故D错误;
故答案选C。
13.D【详解】海水经一系列处理得到苦卤水,苦卤水中含Mg2+,苦卤水中加物质X使
Mg2+转化为Mg(OH) ,过滤除去滤液,煅烧Mg(OH) 得MgO,MgO和C、Cl 经“氯化”
2 2 2
得无水MgCl 。
2
A.物质X的作用是使Mg2+转化为Mg(OH) ,工业上常采用CaO,发生
2CaO+H O=Ca(OH) ,Ca(OH) +Mg2+=Mg(OH) +Ca2+,A正确;
2 2 2 2
B.Mg是较活泼金属,工业上常用电解熔融 制备金属镁,B正确;
C.由图可知“氯化”过程反应物为MgO、氯气、C,生成物之一为MgCl ,C在高温下能
2
将二氧化碳还原为CO,则“气体”为CO,反应方程式为 ,C
正确;
D.“煅烧”后得到MgO,MgO和盐酸反应得到MgCl 溶液,由于MgCl 在溶液中水解为
2 2
氢氧化镁和HCl,将所得溶液加热蒸发HCl会逸出,MgCl 水解平衡正向移动,得到氢氧
2
化镁,得不到无水MgCl ,D错误;
2
选D。
14.C【详解】烟气(含HF)通入吸收塔,加入过量的碳酸钠,发生反应
,向合成槽中通入NaAlO ,发生反应
2
,过滤得到 和含有 的
滤液。
A.陶瓷的成分中含有SiO,SiO 能与烟气中的HF发生反应,因此不宜用陶瓷作吸收塔内
2 2
衬材料,故A正确;
B.采用溶液喷淋法可增大反应物的接触面积,提高吸收塔内烟气吸收效率,故B正确;
C.由上述分析可知,合成槽内发生反应 ,产物是
和 ,故C错误;
D.由上述分析可知,滤液的主要成分为 ,可进入吸收塔循环利用,故D正确;
答案选C。
15.C【详解】硼镁矿(含MgB O•H O、SiO 及少量Fe O、Al O)加入硫酸铵溶液,得到
2 2 5 2 2 2 3 2 3
气体,根据硼镁矿和硫酸铵化学式知,得到的气体应为NH ,用NH HCO 吸收NH 得到
3 4 3 3
(NH )CO;过滤得到的滤渣I应为难溶与硫酸铵溶液的SiO、Fe O、Al O;调节滤液
4 2 3 2 2 3 2 3pH=3.5再过滤得到HBO,此时滤液中主要含有MgSO ,向滤液中加入碳酸铵进行沉镁,
3 3 4
得到Mg(OH) •MgCO,加热分解可以得到轻质MgO;母液中含有(NH )SO ,以此解答该
2 3 4 2 4
题。
A.溶浸时,主要是硼镁矿和硫酸铵反应,根据流程可知该过程有氨气产生,结合元素守
恒可得该过程的化学方程式为MgB O•H O+2(NH )SO =4NH↑+2MgSO +2H BO,产生的
2 2 5 2 4 2 4 3 4 3 3
气体为NH ,A正确
3
B. Fe3+和KSCN溶液混合得到血红色液体,所以可以用KSCN溶液检验铁离子,B正确;
C.在“过滤2”前,将溶液pH调节至3.5,目的是有利于析出HBO,C错误;
3 3
D.HBO 存在解离反应:HBO+H O H++[B(OH) ]-,加入NaOH消耗氢离子,促进
3 3 3 3 2 4
平衡正向移动,Na+结合[B(OH) ]-生成Na[B(OH) ],反应的化学方程式:
4 4
NaOH+H BO=Na[B(OH) ],D正确;
3 3 4
故选:C。
16.(1)C
(2) 5TiO+6C+10Cl 5TiCl +2CO+4CO 随着温度升高,CO 与C发生反应
2 2 4 2 2
(3) 3VOCl +Al=3VOCl +AlCl 蒸馏
3 2 3
(4) 不能 若先“除硅、铝”再“除钒”,“除钒”时需要加入Al,又引入Al
杂质;
(5)AC
【解析】钛渣中加入C、Cl 进行沸腾氯化,转化为相应的氯化物,降温收尘后得到粗
2
TiCl ,加入单质Al除钒,再除硅、铝得到纯TiCl ,加入Mg还原得到Ti。
4 4
(1)① ,② ,③ ,
④ ;
A.由图可知,600℃时 的 ,反应自发进行,故A不符合题意;B.由图可知,600℃时 的 ,反应自发进行,故B不符合题意;
C.由图可知,600℃时 的 ,反应不能自发进行,故
C符合题意;
D.根据盖斯定律, 可由①+③得到,则600℃时其
,反应自发进行,故D不符合题意;
故选C;
(2)①根据表中数据可知,该温度下C主要生成CO和CO,根据相同条件下气体的压强之
2
比是物质的量之比可知TiCl 、CO和CO 的物质的量之比约是5:2:4,所以TiO 与C、
4 2 2
Cl 反应的总化学方程式为5TiO+6C+10Cl 5TiCl +2CO+4CO ,故答案为:
2 2 2 4 2
5TiO+6C+10Cl 5TiCl +2CO+4CO ;
2 2 4 2
②随着温度升高,CO 与C发生反应 ,导致CO含量升高,故答案为:随
2
着温度升高,CO 与C发生反应 ;
2
(3)“降温收尘”后钒元素主要以VOCl 形式存在,加入Al得到VOCl 渣,根据得失电子守
3 2
恒和元素守恒配平方程式为3VOCl +Al=3VOCl +AlCl ;AlCl 、SiCl 与TiCl 沸点差异较大,
3 2 3 3 4 4
“除硅、铝"过程中可采用蒸馏的方法分离AlCl 、SiCl ,故答案为:
3 4
3VOCl +Al=3VOCl +AlCl ;蒸馏;
3 2 3
(4)若先“除硅、铝”再“除钒”,“除钒”时需要加入Al,又引入Al杂质,因此“除
钒”和“除硅、铝”的顺序不能交换,故答案为:不能;若先“除硅、铝”再“除钒”,
“除钒”时需要加入Al,又引入Al杂质;
(5)本工艺中加入Mg冶炼Ti的方法为热还原法;
A.高炉炼铁的原理是用还原剂将铁矿石中铁的氧化物还原成金属铁,属于热还原法,故A符合题意;
B.电解熔融氯化钠制取金属钠的原理是电解法,故B不符合题意;
C.铝热反应制锰是利用Al作还原剂,将锰从其化合物中还原出来,为热还原法,故C符
合题意;
D.Hg为不活泼金属,可以直接用加热分解氧化汞的方法制备汞,故D不符合题意;
故答案选AC,故答案为:AC。
17.(1)+6(2) (3)① + = ↓②
(4)① ② (5)① ②
【解析】由题中信息可知,废催化剂与氢氧化钠一起焙烧后,铝和钼都发生了反应分别转
化为偏铝酸钠和钼酸钠,经水浸、过滤,分离出含镍的固体滤渣,滤液I中加入过量的二
氧化碳,偏铝酸钠转化为氢氧化铝沉淀,过滤得到的沉淀X为氢氧化铝,滤液II中加入适
量的氯化钡溶液沉钼后,过滤得到钼酸钡。
(1)“焙烧”中,有 生成,其中Na和O的化合价为+1和-2,根据化合价的代
数和为0可知, 元素的化合价为+6。
(2)“沉铝”中,偏铝酸钠转化为氢氧化铝,因此,生成的沉淀 为 。
(3)①滤液II中含有钼酸钠,加入氯化钡溶液后生成 沉淀,该反应的离子方程式
为 + = ↓。
②若开始生成 沉淀,则体系中恰好建立如下平衡:
,该反应的化学平衡常数为
。为避免 中混入 沉淀,必须满足 ,由于“沉钼”中 为
7.0, ,所以溶液中 时,开始生
成 沉淀,因此,
时,应停止加入 溶液。
(4)①滤液I中加入过量的二氧化碳,偏铝酸钠转化为氢氧化铝沉淀,同时生成碳酸氢钠,
过滤得到的滤液II中含有碳酸氢钠和钼酸钠。滤液II中加入适量的氯化钡溶液沉钼后,因
此,过滤得到的滤液Ⅲ中,主要存在的钠盐有 和 ,故 为 。
②根据侯氏制碱法的原理可知,往滤液Ⅲ中添加适量 固体后,通入足量 ,再通入
足量 ,可析出 。
(5)①由题中信息可知,致密的保护膜为一种氧化物,是由 与 反应生成的,联
想到金属铝表面容易形成致密的氧化膜可知,该氧化物为 。
②由 和 同族、 和 同族可知, 中显+3价(其最高价)、 显-3价。在
与上层 的反应中, 元素的化合价变为+5价,其化合价升高了8, 元素被
氧化,则该反应的氧化剂为 ,还原剂为 。 中的O元素为-1价,其作为氧
化剂时,O元素要被还原到-2价,每个 参加反应会使化合价降低2,根据氧化还原反
应中元素化合价升高的总数值等于化合价降低的总数值可知,该反应的氧化剂与还原剂物质的量之比为 。