文档内容
第 35 讲 电解原理的综合应用
复习目标 提升应用电解原理解决工业生产、生活中实际问题的能力。
1.电解原理常见的考查点
电解原理及应用是高考高频考点,该类试题往往与生产、生活及新科技等相联系,以装置图
或流程图为载体呈现,题材广、信息新,题目具有一定难度。主要考查阴、阳极的判断、电
极反应式、电解反应方程式的书写、溶液离子浓度变化及有关计算等。
2.“5点”突破电解综合应用题
(1)分清阴、阳极,与电源正极相连的为阳极,与电源负极相连的为阴极,两极反应为“阳
氧阴还”。
(2)剖析离子移向,阳离子移向阴极,阴离子移向阳极。
(3)注意放电顺序,正确判断放电的微粒或物质。
(4)注意介质,正确判断反应产物,酸性介质不出现OH-,碱性介质不出现H+;不能想当然
地认为金属作阳极,电极产物为金属阳离子。
(5)注意得失电子守恒和电荷守恒,正确书写电极反应式。
一、电解原理在物质制备中的应用
1.(2021·广东1月适应性测试,13)环氧乙烷(C HO)常用于医用消毒,一种制备方法为:使
2 4
用惰性电极电解KCl溶液,用Cl-交换膜将电解液分为阴极区和阳极区,其中一区持续通入
乙烯;电解结束,移出交换膜,两区混合反应:HOCH CHCl+OH-===Cl-+HO+
2 2 2
C HO。下列说法错误的是( )
2 4
A.乙烯应通入阴极区
B.移出交换膜前存在反应:Cl+HOHCl+HClO
2 2
C.使用Cl-交换膜阻止OH-通过,可使Cl 生成区的pH逐渐减小
2
D.制备过程的总反应为HC===CH+HO===H+C HO
2 2 2 2 2 4
答案 A
解析 环氧乙烷的制备原理:Cl-在阳极失电子生成 Cl ,Cl 与水发生反应:Cl +
2 2 2
HOHCl+HClO,HClO与乙烯发生加成反应生成 HOCH CHCl;阴极区发生反应:
2 2 2
2HO+2e-===H↑+2OH-,电解结束,移出交换膜,两区混合反应: HOCH CHCl+OH
2 2 2 2
-===Cl-+HO+C HO。根据分析可知阳极区会生成HCl,使用Cl-交换膜阻止OH-通过,
2 2 4
HCl的浓度不断增大,pH逐渐减小,故C正确;根据分析可知该反应过程中KCl并没有被
消耗,实际上是水、乙烯反应,总反应为HC===CH+HO===H+C HO,故D正确。
2 2 2 2 2 4二、电解原理应用与污水处理
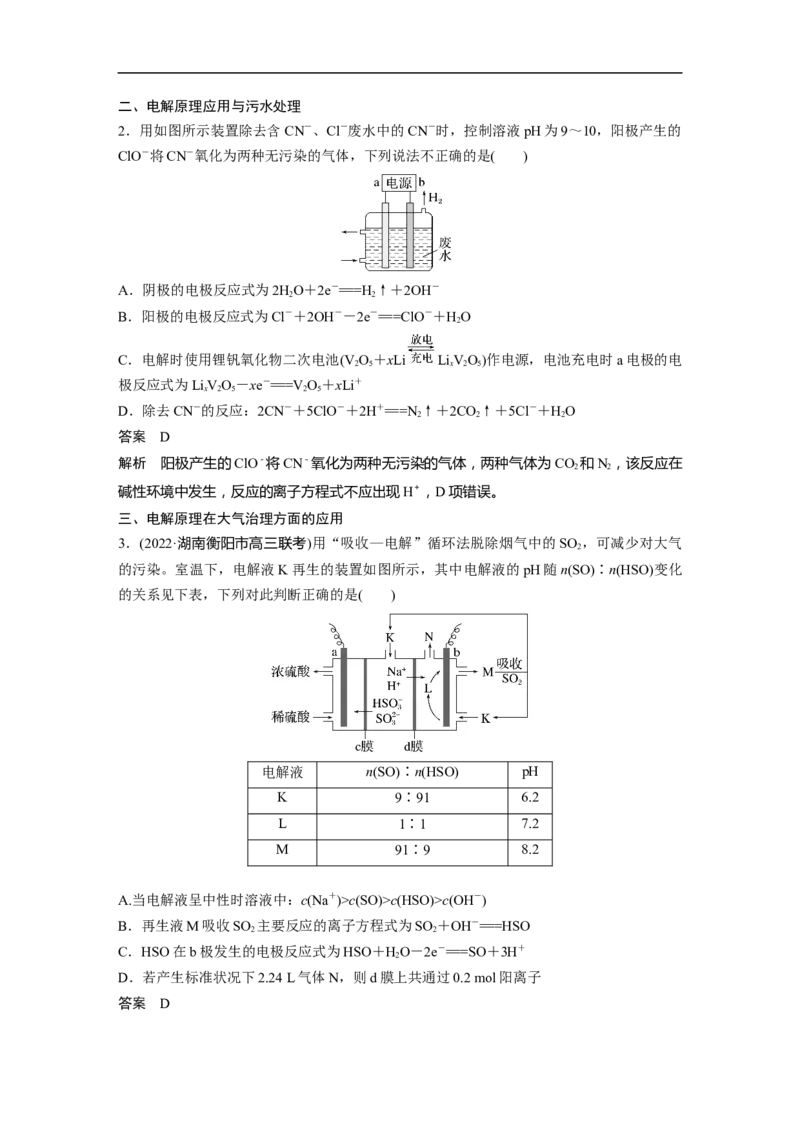
2.用如图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的
ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )
A.阴极的电极反应式为2HO+2e-===H↑+2OH-
2 2
B.阳极的电极反应式为Cl-+2OH--2e-===ClO-+HO
2
C.电解时使用锂钒氧化物二次电池(V O+xLi LiVO)作电源,电池充电时a电极的电
2 5 x 2 5
极反应式为LiVO-xe-===VO+xLi+
x 2 5 2 5
D.除去CN-的反应:2CN-+5ClO-+2H+===N↑+2CO↑+5Cl-+HO
2 2 2
答案 D
解析 阳极产生的ClO-将CN-氧化为两种无污染的气体,两种气体为CO 和N ,该反应在
2 2
碱性环境中发生,反应的离子方程式不应出现H+,D项错误。
三、电解原理在大气治理方面的应用
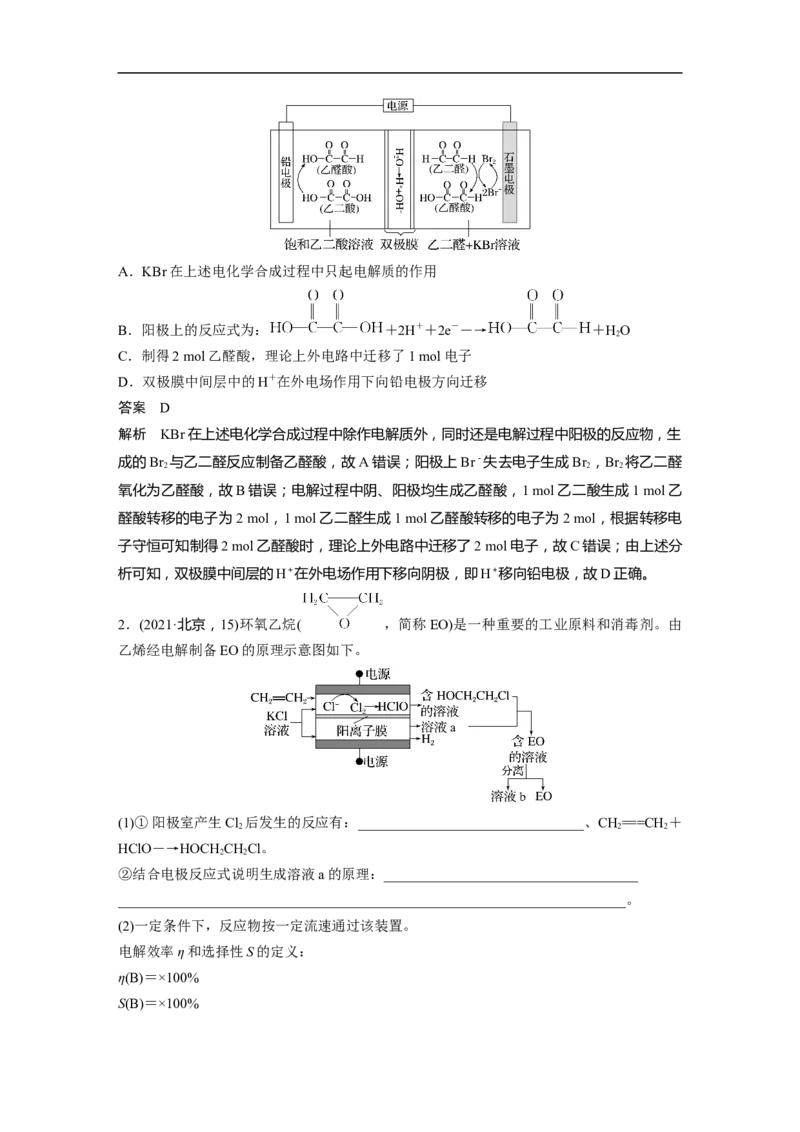
3.(2022·湖南衡阳市高三联考)用“吸收—电解”循环法脱除烟气中的SO ,可减少对大气
2
的污染。室温下,电解液K再生的装置如图所示,其中电解液的pH随n(SO)∶n(HSO)变化
的关系见下表,下列对此判断正确的是( )
电解液 n(SO)∶n(HSO) pH
K 9∶91 6.2
L 1∶1 7.2
M 91∶9 8.2
A.当电解液呈中性时溶液中:c(Na+)>c(SO)>c(HSO)>c(OH-)
B.再生液M吸收SO 主要反应的离子方程式为SO +OH-===HSO
2 2
C.HSO在b极发生的电极反应式为HSO+HO-2e-===SO+3H+
2
D.若产生标准状况下2.24 L气体N,则d膜上共通过0.2 mol阳离子
答案 D解析 根据装置图,阴离子通过c膜向a极移动,可知a极为阳极,发生的反应为HSO-2e
-+HO===SO+3H+;b 极为阴极,发生的反应为 2H++2e-===H↑,气体 N 为 H 。
2 2 2
n(SO)∶n(HSO)=9∶91时,电解液pH=6.2,n(SO)∶n(HSO)=1∶1时,电解液pH=7.2,
由此推知当电解液呈中性时,c(HSO)>c(SO),A项错误;M吸收SO 主要发生的反应为SO
2
+SO +HO===2HSO,B项错误;若产生标准状况下2.24 L气体N(0.1 mol H ),阴极消耗
2 2 2
0.2 mol H+,减少0.2 mol正电荷,需要补充0.2 mol正电荷以达到平衡,则d膜上会通过0.2
mol阳离子,D项正确。
四、电解原理应用与金属处理
4.(2022·浙江重点中学联考)电解精炼法提纯镓(Ga)是工业上常用的方法,具体原理如图所
示。已知:金属活动性顺序:Zn>Ga>Fe;镓的化学性质与铝相似。下列说法错误的是(
)
A.该装置中电流方向为N极→粗Ga→NaOH溶液→高纯Ga→M极
B.电解精炼镓时产生阳极泥的主要成分为Fe、Cu
C.阴极发生的电极反应为Ga3++3e-===Ga
D.电解过程中需控制合适的条件,否则阴极可能会产生H 导致电解效率下降
2
答案 C
解析 题图中粗Ga作阳极,纯Ga作阴极,N极为正极,M极为负极。电解池中电流由电
源正极流向电解池阳极,经过电解质溶液到达电解池阴极,再由阴极流向电源负极,A项正
确;根据题中给出的金属活动性顺序,镓比铁、铜活泼,故铁、铜在电解精炼过程中形成阳
极泥,B项正确;“镓的化学性质与铝相似”表明镓具有两性,结合电解质溶液显碱性,可
知“粗 Ga”阳极反应为 Ga-3e-+4OH-===GaO+2HO、Zn-2e-+4OH-===ZnO+
2
2HO,“高纯Ga”阴极反应为GaO+3e-+2HO===Ga+4OH-,C项错误;电解池中,若
2 2
电解质溶液为水溶液,阴极上会存在H+(或水电离出的H+)得电子被还原为H 的竞争反应,
2
若没控制合适的条件,该竞争反应可能会更明显,导致电解效率下降,D项正确。
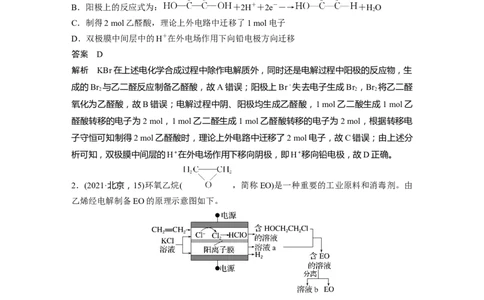
1.(2021·全国甲卷,13)乙醛酸是一种重要的化工中间体,可采用如图所示的电化学装置合
成。图中的双极膜中间层中的HO解离为H+和OH-,并在直流电场作用下分别向两极迁移。
2
下列说法正确的是( )A.KBr在上述电化学合成过程中只起电解质的作用
B.阳极上的反应式为: +2H++2e-―→ +HO
2
C.制得2 mol乙醛酸,理论上外电路中迁移了1 mol电子
D.双极膜中间层中的H+在外电场作用下向铅电极方向迁移
答案 D
解析 KBr在上述电化学合成过程中除作电解质外,同时还是电解过程中阳极的反应物,生
成的Br 与乙二醛反应制备乙醛酸,故A错误;阳极上Br-失去电子生成Br ,Br 将乙二醛
2 2 2
氧化为乙醛酸,故B错误;电解过程中阴、阳极均生成乙醛酸,1 mol乙二酸生成1 mol乙
醛酸转移的电子为2 mol,1 mol乙二醛生成1 mol乙醛酸转移的电子为2 mol,根据转移电
子守恒可知制得2 mol乙醛酸时,理论上外电路中迁移了2 mol电子,故C错误;由上述分
析可知,双极膜中间层的H+在外电场作用下移向阴极,即H+移向铅电极,故D正确。
2.(2021·北京,15)环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。由
乙烯经电解制备EO的原理示意图如下。
(1)①阳极室产生Cl 后发生的反应有:________________________________、CH===CH +
2 2 2
HClO―→HOCH CHCl。
2 2
②结合电极反应式说明生成溶液a的原理:____________________________________
________________________________________________________________________。
(2)一定条件下,反应物按一定流速通过该装置。
电解效率η和选择性S的定义:
η(B)=×100%
S(B)=×100%①若η(EO)=100%,则溶液b的溶质为________________________________________。
②当乙烯完全消耗时,测得η(EO)≈70%,S(EO)≈97%。推测η(EO)≈70%的原因:
Ⅰ.阳极有HO放电
2
Ⅱ.阳极有乙烯放电
Ⅲ.阳极室流出液中含有Cl 和HClO
2
……
i.检验电解产物,推测Ⅰ不成立。需要检验的物质是____________________。
ii.假设没有生成EO的乙烯全部在阳极放电生成CO ,则η(CO)≈________%。经检验阳极
2 2
放电产物没有CO。
2
iii.实验证实推测Ⅲ成立,所用试剂及现象是______________________。
可选试剂:AgNO 溶液、KI溶液、淀粉溶液、品红溶液
3
答案 (1)①Cl+HOHCl+HClO
2 2
②阴极反应:2HO+2e-===H↑+2OH-,K+穿过阳离子膜进入阴极室形成KOH
2 2
(2)①KCl ②i.O ii.13 iii.KI溶液和淀粉溶液,溶液变蓝(或品红溶液,品红褪色或KI溶
2
液,溶液变成棕黄色)
解析 (1)阳极产生氯气后,可以和水发生反应生成次氯酸,其化学方程式为 Cl +
2
HOHCl+ HClO;溶液a是阴极的产物,在阴极发生反应:2HO+2e-===H↑+2OH
2 2 2
-,同时阳极的钾离子会向阴极移动和氢氧根离子结合形成氢氧化钾。
(2)①若η(EO)=100%,则说明在电解过程中只有乙烯中的碳化合价发生变化,其他元素化
合价没有变化。②i.阳极有HO放电时会产生氧气,故需要检验的物质是O ;ii.设EO的物
2 2
质的量为a,则转化的乙烯的物质的量为;生成EO转化的电子的物质的量为2a;此过程转
移电子的总物质的量为;生成CO 的物质的量为2××3%;生成CO 转移的电子的物质的量
2 2
为2××3%×6,则η(CO)=≈13%。
2
iii.实验证实推测Ⅲ成立,则会产生氯气,验证氯气即可。
课时精练
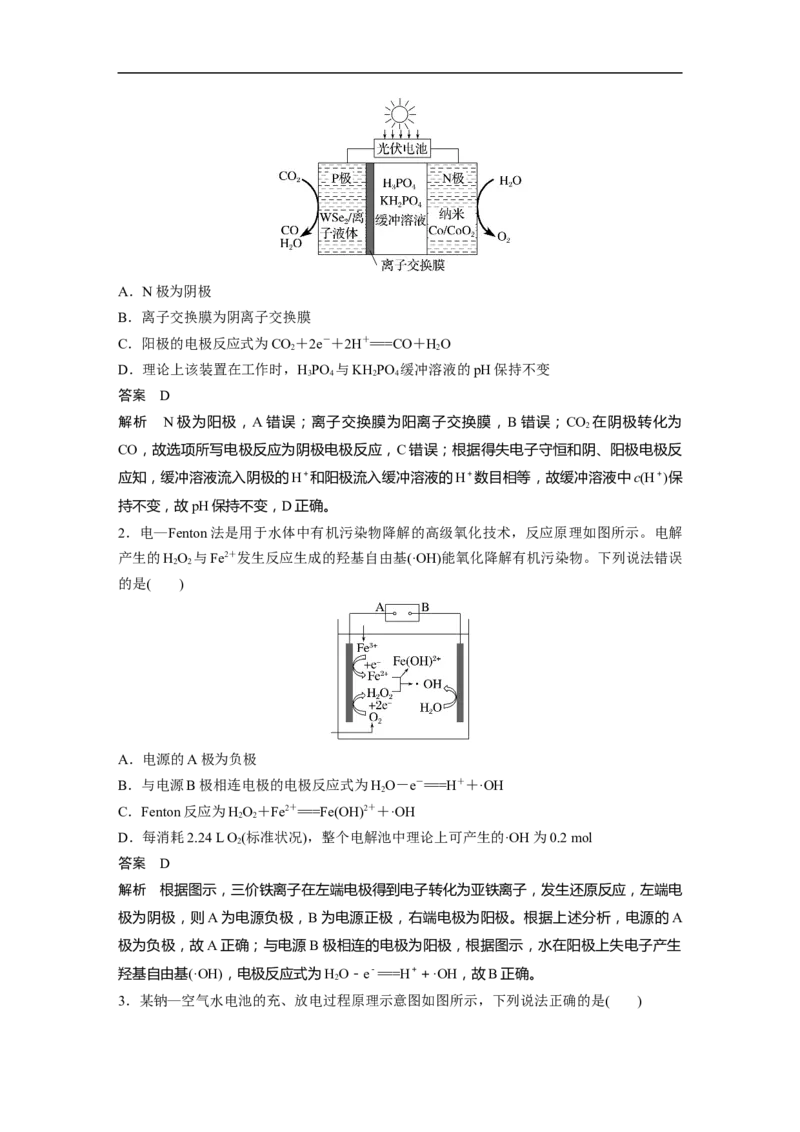
1.(2022·汕头市高三模拟)2021年3月5日,李克强总理在国务院政府报告中指出,扎实做
好碳达峰、碳中和各项工作。科研工作者通过开发新型催化剂,利用太阳能电池将工业排放
的CO 转化为CO,实现节能减排的目标。如图所示,下列有关说法正确的是( )
2A.N极为阴极
B.离子交换膜为阴离子交换膜
C.阳极的电极反应式为CO+2e-+2H+===CO+HO
2 2
D.理论上该装置在工作时,HPO 与KH PO 缓冲溶液的pH保持不变
3 4 2 4
答案 D
解析 N极为阳极,A错误;离子交换膜为阳离子交换膜,B错误;CO 在阴极转化为
2
CO,故选项所写电极反应为阴极电极反应,C错误;根据得失电子守恒和阴、阳极电极反
应知,缓冲溶液流入阴极的H+和阳极流入缓冲溶液的H+数目相等,故缓冲溶液中c(H+)保
持不变,故pH保持不变,D正确。
2.电—Fenton法是用于水体中有机污染物降解的高级氧化技术,反应原理如图所示。电解
产生的HO 与Fe2+发生反应生成的羟基自由基(·OH)能氧化降解有机污染物。下列说法错误
2 2
的是( )
A.电源的A极为负极
B.与电源B极相连电极的电极反应式为HO-e-===H++·OH
2
C.Fenton反应为HO+Fe2+===Fe(OH)2++·OH
2 2
D.每消耗2.24 L O (标准状况),整个电解池中理论上可产生的·OH为0.2 mol
2
答案 D
解析 根据图示,三价铁离子在左端电极得到电子转化为亚铁离子,发生还原反应,左端电
极为阴极,则A为电源负极,B为电源正极,右端电极为阳极。根据上述分析,电源的A
极为负极,故A正确;与电源B极相连的电极为阳极,根据图示,水在阳极上失电子产生
羟基自由基(·OH),电极反应式为HO-e-===H++·OH,故B正确。
2
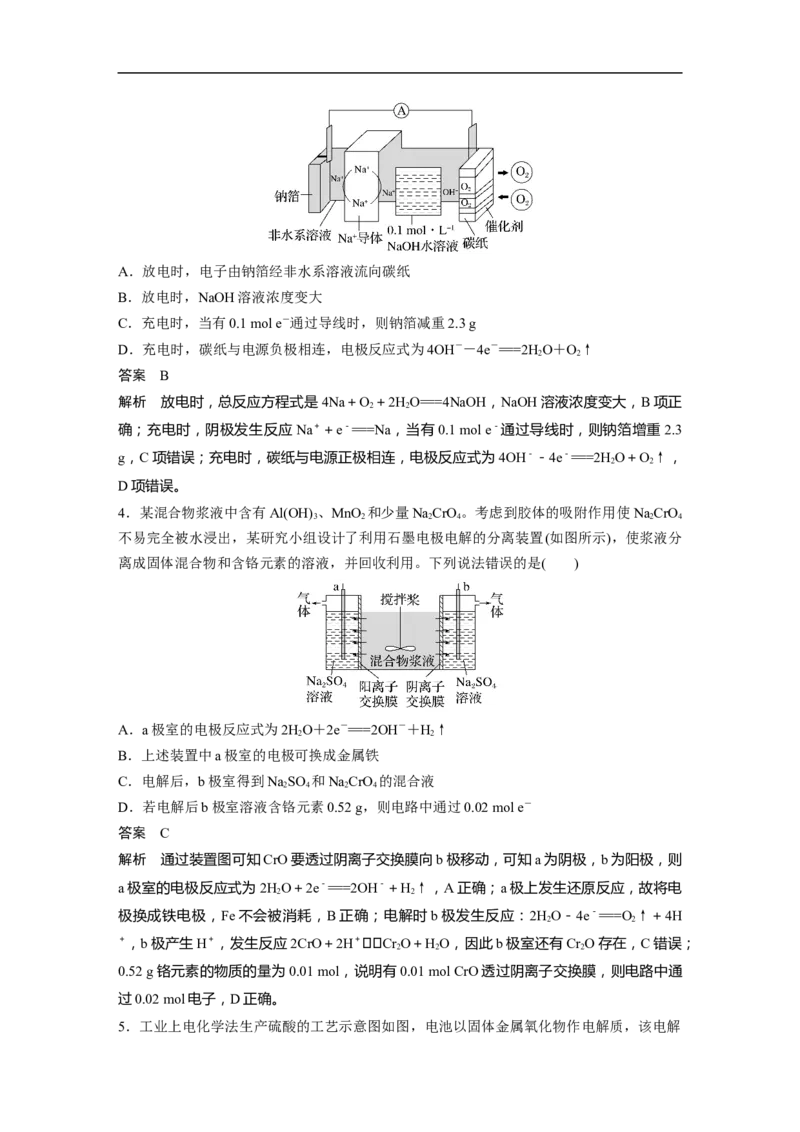
3.某钠—空气水电池的充、放电过程原理示意图如图所示,下列说法正确的是( )A.放电时,电子由钠箔经非水系溶液流向碳纸
B.放电时,NaOH溶液浓度变大
C.充电时,当有0.1 mol e-通过导线时,则钠箔减重2.3 g
D.充电时,碳纸与电源负极相连,电极反应式为4OH--4e-===2HO+O↑
2 2
答案 B
解析 放电时,总反应方程式是4Na+O +2HO===4NaOH,NaOH溶液浓度变大,B项正
2 2
确;充电时,阴极发生反应Na++e-===Na,当有0.1 mol e-通过导线时,则钠箔增重2.3
g,C项错误;充电时,碳纸与电源正极相连,电极反应式为4OH--4e-===2HO+O↑,
2 2
D项错误。
4.某混合物浆液中含有Al(OH) 、MnO 和少量NaCrO。考虑到胶体的吸附作用使NaCrO
3 2 2 4 2 4
不易完全被水浸出,某研究小组设计了利用石墨电极电解的分离装置(如图所示),使浆液分
离成固体混合物和含铬元素的溶液,并回收利用。下列说法错误的是( )
A.a极室的电极反应式为2HO+2e-===2OH-+H↑
2 2
B.上述装置中a极室的电极可换成金属铁
C.电解后,b极室得到NaSO 和NaCrO 的混合液
2 4 2 4
D.若电解后b极室溶液含铬元素0.52 g,则电路中通过0.02 mol e-
答案 C
解析 通过装置图可知CrO要透过阴离子交换膜向b极移动,可知a为阴极,b为阳极,则
a极室的电极反应式为2HO+2e-===2OH-+H↑,A正确;a极上发生还原反应,故将电
2 2
极换成铁电极,Fe不会被消耗,B正确;电解时b极发生反应:2HO-4e-===O↑+4H
2 2
+,b极产生H+,发生反应2CrO+2H+Cr O+HO,因此b极室还有Cr O存在,C错误;
2 2 2
0.52 g铬元素的物质的量为0.01 mol,说明有0.01 mol CrO透过阴离子交换膜,则电路中通
过0.02 mol电子,D正确。
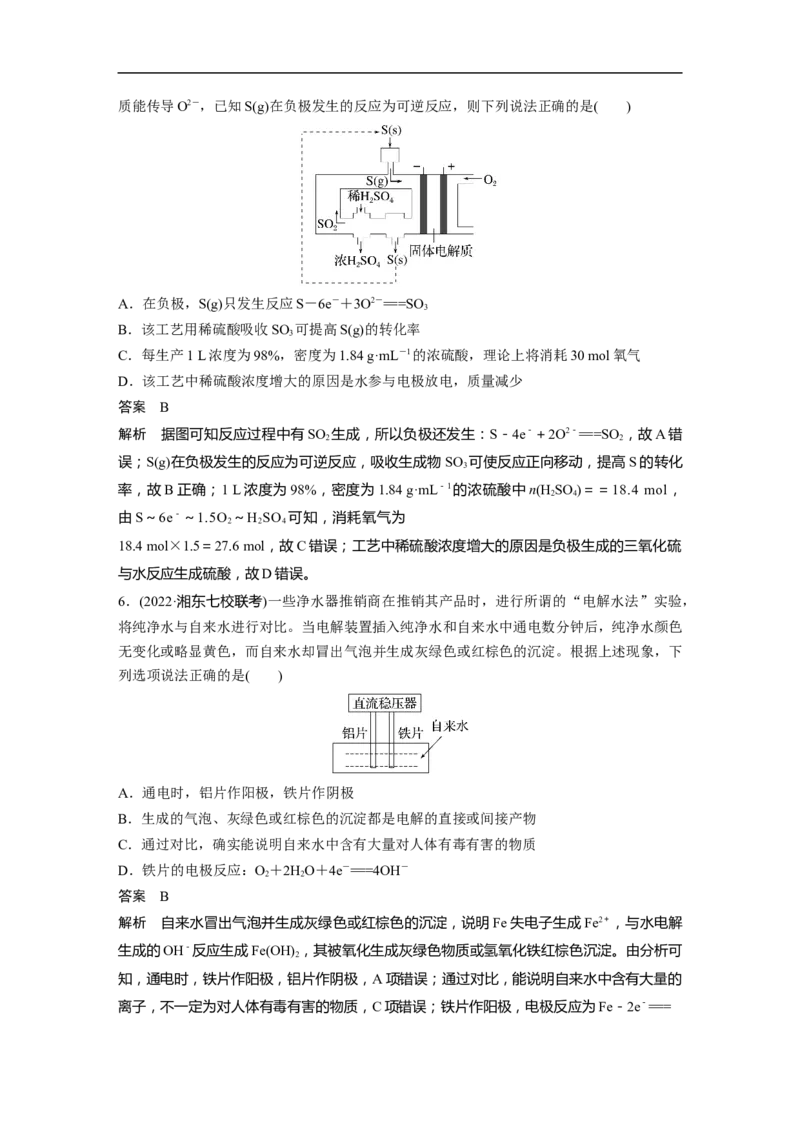
5.工业上电化学法生产硫酸的工艺示意图如图,电池以固体金属氧化物作电解质,该电解质能传导O2-,已知S(g)在负极发生的反应为可逆反应,则下列说法正确的是( )
A.在负极,S(g)只发生反应S-6e-+3O2-===SO
3
B.该工艺用稀硫酸吸收SO 可提高S(g)的转化率
3
C.每生产1 L浓度为98%,密度为1.84 g·mL-1的浓硫酸,理论上将消耗30 mol氧气
D.该工艺中稀硫酸浓度增大的原因是水参与电极放电,质量减少
答案 B
解析 据图可知反应过程中有SO 生成,所以负极还发生:S-4e-+2O2-===SO ,故A错
2 2
误;S(g)在负极发生的反应为可逆反应,吸收生成物SO 可使反应正向移动,提高S的转化
3
率,故B正确;1 L浓度为98%,密度为1.84 g·mL-1的浓硫酸中n(H SO )==18.4 mol,
2 4
由S~6e-~1.5O ~H SO 可知,消耗氧气为
2 2 4
18.4 mol×1.5=27.6 mol,故C错误;工艺中稀硫酸浓度增大的原因是负极生成的三氧化硫
与水反应生成硫酸,故D错误。
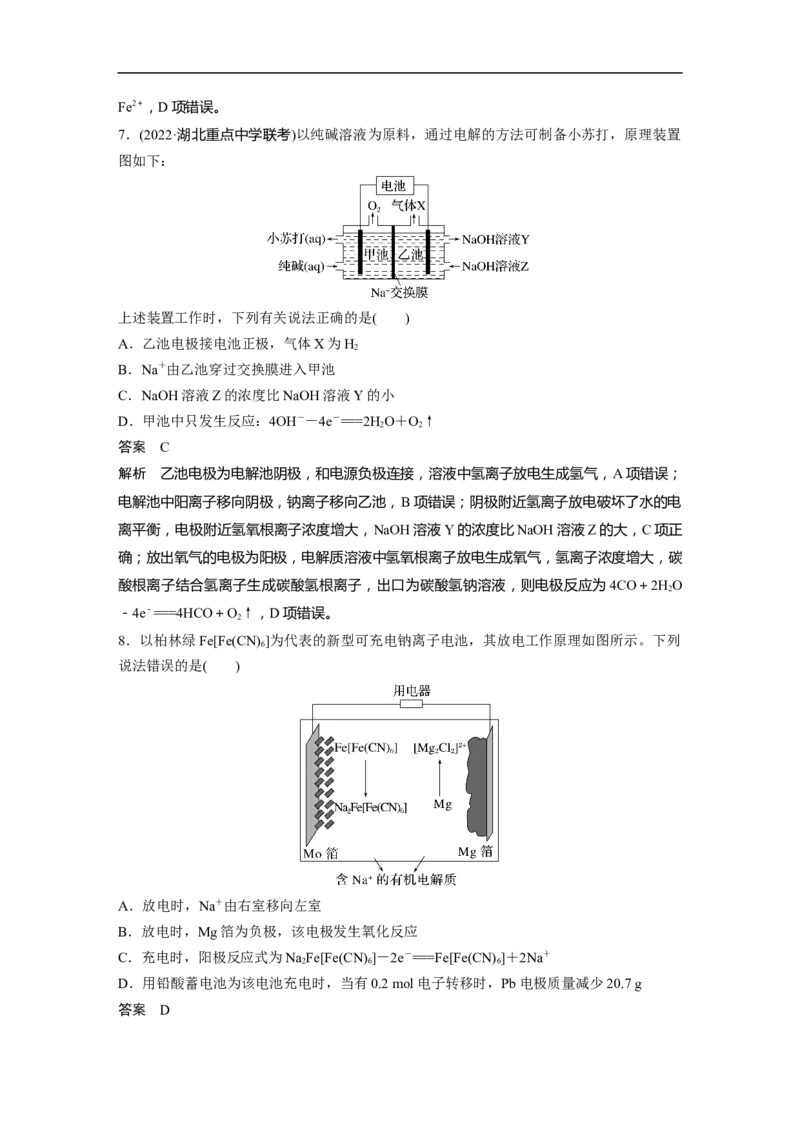
6.(2022·湘东七校联考)一些净水器推销商在推销其产品时,进行所谓的“电解水法”实验,
将纯净水与自来水进行对比。当电解装置插入纯净水和自来水中通电数分钟后,纯净水颜色
无变化或略显黄色,而自来水却冒出气泡并生成灰绿色或红棕色的沉淀。根据上述现象,下
列选项说法正确的是( )
A.通电时,铝片作阳极,铁片作阴极
B.生成的气泡、灰绿色或红棕色的沉淀都是电解的直接或间接产物
C.通过对比,确实能说明自来水中含有大量对人体有毒有害的物质
D.铁片的电极反应:O+2HO+4e-===4OH-
2 2
答案 B
解析 自来水冒出气泡并生成灰绿色或红棕色的沉淀,说明Fe失电子生成Fe2+,与水电解
生成的OH-反应生成Fe(OH) ,其被氧化生成灰绿色物质或氢氧化铁红棕色沉淀。由分析可
2
知,通电时,铁片作阳极,铝片作阴极,A项错误;通过对比,能说明自来水中含有大量的
离子,不一定为对人体有毒有害的物质,C项错误;铁片作阳极,电极反应为Fe-2e-===Fe2+,D项错误。
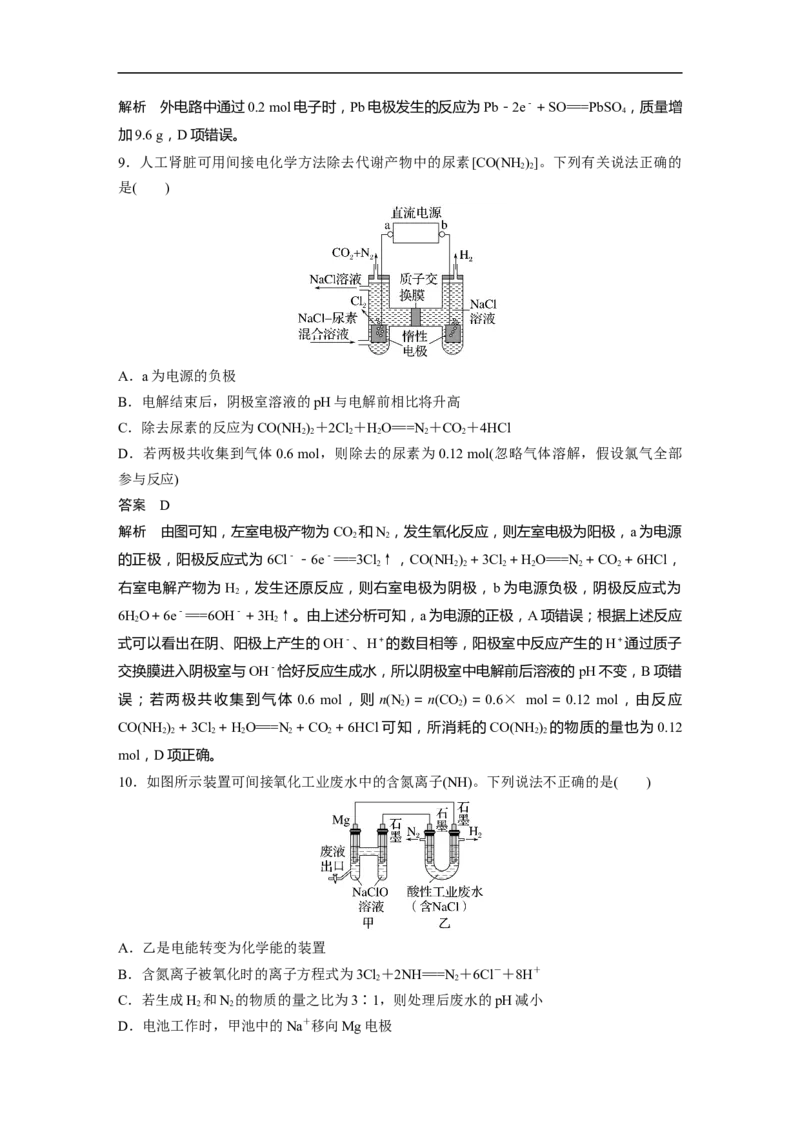
7.(2022·湖北重点中学联考)以纯碱溶液为原料,通过电解的方法可制备小苏打,原理装置
图如下:
上述装置工作时,下列有关说法正确的是( )
A.乙池电极接电池正极,气体X为H
2
B.Na+由乙池穿过交换膜进入甲池
C.NaOH溶液Z的浓度比NaOH溶液Y的小
D.甲池中只发生反应:4OH--4e-===2HO+O↑
2 2
答案 C
解析 乙池电极为电解池阴极,和电源负极连接,溶液中氢离子放电生成氢气,A项错误;
电解池中阳离子移向阴极,钠离子移向乙池,B项错误;阴极附近氢离子放电破坏了水的电
离平衡,电极附近氢氧根离子浓度增大,NaOH溶液Y的浓度比NaOH溶液Z的大,C项正
确;放出氧气的电极为阳极,电解质溶液中氢氧根离子放电生成氧气,氢离子浓度增大,碳
酸根离子结合氢离子生成碳酸氢根离子,出口为碳酸氢钠溶液,则电极反应为4CO+2HO
2
-4e-===4HCO+O↑,D项错误。
2
8.以柏林绿Fe[Fe(CN) ]为代表的新型可充电钠离子电池,其放电工作原理如图所示。下列
6
说法错误的是( )
A.放电时,Na+由右室移向左室
B.放电时,Mg箔为负极,该电极发生氧化反应
C.充电时,阳极反应式为NaFe[Fe(CN) ]-2e-===Fe[Fe(CN) ]+2Na+
2 6 6
D.用铅酸蓄电池为该电池充电时,当有0.2 mol电子转移时,Pb电极质量减少20.7 g
答案 D解析 外电路中通过0.2 mol电子时,Pb电极发生的反应为Pb-2e-+SO===PbSO ,质量增
4
加9.6 g,D项错误。
9.人工肾脏可用间接电化学方法除去代谢产物中的尿素[CO(NH)]。下列有关说法正确的
2 2
是( )
A.a为电源的负极
B.电解结束后,阴极室溶液的pH与电解前相比将升高
C.除去尿素的反应为CO(NH)+2Cl+HO===N+CO+4HCl
2 2 2 2 2 2
D.若两极共收集到气体0.6 mol,则除去的尿素为0.12 mol(忽略气体溶解,假设氯气全部
参与反应)
答案 D
解析 由图可知,左室电极产物为CO 和N,发生氧化反应,则左室电极为阳极,a为电源
2 2
的正极,阳极反应式为6Cl--6e-===3Cl↑,CO(NH) +3Cl +HO===N +CO +6HCl,
2 2 2 2 2 2 2
右室电解产物为 H ,发生还原反应,则右室电极为阴极,b为电源负极,阴极反应式为
2
6HO+6e-===6OH-+3H↑。由上述分析可知,a为电源的正极,A项错误;根据上述反应
2 2
式可以看出在阴、阳极上产生的OH-、H+的数目相等,阳极室中反应产生的H+通过质子
交换膜进入阴极室与OH-恰好反应生成水,所以阴极室中电解前后溶液的pH不变,B项错
误;若两极共收集到气体 0.6 mol,则 n(N )=n(CO)=0.6× mol=0.12 mol,由反应
2 2
CO(NH) +3Cl +HO===N +CO +6HCl可知,所消耗的CO(NH) 的物质的量也为0.12
2 2 2 2 2 2 2 2
mol,D项正确。
10.如图所示装置可间接氧化工业废水中的含氮离子(NH)。下列说法不正确的是( )
A.乙是电能转变为化学能的装置
B.含氮离子被氧化时的离子方程式为3Cl+2NH===N+6Cl-+8H+
2 2
C.若生成H 和N 的物质的量之比为3∶1,则处理后废水的pH减小
2 2
D.电池工作时,甲池中的Na+移向Mg电极答案 D
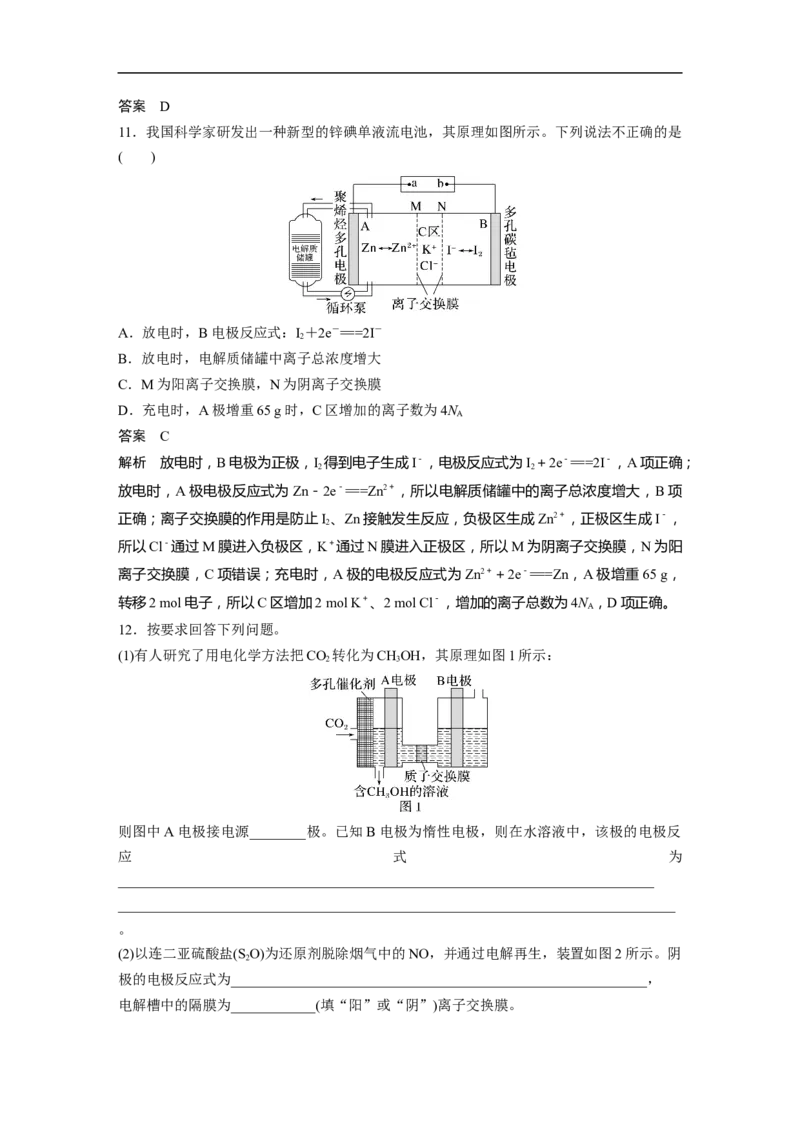
11.我国科学家研发出一种新型的锌碘单液流电池,其原理如图所示。下列说法不正确的是
( )
A.放电时,B电极反应式:I+2e-===2I-
2
B.放电时,电解质储罐中离子总浓度增大
C.M为阳离子交换膜,N为阴离子交换膜
D.充电时,A极增重65 g时,C区增加的离子数为4N
A
答案 C
解析 放电时,B电极为正极,I 得到电子生成I-,电极反应式为I+2e-===2I-,A项正确;
2 2
放电时,A极电极反应式为Zn-2e-===Zn2+,所以电解质储罐中的离子总浓度增大,B项
正确;离子交换膜的作用是防止I 、Zn接触发生反应,负极区生成Zn2+,正极区生成I-,
2
所以Cl-通过M膜进入负极区,K+通过N膜进入正极区,所以M为阴离子交换膜,N为阳
离子交换膜,C项错误;充电时,A极的电极反应式为Zn2++2e-===Zn,A极增重65 g,
转移2 mol电子,所以C区增加2 mol K+、2 mol Cl-,增加的离子总数为4N ,D项正确。
A
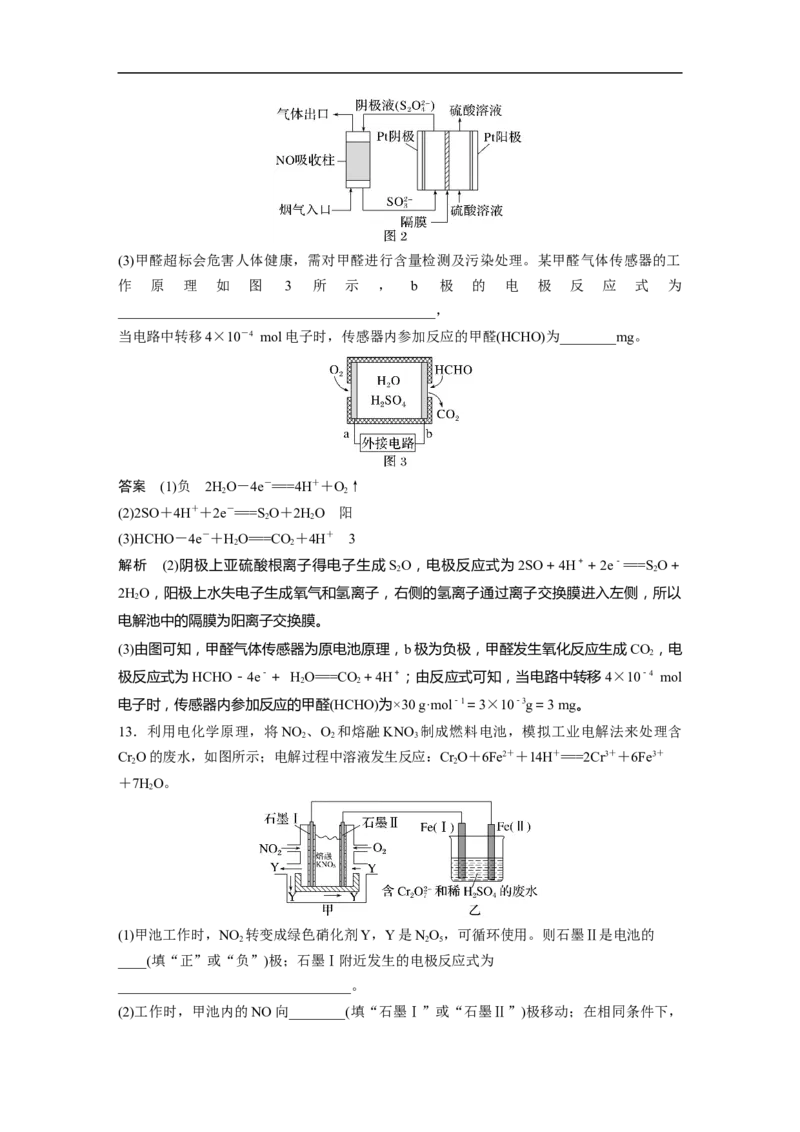
12.按要求回答下列问题。
(1)有人研究了用电化学方法把CO 转化为CHOH,其原理如图1所示:
2 3
则图中A电极接电源________极。已知B电极为惰性电极,则在水溶液中,该极的电极反
应 式 为
____________________________________________________________________________
_______________________________________________________________________________
。
(2)以连二亚硫酸盐(S O)为还原剂脱除烟气中的NO,并通过电解再生,装置如图2所示。阴
2
极的电极反应式为___________________________________________________________,
电解槽中的隔膜为____________(填“阳”或“阴”)离子交换膜。(3)甲醛超标会危害人体健康,需对甲醛进行含量检测及污染处理。某甲醛气体传感器的工
作 原 理 如 图 3 所 示 , b 极 的 电 极 反 应 式 为
_____________________________________________,
当电路中转移4×10-4 mol电子时,传感器内参加反应的甲醛(HCHO)为________mg。
答案 (1)负 2HO-4e-===4H++O↑
2 2
(2)2SO+4H++2e-===SO+2HO 阳
2 2
(3)HCHO-4e-+HO===CO+4H+ 3
2 2
解析 (2)阴极上亚硫酸根离子得电子生成SO,电极反应式为2SO+4H++2e-===SO+
2 2
2HO,阳极上水失电子生成氧气和氢离子,右侧的氢离子通过离子交换膜进入左侧,所以
2
电解池中的隔膜为阳离子交换膜。
(3)由图可知,甲醛气体传感器为原电池原理,b极为负极,甲醛发生氧化反应生成CO ,电
2
极反应式为HCHO-4e-+ HO===CO +4H+;由反应式可知,当电路中转移4×10-4 mol
2 2
电子时,传感器内参加反应的甲醛(HCHO)为×30 g·mol-1=3×10-3g=3 mg。
13.利用电化学原理,将NO 、O 和熔融KNO 制成燃料电池,模拟工业电解法来处理含
2 2 3
CrO的废水,如图所示;电解过程中溶液发生反应:CrO+6Fe2++14H+===2Cr3++6Fe3+
2 2
+7HO。
2
(1)甲池工作时,NO 转变成绿色硝化剂Y,Y是NO,可循环使用。则石墨Ⅱ是电池的
2 2 5
____(填“正”或“负”)极;石墨Ⅰ附近发生的电极反应式为
_________________________________。
(2)工作时,甲池内的NO向________(填“石墨Ⅰ”或“石墨Ⅱ”)极移动;在相同条件下,消耗的O 和NO 的体积比为__________。
2 2
(3)乙池中Fe(Ⅰ)棒上发生的电极反应为____________________________________________
______________________________________________________________________________。
(4)若溶液中减少了0.01 mol Cr O,则电路中至少转移了________ mol电子。
2
答案 (1)正 NO +NO-e-===NO
2 2 5
(2)石墨Ⅰ 1∶4 (3)Fe-2e-===Fe2+
(4)0.12
解析 (1)根据图示知甲池为燃料电池,电池工作时,石墨Ⅰ附近NO 转变成NO ,发生氧
2 2 5
化反应,电极反应式为NO +NO-e-===NO ;石墨Ⅱ是电池的正极,O 得电子发生还原
2 2 5 2
反应,电极反应式为O+4e-+2NO===4NO。(2)电池工作时,电解质溶液中的阴离子移向
2 2 5
负极,即甲池内的NO向石墨Ⅰ极移动;根据两极的电极反应式及得失电子守恒知,在相同
条件下,消耗O 和NO 的体积比为1∶4。(3)乙池为电解池,Fe(Ⅰ)棒为电解池的阳极,发
2 2
生的电极反应为Fe-2e-===Fe2+。(4)根据反应Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
知,若溶液中减少了0.01 mol Cr O,则参加反应的Fe2+为0.06 mol,根据电极反应:Fe-2e
2
-===Fe2+知电路中至少转移了0.12 mol电子。