文档内容
专题 03 离子反应
1.(2021·浙江高考真题)下列物质属于强电解质的是
A.KOH B.HPO C.SO D.CHCHO
3 4 3 3
【答案】A
【分析】在水溶液中或熔融状态下能够完全电离的化合物为强电解质。
【解析】A.KOH在水溶液中或熔融状态下能够完全电离出K+和OH-,KOH为强电解质,A符合题意;
B.HPO 在水溶液中或熔融状态下能不够完全电离,HPO 为弱电解质,B不符合题意;
3 4 3 4
C.SO 在水溶液中或熔融状态下不能电离,SO 属于非电解质,C不符合题意;
3 3
D.CHCHO在水溶液中或熔融状态下不能电离,CHCHO属于非电解质,D不符合题意;
3 3
故答案选A。
2.(2021·浙江高考真题)下列物质属于弱电解质的是
A.CO B.HO C.HNO D.NaOH
2 2 3
【答案】B
【分析】在水溶液中或熔融状态下不能够完全电离的电解质叫做若电解质。
【解析】A.CO 在水溶液中或熔融状态下不能够电离,为非电解质,A不符合题意;
2
B.HO在水溶液中或熔融状态下能够部分电离,为弱电解质,B符合题意;
2
C.HNO 为一种强酸,在水溶液中或熔融状态下能够完全电离,为强电解质,C不符合题意;
3
D.NaOH为一种强碱,在水溶液中或熔融状态下能够完全电离,为强电解质,D不符合题意;
故答案选B。
3.(2021·全国高考乙卷真题)下列过程中的化学反应,相应的离子方程式正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙:
B.过量铁粉加入稀硝酸中:
C.硫酸铝溶液中滴加少量氢氧化钾溶液:
D.氯化铜溶液中通入硫化氢:
【答案】A【解析】A.硫酸钙微溶,用碳酸钠溶液处理水垢中的硫酸钙转化为难溶的碳酸钙,离子方程式为:C
+CaSO =CaCO +S ,故A正确;
4 3
B.过量的铁粉与稀硝酸反应生成硝酸亚铁、一氧化氮和水,离子方程式应为:3Fe+8H++2N =3Fe2+
+2NO↑+4HO,故B错误;
2
C.硫酸铝溶液与少量氢氧化钾溶液反应生成氢氧化铝沉淀和硫酸钾,离子方程式应为:Al3++3OH-
=Al(OH) ↓,故C错误;
3
D.硫化氢为弱电解质,书写离子方程式时不能拆,离子方程式应为:Cu2++H S=CuS↓+2H+,故D错误;
2
答案选A。
4.(2021·湖南高考真题)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
粒子组 判断和分析
不能大量共存,因发生反应:
A 、 、 、
不能大量共存,因发生反应:
B 、 、 、
C 、 、 、 能大量共存,粒子间不反应
D 、 、 、 能大量共存,粒子间不反应
【答案】B
【解析】A.Al3+和NH HO生成Al(OH) 沉淀而不是生成Al ,故A错误;
3 2 3
B.S 和H+反应生成单质硫、二氧化硫和水,离子方程式为:2H++ S =S↓+SO ↑+H O,故B正确;
2 2 2 2
C.Fe3+可以将HO 氧化得Fe2+和O,不能大量共存,故C错误;
2 2 2
D.在酸性条件下Mn 能将Cl-氧化为Cl,不能大量共存,故D错误;
2
答案选B。
5.(2021·浙江高考真题)不能正确表示下列变化的离子方程式是
A.碳酸镁与稀盐酸反应:B.亚硫酸氢钠的水解:
C.锌溶于氢氧化钠溶液:
D.亚硝酸钠与氯化铵溶液受热反应:
【答案】A
【解析】A.碳酸镁与稀盐酸反应生成氯化镁、二氧化碳和水,反应的离子方程式为MgCO +2H+=Mg2+
3
+H O+CO↑,故A错误;
2 2
B.亚硫酸氢钠是弱酸的酸式盐,在溶液中水解生成亚硫酸和氢氧化钠,水解的离子方程式为HSO +H O
2
H SO +OH-,故B正确;
2 3
C.锌与氢氧化钠溶液反应生成偏锌酸钠和氢气,反应的离子方程式为Zn+2OH-+2H O=[Zn(OH) ]-+H ↑,
2 4 2
故C正确;
D.亚硝酸钠溶液与氯化铵溶液共热反应生成氯化钠、氮气和水,反应的离子方程式为NO +NH
N↑+2H O,故D正确;
2 2
故选A。
6.(2021·浙江高考真题)下列反应的方程式不正确的是
A.石灰石与醋酸反应:CO +2CH COOH=2CH COO- +CO ↑+H O
3 3 2 2
B.铜片上电镀银的总反应(银作阳极,硝酸银溶液作电镀液):Ag(阳极) Ag(阴极)
C.铜与稀硝酸反应:3Cu+2NO +8H+=3Cu2+ +2NO↑+4H O
2
D.明矾溶液中加入少量氢氧化钡溶液:2Al3+ +3SO + 3Ba2++6OH-=2Al(OH) ↓+ 3BaSO↓
3 4
【答案】A
【解析】A.碳酸钙难溶于水,在离子方程式中应以化学式保留,石灰石与醋酸反应的离子方程式为
CaCO +2CH COOH=Ca2++2CH COO-+H O+CO↑,A错误;
3 3 3 2 2
B.银作阳极,阳极的电极反应式为Ag-e-=Ag+,铜片作阴极,阴极的电极反应式为Ag++e-=Ag,总反应为Ag(阳极) Ag(阴极),B正确;
C.Cu与稀硝酸反应生成Cu(NO )、NO和水,反应的离子方程式为3Cu+8H++2 =3Cu2+
3 2
+2NO↑+4HO,C正确;
2
D.明矾溶液中加入少量Ba(OH) 溶液,参与反应的Ba2+与OH-物质的量之比为1:2,生成的Al(OH) 与
2 3
BaSO 沉淀物质的量之比为2:3,反应的离子方程式为2Al3++3 +3Ba2++6OH-=2Al(OH) ↓+3BaSO ↓,D
4 3 4
正确;
答案选A。
1.(2021·天津高三三模)下列化学用语表述不正确的是
A.电解 溶液:
B.使用 检验
C.泡沫灭火器工作原理:
D. 在水中发生水解:
【答案】A
【解析】
A.用惰性电极电解MgCl 溶液的离子反应为Mg2++2Cl-+2H O Mg(OH) ↓+H ↑+Cl↑,故A错误;
2 2 2 2 2
B.K[Fe(CN) ]检验Fe2+生成蓝色沉淀,离子反应为 ,故B正确;
3 6
C.发生相互促进水解反应生成沉淀和气体,离子反应为 ,故C正
确;
D.NH Cl是强酸弱碱盐,铵根在水中能发生水解,存在平衡,用“⇌”使溶液显酸性:
4,故D正确;
故选:A。
2.(2021·辽宁高三模拟)对于下列实验,能正确描述其反应的离子方程式的是
A.用NaClO溶液吸收少量
B.用惰性电极电解 水溶液:
C. 溶液中通入少量
D.二氧化硫使酸性高锰酸钾溶液褪色:
【答案】A
【解析】
A.用NaClO溶液吸收少量 ,生成的 再与过量的 反
应生成HClO,发生的总离子反应为 ,选项A正确;
B.用惰性材料为电极电解 溶液,阳极反应为: ,阴极反应为: ,
总反应的离子方程式为: ,选项B错误;
C.苯酚钠中无论通入少量还是过量二氧化碳都生成苯酚和碳酸氢钠,因为苯酚的酸性弱于碳酸而强于碳
酸氢根离子,故正确的离子方程式为: ,选项C错误;
D.电荷不守恒,正确的离子方程式为: ,选项D错误。
答案选A。
3.(2021·吉林松原市·高三模拟)下列离子反应方程式正确的是
A.Fe与稀硝酸反应,当n(Fe):n(HNO)=1:2时,3Fe+2NO +8H+=3Fe2++2NO↑+4HO
3 2B.CuSO 与过量浓氨水反应的离子方程式:Cu2++2NH·H O=Cu(OH) ↓+2NH
4 3 2 2
C.向硫酸铝铵溶液滴加足量的氢氧化钡溶液:Al3++2SO +2Ba2++4OH-=AlO +2BaSO ↓+2H O
4 2
D.向NaHSO 溶液中逐滴加入Ba(OH) 溶液至SO 刚好沉淀完全:2H++SO +Ba2++2OH-=2H O+BaSO↓
4 2 2 4
【答案】A
【解析】
A.当n(Fe):n(HNO)=1:4时,发生反应Fe+NO +4H+=Fe3++NO↑+2HO,再增加1倍的Fe时,2Fe3+
3 2
+Fe=3Fe2+,铁过量,故A正确;
B.CuSO 与过量浓氨水反应Cu2++4NH·H O=[Cu(NH )]2++4H O,故B错误;
4 3 2 3 4 2
C.向硫酸铝铵[NH Al(SO )]溶液中滴加足量Ba(OH) 溶液,离子反应方程式为NH +Al3++2SO +2Ba2+
4 4 2 2
+5OH-= AlO +2BaSO ↓+NH·H O+ 2H O,故C错误;
4 3 2 2
D.向NaHSO 溶液中逐滴加入Ba(OH) 溶液至SO 刚好沉淀完全:H++ SO +Ba2++OH-=H O+BaSO↓,
4 2 2 4
故D错误;选A。
4.(2021·浙江高三三模)下列反应的方程式正确的是
A. 与水反应:
B. 溶液与澄清石灰水反应:
C.粗铜电解精炼(粗铜作阳极, 溶液作电解液)的总反应:
D. 溶液中通少量 :
【答案】B
【解析】
A. 与水反应反应生成 和 , 为一元弱酸,书写离子方程式是不能拆成离子形式,故
A错误;B. 溶液与澄清石灰水反应,碳酸氢钙为易溶弱酸酸式盐,可以拆分成 和 ,澄清
石灰水可以拆分成 和 ,所以离子方程式为 ,故B正确;
C.粗铜电解精炼时粗铜为阳极,粗铜里面含有铁、锌等比铜活泼的杂质会先于铜在阳极放电,所以总反
应并不唯一,所以C错误;
D. 溶液中通少量 时正确的离子方程式为 ,D选项中离子
方程式不满足电荷守恒,故D错误;
答案为B。
5.(2021·辽宁高三模拟)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.水电离的 的溶液中: K+、Na+、 、
B. 的溶液中: 、Na+、 、
C.0.1mol/L氨水溶液中:Na+、K+、 、
D.含大量 的溶液: 、 、 、K+
【答案】C
【解析】
A.水电离的 的溶液,可能是酸性溶液或碱性溶液, 、 在酸性溶液中
不能大量存在,选项A不符合题意;
B. 的溶液呈碱性,铵根离子不能大量存在,选项B不符合题意;
C.0.1mol/L氨水溶液中:Na+、K+、 、 各离子相互不反应,能大量共存,选项C符合题意;
D.Fe3+与SCN-不能大量共存,选项D不符合题意;
答案选C。
6.(2021·广东高三二模)下列实验对应反应离子方程式书写正确的是
实验 编号 试剂a 含氯物质 现象① NaHS溶液 新制氯水 出现乳黄色沉淀
② NaHCO 溶液 新制氯水 产生无色气体
3
③ KClO 溶液 浓盐酸 产生黄绿色刺激性气味气体
3
④ NaHSO 溶液 浓盐酸 产生刺激性气味气体
3
A.实验①:HS-+Cl=S↓+H++2C1-
2
B.实验②: +Cl=CO ↑+H++C1O-+Cl-
2 2
C.实验③: +6H++C1-=Cl↑+3H O
2 2
D.实验④: +2H+=SO↑+H O
2 2
【答案】A
【解析】
A.Cl 具有强氧化性,能把HS-氧化为S,S为淡黄色沉淀,离子方程式为:HS-+Cl=S↓+H++2C1-,故A正
2 2
确;
B.产生无色气体为CO2,且方程式中HClO为弱酸不能拆,所以正确的离子方程式为:
+Cl=CO ↑+HC1O+Cl-,故B错误;
2 2
C.离子方程式书写错误,电荷不守恒,应该为: +6H++5C1-=3Cl↑+3H O,故C错误;
2 2
D. 为弱酸根,在离子方程式中不能拆解,正确的离子方程式为: +H+=SO↑+H O,故D错误;
2 2
故选A。
7.(2021·天津高三二模)下列离子方程式正确的是
A.氯化铁溶液腐蚀铜箔:Fe3++ Cu ═ Fe2+ + Cu2+
B.用氢氧化铝治疗胃酸过多:Al(OH) +3H+ = Al3++3H O
3 2
C.氢氧化钠溶液吸收氯气制漂白液:Cl + OH﹣═ Cl﹣+ HClO
2
D.用氢氧化钠溶液去除铝条表面的氧化膜:Al O+2OH- ═ 2Al3++H O
2 3 2
【答案】B
【解析】
A.电荷不守恒,正确的离子方程式为2Fe3++ Cu ═ 2Fe2+ + Cu2+,A错误;
B.用氢氧化铝治疗胃酸过多时氢氧化铝与HCl反应生成氯化铝和水,反应的离子方程式为Al(OH) +3H+
3= Al3++3H O,B正确;
2
C.氢氧化钠溶液吸收氯气制漂白液时,氢氧化钠与氯气反应生成氯化钠、次氯酸钠和水,反应的离子方
程式为Cl + 2OH﹣═ Cl﹣+ ClO-+H O,C错误;
2 2
D.氢氧化钠与氧化铝反应生成偏铝酸钠和水,反应的离子方程式为Al O+2OH-═2 +H O,D错误;
2 3 2
答案选B。
8.(2021·浙江金华市·高三二模)能正确表示下列变化的离子方程式是
A.向Ca(HCO) 溶液中加入足量Ca(OH) 溶液:
2 2
B.泡沫灭火器原理:
C.过量铁粉与稀硝酸反应:
D.纯碱溶液显碱性的原因:
【答案】A
【解析】
A.向Ca(HCO) 溶液中加入足量Ca(OH) 溶液: ,符合电荷守恒,
2 2
拆写原则,质量守恒定律,故A正确;
B.泡沫灭火器原理是铝离子和碳酸氢根离子相互促进水解生成氢氧化铝沉淀和二氧化碳气体,正确的离
子方程式是: ,故B错误;
C.过量的铁粉与硝酸反应生成亚铁离子,正确的离子方程式是:
,故C错误;
D.碳酸根离子水解是可逆反应,正确的离子方程式是: ,故D错误;
故选:A。
9.(2021·河北张家口市·高三三模)下列用于解释事实的离子方程式正确的是
A.向 溶液中加入过量盐酸:
B.将NaOH投入足量 饱和溶液中:C.铜与稀硝酸的反应:
D.向碳酸氢钠溶液中滴加少量石灰水:
【答案】A
【解析】
A.向 溶液中加入过量盐酸: ,A项正确;
B.NaOH与足量 饱和溶液反应: ,B项错误;
C.铜与稀硝酸的反应: ,C项错误;
D.向碳酸氢钠溶液中滴加少量石灰水: ,D项错误。
答案选A。
10.(2021·浙江高三模拟)下列反应的方程式不正确的是
A.向饱和氯化钠溶液中依次通入足量NH 和CO:
3 2
B.电解CuSO 溶液的总反应(石墨作阳极、铁作阴极):2Cu2++2H O 2Cu+4H+++O ↑
4 2 2
C.FeO与稀硝酸的反应:3FeO+10H++ =3Fe3++NO↑+5HO
2
D.NaHCO 的水解:
3
【答案】D
【解析】
A.向饱和氯化钠溶液中依次通入足量NH 和CO,发生反应产生NaHCO 晶体和NH Cl,反应的离子方程
3 2 3 4
式为: ,A正确;
B.电解CuSO 溶液,在阳极上水电离产生的OH-失去电子变为O 逸出;在阴极上Cu2+得到电子被还原产
4 2
生Cu单质,电解方程式为:2Cu2++2H O 2Cu+4H++O ↑,B正确;
2 2C.FeO与稀硝酸发生氧化还原反应,产生Fe(NO )、NO、HO,根据电子守恒、电荷守恒及原子守恒,
3 3 2
可得反应的离子方程式为:3FeO+10H++ =3Fe3++NO↑+5HO,C正确;
2
D.NaHCO 是强碱弱酸盐,在溶液中 发生水解反应,产生HCO 和OH-,但盐水解程度是微弱的,
3 2 3
存在水解平衡,水解的离子方程式为: +H O HCO+OH-,D错误;
2 2 3
故合理选项是D。
11.(2021·湖北荆州市·高三模拟)不能正确表示下列反应的离子方程式的是
A.用惰性电极电解 溶液:
B. 溶液与少量 溶液反应:
C.酸性溶液中 与 反应生成 :
D.向偏铝酸钠溶液中通入过量的 :
【答案】A
【解析】
A.用惰性电极电解 溶液的离子方程式为: ,A项
错误;
B. 溶液与少量 溶液反应: ,B项正确;
C.酸性溶液中 与 反应生成I: ,C项正确;
2
D.向偏铝酸钠溶液中通入过量的 : ,D项正确;
答案选A。
12.(2021·江苏盐城市·高三三模)NaSO 溶液是工业上常用的还原剂、防腐剂、去氯剂等。下列离子方
2 3
程式正确的是
A.NaSO 溶液在空气中易被氧化:SO +O =SO
2 3 2B.NaSO 溶液用作去氯剂:Cl+SO +H O=2H++2Cl-+SO
2 3 2 2
C.0.1mol·L-1NaSO 溶液pH>7:SO +2H O HSO +2OH-
2 3 2 2 3
D.过量SO 与NaOH溶液反应生成NaSO 溶液:SO +2OH-=SO +H O
2 2 3 2 2
【答案】B
【解析】
A.亚硫酸钠容易被氧气氧化成硫酸钠,题中所给离子方程式氧原子不守恒,正确的是2SO +O =2SO
2
,故A错误;
B.氯气具有强氧化性,能将亚硫酸钠氧化成硫酸钠,本身被还原成氯离子,离子方程式为Cl+SO
2
+H O=2H++2Cl-+SO ;故B正确;
2
C.亚硫酸钠为强碱弱酸盐,SO 为二元弱酸根,分步水解,即SO +H O HSO +OH-、HSO
2
+H O HSO +OH-,溶液中c(OH-)>c(H+),溶液显碱性,故C错误;
2 2 3
D.过量的SO 能与SO 反应生成HSO ,正确的是SO +OH-=HSO ,故D错误;
2 2
答案为B。
13.(2021·广东茂名市·高三三模)下列指定反应的离子方程式正确的是
A.含等物质的量的 、 、 的溶液中通入适量氯气:
B. 溶液与过量NaOH溶液反应:
C.向氯化钙溶液中通入 气体:
D.次氯酸钠溶液吸收少量二氧化硫气体:
【答案】A
【解析】
A.根据还原性: ,故通入适量氯气后根据先与强的还原性的离子发生反应,故A正确;B.根据氢氧化钠的过量判断, 溶液是少量,故应该反应无剩余,则离子方程式为:
,故B不正确;
C.氯化钙溶液中通入二氧化碳气体,由于碳酸的酸性比盐酸的酸性弱,所以不发生反应,故C不正确;
D.根据二氧化硫的量的多少进行判断反应 ,故D不正确。
故选A。
14.(2021·湖南衡阳市·高三二模)下列反应对应的离子方程式正确的是
A.硫酸铜溶液使PbS转变为更难溶的CuS:
B. 溶液中加足量的烧碱液:
C.漂白粉溶液吸收少量二氧化硫气体:
D.双氧水与酸性高锰酸钾溶液反应:
【答案】A
【解析】
A.硫酸铜溶液使硫化铅转变为更难溶的硫化铜的反应为硫酸铜溶液与硫化铅固体反应生成硫化铜固体和
硫酸铅固体,反应的离子方程式为 ,故A正确;
B.碳酸氢镁溶液与足量氢氧化钠溶液反应生成氢氧化镁沉淀、碳酸钠和水,反应的离子方程式为
,故B错误;
C.漂白粉溶液吸收少量二氧化硫气体的反应为溶液中次氯酸钙与少量二氧化硫发生氧化还原反应生成硫
酸钙沉淀和氯气,反应的离子方程式为 ,故C错误;
D.双氧水与酸性高锰酸钾溶液发生氧化还原反应生成硫酸钾、硫酸锰、氧气和水,反应的离子方程式为
,故D错误;
故选A。
15.(2021·山东泰安市·高三模拟)下列反应的离子方程式书写正确的是A.实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O +2H O=4Fe3++4OH-
2 2
B.用稀硫酸酸化的KMnO 溶液与少量HO 反应:2 +6H++5H O=2Mn2++5O ↑+8H O
4 2 2 2 2 2 2
C.向碳酸氢铵溶液中加入足量的澄清石灰水:Ca2++ +OH-=CaCO ↓+H O
3 2
D.向NaSO 溶液中通入足量的氯气: +2C1 +H O=2 +4C1-+2H+
2 2 3 2 2
【答案】B
【解析】
A.实验室配制的亚铁盐溶液在空气中被氧化生成三价铁,反应的离子方程式为:4Fe2++O +4H+=4Fe3+
2
+2H O,选项A错误;
2
B.用稀硫酸酸化的KMnO 溶液与少量HO 反应,生成硫酸锰、硫酸钾、氧气和水,反应的离子方程式为:
4 2 2
2 +6H++5H O=2Mn2++5O ↑+8H O,选项B正确;
2 2 2 2
C.向碳酸氢铵溶液中加入足量的澄清石灰水,反应生成碳酸钙沉淀、一水合氨和水,反应的离子方程式
为: +Ca2++ +2OH-=CaCO ↓+H O+NH ·H O,选项C错误;
3 2 3 2
D.向NaSO 溶液中通入足量的氯气,反应生成硫酸钠、硫酸和盐酸,反应的离子方程式为:
2 2 3
+4C1 +5H O=2 +8C1-+10H+,选项D错误;
2 2
答案选B。
16.(2021·河北唐山市·高三三模)下列离子方程式正确的是
A. 溶液中通入少量氯气:
B.石灰石溶于醋酸:
C. 与足量 溶液反应:
D.钠与水反应:
【答案】B
【解析】A. 由于I-的还原性强于Fe2+, 溶液中通入少量氯气的离子方程式: ,A错误;
B. 石灰石溶于醋酸的反应的离子方程式为: ,B
正确;
C. 与足量 溶液反应的离子方程式为: ,C错误;
D. 钠与水反应的离子方程式为: ,D错误;
故答案为:B。
17.(2021·福建南平市·高三二模)下列指定反应的离子方程式错误的是
A.铅蓄电池放电的总反应:Pb+PbO+4H++2 =2PbSO↓+2H O
2 4 2
B.足量CO 通入溶有氨的饱和食盐水:CO+NH+H O+Na+=NaHCO↓+
2 2 3 2 3
C.明矾溶液中滴加Ba(OH) 溶液至沉淀质量最大:
2
D.氯气在碱性环境下将I-氧化成 :
【答案】C
【解析】
A.铅蓄电池在放电时,Pb为负极,失去电子,发生氧化反应,电极反应式为:Pb-2e-+ =PbSO;正
4
极上PbO 得到电子,发生还原反应,电极反应式为:PbO +2e-+4H++ = PbSO +2H O,故总反应方程
2 2 4 2
式为:Pb+PbO+4H++2 =2PbSO↓+2H O,A正确;
2 4 2
B.向含有氨的饱和NaCl溶液中通入足量CO 气体,发生反应,产生NaHCO 晶体和NH Cl,反应的离子
2 3 4
方程式为:CO+NH+H O+Na+=NaHCO↓+ ,B正确;
2 3 2 3
C.明矾溶液中滴加Ba(OH) 溶液至沉淀质量最大时, 恰好沉淀完全,此时离子方程式为:Al3++2
2+2Ba2++4OH-=2BaSO ↓+ +2H O,C错误;
4 2
D.氯气在碱性环境下将I-氧化成 ,根据电子守恒、电荷守恒、原子守恒,可得反应的离子方程式为:
,D正确;
故合理选项是C。
18.(2021·广东汕头市·高三二模)下列离子方程式书写正确的是
A.将金属钠投入水中:
B.将铜丝插入稀硝酸中:
C.向硫酸铝溶液中加入过量氨水:
D.向氯化铁溶液中滴加碳酸钠溶液:
【答案】C
【解析】
A. 将金属钠投入水中: ,故A错误;
B. 将铜丝插入稀硝酸中生成NO: ,故B错误;
C. 向硫酸铝溶液中加入过量氨水生成氢氧化铝沉淀和硫酸铵,沉淀不溶于氨水:
,故C正确;
D. 向氯化铁溶液中滴加碳酸钠溶液双水解生成氢氧化铁和二氧化碳:
,故D错误;故选C。
19.(2021·天津高三二模)下列离子方程式的解释或书写正确的是
A.NaCO 溶液显碱性的原因:CO +2H O HCO+2OH-
2 3 2 2 3
B.向一定量的FeBr 溶液中通入少量Cl:2Br-+Cl=Br +2Cl-
2 2 2 2
C.向CuSO 溶液中逐滴滴加氨水直至过量Cu2++2NH·HO=2NH +Cu(OH) ↓
4 3 2 2D.等物质的量浓度的Ba(OH) 溶液与NaHSO 溶液等体积混合:Ba2++OH-+H++SO =BaSO ↓+H O
2 4 4 2
【答案】D
【解析】
A.CO 为多元弱酸酸根离子,应分步水解,水解不能一步完成,故A错误;
B.还原性: ,向一定量的FeBr 溶液中通入少量Cl 时,氯气应该先和 反应,故B错误;
2 2
C.沉淀氢氧化铜可以溶解在过量的氨水中,生成配离子 ,最后沉淀全部溶解,故C错误;
D.等物质的量浓度的Ba(OH) 溶液与NaHSO 溶液等体积混合后,钡离子和硫酸根沉淀,氢离子与氢氧根
2 4
生成水,发生反应Ba2++OH-+H++SO =BaSO ↓+H O,故D正确;
4 2
综上答案为D。
20.(2021·福建宁德市·高三三模)能正确表示下列反应的离子方程式的是
A.乙醇被酸性重铬酸钾溶液氧化:3CHCHOH+2Cr O +16H+=4Cr3++3CH COOH+11H O
3 2 2 3 2
B.电解氯化镁水溶液:2Cl-+2H O 2OH-+Cl↑+H ↑
2 2 2
C.乙酸溶液滴到大理石上产生气泡:2H++CaCO =CO ↑+Ca2++H O
3 2 2
D.硫酸铵溶液和氢氧化钡溶液反应:Ba2++SO =BaSO ↓
4
【答案】A
【解析】
A.乙醇有还原性,可被酸性重铬酸钾溶液氧化为乙酸,Cr元素被还原为Cr3+,反应的离子方程式为
3CHCHOH+2Cr O +16H+=4Cr3++3CH COOH+11H O,A正确;
3 2 2 3 2
B.若阳极为惰性电极,则电解氯化镁溶液,则会形成氢氧化镁沉淀,离子方程式为Mg2++2Cl-+2H O
2
Mg(OH) ↓+Cl↑+H ↑;若阳极为活性电极,则阳极反应为电极材料失电子,总反应中无氯离子,B错误;
2 2 2
C.乙酸是弱酸,应保留化学式,正确的离子方程式为2CHCOOH +CaCO =CO ↑+Ca2++H O+2CHCOO-,
3 3 2 2 3
C错误;D.硫酸铵和氢氧化钡反应生成硫酸钡沉淀和一水合氨,反应的离子方程式为2 +Ba2++SO +2OH-
=BaSO ↓+2NH·H O,D错误;
4 3 2
答案选A。
21.(2021·山东济南市·高三二模)下列离子方程式书写正确的是
A.向硫酸铜溶液中加人少量过氧化钠:2NaO +2Cu2+ +2H O=4Na+ +2Cu(OH) ↓+O ↑
2 2 2 2 2
B.将氯气通入氢氧化钠溶液中:Cl+OH-=Cl-+ClO- +H O
2 2
C.等物质的量的CaCl 、Ba(OH) 和HCl溶液混合:Ca2++2OH-=Ca(OH) ↓
2 2 2
D.氧化亚铁溶于稀硝酸:FeO+2H+=Fe2+ +H O
2
【答案】A
【解析】
A.向硫酸铜溶液中加人少量过氧化钠,过氧化钠先和水反应生成NaOH和氧气,之后NaOH和硫酸铜反
应生成氢氧化铜沉底,总的离子方程式为2NaO +2Cu2+ +2H O=4Na+ +2Cu(OH) ↓+O ↑,A正确;
2 2 2 2 2
B.选项所给离子方程式元素不守恒,正确离子方程式为Cl+2OH-=Cl-+ClO- +H O,B错误;
2 2
C.等物质的量的CaCl 、Ba(OH) 和HCl溶液混合,H+优先和OH-反应,但只能消耗一半OH-,剩余部分
2 2
和Ca2+产生沉淀,离子方程式应为2H++Ca2++4OH-=Ca(OH) ↓+2H O,C错误;
2 2
D.稀硝酸会将亚铁离子氧化,正确离子方程式为3FeO+10H++NO =3Fe3++NO↑+5H O,D错误;
2
综上所述答案为A。
22.(2021·福建龙岩市·高三三模)下列有关离子方程式书写错误的是
A.NaHCO 加入过量的Ba(OH) 溶液:
3 2
B.用高锰酸钾标准溶液滴定草酸:
C.SO 通入BaCl 溶液无现象,再通入Cl 后产生白色沉淀:Cl+SO+Ba2++2H O=BaSO+2Cl-+4H+
2 2 2 2 2 2 4
D.用FeS除去废水中的Hg2+:FeS+Hg2+=HgS+Fe2+
【答案】B
【解析】
A. 根据少定多变的规律:NaHCO 加人过量的Ba(OH) 溶液: ,故
3 2
A正确;
B. 草酸是弱电解质,用化学式表示,用高锰酸钾标准溶液滴定草酸:,故B错误;
C.氯气能将二氧化硫氧化,SO 通入BaCl 溶液无现象,再通入Cl 后产生白色沉淀:Cl+SO+Ba2+
2 2 2 2 2
+2H O=BaSO+2Cl-+4H+,故C正确;
2 4
D. FeS的溶解度大于HgS,溶解度大的较易转化为溶解度小的,用FeS除去废水中的Hg2+:
FeS+Hg2+=HgS+Fe2+,故D正确;
故选B。
23.(2021·福建漳州市·高三三模)下列反应的离子方程式书写正确的是
A. 溶液加入铁粉:
B. 溶液通入少量 :
C.二氧化硫使酸性高锰酸钾溶液褪色:
D.往盛有水的烧杯中投入金属钠:
【答案】C
【解析】
A. 溶液加入铁粉: ,选项中的方程式电荷不守恒,错误;
B. 和 溶液不反应,错误;
C.二氧化硫使酸性高锰酸钾溶液褪色,二氧化硫被高锰酸钾氧化为 , 被还原为Mn2+,离子方
程式为: ,正确;
D.往盛有水的烧杯中投入金属钠: ,选项中的方程式元素不守恒,错误;
故选C。
24.(2021·浙江杭州市·高三三模)下列反应的方程式正确的是
A.向Ca(ClO) 溶液中通入过量CO 制次氯酸:2ClO-+H O+CO=2HClO+CO
2 2 2 2
B.[Ag(NH)]OH与较浓盐酸反应生成AgCl:[Ag(NH))]++OH-+3H++Cl-=AgC1↓+2NH +H O
3 2 3 2 2
C.硫酸铵与亚硝钠溶液共热:(NH )SO +2NaNO =Na SO +2NH+NO+NO+HO
4 2 4 2 2 4 3 2 2D.向酸化KMnO 溶液中通入SO :2MnO +5SO+4OH-=2Mn2++5SO +2H O
4 2 2 2
【答案】B
【解析】
A.向Ca(ClO) 溶液中通入过量CO 制次氯酸的离子方程式为:ClO-+H O+CO=HClO+ ,A错误;
2 2 2 2
B.[Ag(NH)]OH与较浓盐酸反应生成AgCl的离子方程式为:[Ag(NH))]++OH-+3H++Cl-=AgC1↓+2NH
3 2 3 2
+H O,B正确;
2
C.硫酸铵与亚硝钠溶液共热的反应方程式为:(NH )SO +2NaNO =Na SO +2N ↑+4H O,C错误;
4 2 4 2 2 4 2 2
D.向酸化KMnO 溶液中通入SO 的离子方程式为:2MnO +5SO+2H O=2Mn2++5SO +4H+,D错误;
4 2 2 2
故答案为:B。
25.(2021·湖北高三模拟)下列离子方程式书写错误的是
A.(NH )Fe(SO ) 溶液与少量Ba(OH) 溶液反应:Fe2++ +Ba2++2OH-=BaSO ↓+Fe(OH) ↓
4 2 4 2 2 4 2
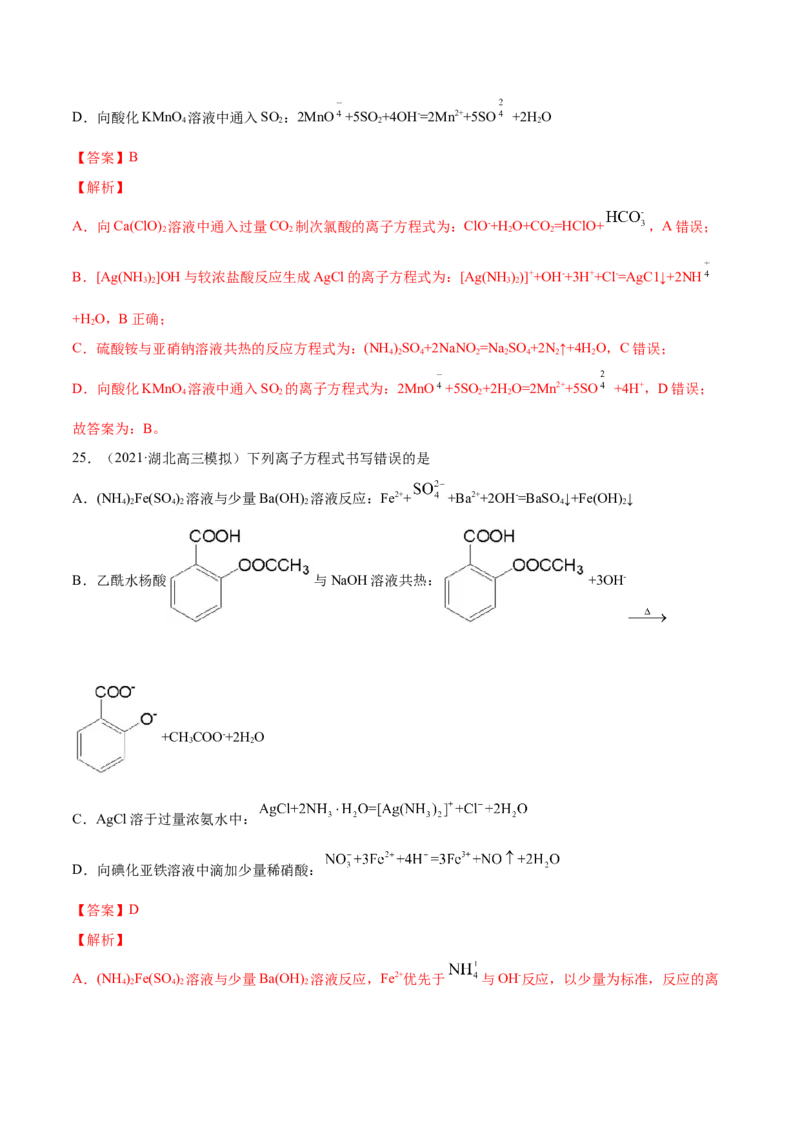
B.乙酰水杨酸 与NaOH溶液共热: +3OH-
+CH COO-+2H O
3 2
C.AgCl溶于过量浓氨水中:
D.向碘化亚铁溶液中滴加少量稀硝酸:
【答案】D
【解析】
A.(NH )Fe(SO ) 溶液与少量Ba(OH) 溶液反应,Fe2+优先于 与OH-反应,以少量为标准,反应的离
4 2 4 2 2子方程式为Fe2++ +Ba2++2OH-=BaSO ↓+Fe(OH) ↓,A正确;
4 2
B.乙酰水杨酸 与NaOH溶液共热,与苯环直接相连的—COOH与NaOH反应生成
—COONa,酯基水解后生成的CHCOOH和酚羟基均会与NaOH发生反应,因此反应的离子反应方程式为
3
+3OH- +CH COO-+2H O,B正确;
3 2
C.AgCl溶于过量浓氨水中生成银氨离子,反应的离子方程式为
,C正确;
D.还原性I->Fe2+,向碘化亚铁溶液中滴加少量稀硝酸,I-与稀硝酸发生氧化还原反应,而不是Fe2+,D错
误;
答案选D。
26.(2021·四川成都市·高三三模)下列方程式能正确解释相应实验的是
A.用惰性电极电解饱和AlCl 溶液:2Cl-+2H O Cl↑+H ↑+2OH-
3 2 2 2
B.实验室制备Fe(OH) 胶体:FeCl +3NaOH=Fe(OH) (胶体)+3NaCl
3 3 3
C.将水垢浸泡在饱和碳酸钠溶液中:CO +Ca2+=CaCO ↓
3
D.将浓氨水滴在氢氧化钠固体上:NH ·H O NH ↑+H O
3 2 3 2
【答案】D
【解析】
A.用惰性电极电解饱和AlCl 溶液过程中,溶液中Cl-在阳极上失去电子发生氧化反应生成Cl,HO电离
3 2 2
出的H+在正极上发生还原反应生成H,溶液中Al3+与OH-会发生复分解反应生成Al(OH) ,因此电解总反
2 3应为2Al3++6Cl-+6H O 3Cl↑+3H ↑+2Al(OH) ↓,故A错误;
2 2 2 3
B.实验室制备Fe(OH) 胶体是利用FeCl 在沸水中发生水解反应,反应方程式为FeCl +3H O Fe(OH) (胶
3 3 3 2 3
体)+3HCl,故B错误;
C.水垢中含有CaSO 等,将水垢浸泡在饱和碳酸钠溶液中发生反应生成CaCO ,CaSO 为微溶物,反应离
4 3 4
子方程式为CaSO(s)+ (aq) CaCO (s)+ (aq) ,故C错误;
4 3
D.浓氨水中存在平衡NH +H O NH ·H O +OH-,将浓氨水滴在氢氧化钠固体上,溶液中
3 2 3 2
OH-浓度增大,平衡逆向移动生成NH 和HO,故D正确;
3 2
综上所述,方程式能正确解释相应实验的是D项,故答案为D。
27.(2021·福建厦门市·高三三模)生活中处处有化学,下列指定反应的离子方程式不正确的是
A.用 治疗胃酸过多:
B.洁厕灵与84消毒液混合后产生氯气:
C.用纯碱除硫酸钙水垢:
D.用足量银氨溶液检测甲醛:
【答案】C
【解析】
A.胃酸主要成分是盐酸,氢氧化铝溶于盐酸生成氯化铝,离子方程式为:
,故A正确;
B.洁厕灵主要成分为HCl、84消毒液的有效成分为HClO,两者混合发生氧化还原反应生成氯气,反应的
离子方程式为: ,故B正确;
C.硫酸钙是微溶物应写化学式,离子方程式为: ,故C错误;D.甲醛能被银氨溶液氧化成碳酸根离子,离子反应为:
,故D正确;
故选:C。
28.(2021·北京高三二模)下列方程式与所给事实不相符的是
A.向 酸性溶液中滴加 溶液,溶液褪色:
B.向沸水中滴加饱和 溶液, 胶体:
C.向银氨溶液中滴加乙醛,水浴加热,析出光亮银镜:
D. 用作潜水艇供氧剂: ;
【答案】B
【解析】
A. 酸性溶液与 溶液反应生成二氧化碳、Mn2+和水,则离子方程式为:
,A正确;
B. 向沸水中滴加饱和 溶液得到 胶体:则 ,B不正确;
C.银氨溶液与乙醛经水浴加热,得到乙酸铵、银、氨气和水:
,C正确;
D. 能分别与水、二氧化碳反应生成氧气,可作供氧剂: ;
,D正确;
答案选B。
29.(2021·福建高三三模)下列指定反应的离子方程式书写正确的是
A.过量铁粉溶于稀硝酸:Fe+2H+=Fe2++H ↑
2B.向0.1mol·L−1Ba(OH) 溶液中滴加NaHSO 至Ba2+完全沉淀:Ba2++OH⁻+H++SO =BaSO ↓+H O
2 4 4 2
C.将Al (SO ) 溶液与NaCO 溶液混合:2Al3++3CO =Al(CO)↓
2 4 2 2 3 2 3 3
D.用食醋来除水壶中的水垢(主要成分CaCO ):CaCO +2H+=Ca2++CO ↑+H O
3 3 2 2
【答案】B
【解析】
A. 过量铁粉溶于稀硝酸生成硝酸亚铁、一氧化氮和水:3Fe+8H++2NO ═3Fe2++2NO↑+4HO↑,故A不选;
2
B. 向0.1mol·L−1Ba(OH) 溶液中滴加NaHSO 至Ba2+完全沉淀,钡离子与硫酸根离子比是1:1,:Ba2+
2 4
+OH⁻+H++SO =BaSO ↓+H O,故B正确;
4 2
C. 将Al (SO ) 溶液与NaCO 溶液混合:2Al3++3CO +3H O =2Al(OH) ↓+3CO ↑
2 4 2 2 3 2 3 2
D. 醋酸是弱酸,用食醋来除水壶中的水垢(主要成分CaCO ):CaCO +2CH COOH=Ca2+
3 3 3
+CO ↑+H O+2CHCOO-,故D错误;
2 2 3
故选B。
30.(2021·江苏高三三模)为检验某久置过氧化钠样品的成分,学习小组依次进行了有关实验。实验中涉
及反应的离子方程式正确的是
A.将过氧化钠样品完全溶于水,产生气泡:NaO+H O=2Na++2OH-+O ↑
2 2 2 2
B.向溶液中滴加BaCl 溶液,产生白色沉淀:CO +Ba2+=BaCO ↓
2 3
C.向沉淀中滴加稀醋酸,产生气体:BaCO +2H+=Ba2++CO ↑+H O
3 2 2
D.将气体通入足量澄清石灰水,出现浑浊现象:CO+Ca2++OH-=CaCO ↓+H O
2 3 2
【答案】B
【解析】
A.将过氧化钠样品完全溶于水,产生气泡,涉及的离子方程式为:2NaO+2H O=4Na++4OH-+O ↑,A错
2 2 2 2
误;
B.向溶液中滴加BaCl 溶液,产生白色沉淀,涉及的离子方程式为::CO +Ba2+=BaCO ↓,B正确;
2 3
C.向沉淀中滴加稀醋酸,产生气体,涉及的离子方程式为: BaCO +2CH COOH=Ba2+
3 3
+CO ↑+H O+2CHCOO-,C错误;
2 2 3
D.将气体通入足量澄清石灰水,出现浑浊现象,涉及的离子方程式为:CO+Ca2++2OH-=CaCO ↓+H O,D
2 3 2错误;故答案为:B。
31.(2021·河南郑州市二模)探究草酸(HC O)性质,进行如下实验。(已知:室温下,
2 2 4
的 )
实验 装置 试剂a 现象
① Ca(OH) 溶液(含酚酞) 产生气泡
2
② 少量NaHCO 溶液 紫色溶液褪色
3
③ 酸性KMnO 溶液 溶液褪色,产生白色沉淀
4
④ C HOH和浓硫酸 加热后产生有香味物质
2 5
下列离子方程式或化学方程式错误的是
A.草酸有酸性:
B.草酸的酸性大于碳酸:
C.草酸有还原性:
D.草酸可发生酯化反应:HOOCCOOH+2C HOH C HOOC-COOC H+2H O
2 5 2 5 2 5 2
【答案】C
【解析】
A.HC O 有酸性,能够与Ca(OH) 溶液发生反应Ca(OH) +H C O=CaC O↓+2H O,对应的离子方程式为
2 2 4 2 2 2 2 4 2 4 2
Ca2++2OH-+H C O═CaC O↓+2H O,故A正确;
2 2 4 2 4 2
B.酸性HC O>HCO,向少量NaHCO 溶液中加入草酸会生成CO 和NaHC O,反应的化学方程式为
2 2 4 2 3 3 2 2 4
NaHCO +H C O═NaHC O+CO ↑+H O,对应的离子方程式为 ,
3 2 2 4 2 4 2 2
故B正确;
C.HC O 有还原性,能被酸性KMnO 溶液氧化生成CO,HC O 是弱电解质,离子方程式中应保留化学
2 2 4 4 2 2 2 4
式,离子方程式为2 +5H C O+6H+═2Mn2++10CO ↑+8H O,故C错误;
2 2 4 2 2
D.HC O 是二元羧酸,可以与乙醇发生酯化反应,其完全酯化的化学方程式为HOOCCOOH+2C HOH
2 2 4 2 5C HOOC-COOC H+2H O,故D正确;
2 5 2 5 2
故选C。
32.(2021·浙江高三二模)下列离子组能大量共存且加入(或通入)试剂发生反应的离子方程式正确的是
选项 离子组 试剂 离子方程式
A 足量Cu粉
B 少量Cl
2
C 少量
D 足量NaOH溶液
【答案】B
【解析】
A.铁离子和铜反应生成亚铁离子和铜离子,则离子方程式为: ,A错误;
B.适量的氯气和亚硫酸根离子反应: ,亚硫酸根过量时,与生成的氢
离子结合生成亚硫酸氢根离子,故少量的氯气和亚硫酸根离子反应:
,B正确;
C.钡离子和硫酸根离子能发生沉淀反应生成硫酸钡沉淀,同时:酸性环境下,硝酸根离子有强氧化性,
能氧化亚铁离子,C错误;
D.足量的氢氧化钠溶液中,铁离子被沉淀、铵离子和氢氧根离子结合成一水合氨,D错误;
答案选B。
33.(2021·天津高三二模)下列指定反应的离子方程式正确的是
A.向明矾溶液中滴加硫化钠溶液:
B.向NaClO溶液中通入少量 制取次氯酸:
C. 溶液中加入盐酸酸化的D.某中性液可能存在: 、 、 、
【答案】B
【解析】
A.向明矾溶液中滴加硫化钠溶液,硫离子与铝离子双水解:
,故A错误;
B.向NaClO溶液中通入少量 ,二氧化碳通入水中形成碳酸,碳酸酸性强于次氯酸,可以制取次氯酸:
,故B正确;
C. 溶液中加入盐酸酸化的 : ,应保持电荷守恒,故
C错误;
D.某中性液不可能存在 ,因为 会水解为氢氧化铁,故D错误;
故选B。
34.(2021·天津高三三模)下列反应的离子方程式表达正确的是
A.用铜电极电解MgCl 溶液:Mg2++2Cl-+2H O H↑+C1 ↑+Mg(OH) ↓
2 2 2 2 2
B.某消毒液的主要成分为NaClO,加白醋可增强消毒效果:CHCOOH+ClO-=HClO+CH COO-
3 3
C.向草酸溶液中逐滴加入酸性高锰酸钾溶液,溶液褪色:2 +5 +16H+=2Mn2++10CO ↑+8H O
2 2
D.水浴加热银氨溶液与葡萄糖的混合溶液,出现银镜:CHOH(CHOH) CHO+2[Ag(NH )]OH
2 4 3 2
CHOH(CHOH) COOH+2Ag↓+4NH +H O
2 4 3 2
【答案】B
【解析】
A.由于Cu不是惰性电极,所以Cu会参与氧化还原反应,阳极Cu失去电子,生成Cu2+,阳极电极反应式
为Cu-2e-=Cu2+,阴极电极方程式为2HO+2e-=H ↑+2OH-,故A错误;
2 2
B.由于HClO酸性较弱,则NaClO可与醋酸反应生成HClO,漂白性增强,离子方程式为CHCOOH+ClO-
3
=HClO+CH COO-,故B正确;
3
C.向草酸溶液中逐滴加入酸性高锰酸钾溶液,溶液褪色,发生了氧化还原反应,由于草酸是弱酸,在离子方程式中应保留分子式,其离子方程式为2 +5H C O+6H+=2Mn2++10CO ↑+8H O,故C错误;
2 2 4 2 2
D.水浴加热银氨溶液与葡萄糖的混合溶液,葡萄糖中醛基被氧化生成羧基,出现银镜,该反应的离子方
程式为CHOH(CHOH) CHO+2[Ag(NH )]++2OH- CHOH(CHOH) COO-+ +3NH+2Ag↓+H O,故
2 4 3 2 2 4 3 2
D错误;
答案为B。
35.(2021·天津高三二模)下列指定反应的离子方程式正确的是
A.0.1mol·L-1MgCl 溶液中加入足量石灰乳:Mg2++Ca(OH) =Mg(OH) +Ca2+
2 2 2
B.0.1mol·L-1CuSO 溶液中加入过量浓氨水:Cu2++2NH·H O=Cu(OH) ↓+2NH
4 3 2 2
C.同浓度同体积NH HSO 溶液与NaOH溶液混合:NH +OH-=NH·H O
4 4 3 2
D.饱和氯水中通入SO 至溶液颜色褪去:Cl+SO+H O=2H++2Cl-+SO
2 2 2 2
【答案】A
【解析】
A.MgCl 溶液中加入足量石灰乳生成氢氧化镁沉淀,石灰乳不能拆成离子,离子方程式为Mg2++
2
Ca(OH) = Mg(OH) + Ca2+,故A正确;
2 2
B.浓氨水过量,应生成铜氨络离子,离子方程式为Cu2++4NH·H O=[Cu(NH )]2++4H O,故B错误;
3 2 3 4 2
C.同浓度同体积NH HSO 溶液与NaOH溶液反应的化学方程式为
4 4
2NH HSO +2NaOH=(NH )SO +Na SO +2H O,其离子方程式为:H+ + OH- == H O,故C错误;
4 4 4 2 4 2 4 2 2
D.选项所给离子方程式氧元素不守恒,电荷不守恒,正确离子方程式为Cl+ SO + 2H O=4H++ 2Cl-+ SO
2 2 2
,故D错误;
本题答案A。
36.(2021·四川德阳市·高三二模)对于下列实验,能正确描述其反应的离子方程式是
A.将少量SO 通入次氯酸钠溶液中:ClO-+SO+H O=Cl-+ +2H+
2 2 2
B.向含CaSO 的水垢中滴入饱和NaCO 溶液:CaSO(s)+ (aq) (aq)+CaCO (s)
4 2 3 4 3
⇌
C.用铁电极电解饱和MgCl 溶液:Mg2++2C1-+2H O Mg(OH) ↓+Cl↑+H ↑
2 2 2 2 2D.向(NH )Fe(SO ) 溶液中加入含等物质的量溶质的Ba(OH) 溶液:Ba2++ + +OH-
4 2 4 2 2
=BaSO ↓+NH·H O
4 3 2
【答案】B
【解析】
A.将少量SO 通入次氯酸钠溶液中:3ClO-+SO+H O=Cl-+ +2HClO,A错误;
2 2 2
B.向含CaSO 的水垢中滴入饱和NaCO 溶液:CaSO(s)+ (aq) (aq)+CaCO (s),B正确;
4 2 3 4 3
⇌
C.用铁电极电解饱和MgCl 溶液,铁失电子生成亚铁离子,没有氯气产生,C错误;
2
D.向(NH )Fe(SO ) 溶液中加入含等物质的量溶质的Ba(OH) 溶液:Fe2++ +Ba2++2OH-
4 2 4 2 2
=BaSO ↓+Fe(OH) ↓,D错误;
4 2
答案选B。
37.(2021·广东茂名市·高三二模)化学与生活关系密切,解释下列应用的离子方程式正确的是
选项 应用 解释(离子方程式)
A 淀粉—KI溶液(稀硫酸酸化)检验碘盐中含KIO
3
B 电解饱和食盐水制氢气和氯气
C 醋酸用于除去水垢
D 氯化铁用于蚀刻铜板
【答案】A
【分析】
电解饱和食盐水的时候,注意水不拆,醋酸是弱电解质不能拆,另外离子方程式也要注意电荷守恒问题。
【解析】
A.电荷守恒,得失电子守恒,A正确;
B.食盐水是中性,电解反应的离子方程式为 ,B错误;
C.醋酸是弱电解质,应该用分子式表示,正确的应该是
,C错误;D.电荷不守恒,正确的应该是 ,D错误;
【点睛】
弱酸是弱电解质不能拆;离子方程式要注意电荷守恒。
38.(2021·广东珠海市·高三二模)下列关于离子共存或者离子反应的说法正确的是
A. 溶液可能大量存在: 、 、 、
B.用NaOH溶液吸收过量CO:
2
C. 氯化亚铁溶液:Na+、 、 、MnO
D.氢氧化铁和碘化氢溶液反应:
【答案】B
【解析】
A. 溶液中碳酸根离子与铜离子反应生成碳酸铜沉淀,不能大量共存,故A错误;
B.氢氧化钠溶液与过量二氧化碳反应生成碳酸氢钠,反应的离子方程式为 ,故B正
确;
C. 氯化亚铁溶液中高锰酸根离子能与亚铁离子发生氧化还原反应,不能大量共存,故C错误;
D.氢氧化铁和碘化氢溶液反应生成碘化亚铁、碘和水,反应的离子方程式为
,故D错误;
故选B。
39.(2021·辽宁沈阳市·高三其他模拟)某溶液中只可能含有
中的几种离子,各离子浓度均为 。某
同学进行了如下实验:下列说法正确的是
A.无法确定原溶液中是否含有
B.原溶液中肯定存在的离子为
C.沉淀A为 ,沉淀C为 和
D.滤液X中大量存在的阳离子有 和
【答案】B
【解析】
加入过量稀硫酸无明显变化,说明溶液中无 ,前者会产生气体,后者会先产生沉淀后溶解 ;
加入硝酸钡有气体产生,因为前面已经加入了硫酸, 在酸性条件下具有强氧化性,说明有亚铁离子
存在且被氧化,沉淀A为硫酸钡;加入过量 溶液有气体生成,说明存在 ,气体为氨气,沉淀
B为红褐色氢氧化铁沉淀;通入少量 产生沉淀, 先与 反应生成 , 再与 反
应生成 沉淀,沉淀C为碳酸钡;因为存在的离子浓度均为 ,从电荷守恒的角度出发,
溶液中不存在 ,只含有 才能保证电荷守恒, 不能存在。
A.根据以上分析可知原溶液中不存在 ,A错误;
B.原溶液中肯定存在的离子有 ,B正确;
C.沉淀A为 ,沉淀C为 ,C错误;
D.滤液X中大量存在的阳离子有 和 ,D错误;
答案选B。
40.(2021·贵州高三二模)下列离子方程式书写不正确的是A.酸化的KI溶液置于空气中:
B.向明矾溶液中加过量氨水:
C.用小苏打治疗胃酸过多:
D.将氯化铵溶液滴入氢氧化镁悬浊液中:
【答案】C
【解析】
A.空气中的氧气将酸化的 氧化成 ,自身被还原为 ,所以反应的离子方程式为
,故A正确;
B.氨水中 为一元弱碱,写成离子方程式时不能拆分, 沉淀在 一元弱碱中
不能溶解,所以离子方程式为 ,故B正确;
C.小苏打的成分为 ,治疗胃酸过多的离子方程式为 ,故C错误;
D.氢氧化镁悬浊液不能拆成离子形式, 在水中部分水解生成 和 , 与
反应生成 和 ,所以总离子方程式为
,故D正确;
综上答案为C。
41.(2021·辽宁高三其他模拟)下列各组离子在给定条件下,因发生配合反应而不能大量共存的一组是
A. 的溶液中: 、 、 、
B.含大量 的溶液: 、 、 、
C.含有大量 的溶液: 、 、 、D.溶解少量 气体的溶液: 、 、 、
【答案】C
【分析】
分子或离子与金属离子结合形成很稳定的新的离子的过程叫配位反应,也称配合反应。
【解析】
A. 的溶液中,溶液中含有大量的H+,H+会与 反应生成二氧化碳和水,是复分解反应,不是
配合反应,故A错误;
B. 和 发生双水解反应,不是配合反应,故B错误;
C. 和 反应生成铁氰配合物,该反应为配合反应,故C正确;
D. 溶于水生成亚硫酸,亚硫酸具有还原性,会和 反应生成 和Cl-,发生的是氧化还原反应,
不是配合反应,故D错误;
答案选C。