文档内容
专题 十一
物质结构与性质
××
命 题 趋 势
从近几年新课标的高考试题来看,“物质结构和性质” 模块作为选考内容,仅命制一个大题——主观题
该题目一般是以元素推断或某主族元素为背景,下设4至6个小题,10个空左右进行设计,以 “拼盘”形式
呈现,题目变化多端,知识覆盖较广,考查主要涉及以下内容:
(1)原子结构:能量最低原理的应用;电子排布式、电子排布图的书写;电离能、电负性的大小比较和应
用等。
(2)分子结构:σ键、π键、配位键的分析和判断;分子的构型、分子的极性的判断;“相似相溶原理”、
等电子原理、氢键的性质等知识的应用。
(3)晶体结构:晶体中粒子数目的确定;共价键、分子间作用力、离子键和金属键的判断以及对晶体性质
的影响;常见晶体的结构及熔、沸点的比较。
今后的高考命题仍会侧重上述知识点进行设计,题型也不会有太大变化,但试题的背景会更加新颖,题
目会更加综合,更注重体现科学新成果或新发现,更注重考生 “结构决定性质”思想的树立和空间想象能力
的考查。
考 点 清 单
一、原子结构与性质
1、原子核外电子运动状态,以及电子云、电子层(能层)、原子轨道(能级)的含义。
电子云:用小黑点的疏密来描述电子在原子核外空间出现的机会大小所得的图形叫电子云图。离核越近,
电子出现的机会大,电子云密度越大;离核越远,电子出现的机会小,电子云密度越小。
电子层(能层):根据电子的能量差异和主要运动区域的不同,核外电子分别处于不同的电子层。原子
由里向外对应的电子层符号分别为K、L、M、N、O、P、Q。
原子轨道(能级即亚层):处于同一电子层的原子核外电子,也可以在不同类型的原子轨道上运动,分
别用s、p、d、f表示不同形状的轨道,s轨道呈球形、p轨道呈纺锤形,d轨道和f轨道较复杂。各轨道的伸
展方向个数依次为1、3、5、7。
2、能级交错图和1-36号元素的核外电子排布式。①根据构造原理,基态原子核外电子的排布遵循图⑴箭头所示的顺序。
②根据构造原理,可以将各能级按能量的差异分成能级组如图⑵所示,由下而上表示七个能级组,其能
量依次升高;在同一能级组内,从左到右能量依次升高。基态原子核外电子的排布按能量由低到高的顺序依
次排布。
3、元素电离能和元素电负性
(1)第一电离能:气态电中性基态原子失去1个电子,转化为气态基态正离子所需要的能量叫做第一电
离能。常用符号I 表示,单位为kJ/mol。
1
(2)元素的电负性:元素的原子在分子中吸引电子对的能力叫做该元素的电负性。
二、化键与物质的性质
1、离子键
(1)化学键:相邻原子之间强烈的相互作用,化键包括离子键、共价键和金属键。
(2)离子键:阴、阳离子通过静电作用形成的化键。
离子键强弱的判断:离子半径越小,离子所带电荷越多,离子键越强,离子晶体的熔沸点越高。
2、共价键的主要类型σ键和π键
(1)共价键的分类和判断:σ键(“头碰头”重叠)和π键(“肩碰肩”重叠)、极性键和非极性键,
还有一类特殊的共价键-配位键。
3、极性键和非极性键
(1)共价键:原子间通过共用电子对形成的化键
(2)键的极性
极性键:不同种原子之间形成的共价键,成键原子吸引电子的能力不同,共用电子对发生偏移。
非极性键:同种原子之间形成的共价键,成键原子吸引电子的能力相同,共用电子对不发生偏移。
(3)分子的极性
非极性分子和极性分子的比较
非极性分子 极性分子
形成原因 整个分子的电荷分布均匀,对称 整个分子的电荷分布不均匀、不对称
存在的共价键 非极性键或极性键 极性键分子内原子排列 对称 不对称
举例说明:
分子 共价键的极性 正负电荷中心 结论 举例
同核双原子分子 非极性键 重合 非极性分子 H、N、O
2 2 2
异核双原子分子 极性键 不重合 极性分子 CO、HF、HCl
分子中各键的向
重合 非极性分子 CO、BF、CH
量和为零 2 3 4
异核多原子分子
分子中各键的向
不重合 极性分子 HO、NH 、CHCl
量和不为零 2 3 3
相似相溶原理:极性分子易溶于极性分子溶剂中(如HCl易溶于水中),非极性分子易溶于非极性分子
溶剂中(如CO 易溶于CS 中)
2 2
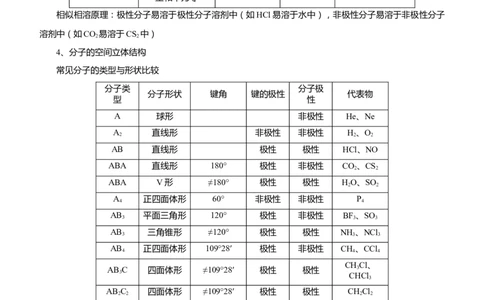
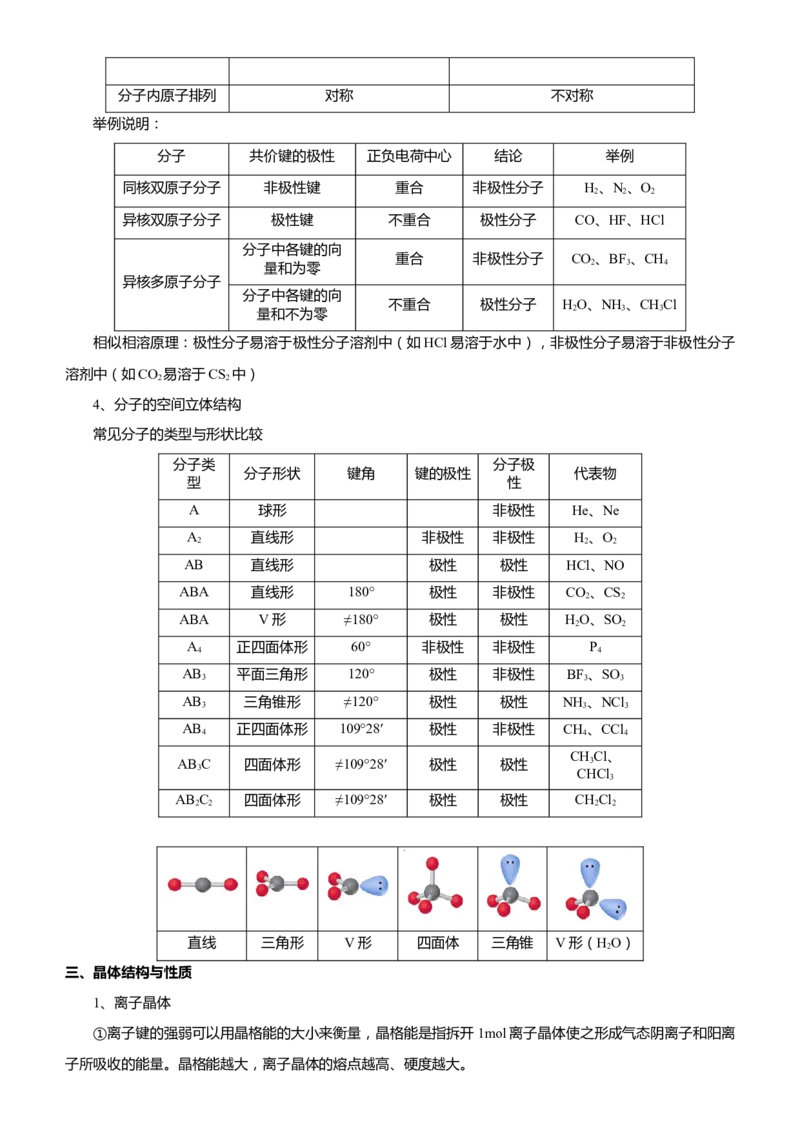
4、分子的空间立体结构
常见分子的类型与形状比较
分子类 分子极
分子形状 键角 键的极性 代表物
型 性
A 球形 非极性 He、Ne
A 直线形 非极性 非极性 H、O
2 2 2
AB 直线形 极性 极性 HCl、NO
ABA 直线形 180° 极性 非极性 CO、CS
2 2
ABA V形 ≠180° 极性 极性 HO、SO
2 2
A 正四面体形 60° 非极性 非极性 P
4 4
AB 平面三角形 120° 极性 非极性 BF、SO
3 3 3
AB 三角锥形 ≠120° 极性 极性 NH 、NCl
3 3 3
AB 正四面体形 109°28′ 极性 非极性 CH、CCl
4 4 4
CHCl、
AB C 四面体形 ≠109°28′ 极性 极性 3
3 CHCl
3
AB C 四面体形 ≠109°28′ 极性 极性 CHCl
2 2 2 2
直线 三角形 V形 四面体 三角锥 V形(HO)
2
三、晶体结构与性质
1、离子晶体
①离子键的强弱可以用晶格能的大小来衡量,晶格能是指拆开1mol离子晶体使之形成气态阴离子和阳离
子所吸收的能量。晶格能越大,离子晶体的熔点越高、硬度越大。②离子晶体:通过离子键作用形成的晶体。
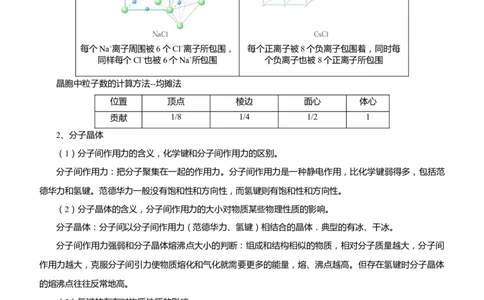
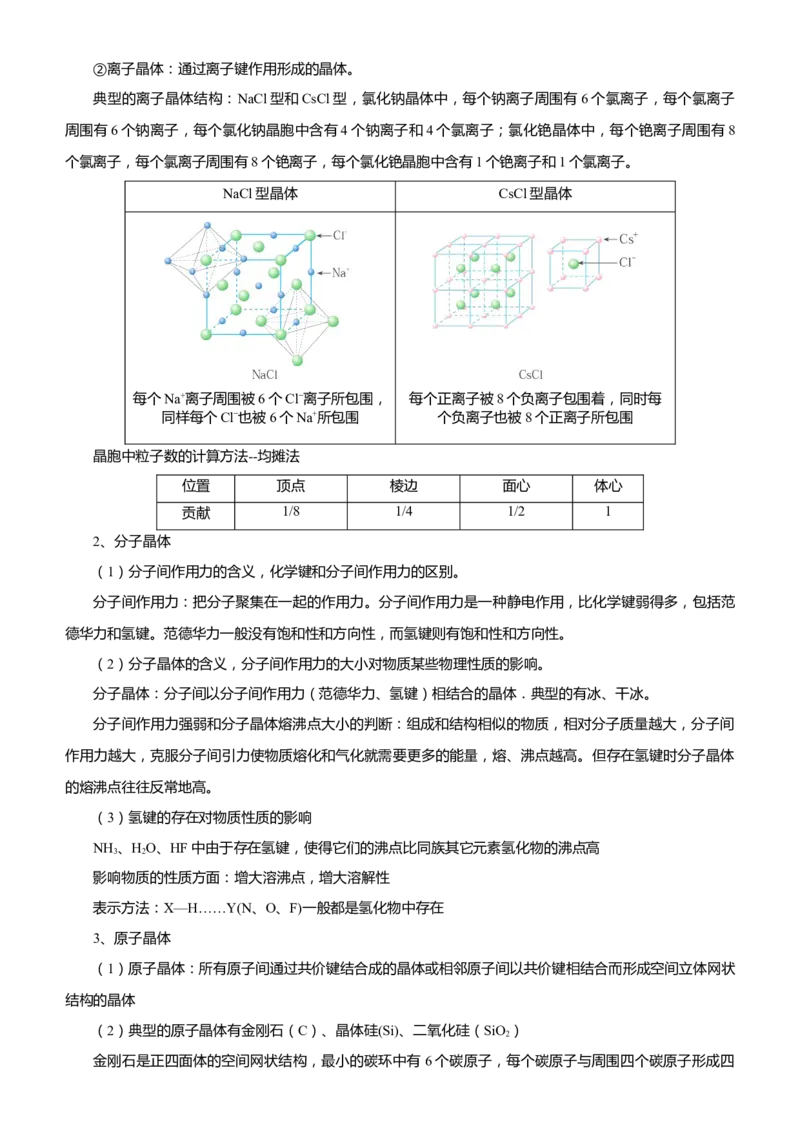
典型的离子晶体结构:NaCl型和CsCl型,氯化钠晶体中,每个钠离子周围有6个氯离子,每个氯离子
周围有6个钠离子,每个氯化钠晶胞中含有4个钠离子和4个氯离子;氯化铯晶体中,每个铯离子周围有8
个氯离子,每个氯离子周围有8个铯离子,每个氯化铯晶胞中含有1个铯离子和1个氯离子。
NaCl型晶体 CsCl型晶体
每个Na+离子周围被6个Cl−离子所包围, 每个正离子被8个负离子包围着,同时每
同样每个Cl−也被6个Na+所包围 个负离子也被8个正离子所包围
晶胞中粒子数的计算方法--均摊法
位置 顶点 棱边 面心 体心
贡献 1/8 1/4 1/2 1
2、分子晶体
(1)分子间作用力的含义,化学键和分子间作用力的区别。
分子间作用力:把分子聚集在一起的作用力。分子间作用力是一种静电作用,比化学键弱得多,包括范
德华力和氢键。范德华力一般没有饱和性和方向性,而氢键则有饱和性和方向性。
(2)分子晶体的含义,分子间作用力的大小对物质某些物理性质的影响。
分子晶体:分子间以分子间作用力(范德华力、氢键)相结合的晶体.典型的有冰、干冰。
分子间作用力强弱和分子晶体熔沸点大小的判断:组成和结构相似的物质,相对分子质量越大,分子间
作用力越大,克服分子间引力使物质熔化和气化就需要更多的能量,熔、沸点越高。但存在氢键时分子晶体
的熔沸点往往反常地高。
(3)氢键的存在对物质性质的影响
NH 、HO、HF中由于存在氢键,使得它们的沸点比同族其它元素氢化物的沸点高
3 2
影响物质的性质方面:增大溶沸点,增大溶解性
表示方法:X—H……Y(N、O、F)一般都是氢化物中存在
3、原子晶体
(1)原子晶体:所有原子间通过共价键结合成的晶体或相邻原子间以共价键相结合而形成空间立体网状
结构的晶体
(2)典型的原子晶体有金刚石(C)、晶体硅(Si)、二氧化硅(SiO)
2
金刚石是正四面体的空间网状结构,最小的碳环中有 6个碳原子,每个碳原子与周围四个碳原子形成四个共价键;晶体硅的结构与金刚石相似;二氧化硅晶体是空间网状结构,最小的环中有6个硅原子和6个氧
原子,每个硅原子与4个氧原子成键,每个氧原子与2个硅原子成键
(3)共价键强弱和原子晶体熔沸点大小的判断:原子半径越小,形成共价键的键长越短,共价键的键能
越大,其晶体熔沸点越高。如熔点:金刚石>碳化硅>晶体硅。
4、分子晶体与原子晶体、离子晶体、金属晶体的结构微粒、微粒间作用力的区别
晶体类型 原子晶体 分子晶体 金属晶体 离子晶体
粒子 原子 分子 金属阳离子、自由电子 阴、阳离子
粒子间作
共价键 分子间作用力 复杂的静电作用 离子键
用(力)
熔沸点 很高 很低 一般较高,少部分低 较高
硬度 很硬 一般较软 一般较硬,少部分软 较硬
易溶于极性
溶解性 难溶解 相似相溶 难溶(Na等与水反应)
溶剂
固体不导
不导电
电,熔化或
导电情况 一般不导电 良导体
溶于水后导
(除硅)
电
金刚石、 NaCl、
干冰、冰、纯
CaCO
实例 水晶、碳 Na、Mg、Al等 3
硫酸、H(S)
化硅等 2 NaOH等精 题 集 训
(70分钟)
经典训练题
1.(双选) Al、 P、 S、 Cl是周期表中的短周期主族元素。下列有关说法正确的是( )
13 15 16 17
A.元素Al在周期表中位于第3周期ⅢA族
B.元素P的简单气态氢化物的化学式为PH
4
C.第一电离能:I(Al)I (S),故C错误;D.非金属性越强,最高价氧化物的水化物的酸性越强,非金属性
1 1
PZ>X D.WY 是一种非极性分子
2
【答案】B
【解析】W元素2p轨道电子数为2,则电子排布式为:1s22s22p2,则W为C;X素在短周期中第一电离能
最小,同一周期,第ⅠA方族元素第一电离能最小,同一主族,从上到下,第一电离能减小,则 X为Na;Y
元素3p轨道有2个单电子有两种情况:一种是3p轨道只有2个电子,且为单电子,另一种是3p轨道有4个
电子,2个成对,2个单电子,对应的为Si、S,但W、X、Y、Z处于不同主族,所以Y为S;短周期元素
W、X、Y、Z的原子序数依次增大,所以Z为Cl。A.同一周期元素从左到右,电负性逐渐增加,元素电负
性SO-H>F-H 电负性:NHS 两种元素同主族,且半径OHBr>HCl HI、HBr、HCl中的范德华力逐渐减小
【答案】B
【解析】A.电负性:NHBr>HCl,HI、
HBr、HCl中共价键越来越强,在水中电离能力变弱,故D错误;故答案为B。
3.铑的配合物离子 可催化甲醇羰基化,反应过程如图所示:
下列叙述错误的是( )A.中心离子Rh的配位数在反应过程中没有发生变化
B.CHCOI是反应中间体
3
C.CO分子中的 键有一半为配位键
D. 的空间构型为八面体型
【答案】A
【解析】A.根据图示整个过程中中心离子Rh的变化为 、 、 、
,中心离子所连共价键数分别为4、6、5、6,所以配位数也发生了变化,故A错误;B.中间体是指在反应
过程中生成,既不是反应物,也不是最终的生成物,图示中CHCOI是反应中间体,故B正确;C.CO分子
3
的结构式为 :其与N 的结构相似,均含三重建,有一个σ键和两个π键,但在CO分子中,有一对共
2
用电子对由O提供,形成配位键,用箭头表示,故C正确;D. 结构中中心离子的配位数为6,其
空间构型为八面体,故D正确;故选A。
4.“中国芯”的主要原材料是高纯单晶硅,反应 SiCl (g)+2H(g)=====Si(s)+4HCl(g)可用于纯硅的制备。下
4 2
列有关说法正确的是( )
A.SiCl 为极性分子 B.HCl的电子式为
4
C.单晶硅为分子晶体 D.Si原子的结构示意图为
【答案】B
【解析】A.SiCl 和CH 的空间构型一样,都是正四面体构型,结构对称,为非极性分子,A错误;B.
4 4
HCl的电子式为 ,B正确;C.单晶硅与金刚石的晶体结构相似,为空间网状结构,为原子晶体,C错
误;D.Si原子的结构示意图为 ,D错误;故选B。
5.硼烯具有优异的电学、力学、热学等属性,将成为继石墨烯之后又一种“神奇纳米材料”。科学家已成功
合成多种结构的硼烯,如图为“皱褶”式硼烯的结构。下列说法错误的是( )A.“皱褶”式硼烯中每个硼原子共用3对电子
B.“皱褶”式硼烯中硼原子达到8电子稳定结构
C.硼烯有望代替石墨烯作电极材料
D.氧化硼的水化物是一种弱酸,与过量OH−反应可生成B(OH)或BO
【答案】B
【解析】A.硼原子最外层最多有3个电子,可形成3对共用电子对,达到6个电子,因此“皱褶”式硼
烯中每个硼原子共用3对电子,故A正确;B.硼原子最外层最多有3个电子,可形成3对共用电子对,达到
6个电子,因此“皱褶”式硼烯中硼原子未达到8电子稳定结构,故B错误;C.由于硼烯有着很高的表面活
性,也更容易发生化学反应,故硼烯有望代替石墨烯作电极材料,故C正确;D.氧化硼的水化物是一种弱
酸,与过量OH−反应可生成B(OH)或BO和HO,故D正确。综上所述,答案为B。
2
精准预测题
1.在催化剂作用下,O 与CO反应生成CO 的历程如下(个别微粒未画出)
2 2
下列说法不正确的是( )
A.CO 分子的空间结构是直线形
2
B.在催化剂作用下,CO中的化学键未完全断裂
C.生成CO 的过程中有非极性键形成
2
D.吸附在催化剂表面的氧原子和一氧化碳分子发生了反应
【答案】C
【解析】A.CO 分子的空间结构是直线形,故A正确;B.根据图示,在催化剂作用下,CO中的化学键
2
未完全断裂,故B正确;C.生成CO 的过程中有C=O键形成,没有形成非极性键,故C错误;D.根据图
2
示,吸附在催化剂表面的氧原子和一氧化碳分子发生反应生成二氧化碳,故D正确;选C。
2.下列说法正确的是( )
A.水稳定是因为水中含有大量的氢键
B.邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点高C.可燃冰(CH·8H O)的形成是由于甲烷分子与水分子之间存在氢键
4 2
D.氨气极易溶于水,原因之一是氨分子与水分子之间形成了氢键
【答案】D
【解析】A.水很稳定是因为水分子内的共价键较强,与氢键无关,故A错误;B.能形成分子间氢键的
熔、沸点高,邻羟基苯甲醛是分子内形成氢键,对羟基苯甲醛是分子间形成氢键,邻羟基苯甲醛的熔、沸点
比对羟基苯甲醛的熔、沸点低,故B错误;C.甲烷分子与水分子之间不存在氢键,故C错误;D.氨分子
与水分子之间形成了氢键,使氨气的溶解度增大,所以氨气极易溶于水,故D正确;故选D。
3.(双选)TiO 的“纳米材料”有广泛的应用,工业上可利用 TiCl 制取。TiCl 熔点为-25℃,沸点为
2 4 4
136.4℃。制取TiO 的反应为①2FeTiO+7Cl+3C=2TiCl +2FeCl +3CO ,②TiCl +O =TiO +2Cl ,下列说法
2 3 2 4 3 2 4 2 2 2
错误的是( )
A.CO 和CCl 中碳的杂化方式不同
2 4
B.O、Cl、CO 都是含有非极性键的非极性分子
2 2 2
C.TiCl 晶体是离子晶体,配位数为4
4
D.FeCl 与KSCN溶液生成的[Fe(SCN) ]3−中,Fe3+为中心离子,SCN−为配体
3 6
【答案】BC
【解析】A.CO 中的C为sp杂化,CCl 中的C为sp3杂化,故A正确;B.CO 结构对称,正负电荷中心
2 4 2
重合,含有极性键,但是非极性分子,故B错误;C.TiCl 晶体是分子晶体,配位数为4,故C错误;D.
4
FeCl 与KSCN溶液生成的[Fe(SCN) ]3−中,Fe3+连接了6个SCN−,则Fe3+为中心离子,SCN−为配体,故D正
3 6
确;故选BC。
4.已知:NaF的熔点993℃、MgF 的熔点1261℃。下列分析错误的是( )
2
A.NaF和MgF 均由阴、阳离子构成
2
B.离子半径和离子所带电荷数决定离子键强弱
C.NaF中的离子键比MgF 中的弱
2
D.MgF 的摩尔质量比NaF的大,所以MgF 熔点高
2 2
【答案】D
【解析】A.NaF与MgF 均为离子化合物,由阴阳离子构成,A正确;B.离子键的强弱与离子半径和离
2
子所带电荷有关,一般来说,离子半径越小,离子所带电荷越多,离子键越强,B正确;C.由于半径:
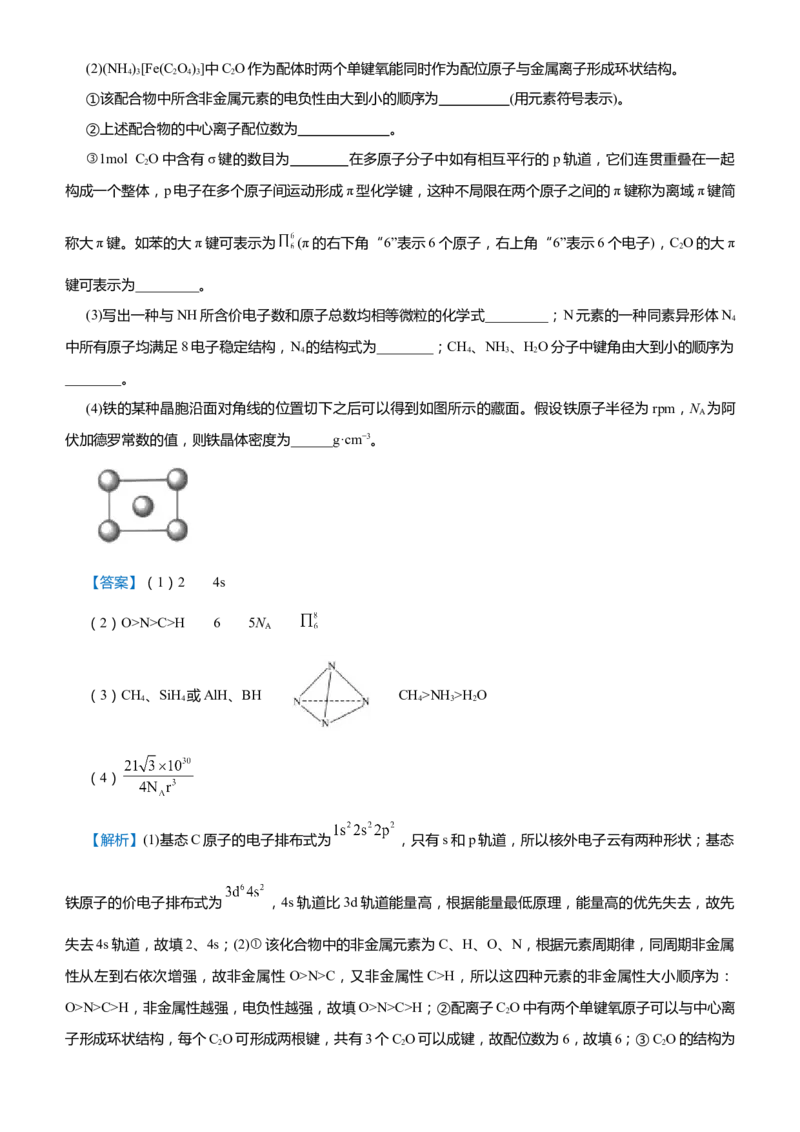
r(Mg2+)N>C>H 6 5N
A
(3)CH、SiH 或AlH、BH CH >NH>H O
4 4 4 3 2
(4)
【解析】(1)基态C原子的电子排布式为 ,只有s和p轨道,所以核外电子云有两种形状;基态
铁原子的价电子排布式为 ,4s轨道比3d轨道能量高,根据能量最低原理,能量高的优先失去,故先
失去4s轨道,故填2、4s;(2)①该化合物中的非金属元素为C、H、O、N,根据元素周期律,同周期非金属
性从左到右依次增强,故非金属性 O>N>C,又非金属性C>H,所以这四种元素的非金属性大小顺序为:
O>N>C>H,非金属性越强,电负性越强,故填O>N>C>H;②配离子C O中有两个单键氧原子可以与中心离
2
子形成环状结构,每个C O可形成两根键,共有3个C O可以成键,故配位数为6,故填6;③C O的结构为
2 2 2,其中碳氧双键中各含一个σ键和一个π键,碳氧单键、碳碳单键之间均为σ键,共有5个σ
键,即1mol C O中存在5N 个σ键,C O中碳氧双键的离域电子数为2,两个双键,共4个离域电子,碳氧
2 A 2
单键中的氧原子提供两个离域电子,这样的离域电子有 4个,共计8个离域电子,综上草酸离子的大π键可
表示为 ,故填5N 、 ;(3)价电子数=(最外层电子数—电荷数)÷2,正电荷即减,负电荷即加,铵根价电
A
子数为(5+4×1-1)÷2=4,满足价电子数为4,且原子个数为5的微粒有CH 、SiH 、AlH、BH;N 中,要N原
4 4 4
子满足8电子稳定结构,则每个N原子连三根键,满足此条件的N 的空间结构为正四面体,结构简式为
4
;电负性越强,成键电子对更偏向于电负性强的原子,NH 、CH 、HO三种物质的中心原子都是
3 4 2
sp3杂化,杂化轨道都是正四面体构形,其中CH 是等性杂化,四条杂化轨道都是成键电子,键角=正常正四
4
面体键角=109°28′,NH 和HO都是不等性杂化,中心原子N、O分别有1条、2条杂化轨道填入孤对电子,
3 2
孤对电子的排斥力比成键电子大,因此键角被压缩,孤对电子数越多,斥力越大,键角被压缩的越小,所以
键角大小顺序为CH>NH>H O。故填CH 或SiH 、AlH、BH、 、CH>NH>H O;(4)在铁晶胞中,
4 3 2 4 4 4 3 2
与一个铁原子最近的铁原子距离为立方体边长的 ,这样的原子有八个,因为铁原子的半径是r pm,根据铁
晶胞的结构可知,晶胞的边长为 ,在每个晶胞中含有铁原子的数目为 =2个,晶胞密度ρ= =
= = =
,故填 。
【点评】孤对电子的斥力大于成键电子对,孤对电子越多,斥力越大。
7.