文档内容
绝密★使用前
大连市第二十四中学 2022-2023 学年度高考适应性测试(一)
高 三 化 学
考生注意:
1.本试卷共100分,考试时间75分钟。共三大题,20小题,共8页
2.请将各题答案填写在答题卡上。
3.本试卷主要考试内容:高考全部内容
一、选择题(本题共12小题,每小题3分,共36分.在每小题给出的四个选项中,只有一项是符合题目要
求的)
1.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.7.8 g的NaS和NaO 的混合物中含有阴、阳离子总数为0.3 N
2 2 2 A
B.常温常压下,22.4 LCO 中含有N 个CO 分子
2 A 2
C.1.0 L 1.0 mol·L-1的NaClO水溶液中含有的氧原子数为N
A
D.常温常压下,18 g羟基(-O2H)中所含的中子数为8 N
A
2.在体积相同的两个密闭容器中分别充满C2H4、C3H6气体,当这两个容器内温度和气体密度相等时,下列说法
正确的是
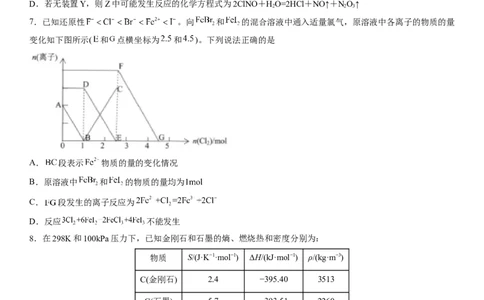
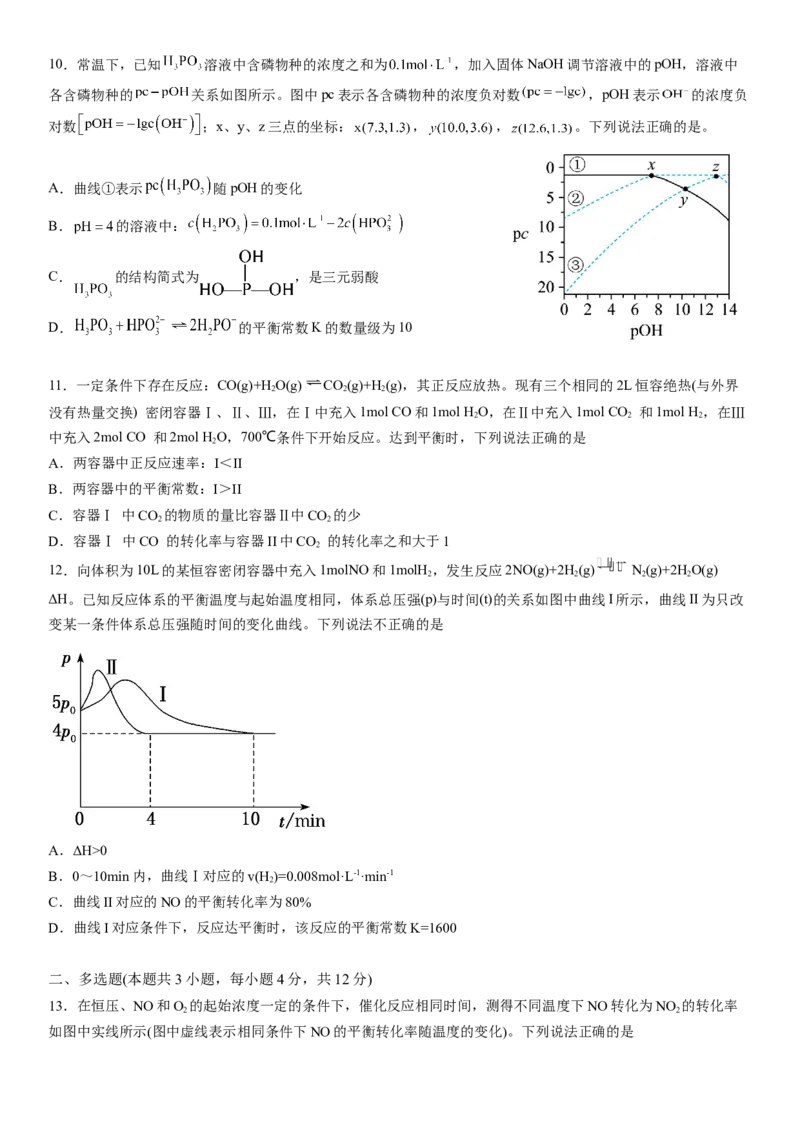
A.两种气体的压强是P(C2H4)0
B.0~10min内,曲线Ⅰ对应的v(H )=0.008mol·L-1·min-1
2
C.曲线II对应的NO的平衡转化率为80%
D.曲线I对应条件下,反应达平衡时,该反应的平衡常数K=1600
二、多选题(本题共3小题,每小题4分,共12分)
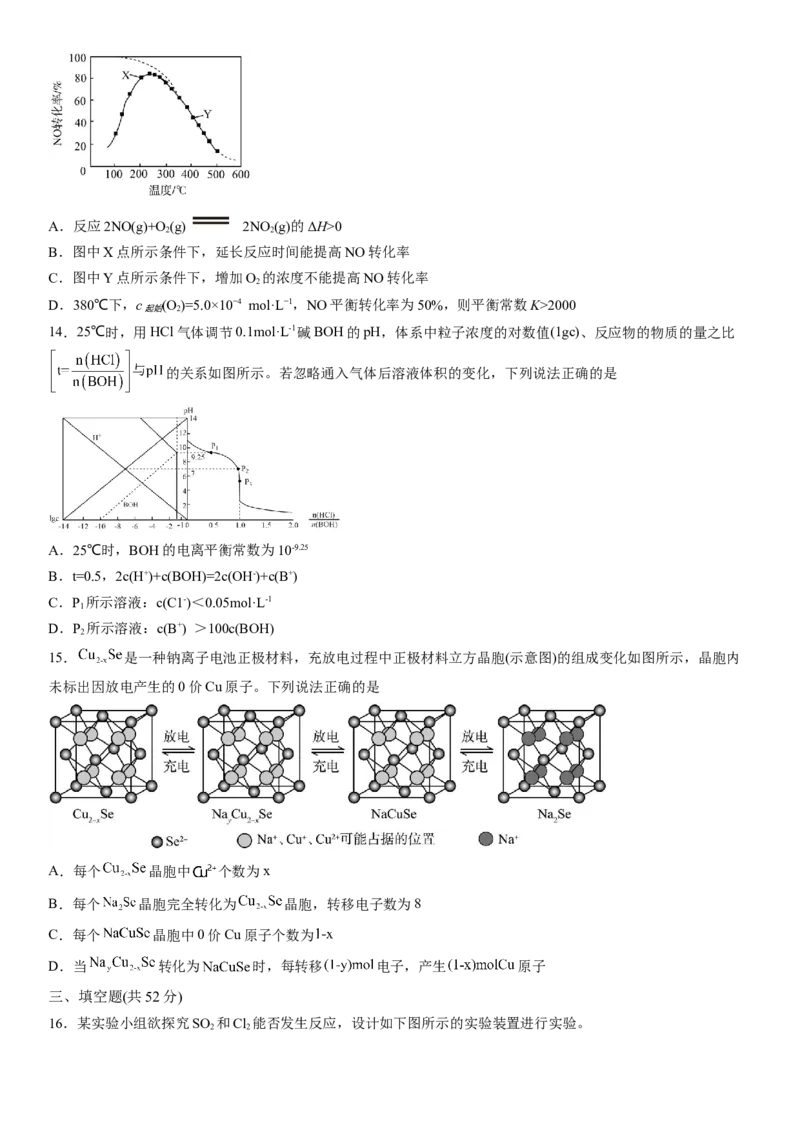
13.在恒压、NO和O 的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO 的转化率
2 2
如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是A.反应2NO(g)+O (g) 2NO (g)的ΔH>0
2 2
B.图中X点所示条件下,延长反应时间能提高NO转化率
C.图中Y点所示条件下,增加O 的浓度不能提高NO转化率
2
D.380℃下,c (O )=5.0×10−4 mol·L−1,NO平衡转化率为50%,则平衡常数K>2000
起始 2
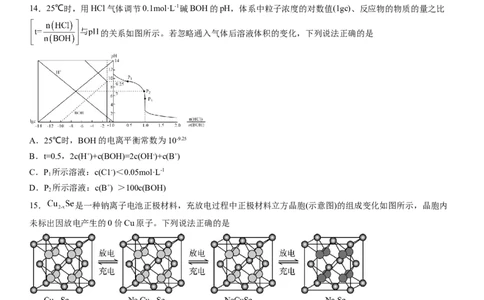
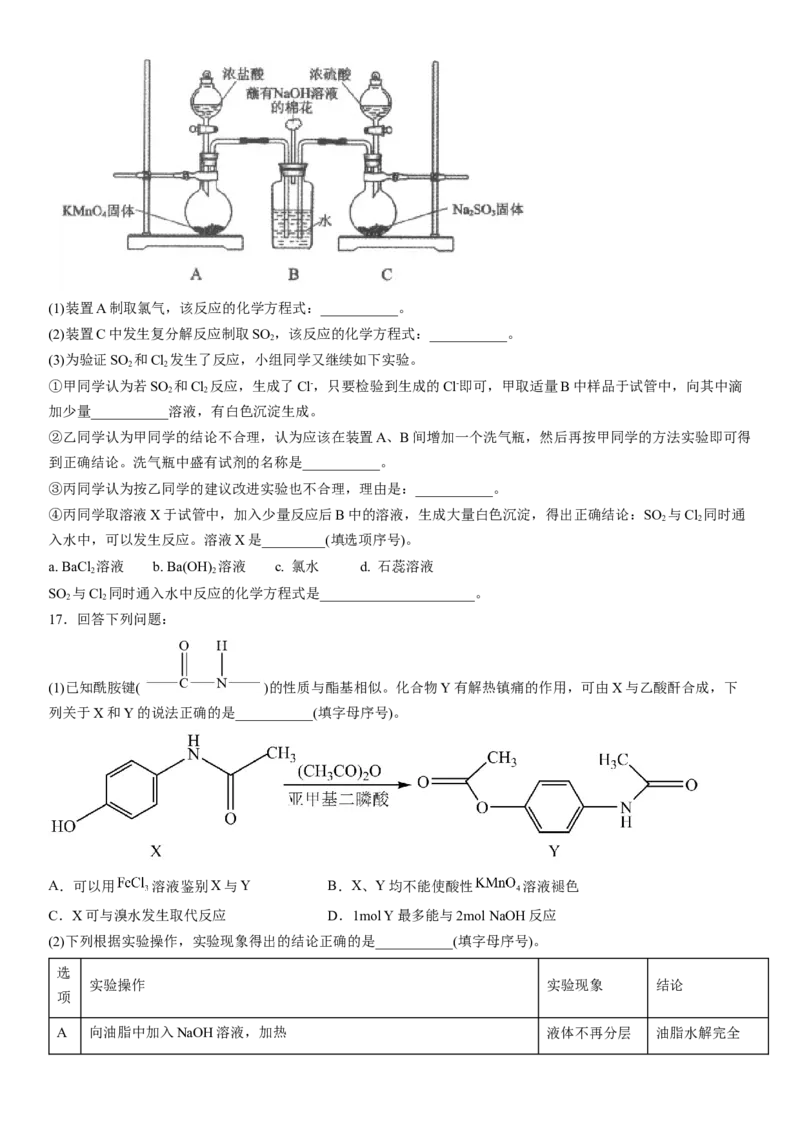
14.25℃时,用HCl气体调节0.1mol·L-1碱BOH的pH,体系中粒子浓度的对数值(1gc)、反应物的物质的量之比
的关系如图所示。若忽略通入气体后溶液体积的变化,下列说法正确的是
A.25℃时,BOH的电离平衡常数为10-9.25
B.t=0.5,2c(H+)+c(BOH)=2c(OH-)+c(B+)
C.P 所示溶液:c(C1-)<0.05mol·L-1
1
D.P 所示溶液:c(B+) >100c(BOH)
2
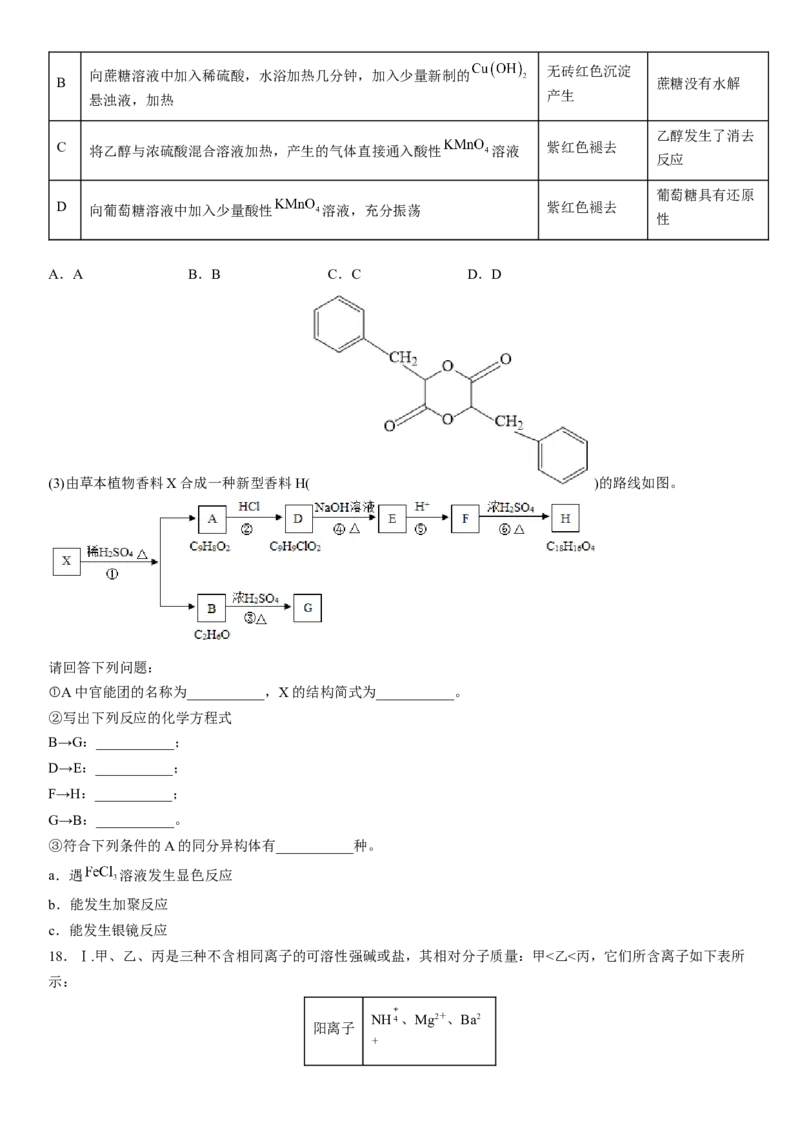
15. 是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)的组成变化如图所示,晶胞内
未标出因放电产生的0价Cu原子。下列说法正确的是
A.每个 晶胞中 个数为x
B.每个 晶胞完全转化为 晶胞,转移电子数为8
C.每个 晶胞中0价Cu原子个数为
D.当 转化为 时,每转移 电子,产生 原子
三、填空题(共52分)
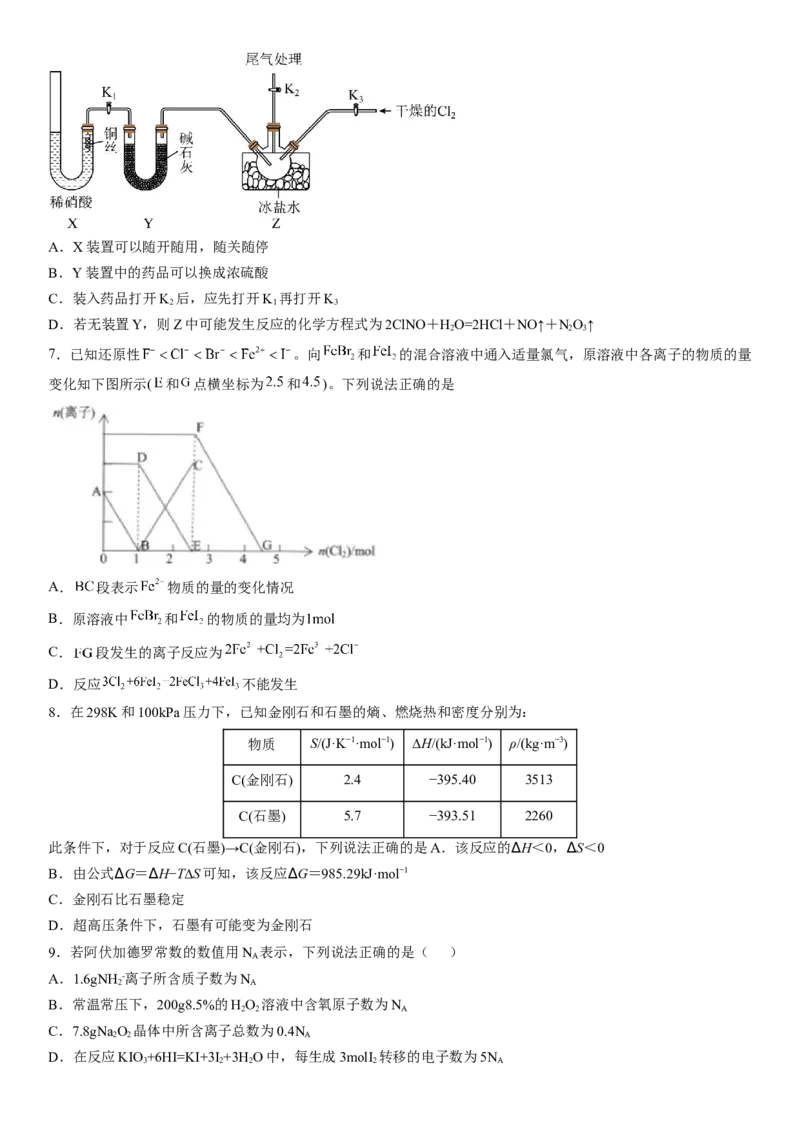
16.某实验小组欲探究SO 和Cl 能否发生反应,设计如下图所示的实验装置进行实验。
2 2(1)装置A制取氯气,该反应的化学方程式:___________。
(2)装置C中发生复分解反应制取SO ,该反应的化学方程式:___________。
2
(3)为验证SO 和Cl 发生了反应,小组同学又继续如下实验。
2 2
①甲同学认为若SO 和Cl 反应,生成了Cl-,只要检验到生成的Cl-即可,甲取适量B中样品于试管中,向其中滴
2 2
加少量___________溶液,有白色沉淀生成。
②乙同学认为甲同学的结论不合理,认为应该在装置A、B间增加一个洗气瓶,然后再按甲同学的方法实验即可得
到正确结论。洗气瓶中盛有试剂的名称是___________。
③丙同学认为按乙同学的建议改进实验也不合理,理由是:___________。
④丙同学取溶液X于试管中,加入少量反应后B中的溶液,生成大量白色沉淀,得出正确结论:SO 与Cl 同时通
2 2
入水中,可以发生反应。溶液X是_________(填选项序号)。
a. BaCl 溶液 b. Ba(OH) 溶液 c. 氯水 d. 石蕊溶液
2 2
SO 与Cl 同时通入水中反应的化学方程式是______________________。
2 2
17.回答下列问题:
(1)已知酰胺键( )的性质与酯基相似。化合物Y有解热镇痛的作用,可由X与乙酸酐合成,下
列关于X和Y的说法正确的是___________(填字母序号)。
A.可以用 溶液鉴别X与Y B.X、Y均不能使酸性 溶液褪色
C.X可与溴水发生取代反应 D.1mol Y最多能与2mol NaOH反应
(2)下列根据实验操作,实验现象得出的结论正确的是___________(填字母序号)。
选
实验操作 实验现象 结论
项
A 向油脂中加入NaOH溶液,加热 液体不再分层 油脂水解完全无砖红色沉淀
向蔗糖溶液中加入稀硫酸,水浴加热几分钟,加入少量新制的
B 蔗糖没有水解
产生
悬浊液,加热
乙醇发生了消去
C 将乙醇与浓硫酸混合溶液加热,产生的气体直接通入酸性 溶液 紫红色褪去
反应
葡萄糖具有还原
D 向葡萄糖溶液中加入少量酸性 溶液,充分振荡 紫红色褪去
性
A.A B.B C.C D.D
(3)由草本植物香料X合成一种新型香料H( )的路线如图。
请回答下列问题:
①A中官能团的名称为___________,X的结构简式为___________。
②写出下列反应的化学方程式
B→G:___________;
D→E:___________;
F→H:___________;
G→B:___________。
③符合下列条件的A的同分异构体有___________种。
a.遇 溶液发生显色反应
b.能发生加聚反应
c.能发生银镜反应
18.Ⅰ.甲、乙、丙是三种不含相同离子的可溶性强碱或盐,其相对分子质量:甲<乙<丙,它们所含离子如下表所
示:
NH 、Mg2+、Ba2
阳离子
+阴离子 OH-、NO 、Cl-
(1)丙是_________。
(2)甲有两种可能,为了确定是哪种可能,请设计实验确定甲的物质组成,操作为:_________。
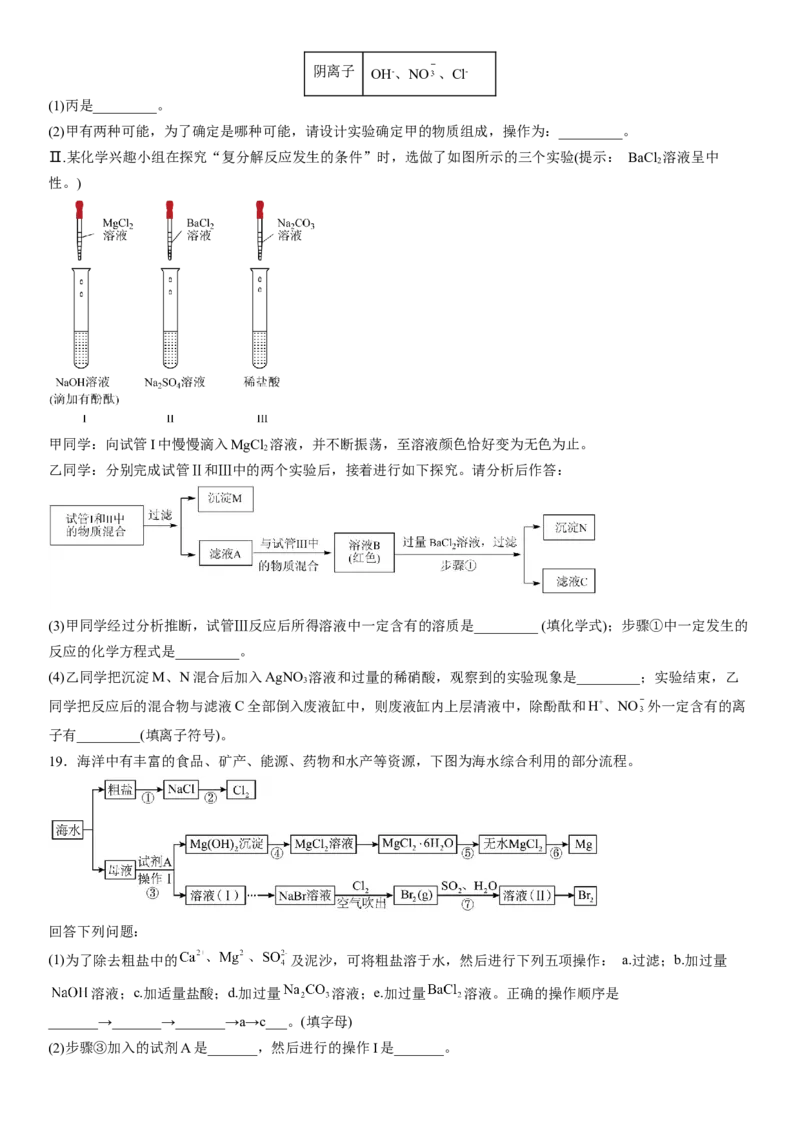
Ⅱ.某化学兴趣小组在探究“复分解反应发生的条件”时,选做了如图所示的三个实验(提示: BaCl 溶液呈中
2
性。)
甲同学:向试管I中慢慢滴入MgCl 溶液,并不断振荡,至溶液颜色恰好变为无色为止。
2
乙同学:分别完成试管Ⅱ和Ⅲ中的两个实验后,接着进行如下探究。请分析后作答:
(3)甲同学经过分析推断,试管Ⅲ反应后所得溶液中一定含有的溶质是_________ (填化学式);步骤①中一定发生的
反应的化学方程式是_________。
(4)乙同学把沉淀M、N混合后加入AgNO 溶液和过量的稀硝酸,观察到的实验现象是_________;实验结束,乙
3
同学把反应后的混合物与滤液C全部倒入废液缸中,则废液缸内上层清液中,除酚酞和H+、NO 外一定含有的离
子有_________(填离子符号)。
19.海洋中有丰富的食品、矿产、能源、药物和水产等资源,下图为海水综合利用的部分流程。
回答下列问题:
(1)为了除去粗盐中的 及泥沙,可将粗盐溶于水,然后进行下列五项操作: a.过滤;b.加过量
溶液;c.加适量盐酸;d.加过量 溶液;e.加过量 溶液。正确的操作顺序是
_______→_______→_______→a→c___。(填字母)
(2)步骤③加入的试剂A是_______,然后进行的操作I是_______。(3)步骤①~⑦中,涉及氧化还原反应的步骤有_______。
(4)步骤⑥的化学方程式为_______。
(5)步骤⑦的离子方程式为_______。
(6)将 海水浓缩至 ,使用上述流程中的生产方法最终得到 ,若 的提取率为55%,则海水中溴的浓
度为_______ 。(计算结果保留两位有效数字)
20.氟是人体必需元素之一,氟化物有阻止龋齿发生的作用,含氟牙膏使人们的牙齿更健康。
(1)基态F原子的电子排布图为___________。
(2) 和 的晶格能由大到小的顺序是___________;元素 中第一电离能最小的是___________。
(3) 分子中氧原子的杂化轨道类型为___________。 分子的立体构型为___________。 和 的沸点
依次升高的原因是___________。
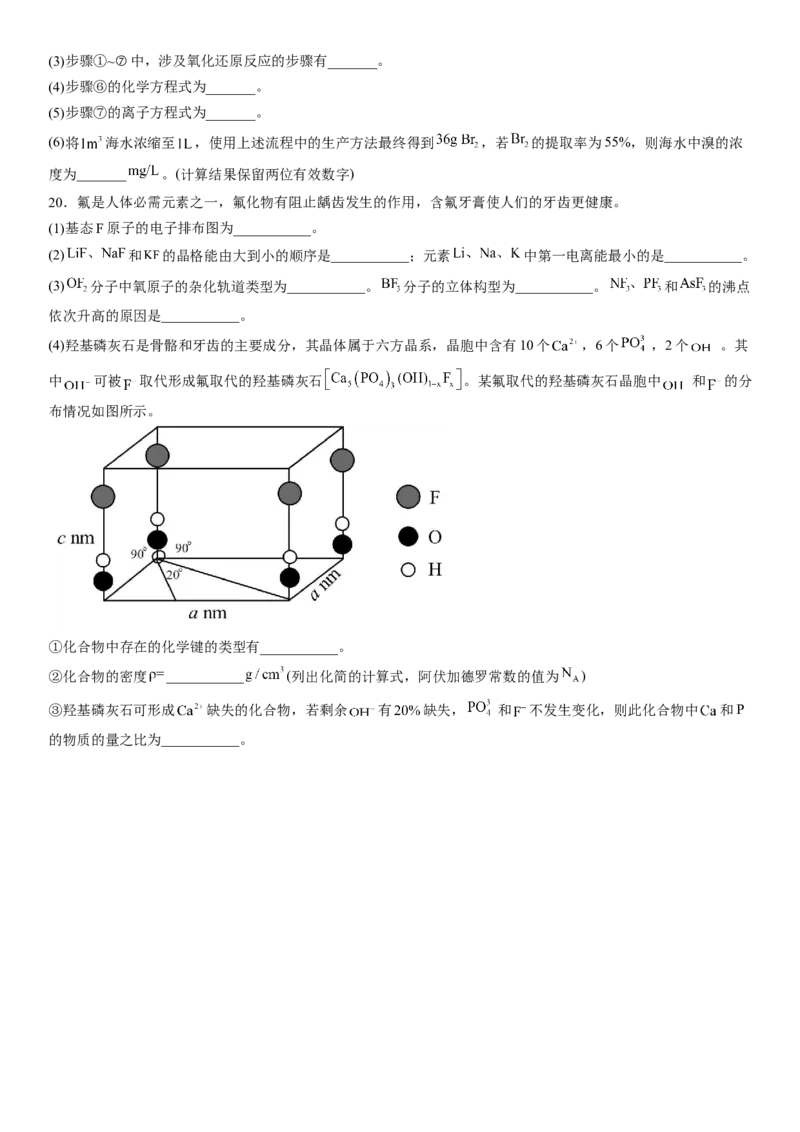
(4)羟基磷灰石是骨骼和牙齿的主要成分,其晶体属于六方晶系,晶胞中含有10个 ,6个 ,2个 。其
中 可被 取代形成氟取代的羟基磷灰石 。某氟取代的羟基磷灰石晶胞中 和 的分
布情况如图所示。
①化合物中存在的化学键的类型有___________。
②化合物的密度 ___________ (列出化简的计算式,阿伏加德罗常数的值为 )
③羟基磷灰石可形成 缺失的化合物,若剩余 有 缺失, 和 不发生变化,则此化合物中 和P
的物质的量之比为___________。