文档内容
第二章 分子结构与性质
第一节 共价键
2.1.2 键参数—键能、键长与键角
一.选择题
1.键长、键角和键能是描述共价键的三个重要参数,下列叙述正确的是( )
A. 键角是描述分子立体构型的重要参数
B. 因为H—O键的键能小于H—F键的键能,所以O、F 与H 反应的能力逐渐减弱
2 2 2
C. 水分子的结构可表示为H—O—H,分子中的键角为180°
D. H—O键的键能为463 kJ·mol-1,即18 g HO分解成H 和O 时,消耗的能量为2×463 kJ
2 2 2
【答案】A
【解析】H—O键、H—F键的键能依次增大,意味着形成这些键时放出的能量依次增大,化学键越
来越稳定,O 、F 与H 反应的能力逐渐增强,B项错误;水分子呈V形,键角为105°,C项错误;
2 2 2
H—O键的键能为463 kJ·mol-1,指的是断开1 mol H—O键形成气态氢原子和气态氧原子所需吸收
的能量为463 kJ,18 g H O即1 mol H O中含2 mol H—O键,断开时需吸收2×463 kJ的能量形成气
2 2
态氢原子和气态氧原子,再进一步形成H 和O 时,还会释放出一部分能量,D项错误。
2 2
2.下列分子或离子中键角由大到小的排列顺序是( )
①SO ②NH ③HO ④CH ⑤CO
2 3 2 4 2
A. ⑤④①②③ B. ⑤①④②③ C. ④①②⑤③ D. ③②④①⑤
【答案】B
【解析】①SO 分子为V形结构,键角为120°;②NH 为三角锥形结构,键角为107°;③HO为
2 3 2
V形结构,键角为105°;④CH 为正四面体结构,键角为109°28′;⑤CO 为直线形结构,键角为
4 2
180°。所以键角的大小顺序为CO>SO>CH >NH>H O,所以B正确。
2 2 4 3 2
3.根据如表所列键能数据,下列分子中最不稳定的是( )
A. HCl B. HBr C. H D. Br
2 2
【答案】D
【解析】由题表中数据可知,分子中键能:E(H )>E(HCl)>E(HBr)>E(Cl )>E(Br),键能越大越稳定,
2 2 2
故Br 分子最不稳定,D项符合题意。
24.三氯化磷分子的立体构型是三角锥形而不是平面正三角形,下列关于三氯化磷分子立体构型理由
的叙述,不正确的是( )
A. PCl 分子中三个P—Cl共价键的键长、键角均相等
3
B. PCl 分子中三个P—Cl共价键的键能、键角均相等
3
C. PCl 分子中的P—Cl键属于极性共价键
3
D. PCl 是非极性分子
3
【答案】D
【解析】PCl 分子是由P—Cl极性键构成的极性分子,其结构类似于NH 。
3 3
5.已知 N—N、N==N、N≡N 键能之比为 1.00∶2.17∶4.90,而 C—C,C==C,C≡C 键能之比为
1.00∶1.17∶2.34。下列有关叙述,不正确的是( )
A. 乙烯分子中σ键、π键的电子云形状对称性不同
B. 乙炔分子中π键重叠程度比σ键小,易发生加成反应
C. 氮分子中的N≡N键非常牢固,不易发生加成反应
D. 氮气和乙炔都易在空气中点燃燃烧
【答案】D
【解析】由题意知,N≡N键键能大于N—N键键能的三倍,N==N键键能大于N—N键键能的两倍;
而C≡C键键能小于C—C键键能的三倍,C==C键键能小于C—C键键能的两倍。由键能知,乙炔
分子和乙烯分子中的π键不牢固,易发生加成反应,也易发生氧化反应;而氮分子中的 N≡N键非
常牢固,化学性质稳定,不易发生加成反应及氧化反应,B、C正确,D错误。σ键的电子云形状呈
轴对称,π键的电子云形状呈镜面对称,A正确。
6.下列共价键的键能最大的是( )
A. H—F B. H—O C. H—N D. H—C
【答案】A
【解析】因为原子半径C>N>O>F,H原子半径相同,键长由大到小依次为H—C> H—N> H—O> H
—F,键长越大键能越小,所以键能由大到小依次E >E >E >E 。
H—F H—O H—N H—C
7.下列说法中正确的是( )
A. 分子中键能越大,键长越长,则分子越稳定
B. 元素周期表中的ⅠA族(除H外)和ⅦA族元素的原子间可能形成共价键
C. 水分子可表示为H—O—H,分子中键角为180°
D. H—O键键能为463 kJ/mol,即18 g HO分解成H 和O 时,消耗能量为2×463 kJ
2 2 2
【答案】B
【解析】D中H—O键键能为463 kJ/mol,指的是气态基态氢原子和氧原子形成1 mol H—O键时释
放的最低能量,则拆开1 mol H—O键形成气态氢原子和氧原子所需吸收的能量也为463 kJ,18 g H O
2即1 mol H O中含2 mol H—O键,断开时需吸收2×463 kJ的能量形成气态氢原子和氧原子,再进一
2
步形成H 和O 时,还需释放出一部分能量,需知H—H和O===O的键能,故D错;Li的电负性
2 2
为1.0,I的电负性为2.5,其差值为1.5<1.7,所以LiI以共价键成分为主,B项正确。
8.下列事实不能用键能的大小来解释的是( )
A. N元素的电负性较大,但N 的化学性质很稳定
2
B. 惰性气体一般难发生反应
C. HF、HCl、HBr、HI的稳定性逐渐减弱
D. F 比O 更容易与H 反应
2 2 2
【答案】B
【解析】本题主要考查键参数的应用。由于N 分子中存在三键,键能很大,破坏共价键需要很大
2
的能量,所以N 的化学性质很稳定;惰性气体都为单原子分子,分子内部没有化学键;卤族元素
2
从F到I原子半径逐渐增大,其氢化物中的键长逐渐变长,键能逐渐变小,所以稳定性逐渐减弱;
由于H—F的键能大于H—O,所以二者比较,更容易生成HF。
9.碳化硅(SiC)的一种晶体具有类似金刚石的结构,其中碳原子与硅原子的位置是交替的,在
下列三种晶体中,它们的熔点从高到低的顺序是( )
①金刚石 ②晶体硅 ③碳化硅
A. ①③② B. ②③① C. ③①② D. ②①③
【答案】A
【解析】 这三种晶体属同种类型,熔化时需破坏共价键,①金刚石中为C—C键,②晶体硅中为
Si—Si键,③SiC中为Si—C键,由原子半径可知Si—Si键键长最大,C—C键键长最小,
键长越短共价键越稳定,破坏时需要的热量越多,故熔点从高到低顺序为①③②。
10.下列说法中正确的是( )
A. 双原子分子中化学键键能越大,分子越稳定
B. 双原子分子中化学键键长越长,分子越稳定
C. 双原子分子中化学键键角越大,分子越稳定
D. 在双键中,σ键的键能要小于π键的
【答案】 A
【解析】 在双原子分子中没有键角,故C错;当其键能越大,键长越短时,分子越稳定,故A
对,B错;D中σ键的重叠程度要大于π键的,故σ键的键能要大于π键的。
11.根据下表中所列的键能数据,判断下列分子中最不稳定的是( )A. HCl B. HBr C. H D. Br
2 2
【答案】D
【解析】分子中共价键键能越大,键长越短,键越牢固,分子越稳定。
12.(多选)HS分子中两个共价键的夹角接近90°,其原因是( )
2
A. 共价键的饱和性
B. S原子电子排布
C. 共价键的方向性
D. S原子中p轨道的形状
【答案】CD
【解析】 S原子的价电子构型是3s23p4,有2个未成对电子,并且分布在相互垂直的3p 和3p 轨
x y
道中,当与2个H原子配对成键时,形成的两个共价键间夹角应接近90°,这体现了共价
键的方向性是由轨道的伸展方向决定的。
二、填空题
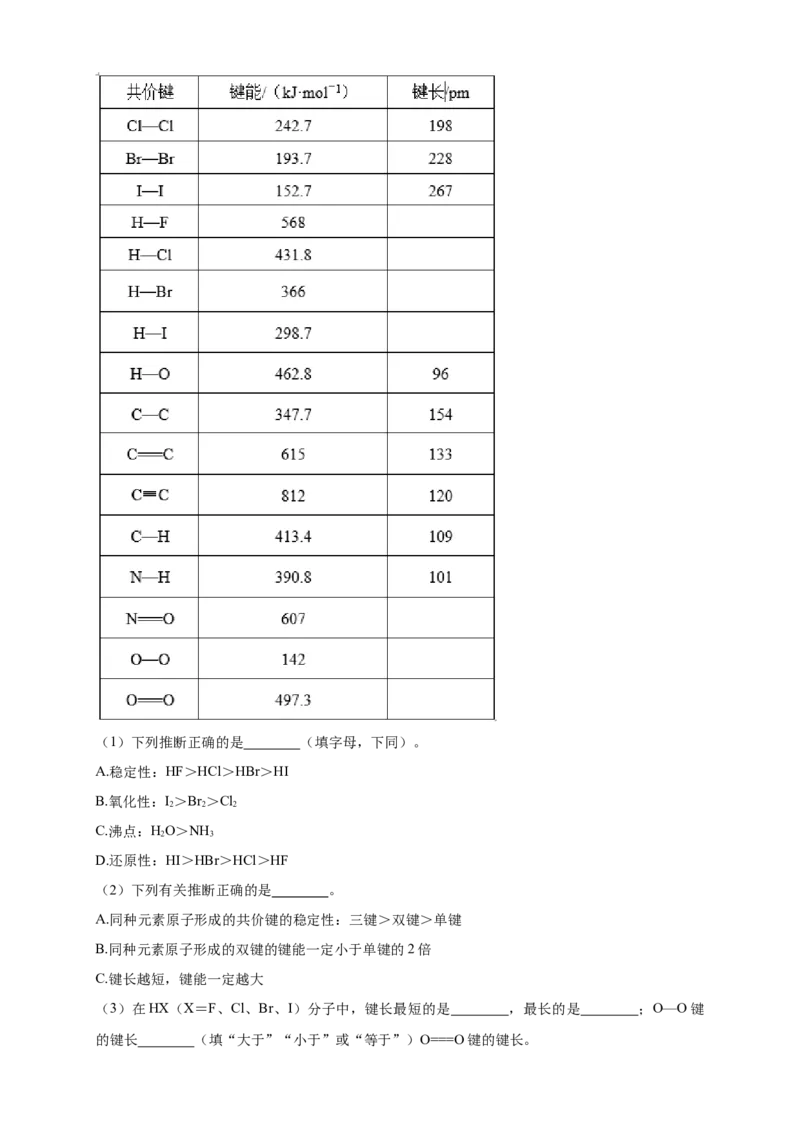
13.已知某些共价键的键能、键长数据如表所示:(1)下列推断正确的是 (填字母,下同)。
A.稳定性:HF>HCl>HBr>HI
B.氧化性:I>Br >Cl
2 2 2
C.沸点:HO>NH
2 3
D.还原性:HI>HBr>HCl>HF
(2)下列有关推断正确的是 。
A.同种元素原子形成的共价键的稳定性:三键>双键>单键
B.同种元素原子形成的双键的键能一定小于单键的2倍
C.键长越短,键能一定越大
(3)在HX(X=F、Cl、Br、I)分子中,键长最短的是 ,最长的是 ;O—O键
的键长 (填“大于”“小于”或“等于”)O===O键的键长。【答案】(1)ACD (2)A (3)HF HI 大于
【解析】(1)根据表中数据知,同主族元素从上至下气态氢化物的键能逐渐减小,稳定性逐渐减
弱,A项正确;从键能看,氯气、溴单质、碘单质的稳定性逐渐减弱,由原子结构知,氧化性也逐
渐减弱,B项错误;HO在常温下为液态,NH 在常温下为气态,则HO的沸点比NH 的高,C项
2 3 2 3
正确;还原性与得失电子能力有关,还原性:HI>HBr>HCl>HF,D项正确。(2)键能越大,化
学键越稳定,越不容易断裂,由表中碳碳键的数据知 A项正确;由O—O键、O===O键的键能知,
B项错误;C—H键的键长大于N—H键的键长,但是N—H键的键能反而较小,C项错误。
14.据报道,科研人员应用计算机模拟出结构类似 C 的物质N ,已知N 分子中每个氮原子均以N
60 60 60
—N键结合三个N原子而形成8电子稳定结构。已知N—N键键能为159 kJ·mol-1,试回答下列问题
(1) 根 据 上 述 信 息 推 测 N 的 结 构 特 点 :
60
_________________________________________________________。
(2)1 mol N 分解成N 时吸收或放出的热量是____kJ。(已知N≡N的键能为946 kJ·mol-1)
60 2
(3) 由 (2) 列 举 N 的 一 些 用 途 :
60
_________________________________________________________________。
(4)若N 分子中只含x个五边形和y个六边形,则x=________,y=____________。(已知:多面体
60
中,棱边数=顶点数+面数-2)
(5)∠NNN=________。
【答案】 (1)全部为N—N单键,共90个N—N单键构成一个N (2)14070 (3)N 可作炸药
60 60
(4)12 20 (5)108°或120°
【解析】 (1)N 中化学键全部为N—N单键,共有 个,即由90个N—N键构成一个
60
N 分子。
60
(2)ΔH=30×946 kJ·mol-1-90×159 kJ·mol-1=14 070 kJ·mol-1。
(3)由于N 分解成N 时放出大量的热量,故可制作高能炸药。
60 2
(4)N 的多面体分子共有90条棱边(N—N键),则可得方程式: ,根据多面体欧拉定
60
律可得方程式:60+(x+y)-90=2,解上述方程式得x=12,y=20。
(5)∠NNN有两种,一种为正五边形夹角,另一种为正六边形夹角。
15.某些化学键的键能如下表所示(单位kJ·mol-1):(1)1 mol H 在2 mol Cl 中燃烧,放出的热量为____kJ。
2 2
(2)在一定条件下,1 mol H 与足量的Cl、Br 、I 分别反应,放出热量由多到少的是________。
2 2 2 2
A.Cl>Br >I B.I>Br >Cl
2 2 2 2 2 2
预测1 mol H 在足量F 中燃烧比在足量Cl 中燃烧放热________________(填“多”或“少”)。
2 2 2
【答案】 (1)184.9 (2)A 多
【解析】由题中键能数据求反应热:
H+Cl===2HCl
2 2
ΔH=436.0 kJ·mol-1+242.7 kJ·mol-1-2×431.8 kJ·mol-1=-184.9 kJ·mol-1
H+Br ===2HBr
2 2
ΔH=436.0 kJ·mol-1+193.7 kJ·mol-1-2×366 kJ·mol-1=-102.3 kJ·mol-1
H+I==2HI
2 2
ΔH=436.0 kJ·mol-1+152.7 kJ·mol-1-2×298.7 kJ·mol-1=-8.7 kJ·mol-1
16.氮是地球上极为丰富的元素。
(1)Li N晶体中氮以N3-形式存在,基态N3-的电子排布式为________________。
3
(2)N≡N的键能为945 kJ·mol-1,N—N单键的键能为247 kJ·mol-1,计算说明N 中的________键
2
比____________________________________________________________键稳定(填“σ”或“π”)。
【答案】 (1)1s22s22p6 (2)π σ
【解析】 (1)由LiN晶体中氮以N3-形式存在,则N3-的最外层应达到8电子,即电子排布式为
3
1s22s22p6。
(2)N≡N中有两个π键和一个σ键,而N—N键为σ键,键能为247 kJ·mol-1,由N≡N的键能为945
kJ·mol-1,则π键键能为
=349 kJ·mol-1。