AI生成纳米抗体,复旦团队用文字生成器的思路“编写”纳米抗体,体外验证有效
复旦大学黄强团队在 《Computational and Structural Biotechnology Journal》 发表研究,开发了生成对抗网络模型AiCDR,实现了从序列生成到结构表位分析的全流程计算纳米抗体设计。该方法无需动物免疫,仅通过生成多样化CDR3序列并嫁接至人源化支架,即构建了包含5,194个高置信度结构的纳米抗体库。针对SARS-CoV-2 Omicron RBD的验证中,两个候选纳米抗体表现出体外中和活性,证明基于深度学习的“无中生有”抗体设计策略切实可行。
研究流程:
构建AiCDR模型(双外部引导器)→ 训练170万天然CDR3 → 生成9,984条序列 → 嫁接至Caplacizumab支架 → AlphaFold2预测结构 → pLDDT筛选得5,194个高质量模型 → 对接六种靶蛋白 → 高通量表位分析 → 筛选10个候选 → 假病毒中和验证

一、为什么是突破?——“GAN文字生成器”让纳米抗体设计从实验走向“思维”
方法+成果:首次将生成对抗网络与结构表位分析深度融合,实现无需动物免疫的纳米抗体计算设计。AiCDR通过双外部引导器(区分随机序列与功能多肽)提升生成序列的天然性与多样性,95.69%为全新序列,经计算筛选的候选在体外具有中和活性,形成“生成-预测-验证”完整闭环。
二、实验如何环环相扣?——从AI训练到实验验证的严密逻辑链
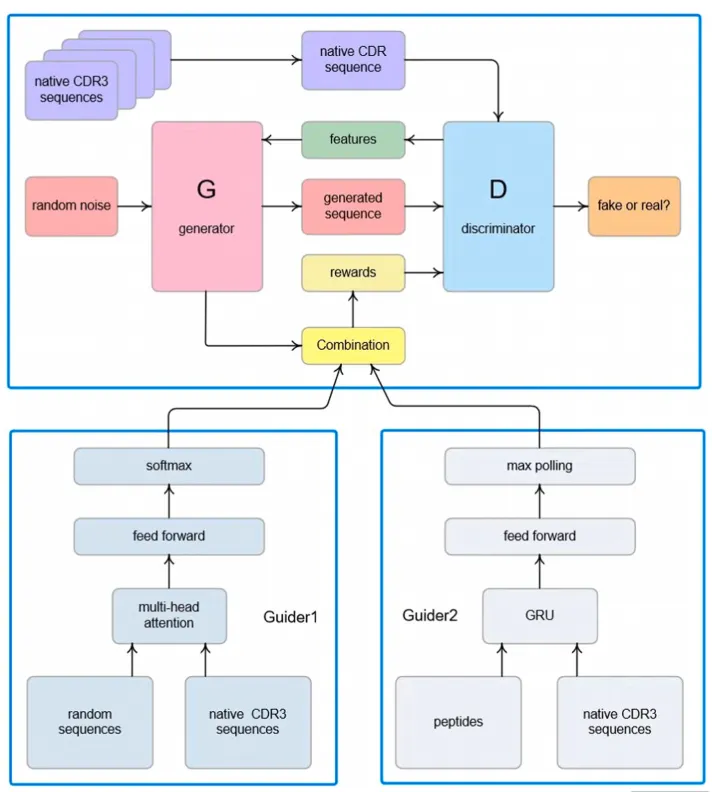
1. 模型架构与训练
AiCDR基于LeakGAN框架,包含生成器、判别器和两个外部引导器。Guider1(自注意力)区分CDR3与随机序列;Guider2(GRU)区分CDR3与功能多肽。训练集含170万天然CDR3。经61组权重组合筛选,α=0.6、β=0.3、γ=0.1时效果最佳(第198个epoch相似性峰值284)。
意义:双引导器使生成序列“像天然CDR3”而非随机序列或功能多肽。
2. 生成序列自然性与多样性
生成9,984条CDR3(长5-25 aa,主峰16-20 aa)。氨基酸组成及9种理化性质与天然CDR3高度一致(t-SNE重叠)。95.69%为全新序列,聚成1,308个独特簇,证明模型具备“创造”而非“复述”能力。
意义:生成序列空间高度多样,可用于多靶点筛选。
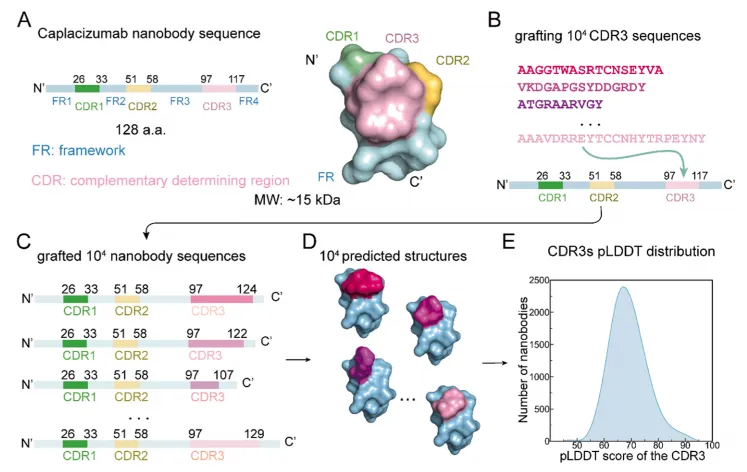
3. 纳米抗体结构库构建
将9,984条CDR3嫁接入人源化支架Caplacizumab(已上市,低免疫原性)的CDR3区。AlphaFold2预测结构后,经pLDDT>65筛选,获5,194个高置信度纳米抗体模型。
意义:从序列到结构规模化转化,为高通量虚拟筛选奠基。
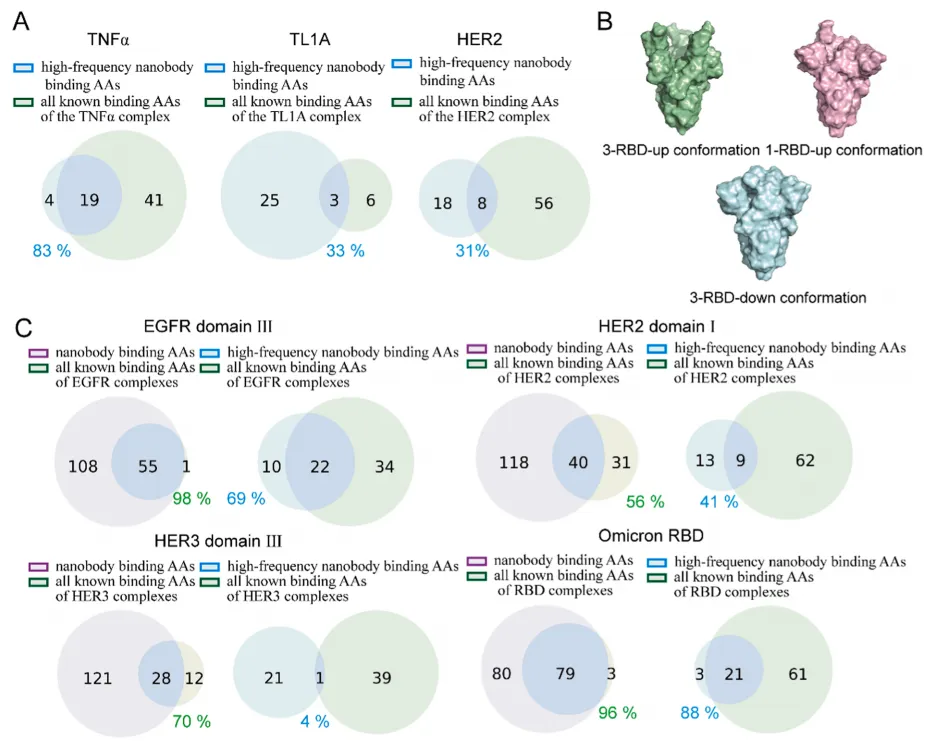
4. 表位全景分析
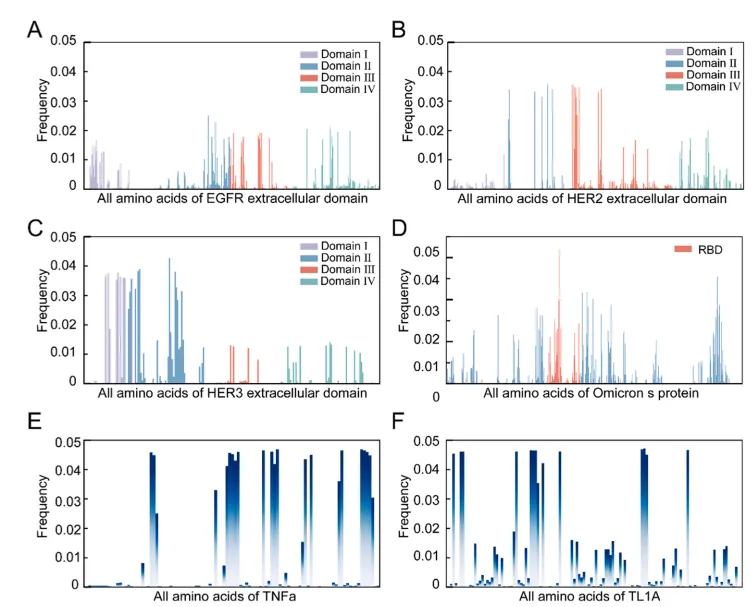
针对TNFα、TL1A、EGFR、HER2、HER3、Omicron S六种靶点,进行5,194×6=31,164次HDOCK对接。设高频接触阈值19.2%(至少被1,000个纳米抗体接触)。TNFα、TL1A、HER2的高频区与已知表位重叠80-100%;Omicron S全蛋白仅1.8%,聚焦RBD域后提升至88%。
意义:结构库能识别功能相关表位,多结构域靶点需功能域聚焦分析。
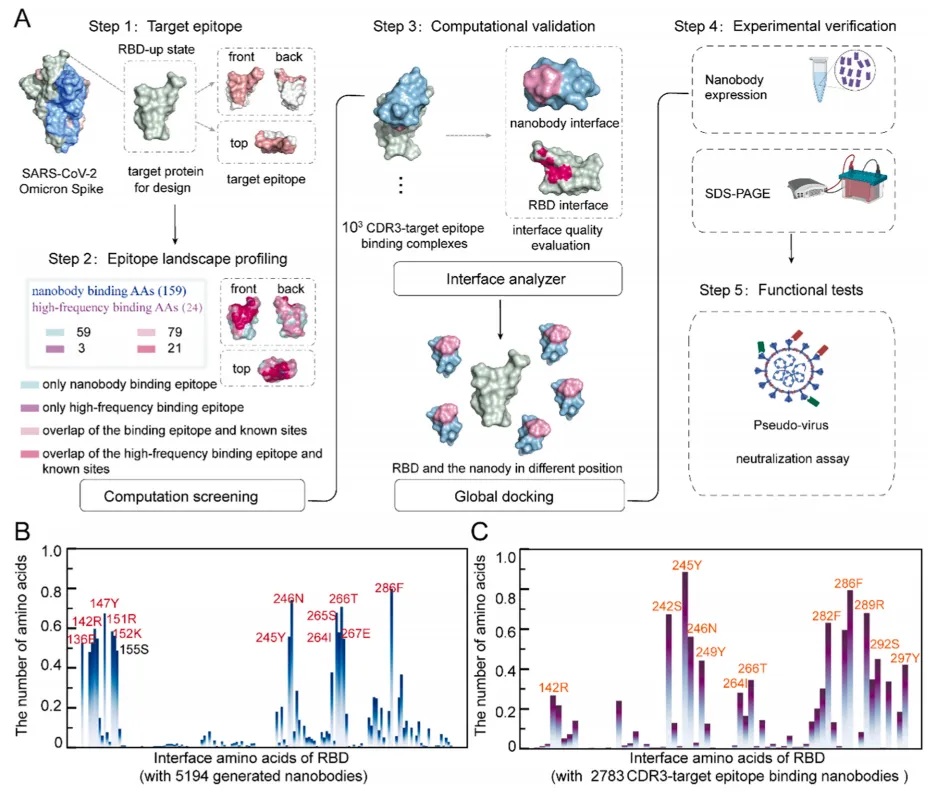
5. Omicron RBD候选筛选
从5,194个中筛出2,783个CDR3直接结合RBD的复合物,经Rosetta Interface Analyzer评分后选10个结合能最低的候选。假病毒中和实验显示,Nb9469(58%抑制)和Nb3022(28%抑制) 呈剂量依赖性中和。10个候选的CDR3均不与已知CoV-AbDab库(800条)匹配,确认为全新序列。
意义:计算直接到功能,验证策略有效性。
6. 分子机制解析
Nb9469通过氢键结合RBD Ser145/Ala148,疏水结合Leu248/Ala280;Nb3022结合Glu46/Lys240。两者均不与ACE2竞争,可能通过空间位阻或别构效应中和。
意义:为后续亲和力优化提供结构指导。
三、结果验证——多维度证据链,层层揭示价值
生成序列真实性
长度分布、氨基酸组成、理化性质与天然CDR3高度一致,95.69%为全新序列,1,308个簇。
价值:生成序列具有“天然质感”且不重复,探索全新结合模式。
结构库质量与规模
5,194个高质量模型,CDR3平均pLDDT≈68。
价值:“虚拟纳米抗体库”可反复用于多种靶点计算筛选。
表位识别准确性
经典靶点重叠率80-100%;Omicron RBD聚焦后达88%。
价值:功能域聚焦分析提高命中率。
体外中和验证
10个计算候选经表达纯化,2个具有剂量依赖性中和活性。
价值:首次在不依赖动物免疫条件下,纯计算设计获得活性纳米抗体。
分子机制指导优化
两种纳米抗体结合RBD不同区域,均不竞争ACE2。
价值:提供分子机制线索,便于定向进化。
四、为什么选择“AI生成+结构筛选”路线?——三大核心优势
-
免动物免疫:传统方法需数月、多动物;AiCDR直接生成序列,规避伦理与批次差异。
-
高通量虚拟筛选:一次生成5,194个高质量模型,可反复用于多靶点对接,实现“一次建库、持续使用”。
-
CDR3中心设计:仅改造CDR3,嫁接至低免疫原性人源化支架,降低全长设计不确定性,保留足够多样性。
五、意义与展望
科学意义:
-
首次将深度生成模型与结构表位分析整合,构建从“序列生成→结构预测→表位筛选→功能验证”的完整计算纳米抗体设计管线。
-
证明CDR3单独改造策略的可行性,简化抗体工程。
-
在无动物免疫条件下获得新冠病毒Omicron活性纳米抗体,为快速响应新发突变提供策略。
未来方向:
-
扩展生成至CDR1和CDR2,提升亲和力上限。
-
应用于难药靶点(GPCR、离子通道),探索通用性。
-
整合亲和力成熟模型,在计算阶段完成微型定向进化。
一句话总结:用AI文字生成器“编写”纳米抗体的CDR3,再通过AlphaFold2“画出”结构——抗体发现从“大海捞针”变成了“按需定制”。
文献来源:Huo L., Tian T., Xu Y. et al. Computational nanobody design through deep generative modeling and epitope landscape profiling. Comput Struct Biotechnol J (2025).
https://doi.org/10.1016/j.csbj.2025.07.052
纳米抗体筛选、小鼠单抗筛选、兔单抗筛选、抗体人源化、抗体亲和力成熟、AI抗体设计,欢迎交流咨询。

 夜雨聆风
夜雨聆风




