学术前沿 | 迷你型基因编辑器新突破

腺相关病毒(AAV)载体因其低免疫原性和良好的组织靶向性,已成为体内基因治疗中广泛应用的递送系统。然而,传统CRISPR核酸酶(如SpCas9,全长超过1000个氨基酸)的尺寸已接近AAV的包装容量上限(约4.7 kb),导致AAV难以同时装载该核酸酶、sgRNA及其他调控或效应元件。因此,开发尺寸更小的核酸酶一直是基因编辑领域的重要目标。近年来虽发现了如Cas12f家族(400–700 aa)等紧凑型核酸酶,具备尺寸优势,但其编辑效率显著低于Cas9/Cas12a,且对原间隔序列邻近基序(PAM)的要求较为严格(例如Un1Cas12f1识别5′-TTTR序列),这大大限制了其在基因组中的靶向范围。
1
Un1Cas12f1
2025年8月5日,PNAS上发表题为《Engineered Un1Cas12f1 with boosted gene-editing activity and expanded genomic coverage》的研究论文。该研究团队成功开发出名为MiniCasUltra的新型基因编辑系统,其尺寸极小(仅529个氨基酸),可适配单个AAV递送载体。相比野生型Un1Cas12f1及当前最优变体,MiniCasUltra的编辑效率显著提高(图1)。此外,团队利用自主建立的SNV-PAMDA(单核苷酸变异PAM鉴定方法)技术,系统测定了适配MiniCasUltra的PAM序列,突破了经典5′-TTTR的限制,可识别非经典PAM(5′-WBTR),使基因组覆盖范围提升了5倍,显著优于Un1Cas12f1(图2)。得益于其超小体积,MiniCasUltra能与两条sgRNA共同装载于单个AAV载体中,实现多基因靶向。研究团队将靶向肿瘤抑制基因PTEN与酪氨酸代谢酶基因FAH的sgRNA与MiniCasUltra一同包装于单个AAV载体,成功在小鼠肝脏中实现了高效基因编辑,验证了该超紧凑系统在多重基因编辑中的应用潜力(图3)。进一步地,团队通过AAV递送靶向人类VEGFA基因中非典型5′-TCTG PAM位点的MiniCasUltra,在激光诱导的脉络膜新生血管(CNV)小鼠模型(新生血管性年龄相关性黄斑变性的主要动物模型)中显著减少了CNV病灶面积。该疾病是全球范围内导致失明的主要原因之一。
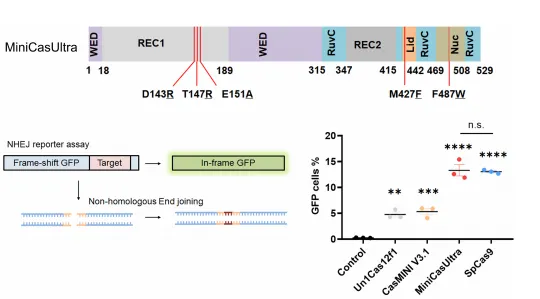
图1 MiniCasUltra突变位点示意图与Un1Cas12f1、CasMINI V3.1和SpCas9的基因编辑平行对比
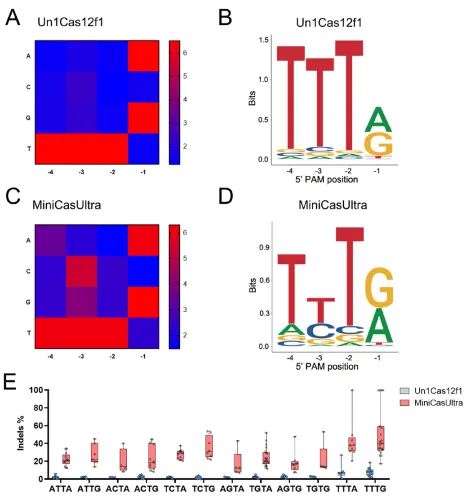
图2 MiniCasUltra的PAM特征分析
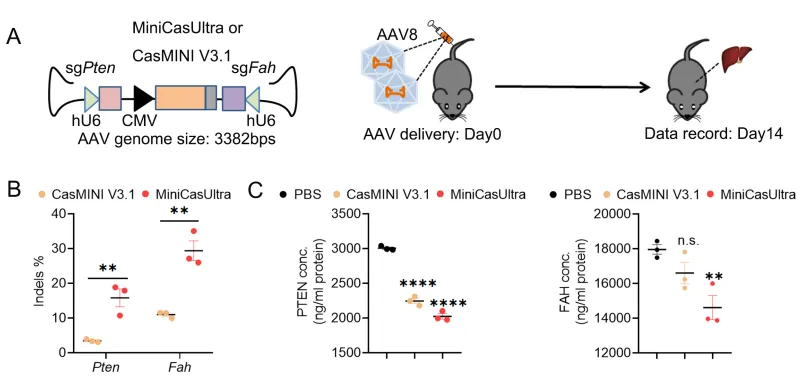
图3 MiniCasUltra靶向小鼠肝脏的体内双位点编辑
2
Al3Cas12f
2026年4月13日,美国德克萨斯大学奥斯汀分校David W. Taylor团队从天然序列中筛选潜在高活性的Cas12f核酸酶,鉴定出来源于Alistipes sp.的Al3Cas12f。该蛋白长度约433–488个氨基酸,显著小于Cas9核酸酶(超过1,300 aa);在体外实验中识别T-rich PAM序列,并在目标链与非目标链上产生特定位点切割。经过哺乳动物细胞中的gRNA筛选,Al3Cas12f在多个靶点表现出稳定的编辑能力,较其他Cas12f同源物活性更强,部分位点上甚至优于LbCas12a(图1)。
进一步地,研究从结构层面解析其作用机制。冷冻电镜结构显示,Al3Cas12f以非对称同源二聚体形式存在,并形成完整的R-loop结构。相比之下,其他同源蛋白在REC结构域尺寸与RuvC定位上存在明显差异,暗示不同Cas12f在DNA识别与切割机制上具有结构基础的多样性。在gRNA层面,OsCas12f与RhCas12f的gRNA呈L形结构并包含4个茎环,而Al3Cas12f缺失stem 4区域,形成更紧凑的构象。对gRNA进行截短发现,OsCas12f删除stem 4后编辑活性提高约10倍,而RhCas12f对stem 2依赖显著,进一步体现蛋白—RNA互作方式的差异。结构分析表明,RhCas12f的stem 2区域与PAM识别残基相互作用,而Al3Cas12f则通过紧凑gRNA直接稳定REC结构域,减少非生产性构象的形成。随着gRNA特征逐步明确,研究进而聚焦二聚体界面。OsCas12f与RhCas12f主要通过REC结构域的α1螺旋及下方loop形成双层界面,而Al3Cas12f则形成更复杂的多层互作结构:其REC结构域额外延伸约50–60个氨基酸,形成类似榫卯的嵌合界面,增强二聚体稳定性(图5)。关键界面残基突变后,酶活显著下降;质量光度分析进一步表明,破坏界面会降低二聚体稳定性,从而削弱整体编辑能力。
基于上述结构洞察,研究通过在DNA、gRNA氢键结合距离内增加残基的正电荷,设计了Al3Cas12f的单突变与组合突变体。35个组合突变体中,21个在SOD1位点的编辑效率超过75%。筛选获得最优三突变体K79R/M190K/E222K(命名为Al3Cas12f RKK),在8个测试基因组位点中,6个位点的插入缺失(indels)效率超过80%,其中在EMC6位点的编辑活性最高提升26倍,大幅降低了野生型的位点依赖性差异(图6)。
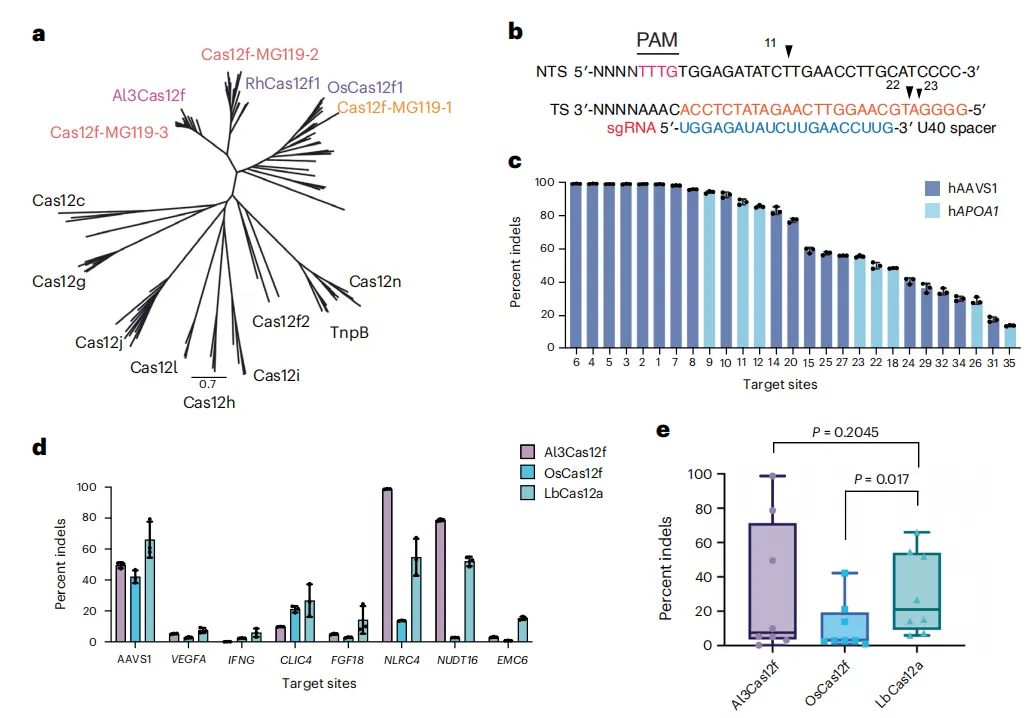
图4 紧凑型V型Al3Cas12f核酸酶的初步发现与特征分析
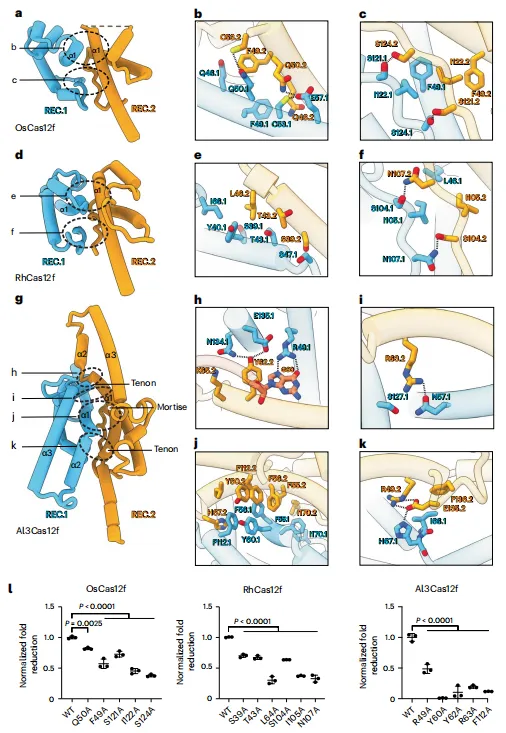
图5 OsCas12f、RhCas12f 的二聚化互作模式,以及 Al3Cas12f 独特的 “榫卯式” 二聚化界面图
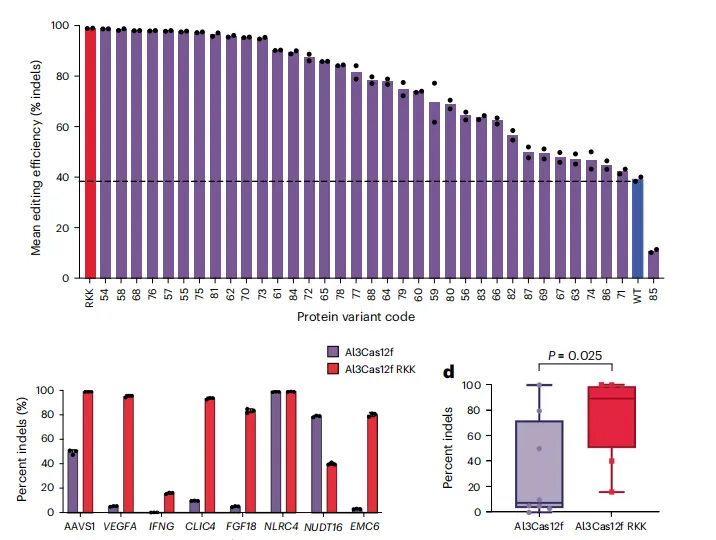
图6 Al3Cas12f 的工程化改造与活性验证
3
AsCas12f1
2026年6月,上海交通大学生命科学技术学院杨广宇研究员团队与华东师范大学生命科学学院李大力研究员团队基于AsCas12f1‑sgRNA‑dsDNA冷冻电镜结构,分析PAM近端残基对序列特异性的调控作用,以及WED–RuvC二聚界面正电中心沟残基对DNA骨架的稳定作用,共锁定18个PAM互作残基与23个DNA结合残基,旨在弱化碱基特异性氢键与范德华力,放松PAM序列约束,同时增强非特异性DNA骨架静电结合,提升DNA结合与切割效率。研究团队利用基于大肠杆菌生长偶联的高通量筛选平台,添加阿拉伯糖诱导ccdB基因表达,使无法切割靶序列的细菌死亡;只有能高效识别并切割含目标PAM的靶序列的突变体才能存活。经过五轮迭代组合突变,逐步累积优势突变,最终获得性能最优的M5变体(图7)。
为直接评估AsCas12f1变体的PAM识别能力和核酸酶活性,作者开展了体外切割实验。结果显示,野生型AsCas12f1仅能高效切割经典的5′-TTR PAM,而M5变体对经典的5′-TTR以及非经典的5′-TYN PAM均表现出高核酸酶活性。进一步的 time‑course 切割实验(0–60分钟)评估了经典PAM(5′-TTA、5′-TTG)与非经典PAM(5′-TTC、5′-TTT、5′-TCN)的反应动力学。M5在所有测试的PAM位点上,均能在15–30分钟内完成近乎完全的底物切割;相比之下,野生型AsCas12f1和M4变体在非经典PAM位点上仅表现出极其微弱的切割效果。这些结果表明,M5同时具备扩展的PAM识别范围和增强的核酸酶活性,体现在其在多种PAM位点上更快的切割动力学(图8)。
研究进一步评估了M5在体内基因组编辑中的应用潜力。作者靶向小鼠肝脏中的Ttr基因-该基因在人类中的同源基因有害遗传变异是导致转甲状腺素蛋白淀粉样变性病的原因。团队设计了三个靶向不同PAM(5′-TTG、5′-TCA、5′-TCC)的sgRNA,并通过8型腺相关病毒(AAV8)递送M5(每只小鼠1×10⁸或1×10¹⁰病毒基因组)。血浆分析显示,M5组小鼠在所有三种PAM位点上均出现循环转甲状腺素蛋白水平的显著下降,2–4周内降幅达12.5%–30%。相比之下,AAV递送的野生型AsCas12f1在这些位点上仅产生极其微弱的编辑效果(降幅<5%)。通过靶向深度测序定量肝组织中的插入缺失突变频率,M5在Ttr位点实现了约30%–35%的编辑效率,与观察到的循环转甲状腺素蛋白下降水平一致。这些结果证明,M5扩展的PAM识别能力能够在体内实现对经典(如5′-TTG)和非经典(如5′-TCA、5′-TCC)PAM位点的高效基因组编辑(图9)。
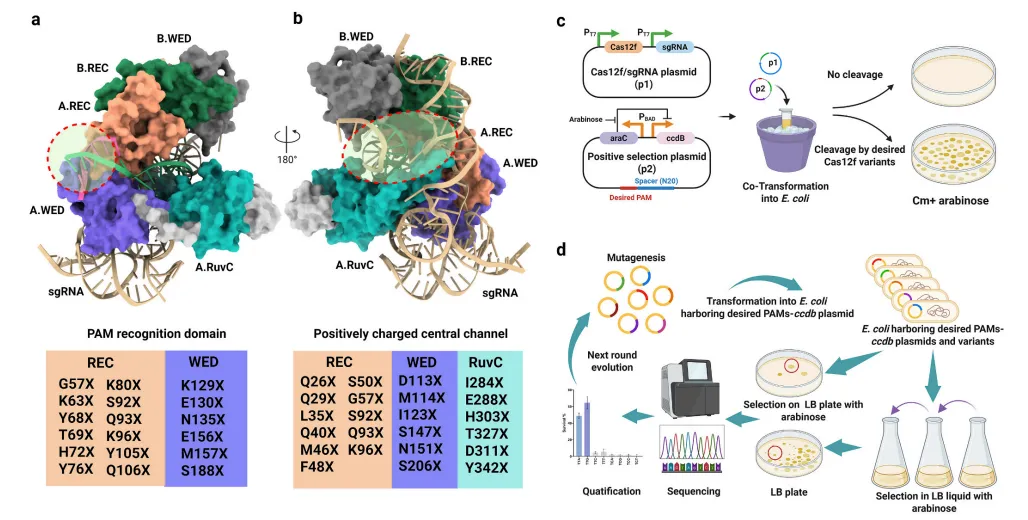
图7 半理性设计并筛选AsCas12f1以扩展PAM识别并增强核酸酶活性
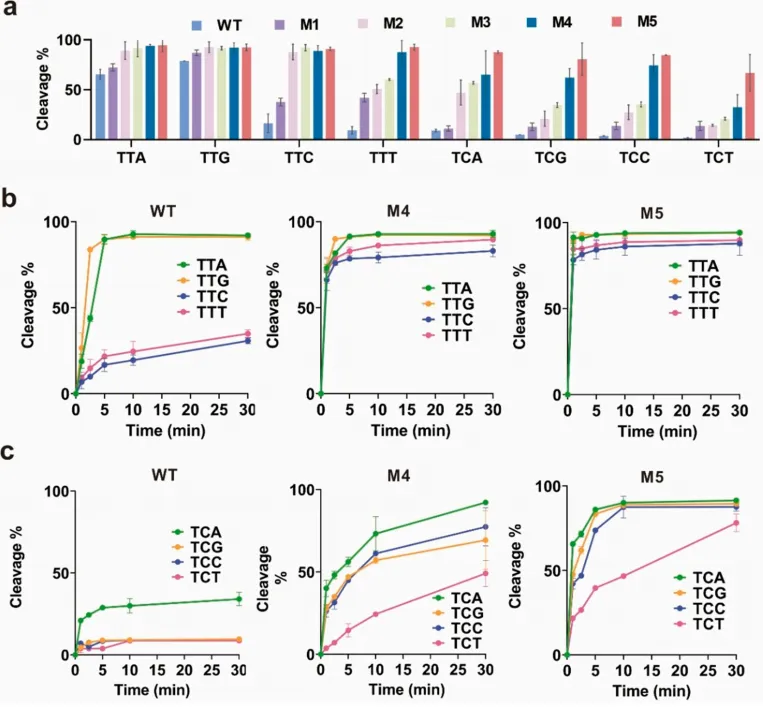
图8 AsCas12f1 变体的 PAM 识别和核酸酶活性的体外评估
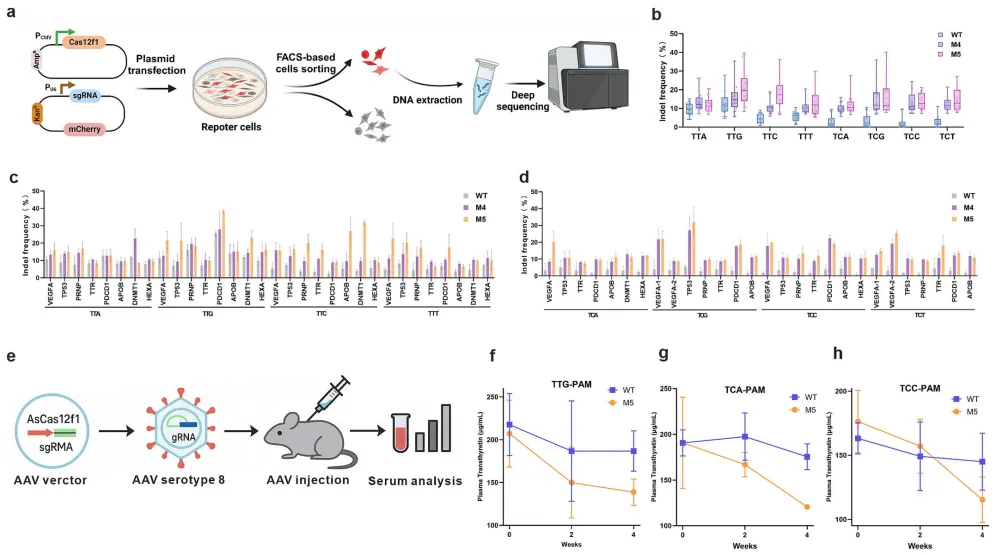
图9 M5变体可在小鼠体内实现高效基因组编辑
以 Cas12f 为核心骨架,开发单碱基编辑器、先导编辑器及表观遗传修饰器等系列衍生工具,将充分发挥其尺寸紧凑的独特优势,实现单一 AAV 载体的完整包装与高效递送,从而突破现有大型编辑工具在体内递送方面的技术瓶颈,拓展其在单基因遗传病、肿瘤、感染性疾病等领域的应用前景。
参考文献
[1] Chen, L., Zhou, X., Huang, C., Zhang, Y., Xin, C., Hong, J., & Wang, Y. (2025). Engineered Un1Cas12f1 with boosted gene-editing activity and expanded genomic coverage.Proceedings of the National Academy of Sciences, 122(32), e2501292122.
[2] Guan, K., Ocampo, R. F., Matheus Carnevali, P. B., Castelle, C. J., Gonzalez-Osorio, L., Castanzo, D. T., … & Taylor, D. W. (2026). Comparative characterization of Cas12f orthologs reveals mechanistic features underlying enhanced genome editing efficiency.Nature Structural & Molecular Biology, 1-12.
[3] Li, Z., Deng, Y., Huo, Y., Nie, T., Wang, S., Li, D., & Yang, G. Y. (2026). Directed evolution of a miniature Cas12f1 nuclease from Acidibacillus sulfuroxidans for expanded PAM recognition and enhanced nuclease activity. Chemical Engineering Journal, 176417.

About us
华东合成生物学产业技术研究院成立于2023年,由杭州市拱墅区人民政府、浙江工业大学、杭州中美华东制药有限公司三方共同组建,聚焦营养与医药化学品、医美生物、生物材料及健康代糖品四大领域,围绕智能生物制造开展技术创新研究和产业转化研究。

【研究院持续招聘博士后】

为加速推进合成生物学领域创新研究,华东合成生物学产业技术研究院现根据战略发展规划,面向海内外高校及科研机构公开招聘青年科技人才,诚邀合成生物学及相关领域优秀博士加入科研团队!岗位详情及申报流程请参见《华东合成生物学产业技术研究院2026博士后招聘!》。

欢迎关注我们

往期推荐
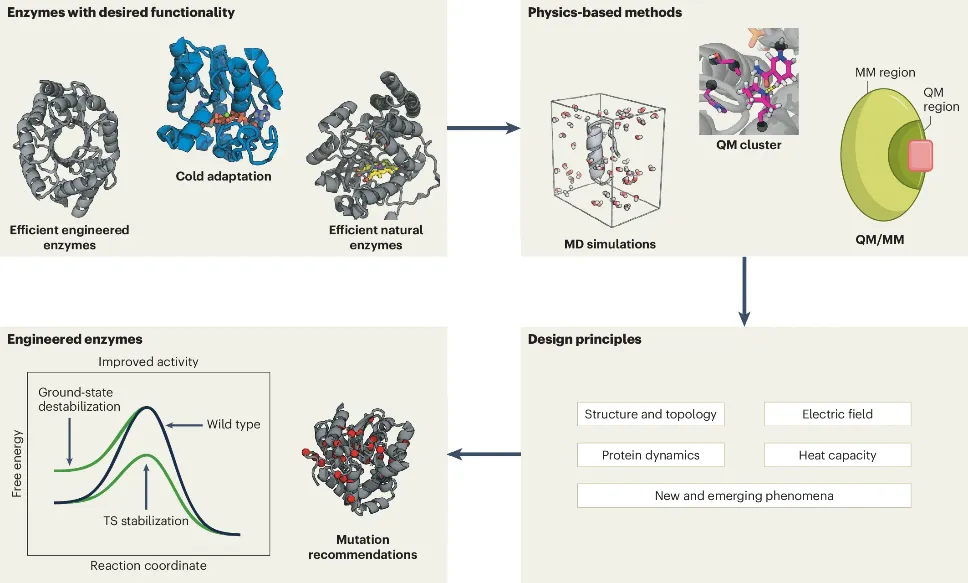
学术前沿 | 让酶工程走出“黑箱”:物理建模正在重塑下一代生物催化设计范式
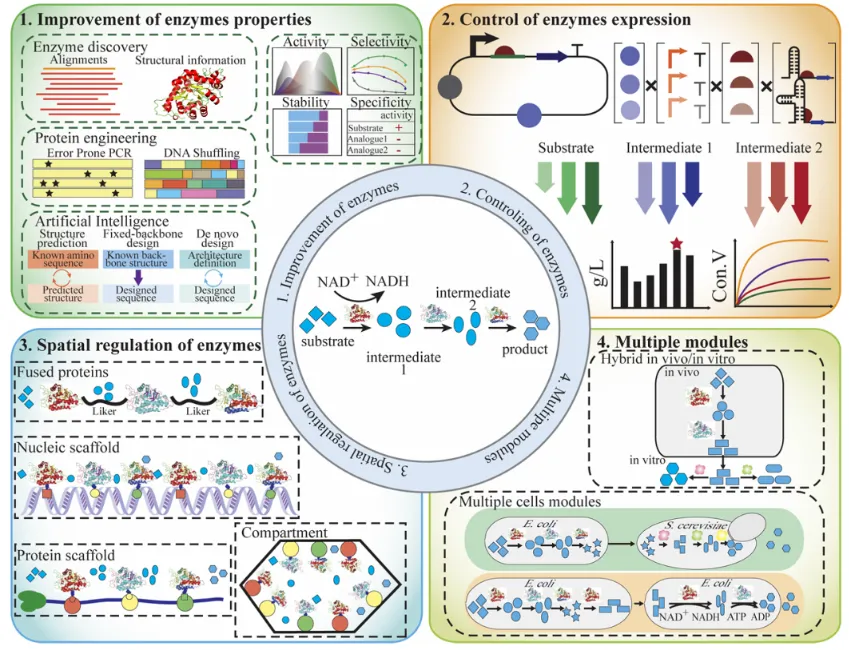
学术动态 | 研究院院长郑裕国院士团队柳志强教授课题组发表论文——驱动体内多酶级联反应前行:提升生物催化效率的调节策略全景综述

阅览导引









<<左右滑动查看栏目>>
资料来源:施晶晶
排版设计:段伊蕾
审核:蔡雪、周秋萍
 夜雨聆风
夜雨聆风




