文档内容
物质的量
第 1 讲 物质的量 气体摩尔体积
课 程 标 准 知 识 建 构
1.了解物质的量及其相关物理量的含义和
应用,体会定量研究对化学科学的重要作
用。
2.能基于物质的量认识物质组成及其化学
变化,运用物质的量、摩尔质量、气体摩尔
体积之间的相互关系进行简单计算。
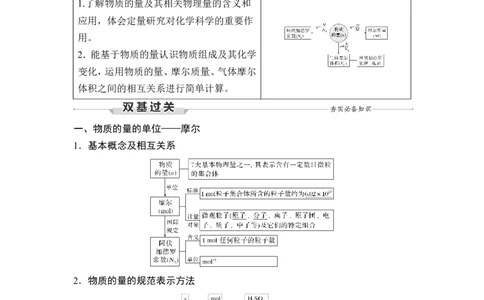
一、物质的量的单位——摩尔
1.基本概念及相互关系
2.物质的量的规范表示方法
如:1 mol H、0.5 mol O 、0.01 mol Na+。
2
3.物质的量与微粒数、阿伏加德罗常数之间的关系
n=或N= n · N 或N =。
A A
【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)阿伏加德罗常数就是6.02×1023( )
(2)仓库里存有1 mol小米( )(3)1 mol水中含有2 mol氢和1 mol氧( )
(4)1 mol任何物质都含有6.02×1023个分子( )
(5)1 mol O 中约含有6.02×1023个氧气分子( )
2
(6)等物质的量的O 和O ,所含氧原子数相同( )
2 3
答案 (1)× (2)× (3)× (4)× (5)√ (6)×
二、摩尔质量
1.基本概念
2.物质的量(n)、质量(m)、摩尔质量(M)之间的关系
n=或m= n · M 或M=。
【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)摩尔质量就是1 mol物质的质量( )
(2)硫酸的摩尔质量为98 g( )
(3)1 mol OH-的质量是17 g·mol-1 ( )
(4)2 mol H O是1 mol H O摩尔质量的2倍( )
2 2
(5)1 mol O 的质量与它的相对分子质量相同( )
2
(6)22 g CO 中含有的氧原子数为N ( )
2 A
答案 (1)× (2)× (3)× (4)× (5)× (6)√
三、气体摩尔体积
1.影响物质体积的因素
2.气体摩尔体积3.物质的量与气体体积、气体摩尔体积之间的关系
V =或V= n · V 或n=。
m m
【诊断3】 下列叙述正确的是( )
A.1 mol任何气体的体积都为22.4 L
B.1 mol任何物质在标准状况下所占的体积都为22.4 L
C.标准状况下,1 mol水所占的体积是22.4 L
D.标准状况下,22.4 L任何气体的物质的量都是1 mol
答案 D
解析 A项没有指明气体所处的状况,即温度、压强,错误;B项没有指明该物质
的状态,错误;C项水在标准状况下不是气体,错误;D项是对气体摩尔体积概念
的应用,正确。
四、阿伏加德罗定律
1.阿伏加德罗定律
可简单总结为“四同”:同温、同压、同体积、同分子数,并且“三同定一同”。
2.阿伏加德罗定律的推论
公式 语言叙述
= 同温、同压下,气体的体积与其物质的量成正比
T、p相同 同温、同压下,气体的密度与其摩尔质量(或相对分
=
子质量)成正比
温度、体积相同的气体,其压强与其物质的量成正
T、V相同 =
比
【诊断4】 判断下列说法是否正确,正确的打√,错误的打×。
(1)在标准状况下,1 mol氧气和1 mol氦气的体积相同,含有原子数也相同( )
(2)同温同压下,等质量的12C18O和NO体积相同( )(3)标准状况下,11.2 L SO 中含有的原子数为2N ( )
3 A
(4)不同温度下,相同体积的CO和N 密度相同,则二者含有的原子数相同( )
2
(5)同温同体积的条件下,等质量的SO 和O 的压强比为2∶1( )
2 2
(6)同温、同压、同体积的CH 和NH 含有的质子数相等( )
4 3
答案 (1)× (2) √ (3)× (4) √ (5)× (6)√
考点一 物质的量、摩尔质量的有关计算
【典例1】 根据相关量的关系,完成下列填空:
(1)有以下四种物质:①22 g二氧化碳 ②8 g氢气
③1.204×1024个氮气分子 ④ 4 ℃时 18 mL 水,它们所含分子数最多的是
________,所含原子数最多的________,质量最大的是________,所含电子数最
多的是________(填序号)。
(2)12.4 g Na R含Na+ 0.4 mol,则Na R的摩尔质量为________,R的相对原子质
2 2
量为________,含R的质量为1.6 g的Na R,其物质的量为________。
2
(3)最近材料科学家研究发现了首例带结晶水的晶体在5 K下呈现超导性。据报
道,该晶体的化学式为Na CoO ·1.3H O。若用N 表示阿伏加德罗常数,试计算
0.35 2 2 A
12.2 g该晶体中含氧原子数为________,氢原子的物质的量为________ mol。
答案 (1)② ② ③ ③
(2)62 g·mol-1 16 0.1 mol
(3)0.33N 0.26
A
解析 (1)①22 g二氧化碳的物质的量为=0.5 mol;②8 g氢气的物质的量为=4
mol;
③1.204×1024个氮气分子的物质的量为=2 mol,质量为2 mol×28 g/mol=56 g;
④4 ℃时18 mL水,其质量为18 mL×1 g/mL=18 g,物质的量为=1 mol;故所
含分子数最多的是②8 g氢气;质量最大是③1.204×1024个氮气分子;
①22 g二氧化碳,含有原子物质的量为0.5 mol×3=1.5 mol;②8 g氢气,含有原
子物质的量为4 mol×2=8 mol;③1.204×1024个氮气分子,含有原子物质的量
为2 mol×2=4 mol;④4 ℃时18 mL水,含有原子物质的量为1 mol×3=3 mol;
故所含原子数最多的是②8 g氢气;
①22 g二氧化碳,含有电子物质的量为0.5 mol×22=11 mol;②8 g氢气,含有电
子物质的量为4 mol×2=8 mol;③1.204×1024个氮气分子,含有电子物质的量
为2 mol×14=28 mol;④4 ℃时18 mL水,含有电子物质的量为1 mol×10=10mol;故所含电子数最多的是③1.204×1024个氮气分子。
(2)1 mol Na R中含2 mol Na+,题目中有Na+ 0.4 mol,则有0.2 mol Na R。运用公
2 2
式M=得==62 g·mol-1。M(Na R)=62,求得M(R)=62-2×23=16。根据n=,
r 2 r
得n(R)=0.1 mol,则n(Na R)=0.1 mol。
2
(3)Na CoO ·1.3H O的摩尔质量约为 122 g·mol-1,12.2 g Na CoO ·1.3H O的物
0.35 2 2 0.35 2 2
质的量为=0.1 mol,因此12.2 g晶体的氧原子数为0.1N ×3.3=0.33N ,氢原子
A A
的物质的量为0.1 mol×2.6=0.26 mol。
物质中某指定微粒数目的计算技巧
(1)明确整体与部分的关系:谁是整体?谁是部分?
(2)原子(电子)的物质的量=分子(或特定组合)物质的量×1个分子(或特定组合)
中所含这种原子(电子)个数
如典例1(3)中,Na CoO ·1.3H O是整体,计算对象氧原子、氢原子为部分,它们
0.35 2 2
的关系为:
Na CoO ·1.3H O~3.3O~2.6H
0.35 2 2
【对点练1】 (有关n==的应用)在0.5 mol Na SO 中含有的离子的个数和氧原子
2 4
的质量分别是( )
A.1.5N 2 mol B.1.5N 32 g
A A
C.3.01×1023 4 mol D.N 64 g
A
答案 B
【对点练2】 (平均摩尔质量的计算)根据相关量的关系,完成下列填空:
(1)由8 g O 和28 g N 组成的混合气体的平均摩尔质量是________。
2 2
(2)在空气中N 、O 、Ar的体积分数分别约为78%、21%、1%,则空气的平均摩尔
2 2
质量为________。
答案 (1)28.8 g·mol-1 (2)28.96 g·mol-1
解析 (1)=28.8 g·mol-1
(2)28 g·mol-1×78%+32 g·mol-1×21%+40 g·mol-1×1%=28.96 g·mol-1。
【对点练3】 (物质中某指定微粒数目的计算)国家地质调查局“海洋六号”考查
船在我国南海北部发现了大量“可燃冰”,它是由水和甲烷在一定条件下形成的
类冰结晶化合物。
(1)32 g甲烷和________ g水所含的氢原子数相同。(2)0.3 mol CH 分子中所含电子数与________个H O分子中所含电子数相等。1.5
4 2
g CH中的电子数为________。
(3)已知,1.6 g“可燃冰”(CH ·xH O)的物质的量与6.02×1021个水分子的物质的
4 2
量相等,则该“可燃冰”的摩尔质量为________,x的值为________。
答案 (1)72 (2)0.3N (或1.806×1023) 0.8N
A A
(3)160 g·mol-1 8
解析 (1)32 g CH 的物质的量为=2 mol,即含8 mol氢原子,n(H O)==4 mol,
4 2
m(H O)=4 mol×18 g·mol-1=72 g。(2)CH 和H O分子均含10个电子,则与0.3
2 4 2
mol CH 中所含电子数相等的水的物质的量为 0.3 mol,则 N=nN =0.3N 或
4 A A
1.806×1023,1.5 g CH的物质的量为=0.1 mol,每个CH中含有8个电子,故1.5 g
CH含电子数为0.8N 。(3)由n=,得水的物质的量为=0.01 mol,则可燃冰的物质
A
的量为0.01 mol,M==160 g·mol-1,由16+18x=160可得x=8。
摩尔质量的计算方法
考点二 气体摩尔体积、阿伏加德罗定律的应用
【典例2】 三种气体X、Y、Z的相对分子质量关系为M(X)