AI开始按结构“现做”蛋白binder了 | Nature:BindCraft把one design-one binder推到了真正可讨论的阶段
阅读时间:约8分钟 | 基于Nature论文《One-shot design of functional protein binders with BindCraft》。
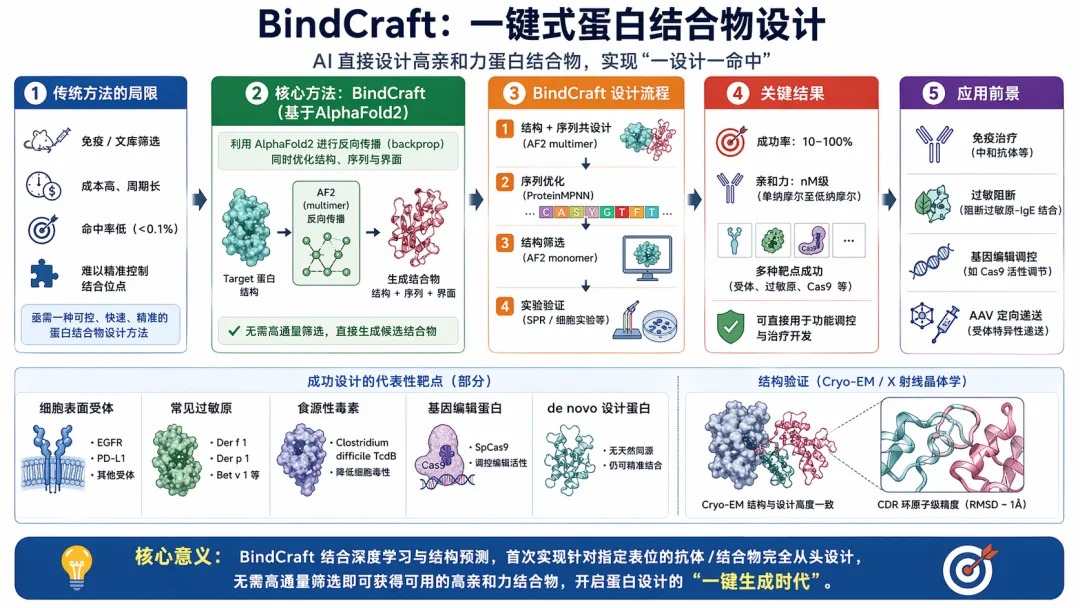
过去几年,蛋白结构 AI 最出圈的成就,是把“看结构”这件事做到了前所未有的高度。但这篇 Nature 真正更进一步的地方,不是再把某个蛋白折得更准,而是试图把“给定目标结构 -> 直接生成可用 binder”这条路走通。作者把 AlphaFold2 multimer 变成了一个会“边看目标边设计界面”的生成器,再配合 MPNN_sol 和 AF2 / Rosetta 过滤,把 wet lab 要面对的候选空间压缩到更小、更像 hit 的集合里。
这篇工作的强点,在于它没有把结果停留在一两条 BLI / SPR 曲线上。论文跨 12 个具有生物医学意味的靶点做了实验,覆盖受体、过敏原、人工蛋白与核酸酶四类问题;最好的亲和力做到 nM 量级,单靶点成功率从 10% 到 100%,论文给出的平均成功率为 46.3%。更重要的是,它把结果继续推到了过敏阻断、Cas9 调控、Ago 抑制和 AAV 重定向这些真正有功能含义的 readout 上。
但这篇论文也不能被吹成“以后不需要筛选了”。从作者自己给的数据看,命中率仍然明显依赖靶点;有的结果很亮眼,有的仍停留在数百 nM 甚至 μM 水平;很多结论依然靠 BLI / SPR / 结构学和细胞实验来兜底。真正值得记住的,不是“binder 设计已被彻底解决”,而是蛋白结构 AI 已经开始从“预测结构”稳步切进“按结构设计功能分子”的阶段。
|
一句话核心结论:BindCraft 最重要的,不是又多了一个 binder 模型,而是它第一次把“目标结构 -> 候选分子 -> 功能 readout”这条链条做得足够顺,足以让科研实验室认真把它当工具看。 |
|
论文题目 |
One-shot design of functional protein binders with BindCraft |
|
期刊与时间 |
Nature 646, 483-492 (2025);2025-08-27 online |
|
研究对象 |
12 个靶点,涵盖受体、过敏原、人工蛋白、SpCas9 与 CbAgo |
|
核心技术 |
AF2 multimer 反向传播 + target flexibility + MPNN_sol + AF2 monomer / Rosetta 过滤 |
|
最值得看之处 |
不只做出“能结合”的 binder,而是一路推到了功能验证和递送应用 |
注:本文配图均为根据原文结果重新整理绘制,并非论文原始插图。
01 这篇文章到底解决了什么问题
传统 binder 发现往往有两个麻烦。第一,前端高度依赖免疫、展示文库或高通量筛选,实验负担大。第二,即便你先找到了“能结合”的分子,也未必正好打在你真正关心的功能位点上。对很多生物医学问题来说,关键不是有没有 binder,而是 binder 是否能打中受体界面、过敏表位、核酸结合口袋或递送入口这些真正决定功能的位置。
BindCraft 想解决的,就是“能不能只给目标结构,尽量少做盲筛,就直接拿到命中位点的 binder”。作者用 AF2 multimer 进行 binder-backbone-界面共设计,而且不是把靶蛋白 rigid 地冻住,而是允许 target 和 binder 在每轮迭代里一起微调;随后再用 MPNN_sol 优化 binder 的非界面区域,用 AF2 monomer 与 Rosetta 指标做后验过滤。

图1|BindCraft 设计闭环。真正的区别在于:它不是把 target 当固定模板,而是允许 target 在设计过程中跟着动。
这个逻辑非常像把“结构约束”提前到生成端,而不是等拿到候选以后再去解释它打到了哪里。论文还给出三个很关键的量化信号:设计过程中,target backbone 的 RMSD 可到 0.5-5.5 Å;不同靶点初始 AF2 轨迹通过率为 16.8%-62.7%;最终通过 AF2 monomer + Rosetta 过滤后留下的比例为 0.6%-65.9%。这说明它并不是“随便生一堆就有 hit”,而是把筛选压力前移到了模型与过滤器这一端。
02 BindCraft 真正不同在哪里
如果只从流程名字看,它像“AF2 + MPNN”的又一版组合;但真正重要的差异,是 target flexibility 和 complex reprediction。对很多 protein-protein interaction 来说,位点不是一个完全刚性的坑,而是伴随 side chain / backbone 的诱导契合。BindCraft 把这个问题正面纳入设计过程,所以它更像是在做“受结构约束的分子生成”,而不是传统意义上的静态 interface packing。
03 他们具体做出了什么:12 个靶点的成绩单
广度是这篇论文最容易被低估的地方。作者不是只在一个熟悉的靶点上反复打磨,而是一次性把 BindCraft 推到了 12 个难度很不一样的对象上:PD-1、PD-L1、CD45、CLDN1、IFNAR2 这类受体;Der f7、Der f21、Bet v1 这类过敏原;没有天然同源的 BBF-14 和装配相关的 SAS-6;以及 SpCas9、CbAgo 这类核酸引导核酸酶。
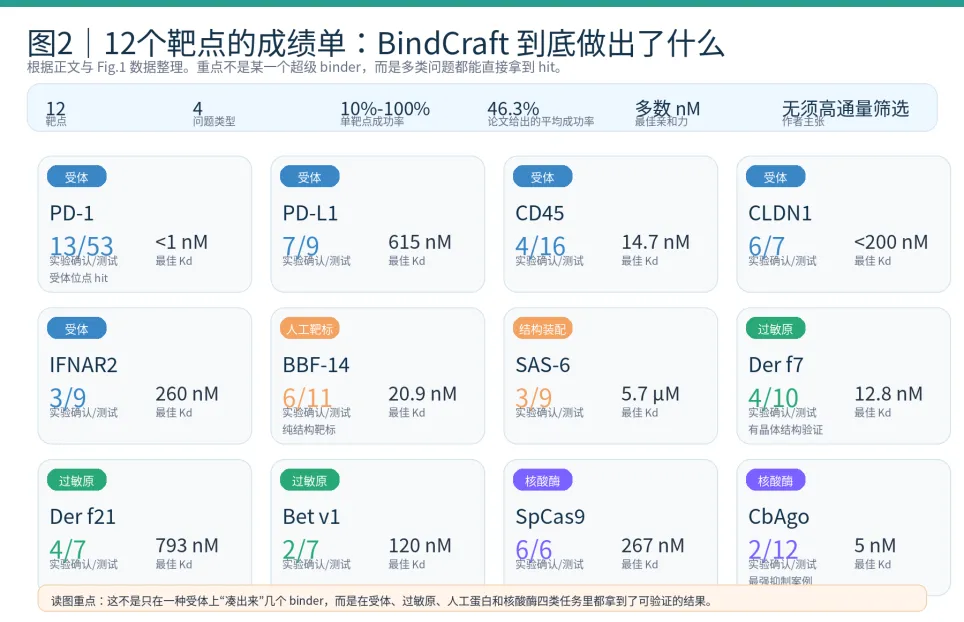
图2|12 个靶点成绩单。真正有说服力的地方,不是某一个特别好的数值,而是四类问题里都拿到了可验证的结果。
结果并不是“每个靶点都惊艳”,但已经足以说明问题。强项很明显:PD-1 最佳 binder 低于 1 nM,CLDN1 最佳结果低于 200 nM,CbAgo binder2 到了 5 nM;而即便是更难的人工蛋白 BBF-14,也能做到 20.9 nM。弱项也同样清楚:Der f21 为 793 nM,SAS-6 仍在 5.7 μM 量级。正因为有这种高低起伏,这份成绩单才更可信——它不是挑一个漂亮案例讲故事,而是在不同问题类型上给出了真实的命中分布。
另外一个经常被忽略的点,是这些 binder 并不只是“照着天然复合物抄”。论文报告设计骨架到最近 PDB 命中的平均 TM score 为 0.62、序列 identity 仅 14.4%;而设计界面相对已知 PPI 的平均 TM score 只有 0.15。这意味着 BindCraft 不是简单重放已知复合物,而是在已知折叠空间里做出了新的 interface 组合。
04 真正站住脚的,是“能结合以外”的功能验证
如果一篇 binder 论文只告诉你“测到了结合”,那它对生物医学研究的意义通常还很有限。BindCraft 真正站住脚的地方,在于作者用四类完全不同的 readout 去问同一个问题:这些 AI 设计出来的 binder,能不能真的改生物学行为?
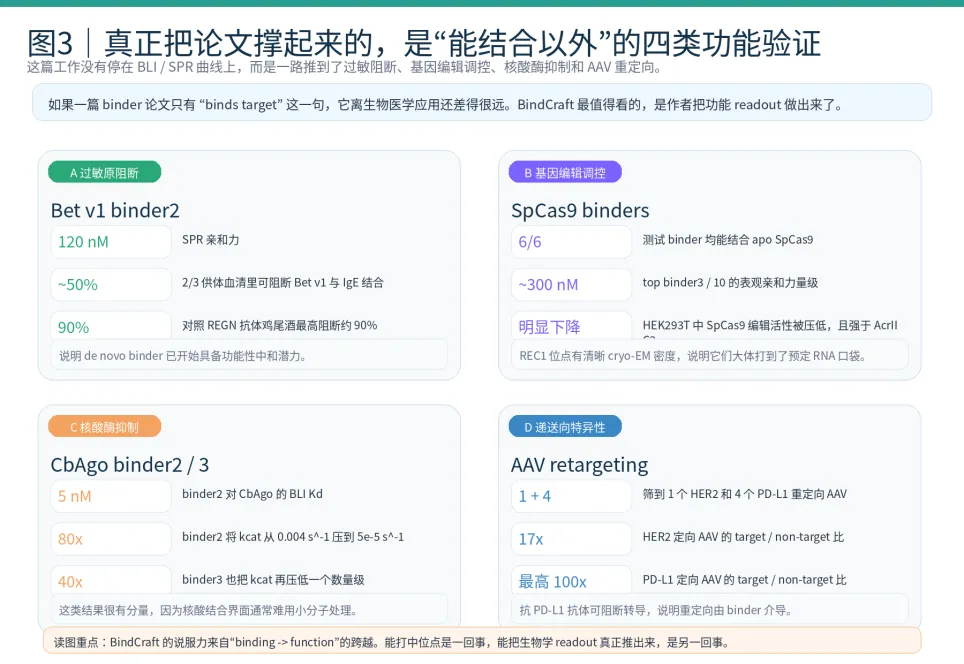
图3|BindCraft 的说服力来自“binding -> function”的跨越。它已经开始不只是命中蛋白,还能推动过敏阻断、核酸酶抑制和递送向特异性。
针对 Bet v1,作者拿到的 binder2 只有一个,不是抗体鸡尾酒,却能在 3 位患者中的 2 位里把 Bet v1 与 IgE 的结合最高压到约 50%;对照 REGN 抗体混合物最高约 90%。这说明 de novo binder 已经开始具备“单分子做中和”的潜力,而不只是作为结构探针。
更有意思的是核酸酶部分。SpCas9 的设计 binder 都能结合 apo enzyme,并且在 HEK293T 里压低基因编辑活性;CbAgo 的 binder2 不仅亲和力到 5 nM,还能把 kcat 从 0.004 s^-1 压到 5 x 10^-5 s^-1,等于直接慢了 80 倍。再加上 AAV 这部分拿到 1 个 HER2 和 4 个 PD-L1 的重定向载体、目标/非目标比最高可到 17x 和 100x,你会发现这篇论文真正想证明的不是“我会造 binder”,而是“我会把 binder 接到功能系统里”。
05 为什么这篇论文对蛋白结构 AI 特别重要
过去很多结构 AI 论文,解决的是“能不能更准确地看懂结构”或“能不能在固定靶标上设计一个结合分子”。BindCraft 更重要的地方在于,它让结构模型开始承担“前端生成”的角色:结构不是验证终点,而是生成约束的起点。对做蛋白工程、受体药理学、结构生物学或者递送改造的人来说,这个变化很实在,因为它对应的不是 leaderboard 上多几个百分点,而是实验 workflow 会不会被重写。
而且这篇论文并不只靠功能结果站台。Der f7 binder2 拿到了 2.2 Å 和 3.0 Å 的晶体结构,按 allergen 对齐后 backbone r.m.s.d. 约 1.7 Å;Der f21 binder10 的晶体结构分辨率为 2.6 Å,对齐后的 r.m.s.d. 约 3.1 Å;BBF-14 的 binder4 也给出了 1.7 Å 级别的结构吻合。即便 SpCas9 没有拿到可建原子模型的 cryo-EM,REC1 位点的密度也足够清楚,至少说明它们大体上是按预定区域在结合。

图4|把这篇论文的推进与局限放在一张图里看,判断会更稳。
06 别高估它:这离“一键出药”还很远
首先,命中率仍然明显依赖靶点。最好和最差的任务差别很大,说明 binder 设计还远没有进入“输入结构就稳定出答案”的阶段。其次,很多结果的实用性还要继续打磨:有的 binder 是二聚体,有的亲和力仍在 μM 级别,有的只能说明“会结合”和“会抑制”,离真正的体内药理闭环还远。
再往转化层面看,AAV 重定向虽然很有想象力,但目前主要还是细胞层面的特异性证明;稳定性、制备、体内暴露、免疫原性以及长期安全性,都不是这篇论文已经解决的问题。实话实说,这篇 Nature 提供的是一条非常有前景的工具路线,而不是已经封装好的药物开发平台。
07 我的判断:科研读者最值得记住什么
如果你做的是蛋白工程、结合蛋白发现、结构生物学、受体功能研究,或者任何需要“命中某个功能位点”的工作,我觉得这篇文章最值得记住的不是哪一个单独的 Kd 数字,而是一整条 workflow 出现了:目标结构定义 -> AI 共同设计 -> 严格过滤 -> 小规模实验验证 -> 直接接功能 readout。这个闭环一旦能稳定复现,后面再叠加 developability、亲和成熟、表达优化和体内测试,就有了真正往转化走的接口。
再往前看,未来最成熟的形态,恐怕不会是“单独一个 BindCraft”或“单独一个 AlphaFold”,而是“结构模型 + 生成设计 + 过滤器 + focused validation”的组合系统。谁能把这几步之间的信息打通,谁更有可能把蛋白结构 AI 从论文结果推进成生物医学工具。
|
一句话总结:AlphaFold 让我们更会看结构;而 BindCraft 这篇 Nature 说明,AI 已经开始按结构去做 binder,并且第一次把它推到了真正可用、可争论、也可继续扩展的阶段。 |
附参考文献与原文信息
1. Pacesa M, Nickel L, Schellhaas C, et al. One-shot design of functional protein binders with BindCraft. Nature. 2025;646:483-492. DOI: 10.1038/s41586-025-09429-6.
2. BindCraft 代码仓库:GitHub(MIT license,论文作者公开提供安装说明、设计协议与 Colab notebook)。
3. 本文内容主要依据论文正文、图注与公开代码信息整理,面向科研读者做中文重写与重点提炼。
 夜雨聆风
夜雨聆风




