AAV递送新突破:超迷你基因编辑器AsCas12f1-M5通过工程化改造实现靶点覆盖与活性跃升
|
🔬 Highlights · 上海交通大学与华东师范大学团队合作,通过定向进化改造出超迷你基因编辑器AsCas12f1-M5。 · 新变体将可靶向的基因组位点覆盖率从约4%提升至约15%,编辑活性在细胞中最高提升超10倍。 · 该编辑器可被单个腺相关病毒载体完整装载,并在小鼠体内实现安全高效编辑,未引起明显肝损伤或免疫反应。 · 研究为更多遗传病的基因治疗提供了新的工具和改造范式。 |
在基因治疗领域,如何将CRISPR基因编辑工具安全、高效地递送到人体特定细胞,始终是核心挑战。腺相关病毒(AAV)是理想的递送载体,但其装载容量有限,难以容纳Cas9等大型编辑器。如今,一项关于“超迷你”基因编辑器的研究取得了关键进展,不仅解决了装载难题,更在性能上实现了全面跃升。
近日,上海交通大学杨广宇研究员团队与华东师范大学李大力研究员团队在 Chemical Engineering Journal 上发表了重要研究成果。他们通过对目前已知最小的DNA靶向CRISPR核酸酶——AsCas12f1(仅422个氨基酸)进行定向进化改造,成功开发出高性能变体AsCas12f1-M5。这款新型编辑器将靶点识别范围扩大了3至4倍,在哺乳动物细胞中的编辑活性最高提升了超过10倍,并在小鼠体内实现了安全高效的基因编辑,为遗传病的临床治疗提供了强有力的下一代工具。

https://doi.org/10.1016/j.cej.2026.176417
微型工具的“靶点荒”与进化破局
基因编辑的“精准制导”依赖于PAM序列,它像是基因上的一个特定“邮政编码”,编辑器必须识别它才能进行切割。然而,天然的“超迷你”编辑器AsCas12f1虽能被单个AAV轻松装载,其PAM识别却极为严格(仅识别5‘-TTR序列),导致其在人类基因组中可编辑的位点覆盖率仅为约4%,应用价值因此受限。
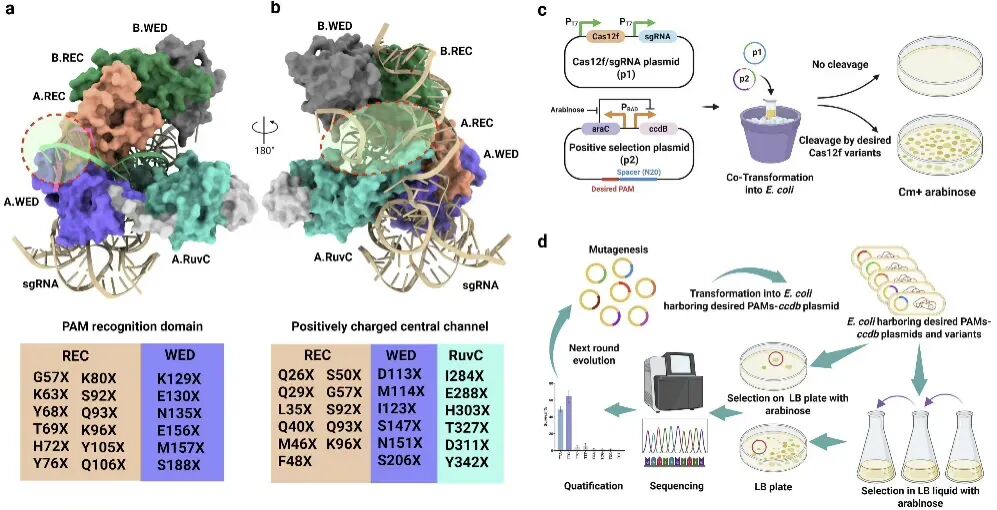
为了突破这一瓶颈,研究团队采用了“结构指导+定向进化”的组合策略。他们首先解析了AsCas12f1的三维结构,精准锁定了41个与PAM识别及DNA结合相关的关键氨基酸位点。随后,构建了一个巧妙的高通量筛选平台:将大肠杆菌的生长与编辑器的切割功能相偶联,只有那些能成功切割靶DNA序列的酶突变体,才能让细菌存活。
经过多轮迭代筛选与优势突变积累,研究团队最终获得了汇聚五个关键突变(G57R/M114Y/M157V/S188R/D311K)的最优变体——AsCas12f1-M5。
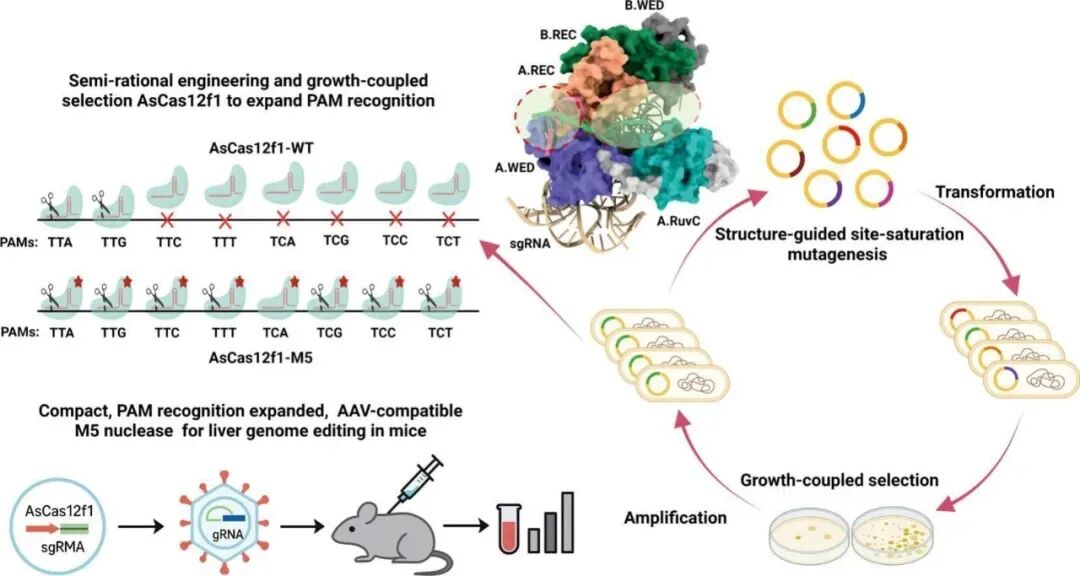
性能飞跃:从“特挑食”到“高效率”
经过改造的M5变体,其性能实现了全方位的显著提升:
靶点范围大幅扩展:M5的PAM识别范围从原来的5‘-TTR成功扩展至5’-TYN(包括TTA, TTG, TTC, TTT, TCA, TCC, TCG, TCT共8种)。这使得其理论可靶向的基因组位点覆盖率从约4%跃升至约15%,可用靶点数量扩大了3-4倍。
编辑活性显著增强:在体外切割实验中,针对经典的TTA/TTG PAM,M5在15-30分钟内即可完成高效切割;而对于野生型几乎无活性的TTC、TTT等新PAM序列,M5同样展现出强劲的切割能力。在HEK293T细胞报告实验中,M5在经典PAM位点的编辑效率(eGFP荧光激活)提升至62%-67%。在非经典PAM位点,其活性也普遍超过20%,部分位点甚至突破50%。在TP53、PDCD1等多个内源基因位点的测试中,M5的编辑效率均显著优于其他已报道的变体,证明了其扩展能力的普适性和高效性。
体内治疗验证:安全高效的“微型战舰”
研究的最终目的是应用于活体治疗。团队进一步在动物模型中验证了M5的实际疗效与安全性。
在细胞层面,针对覆盖全部8种TYN PAM的60个内源位点测试表明,M5在所有类型PAM上均能实现高效编辑,证明其在真实的染色质环境中同样稳定可靠。
更重要的是,在小鼠肝脏模型中,研究人员通过单次AAV递送,成功将M5系统送达肝脏细胞。结果表明,目标蛋白在血清中的水平下降了约30%,肝脏组织显示出了高效的编辑效果,且低剂量即可起效。同时,小鼠的肝功能指标和炎症因子水平均未出现异常,表明该编辑系统具有良好的体内安全性和耐受性,未引起明显的肝损伤或免疫反应。
展望:为基因治疗带来全新可能
AsCas12f1-M5的成功开发具有多重意义:
首先,它突破了递送限制。其超小尺寸(422 aa)使得“编辑器+向导RNA”可被完整封装进单个AAV载体,大幅简化了递送系统。其次,更广的PAM识别范围意味着能覆盖更多以往无法触及的致病基因突变,为更多遗传病提供治疗可能。此外,该研究也为其他微型CRISPR工具的工程化改造提供了可借鉴的结构指导与筛选流程。
展望未来,研究团队计划通过对向导RNA(gRNA)进行化学修饰与结构优化,进一步提升M5系统的编辑效率与特异性。凭借超小尺寸、广谱靶向、高效编辑、高安全性四大核心优势,AsCas12f1-M5有望成为治疗肝脏代谢疾病、神经肌肉疾病、眼科遗传病等领域的下一代临床级基因治疗工具,让超迷你编辑器真正承载起治愈疾病的宏大使命。
|
总结 上海交通大学与华东师范大学的研究团队通过定向进化,成功将超迷你基因编辑器AsCas12f1改造为性能更强的M5变体。新编辑器大幅拓宽了靶点识别范围,在细胞和动物模型中都展现出高编辑活性和良好安全性,并能被单个AAV载体递送。这项研究解决了基因治疗中大型工具递送困难与靶点受限的双重难题,为开发更安全、更通用的基因疗法提供了有力的新工具。 |
(免责声明:部分文字及图片来源于网络,仅供学习、交流使用,版权归原作者所有;如有问题请及时联系我们以做处理。部分内容由AI协助生成)
 夜雨聆风
夜雨聆风




